ご利用について
医療専門家向けの本PDQがん情報要約では、非小細胞肺がんの治療について、包括的な、専門家の査読を経た、そして証拠に基づいた情報を提供する。本要約は、がん患者を治療する臨床家に情報を与え支援するための情報資源として作成されている。これは医療における意思決定のための公式なガイドラインまたは推奨事項を提供しているわけではない。
本要約は編集作業において米国国立がん研究所(NCI)とは独立したPDQ Adult Treatment Editorial Boardにより定期的に見直され、随時更新される。本要約は独自の文献レビューを反映しており、NCIまたは米国国立衛生研究所(NIH)の方針声明を示すものではない。
CONTENTS
- 非小細胞肺がん(NSCLC)に関する一般情報
-
NSCLCには、上皮性肺がんのうち、小細胞肺がん(SCLC)を除くすべてのタイプが含まれる。NSCLCで最もよくみられるタイプは、扁平上皮がん、大細胞がん、および腺がんであるが、発生頻度は少ないが他のタイプもいくつかあり、すべてのタイプがまれな組織学的多様体で発生する可能性がある。NSCLCは喫煙と関係があるが、腺がんは喫煙歴がない患者に認められることもある。分類的にNSCLCは、SCLCと比較して相対的に化学療法および放射線療法に対して感受性が低い。病巣が切除可能な患者では、手術単独または手術と術後化学療法により治癒する可能性がある。病巣が切除不能な患者の多くは、放射線療法により局所制御を達成する可能性があるが、治癒がみられるのは少数の患者のみである。局所的に進行し病巣が切除不能な患者では、放射線療法と化学療法の併用により長期生存が得られる可能性がある。進行した転移病変を有する患者では、化学療法、標的化薬、および他の支持療法により、生存の改善および症状の緩和が得られる可能性がある。
発生率および死亡率
米国において、2020年に推定される肺がん(NSCLCとSCLCを合わせて)の新規症例数および死亡数:[ 1 ]
肺がんは、米国におけるがん関連死亡の最も主要な原因である。[ 1 ]1995年から2001年における肺がん患者の5年相対生存率は15.7%であった。5年相対生存率は局所病期(49%)、領域病期(16%)、遠隔病期(2%)の疾患を有する患者で診断時の病期によって顕著に変化する。[ 2 ]
解剖学
NSCLCは、中枢気管支から末梢肺胞までの肺上皮細胞から生じる。NSCLCの組織型は、発生部位に関係し、気管支から肺胞までの気道上皮組織の違いを示している。扁平上皮がんは、通常、中枢気管支の近くが発端となる。腺がんおよび細気管支肺胞がんは、通常、末梢肺組織に起源がある。
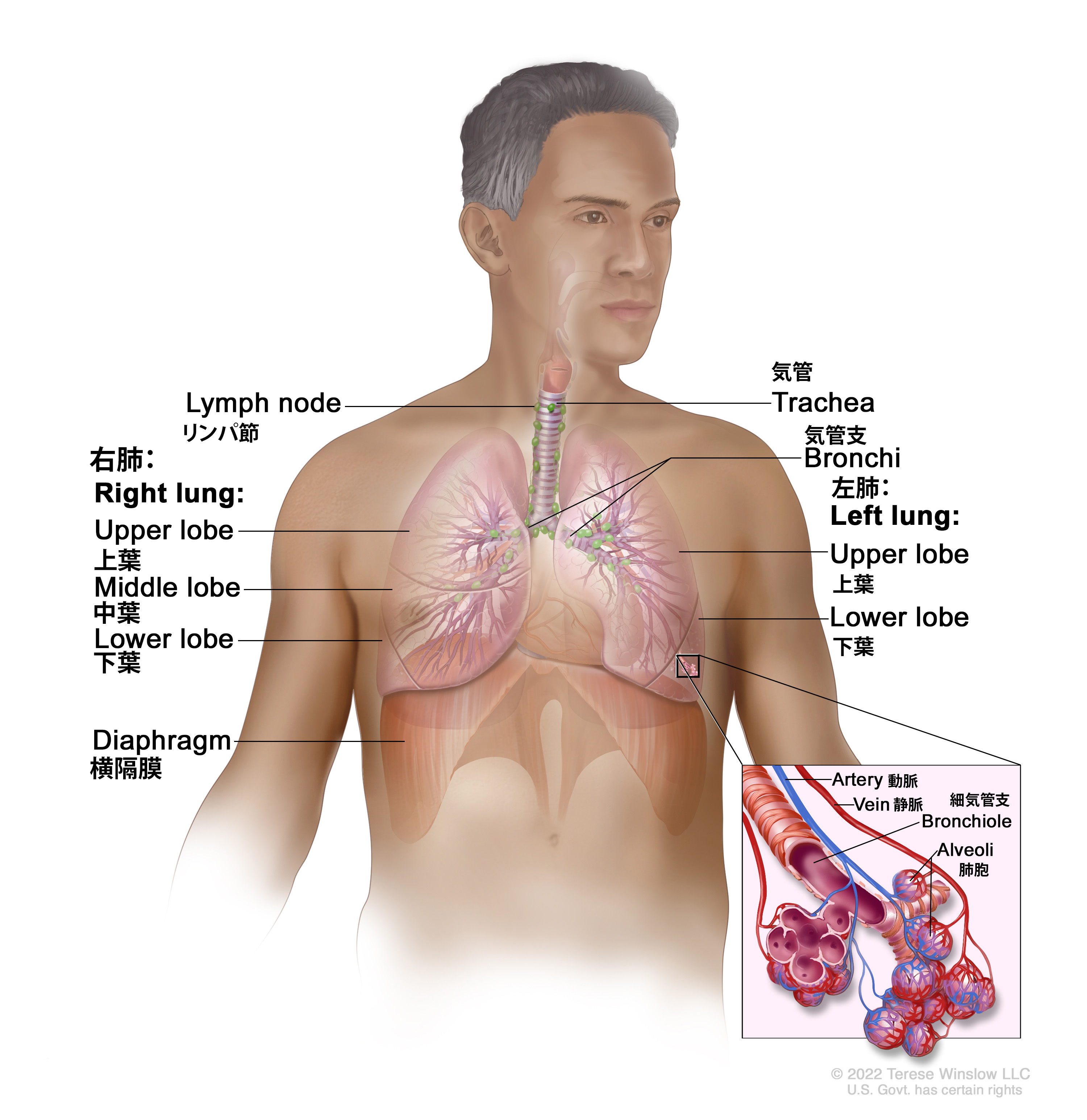
呼吸器系の解剖学。 発生機序
喫煙に関係した肺がん発生は多段階のプロセスである。扁平上皮がんおよび腺がんでは、前がん状態の前駆病変が定義されている。肺上皮は、浸潤するようになる前に、以下を含む形態学的変化を遂げる場合がある:
異形成および上皮内(in situ)がんは、浸潤がんに進行する可能性が高く自然に退縮する可能性が低いため、主要な前がん病変と考えられる。
さらに、肺がん切除後に二次肺がんが発生するリスクは、患者当たり年間1~2%である。[ 3 ]
病理学
NSCLCは、組織学的に不均一な集合体である。最もよくみられる組織型には以下のものがある:
診断、病期分類、予後、および治療に対するアプローチがほぼ同じであるため、これらの組織像はしばしばひとまとめに分類される。
危険因子
加齢はほとんどのがんの最も重要な危険因子である。肺がんに対する他の危険因子には以下のものがある:
肺がん発生に対する最も重要な単一の危険因子は喫煙である。喫煙者では、生涯非喫煙者(生涯に喫煙したタバコの本数が100本未満の人として定義)より、肺がんのリスクが平均して10倍高い。リスクは、喫煙量、喫煙期間、および開始年齢に応じて増加する。
禁煙により、前がん病変の減少および肺がん発生リスクの低下が得られる。前喫煙者は禁煙後も数年間、肺がんに対するリスクが継続して高い。アスベスト曝露は、喫煙による肺がんリスクに対して相乗効果を及ぼしうる。[ 19 ]
予防
喫煙関連の肺がんが治癒したかなりの数の患者が二次悪性腫瘍を発現する。T1期、N0の腫瘍を切除された患者907人を対象にLung Cancer Study Groupが行った試験では、肺以外での二次がん発生率は1.8%/年であり、新たな肺がんの発生率は1.6%/年であった。[ 20 ]長期生存者では、発生率が二次肺がんで10%、すべての二次がんで20%など、リスクがさらに高くなることを報告している別の研究がある。[ 21 ]
前喫煙者では二次肺がん発生のリスクが持続するため、さまざまな化学予防戦略がランダム化比較試験で評価されている。ベータカロチン、レチノール、13-シス-レチノイン酸、[α]-トコフェロール、N-アセチルシステイン、またはアセチルサリチル酸といった薬物を用いる第III相試験で、有益で再現可能な結果を実証しているものはない。[ 22 ][ 23 ][ 18 ][ 24 ][ 25 ][証拠レベル:1iiA]上気道消化管の二次原発がんに対する化学予防は、病期が初期の肺がん患者を対象に臨床評価が実施されている。
(詳しい情報については、肺がんの予防に関するPDQ要約を参照のこと。)
スクリーニング
肺がんを発症するリスクが高いと考えられる患者における早期発見のためのスクリーニング方法で、死亡率を変化させると示されている唯一のものは、低線量ヘリカルCTスキャンである。[ 26 ]胸部X線撮影および喀痰細胞診による肺がんスクリーニングの研究では、スクリーニングにより肺がん死亡率が低下することを実証できていない。
(詳しい情報については、肺がんのスクリーニングに関するPDQ要約の低線量ヘリカルコンピュータ断層撮影法のサブセクションを参照のこと。)
臨床的特徴
肺がんは、症状を伴って現れる場合、または胸部X線検査で偶然発見される場合がある。症状および徴候は、原発局所浸潤の存在、あるいは近隣胸部構造、遠隔転移、または腫瘍随伴性現象による圧迫から生じる場合がある。初診時に最も多くみられる症状は、咳の悪化または胸痛である。その他の主症状には以下のものがある:
- 喀血。
- 倦怠。
- 体重減少。
- 呼吸困難。
- 嗄声。
症状は、局所浸潤から生じる場合、あるいは嚥下困難を引き起こす食道への圧迫、嗄声を引き起こす喉頭神経への圧迫、または顔面浮腫および頭頸部表在静脈の膨張を引き起こす上大静脈への圧迫など、近隣胸部構造の圧迫から生じる場合がある。遠隔転移から症状が現れることもあり、脳転移による神経学的欠損または性格変化、あるいは骨転移による疼痛などがある。頻度は少ないが、ばち状指を伴う肥大性骨関節症、または副甲状腺ホルモン関連蛋白による高カルシウム血症など、腫瘍随伴症の症状および徴候を呈する患者もいる。身体診察により、腫大した鎖骨上部リンパ節腫脹、胸水または肺葉虚脱、器質化肺炎、あるいは慢性閉塞性肺疾患または肺線維症などの関連疾患による症状が認められる場合がある。
診断
NSCLCが疑われる患者の検査は、診断を確定すること、および病巣の範囲を判断することを重点に実施する。患者に対する治療選択肢は、組織型、病期、ならびに患者の全身健康状態および併存疾患によって決定される。
がんの存在を確定するために用いる手段には以下のものがある:
- 病歴。
- 身体診察。
- ルーチンの臨床検査評価。
- 胸部X線。
- 造影剤注入を伴う胸部CTスキャン。
- 生検。
肺がんの治療を開始する前に、肺がんについての経験豊富な病理医が病理材料を十分調べる必要がある。このことが重要な理由は、化学療法に良好な反応を示すため一般に外科的治療を行わないSCLCが、顕微鏡検査ではNSCLCと混同される可能性があるためである。[ 27 ]免疫組織化学および電子顕微鏡検査は診断および亜型分類に有用な技術であるが、ほとんどの肺腫瘍は光学顕微鏡の基準で分類可能である。
(病期判定に用いる検査および手技に関する詳しい情報については、本要約の病期評価のセクションを参照のこと。)
分子的特徴
肺がんにおける突然変異の同定を契機として、転移病変を有する患者サブセットの生存を改善する分子標的療法の開発が行われている。[ 28 ]特に、腺がんのサブセットは現在、上皮成長因子受容体(EGFR)と下流のマイトジェン活性化プロテインキナーゼ(MAPK)およびホスファチジルイノシトール3-キナーゼ(PI3K)シグナル伝達経路の構成要素をコード化する遺伝子に発生した特定の突然変異によって定義されうる。これらの変異は薬物感受性および原発性または後天性のキナーゼ阻害薬への耐性の機序を規定する場合がある。
治療法の決定に関連しうる他の遺伝子異常には、ALK阻害薬に対する感受性が高い未分化リンパ腫キナーゼ(ALK)-チロシンキナーゼ受容体を巻き込んだ転座、肝細胞成長因子受容体をコード化するMET(間葉上皮転換因子)の増幅、ならびにROS1遺伝子および神経栄養性チロシン受容体キナーゼ(NTRK)ファミリーの遺伝子を巻き込んだ頻発性遺伝子融合がある。MET増幅はEGFRチロシンキナーゼ阻害薬への二次耐性に関連している。
予後因子
さまざまな臨床病理学的因子の予後的重要性を確認しようとしている研究は多い。[ 21 ][ 29 ][ 30 ][ 31 ][ 32 ]予後不良と相関している因子として、以下のものがある:
病巣が手術不能な患者では、パフォーマンスステータスの不良および体重の10%を超える減少が、予後に悪影響を与える。これらの患者は、積極的な集学的療法による介入を評価する臨床試験から除外されている。
臨床試験データの複数のレトロスペクティブ解析では、高齢ということだけでは治療時の反応または生存への影響は示されていない。[ 47 ]
(予後に関する詳しい情報については、本要約のNSCLCの各病期の個々の治療セクションを参照のこと。)
ほぼすべてのNSCLC患者に対する治療が満足の行くものではないため、適格な患者は臨床試験への参加を検討されるべきである。現在実施中の臨床試験に関する情報は、NCIウェブサイトから入手することができる。
参考文献- American Cancer Society: Cancer Facts and Figures 2020. Atlanta, Ga: American Cancer Society, 2020. Available online. Last accessed May 12, 2020.[PUBMED Abstract]
- Ries L, Eisner M, Kosary C, et al., eds.: Cancer Statistics Review, 1975-2002. Bethesda, Md: National Cancer Institute, 2005. Available online. Last accessed November 30, 2017.[PUBMED Abstract]
- Johnson BE: Second lung cancers in patients after treatment for an initial lung cancer. J Natl Cancer Inst 90 (18): 1335-45, 1998.[PUBMED Abstract]
- Alberg AJ, Ford JG, Samet JM, et al.: Epidemiology of lung cancer: ACCP evidence-based clinical practice guidelines (2nd edition). Chest 132 (3 Suppl): 29S-55S, 2007.[PUBMED Abstract]
- Tulunay OE, Hecht SS, Carmella SG, et al.: Urinary metabolites of a tobacco-specific lung carcinogen in nonsmoking hospitality workers. Cancer Epidemiol Biomarkers Prev 14 (5): 1283-6, 2005.[PUBMED Abstract]
- Anderson KE, Kliris J, Murphy L, et al.: Metabolites of a tobacco-specific lung carcinogen in nonsmoking casino patrons. Cancer Epidemiol Biomarkers Prev 12 (12): 1544-6, 2003.[PUBMED Abstract]
- Straif K, Benbrahim-Tallaa L, Baan R, et al.: A review of human carcinogens--part C: metals, arsenic, dusts, and fibres. Lancet Oncol 10 (5): 453-4, 2009.[PUBMED Abstract]
- Friedman DL, Whitton J, Leisenring W, et al.: Subsequent neoplasms in 5-year survivors of childhood cancer: the Childhood Cancer Survivor Study. J Natl Cancer Inst 102 (14): 1083-95, 2010.[PUBMED Abstract]
- Gray A, Read S, McGale P, et al.: Lung cancer deaths from indoor radon and the cost effectiveness and potential of policies to reduce them. BMJ 338: a3110, 2009.[PUBMED Abstract]
- Berrington de González A, Kim KP, Berg CD: Low-dose lung computed tomography screening before age 55: estimates of the mortality reduction required to outweigh the radiation-induced cancer risk. J Med Screen 15 (3): 153-8, 2008.[PUBMED Abstract]
- Shimizu Y, Kato H, Schull WJ: Studies of the mortality of A-bomb survivors. 9. Mortality, 1950-1985: Part 2. Cancer mortality based on the recently revised doses (DS86). Radiat Res 121 (2): 120-41, 1990.[PUBMED Abstract]
- Katanoda K, Sobue T, Satoh H, et al.: An association between long-term exposure to ambient air pollution and mortality from lung cancer and respiratory diseases in Japan. J Epidemiol 21 (2): 132-43, 2011.[PUBMED Abstract]
- Cao J, Yang C, Li J, et al.: Association between long-term exposure to outdoor air pollution and mortality in China: a cohort study. J Hazard Mater 186 (2-3): 1594-600, 2011.[PUBMED Abstract]
- Hales S, Blakely T, Woodward A: Air pollution and mortality in New Zealand: cohort study. J Epidemiol Community Health 66 (5): 468-73, 2012.[PUBMED Abstract]
- Lissowska J, Foretova L, Dabek J, et al.: Family history and lung cancer risk: international multicentre case-control study in Eastern and Central Europe and meta-analyses. Cancer Causes Control 21 (7): 1091-104, 2010.[PUBMED Abstract]
- Shiels MS, Cole SR, Kirk GD, et al.: A meta-analysis of the incidence of non-AIDS cancers in HIV-infected individuals. J Acquir Immune Defic Syndr 52 (5): 611-22, 2009.[PUBMED Abstract]
- The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. The Alpha-Tocopherol, Beta Carotene Cancer Prevention Study Group. N Engl J Med 330 (15): 1029-35, 1994.[PUBMED Abstract]
- Omenn GS, Goodman GE, Thornquist MD, et al.: Effects of a combination of beta carotene and vitamin A on lung cancer and cardiovascular disease. N Engl J Med 334 (18): 1150-5, 1996.[PUBMED Abstract]
- Wingo PA, Ries LA, Giovino GA, et al.: Annual report to the nation on the status of cancer, 1973-1996, with a special section on lung cancer and tobacco smoking. J Natl Cancer Inst 91 (8): 675-90, 1999.[PUBMED Abstract]
- Thomas P, Rubinstein L: Cancer recurrence after resection: T1 N0 non-small cell lung cancer. Lung Cancer Study Group. Ann Thorac Surg 49 (2): 242-6; discussion 246-7, 1990.[PUBMED Abstract]
- Martini N, Bains MS, Burt ME, et al.: Incidence of local recurrence and second primary tumors in resected stage I lung cancer. J Thorac Cardiovasc Surg 109 (1): 120-9, 1995.[PUBMED Abstract]
- van Boxem AJ, Westerga J, Venmans BJ, et al.: Photodynamic therapy, Nd-YAG laser and electrocautery for treating early-stage intraluminal cancer: which to choose? Lung Cancer 31 (1): 31-6, 2001.[PUBMED Abstract]
- Blumberg J, Block G: The Alpha-Tocopherol, Beta-Carotene Cancer Prevention Study in Finland. Nutr Rev 52 (7): 242-5, 1994.[PUBMED Abstract]
- Lippman SM, Lee JJ, Karp DD, et al.: Randomized phase III intergroup trial of isotretinoin to prevent second primary tumors in stage I non-small-cell lung cancer. J Natl Cancer Inst 93 (8): 605-18, 2001.[PUBMED Abstract]
- van Zandwijk N, Dalesio O, Pastorino U, et al.: EUROSCAN, a randomized trial of vitamin A and N-acetylcysteine in patients with head and neck cancer or lung cancer. For the EUropean Organization for Research and Treatment of Cancer Head and Neck and Lung Cancer Cooperative Groups. J Natl Cancer Inst 92 (12): 977-86, 2000.[PUBMED Abstract]
- Aberle DR, Adams AM, Berg CD, et al.: Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med 365 (5): 395-409, 2011.[PUBMED Abstract]
- Travis WD, Colby TV, Corrin B, et al.: Histological typing of lung and pleural tumours. 3rd ed. Berlin: Springer-Verlag, 1999.[PUBMED Abstract]
- Pao W, Girard N: New driver mutations in non-small-cell lung cancer. Lancet Oncol 12 (2): 175-80, 2011.[PUBMED Abstract]
- Albain KS, Crowley JJ, LeBlanc M, et al.: Survival determinants in extensive-stage non-small-cell lung cancer: the Southwest Oncology Group experience. J Clin Oncol 9 (9): 1618-26, 1991.[PUBMED Abstract]
- Macchiarini P, Fontanini G, Hardin MJ, et al.: Blood vessel invasion by tumor cells predicts recurrence in completely resected T1 N0 M0 non-small-cell lung cancer. J Thorac Cardiovasc Surg 106 (1): 80-9, 1993.[PUBMED Abstract]
- Ichinose Y, Yano T, Asoh H, et al.: Prognostic factors obtained by a pathologic examination in completely resected non-small-cell lung cancer. An analysis in each pathologic stage. J Thorac Cardiovasc Surg 110 (3): 601-5, 1995.[PUBMED Abstract]
- Fontanini G, Bigini D, Vignati S, et al.: Microvessel count predicts metastatic disease and survival in non-small cell lung cancer. J Pathol 177 (1): 57-63, 1995.[PUBMED Abstract]
- Sayar A, Turna A, Kiliçgün A, et al.: Prognostic significance of surgical-pathologic multiple-station N1 disease in non-small cell carcinoma of the lung. Eur J Cardiothorac Surg 25 (3): 434-8, 2004.[PUBMED Abstract]
- Osaki T, Nagashima A, Yoshimatsu T, et al.: Survival and characteristics of lymph node involvement in patients with N1 non-small cell lung cancer. Lung Cancer 43 (2): 151-7, 2004.[PUBMED Abstract]
- Ichinose Y, Kato H, Koike T, et al.: Overall survival and local recurrence of 406 completely resected stage IIIa-N2 non-small cell lung cancer patients: questionnaire survey of the Japan Clinical Oncology Group to plan for clinical trials. Lung Cancer 34 (1): 29-36, 2001.[PUBMED Abstract]
- Tanaka F, Yanagihara K, Otake Y, et al.: Prognostic factors in patients with resected pathologic (p-) T1-2N1M0 non-small cell lung cancer (NSCLC). Eur J Cardiothorac Surg 19 (5): 555-61, 2001.[PUBMED Abstract]
- Asamura H, Suzuki K, Kondo H, et al.: Where is the boundary between N1 and N2 stations in lung cancer? Ann Thorac Surg 70 (6): 1839-45; discussion 1845-6, 2000.[PUBMED Abstract]
- Riquet M, Manac'h D, Le Pimpec-Barthes F, et al.: Prognostic significance of surgical-pathologic N1 disease in non-small cell carcinoma of the lung. Ann Thorac Surg 67 (6): 1572-6, 1999.[PUBMED Abstract]
- van Velzen E, Snijder RJ, Brutel de la Rivière A, et al.: Lymph node type as a prognostic factor for survival in T2 N1 M0 non-small cell lung carcinoma. Ann Thorac Surg 63 (5): 1436-40, 1997.[PUBMED Abstract]
- Vansteenkiste JF, De Leyn PR, Deneffe GJ, et al.: Survival and prognostic factors in resected N2 non-small cell lung cancer: a study of 140 cases. Leuven Lung Cancer Group. Ann Thorac Surg 63 (5): 1441-50, 1997.[PUBMED Abstract]
- Izbicki JR, Passlick B, Karg O, et al.: Impact of radical systematic mediastinal lymphadenectomy on tumor staging in lung cancer. Ann Thorac Surg 59 (1): 209-14, 1995.[PUBMED Abstract]
- Martini N, Burt ME, Bains MS, et al.: Survival after resection of stage II non-small cell lung cancer. Ann Thorac Surg 54 (3): 460-5; discussion 466, 1992.[PUBMED Abstract]
- Naruke T, Goya T, Tsuchiya R, et al.: Prognosis and survival in resected lung carcinoma based on the new international staging system. J Thorac Cardiovasc Surg 96 (3): 440-7, 1988.[PUBMED Abstract]
- Thomas P, Doddoli C, Thirion X, et al.: Stage I non-small cell lung cancer: a pragmatic approach to prognosis after complete resection. Ann Thorac Surg 73 (4): 1065-70, 2002.[PUBMED Abstract]
- Macchiarini P, Fontanini G, Hardin MJ, et al.: Relation of neovascularisation to metastasis of non-small-cell lung cancer. Lancet 340 (8812): 145-6, 1992.[PUBMED Abstract]
- Khan OA, Fitzgerald JJ, Field ML, et al.: Histological determinants of survival in completely resected T1-2N1M0 nonsmall cell cancer of the lung. Ann Thorac Surg 77 (4): 1173-8, 2004.[PUBMED Abstract]
- Earle CC, Tsai JS, Gelber RD, et al.: Effectiveness of chemotherapy for advanced lung cancer in the elderly: instrumental variable and propensity analysis. J Clin Oncol 19 (4): 1064-70, 2001.[PUBMED Abstract]
- NSCLCの細胞分類
-
悪性非小細胞肺上皮性腫瘍は、世界保健機関(WHO)/International Association for the Study of Lung Cancer(IASLC)により分類されている。非小細胞肺がん(NSCLC)の主要な亜型として、以下の3つがある:
- 扁平上皮がん(肺がんの25%)。
- 腺がん(肺がんの40%)。
- 大細胞がん(肺がんの10%)。
他にも頻度は少ないが数多くの亜型がある。[ 1 ]
WHO/IASLCによるNSCLCの組織学的分類
- 扁平上皮がん。
- 乳頭がん。
- 淡明細胞。
- 小細胞。
- 類基底細胞。
- 腺がん。
- 腺房。
- 乳頭がん。
- 細気管支肺胞がん。
- 粘液非産生型。
- 粘液産生型。
- 粘液産生型と粘液非産生型の混合、または中間細胞型。
- 粘液産生充実腺がん。
- 混合型腺がん。
- 多様体。
- 高分化胎児型腺がん。
- 粘液性(コロイド)腺がん。
- 粘液嚢胞腺がん。
- 印環細胞腺がん。
- 淡明細胞腺がん。
- 大細胞がん。
- 多様体。
- 大細胞神経内分泌がん(LCNEC)。
- 混合性LCNEC。
- 類基底細胞がん。
- リンパ上皮腫様がん。
- 淡明細胞がん。
- ラブドイド表現型を伴う大細胞がん。
- 多様体。
- 腺扁平上皮がん。
- 多形性、肉腫様、または肉腫性成分を伴うがん。
- 紡錘細胞および/または巨細胞を伴うがん。
- 紡錘細胞がん。
- 巨大細胞がん。
- がん肉腫。
- 肺芽腫。
- カルチノイド腫瘍。
- 定型的カルチノイド。
- 非定型的カルチノイド。
- 唾液腺型のがん。
- 粘表皮がん。
- 腺様嚢胞がん。
- その他。
- 分類不能がん。
扁平上皮がん
肺の扁平上皮がんは、ほとんどが肺の中枢寄りの太い方の気管支に発生する。扁平上皮がんは、喫煙との関係がNSCLCの他の型より強い。肺の扁平上皮がんの発生率は近年減少してきている。
腺がん
腺がんは、現在、多くの国で最も多くみられる組織亜型となっており、腺がんの亜型分類は重要である。肺腺がんに関する最も大きな問題の1つは、しばしばみられる組織学的な不均一性である。実際、粘液産生を伴う腺房、乳頭、細気管支肺胞、および充実腺がんの単一の腺がん組織学的亜型のみからなる腫瘍よりも、これらの腺がん組織学的亜型が混在する腫瘍の方が一般的である。
細気管支肺胞がんの診断基準は以前は大きく異なっていた。現行のWHO/IASLC定義は非浸潤性腫瘍のみに限定しているため、多くの病理医が過去に用いていた定義より、はるかに厳格である。
細気管支肺胞がん領域が広範囲に及ぶ腺がんでは、間質、血管、または胸膜への浸潤が同定された場合の分類は、浸潤領域に見られるパターンにもよるが、優勢な細気管支肺胞パターンと、限局的腺房、充実、または乳頭パターンが混合した亜型の腺がんとなる。しかし、細気管支肺胞がんが将来的にも個別の疾患実体とされるかどうかは不透明である;IASLCを代表する集学的な専門家会議とAmerican Thoracic SocietyおよびEuropean Respiratory Societyは2011年に腺がんの分類の主要改訂を提示したが、その中でこれまで細気管支肺胞がんと呼ばれてきた疾患を新たに定義された組織学的亜型に再分類することが含意されている。
WHO/IASLC分類では、腺がんに以下の多様体が認定されている:
- 高分化胎児型腺がん。
- 粘液性(コロイド)腺がん。
- 粘液嚢胞腺がん。
- 印環細胞腺がん。
- 淡明細胞腺がん。
大細胞がん
WHO/IASLC分類では、大細胞がんの一般的なカテゴリーに加えて、まれな多様体がいくつか認定されており、以下の多様体がある:
- LCNEC。
- 類基底細胞がん。
- リンパ上皮腫様がん。
- 淡明細胞がん。
- ラブドイド表現型を伴う大細胞がん。
類基底細胞がんはまた、扁平上皮がんの多様体としても認識されており、まれに、腺がんが類基底細胞パターンを示すこともある;しかしながら、これらの特徴のいずれも伴わない腫瘍では大細胞がんの多様体とみなされる。
神経内分泌腫瘍
LCNECは、組織学的に高悪性度の非小細胞がんとして認識されている。LCNECは小細胞肺がん(SCLC)の予後と同様、きわめて予後不良である。非定型カルチノイドは、中悪性度の神経内分泌腫瘍として認定されており、予後は定型的カルチノイドと高悪性度のSCLCおよびLCNECとの間である。
神経内分泌分化は、免疫組織化学または電子顕微鏡により、神経内分泌の形態学的特徴が全く認められない一般的なNSCLCの10~20%で実証できる。これらの腫瘍は、NSCLCの神経内分泌分化についての臨床および治療的意義がはっきりと確定していないため、WHO/IASLC分類スキーム内では正式に認定されていない。これらの腫瘍は集合的に、神経内分泌分化を伴うNSCLCと呼ばれる。
多形性、肉腫様、または肉腫性成分を伴うがん
これはまれな腫瘍グループである。紡錘細胞がんおよび巨大細胞がんは、肺の全悪性腫瘍のわずか0.4%を占めるのみで、がん肉腫は、肺の全悪性腫瘍のわずか0.1%を占めるのみである。また、このグループの腫瘍は、一連の組織学的異質性に加え、上皮および間葉の分化を反映している。臨床および分子データを基に、二相性肺芽腫は、多形性、肉腫様、または肉腫性の腫瘍を伴う一連の上皮性悪性腫瘍の1つとみなされている。
分子的特徴
肺がんにおける突然変異の同定を契機として、転移病変を有する患者サブセットの生存を改善する分子標的療法の開発が行われている。[ 2 ]特に、腺がんのサブセットは現在、上皮成長因子受容体(EGFR)と下流のマイトジェン活性化プロテインキナーゼ(MAPK)およびホスファチジルイノシトール3-キナーゼ(PI3K)シグナル伝達経路の構成要素をコード化する遺伝子に発生した特定の突然変異によって定義されうる。これらの変異は薬物感受性および原発性または後天性のキナーゼ阻害薬への耐性の機序を規定する場合がある。治療法の決定に関連しうる他の遺伝子異常には、次の遺伝子が関与している:
- カーステンラット肉腫ウイルスがん遺伝子(KRAS)。
- 未分化リンパ腫キナーゼ受容体(ALK)。
- ヒト上皮成長因子受容体2(HER2)。
- V-rafマウス肉腫ウイルスがん遺伝子ホモログB1(BRAF)。
- PI3K触媒蛋白α(PI3KCA)。
- AKTセリン/スレオニンキナーゼ1(AKT1)。
- ROSがん原遺伝子1受容体チロシンキナーゼ(ROS1)。
- 神経栄養性受容体チロシンキナーゼ1(NTRK1)、神経栄養性受容体チロシンキナーゼ2(NTRK2)、および神経栄養性受容体チロシンキナーゼ3(NTRK3)。
- MAPKキナーゼ1(MAP2K1またはMEK1)。
- 肝細胞増殖因子受容体(HGFR)をコード化するMET。
これらの突然変異は、PI3KCAおよびBRAFの突然変異、EGFRの突然変異、またはALK転座が関与するものを除いて、相互に排他的である。[ 3 ][ 4 ]
EGFRおよびALKの突然変異は非喫煙者に発生する腺がんで優位を占め、KRASおよびBRAFの突然変異は喫煙者および前喫煙者により一般的に認められる。EGFR突然変異は、EGFR阻害薬の奏効率および無増悪生存率の改善を強力に予測する。Memorial Sloan Kettering Cancer Centerで治療を受けた患者から採取された2,142個の肺腺がん標本中に、EGFRエクソン19欠失およびL858Rは、前喫煙者の腫瘍の15%(1,218標本中181;95%信頼区間[CI]、13-17)、現喫煙者の腫瘍の6%(344標本中20;95%CI、4-9)、および非喫煙者の52%(580標本中302;95%CI、48-56;喫煙経験者 vs 非喫煙者でP < 0.001)に認められた。[ 5 ]
ALK遺伝子とEML4遺伝子の融合は、非選別のNSCLCにおいて3~7%の幅で発生する転座産物を形成し、クリゾチニブなどの薬剤によるALKの薬理学的阻害に反応する。ALKと他の遺伝子の免疫感作融合(sensitizing fusions)もまた報告されている。NSCLC腫瘍の5%未満で発生するその他の遺伝子変化には、以下のものがある:
- HER2変異、腫瘍の2%に存在。
- PI3KCA変異、腫瘍の2%に存在。
- AKT1変異、腫瘍の1%に存在。
- ROS1融合、腫瘍の1~2%に存在。
- NTRK融合、腫瘍の0.5%未満に存在。
- BRAF突然変異、腫瘍の1~3%に存在。
BRAF突然変異は、EGFR突然変異およびKRAS突然変異と相互に排他的である。MAP2K1(MEKとしても知られる)の体細胞突然変異はNSCLCの1%で同定されている。METがん遺伝子は、肝細胞増殖因子受容体をコード化する。この遺伝子の増幅は、EGFRチロシンキナーゼ阻害薬への二次耐性に関連している。
参考文献- Travis WD, Colby TV, Corrin B, et al.: Histological typing of lung and pleural tumours. 3rd ed. Berlin: Springer-Verlag, 1999.[PUBMED Abstract]
- Pao W, Girard N: New driver mutations in non-small-cell lung cancer. Lancet Oncol 12 (2): 175-80, 2011.[PUBMED Abstract]
- Tiseo M, Gelsomino F, Boggiani D, et al.: EGFR and EML4-ALK gene mutations in NSCLC: a case report of erlotinib-resistant patient with both concomitant mutations. Lung Cancer 71 (2): 241-3, 2011.[PUBMED Abstract]
- Villaruz LC, Socinski MA, Abberbock S, et al.: Clinicopathologic features and outcomes of patients with lung adenocarcinomas harboring BRAF mutations in the Lung Cancer Mutation Consortium. Cancer 121 (3): 448-56, 2015.[PUBMED Abstract]
- D'Angelo SP, Pietanza MC, Johnson ML, et al.: Incidence of EGFR exon 19 deletions and L858R in tumor specimens from men and cigarette smokers with lung adenocarcinomas. J Clin Oncol 29 (15): 2066-70, 2011.[PUBMED Abstract]
- NSCLCの病期情報
-
背景
非小細胞肺がん(NSCLC)において、病期の決定は治療および予後の観点から重要である。原発巣の拡がりと転移巣の有無を明らかにするための注意深い最初の診断的評価が、患者に適切な医療を行う上できわめて重要である。
一般に、遠隔転移の症状、身体的徴候、検査所見、または認識されたリスクにより、遠隔転移が評価される。最初の評価で転移が示唆される場合、または病期がIII期の患者が積極的な局所治療および集学的治療を検討している場合は、骨スキャンおよび脳のコンピュータ断層撮影(CT)/磁気共鳴画像法(MRI)などの追加検査を実施してもよい。
治療選択において病期には重要な役割がある。病期は、臨床的因子および病理学的因子の組み合わせに基づいている。[ 1 ]生存転帰の報告を評価する場合には、臨床的病期と病理学的病期の違いを考慮すべきである。
病期判定に用いられる手段には以下のものがある:
- 病歴。
- 身体診察。
- ルーチンの臨床検査評価。
- 胸部X線。
- 造影剤注入を伴う胸部CTスキャン。
- フッ素18-フルデオキシグルコースポジトロン放射断層撮影(18F-FDG PET)スキャン。
組織標本を得るために用いる手段には、気管支鏡検査、縦隔鏡検査、または前方縦隔切開術などがある。NSCLCの病理学的病期分類には、以下が必要である:
- 腫瘍の検査。
- 切除縁。
- リンパ節。
予後および治療の決定は以下の因子に基づく:
- 組織型の知識。
- 腫瘍の大きさと位置。
- 胸膜浸潤。
- 切除断端。
- リンパ節の節ごとの状態および位置。
- 腫瘍の悪性度。
- リンパ血管性浸潤。
診断時点で、病巣の範囲および治療方法の両者を考慮して、NSCLC患者を以下の3群に分けることができる:
- 外科的に切除可能な病変(一般に腫瘍病期がI期、II期、および一部のIII期)。
- 最も予後良好であるが、腫瘍および宿主のさまざまな因子に左右される。
- 切除可能ながんであっても患者が医学的に手術禁忌であれば、根治的放射線療法が考えられる。
- II期またはIIIA期のNSCLCで切除した患者に対しては、術後のシスプラチンをベースとした併用化学療法により、生存利益が得られる場合がある。
- 局所進行性(T3~T4)および/または領域進行性(N2~N3)の病変。
- 多様な自然経過を示す。
- 腫瘍が局所的に進行した選択患者は集学的治療から利益が得られる場合がある。
- 切除不能またはN2~N3のがんを有する患者は、化学療法と併用する放射線療法で治療される。
- T3またはN2の病変を有する特定の患者には、外科的切除および術前または術後化学療法あるいは化学放射線療法により有効な治療を行うことができる。
- 遠隔転移病変(診断時に発見された遠隔転移[M1]を含む)。
- 原発腫瘍による症状を緩和するために、放射線療法または化学療法を用いて治療してもよい。
- パフォーマンスステータスが良好な患者、女性、遠隔転移が1つの場所に限局している患者は、他の患者よりも長期間生存する。[ 2 ]
- プラチナ製剤をベースにした化学療法は、短期間の症状緩和と生存優位につながる。
- 現在、ルーチンに行うことが推奨される単剤化学療法のレジメンは存在しない。
- 過去にプラチナ製剤併用化学療法による治療を受けた患者では、ドセタキセル、ペメトレキセド、または上皮成長因子受容体阻害薬により、症状の管理および生存利益が得られる場合がある。
病期評価
上縦隔リンパ節転移の評価
外科的評価
治療法を決定するためにリンパ節の正確な評価が必要である場合には、縦隔の外科的病期決定が標準とされている。
縦隔リンパ節の正確な病期分類は、予後に関する重要な情報を提供する。
証拠(リンパ節の状態):
- I期NSCLCを根治的な外科的切除で治療された患者に対して手術中に調べられたリンパ節の数と生存との関連が、1990年から2000年における集団ベースのSurveillance, Epidemiology, and End Results(SEER)データベースで評価された。[
3
]計16,800人の患者が研究に含められた。
- 放射線療法を受けたことがない患者を対象とした全生存解析により、基準群(評価リンパ節が1~4)と比較した場合、術中に評価したリンパ節が5~8の患者は、わずかではあるが、統計的に有意な生存期間の延長を示し、比例ハザード比(HR)は0.90(95%信頼区間[CI]、0.84-0.97)であったことが実証された。評価したリンパ節が9~12の患者のHRは0.86(95%CI、0.79-0.95)で、評価したリンパ節が13~16の患者のHRは0.78(95%CI、0.68-0.90)であった。16を超えるリンパ節を評価しても追加の改善は得られないようであった。肺がん特異的死亡率および放射線療法を受けた患者に対して相当する結果は実質的に変わらなかった。
- これらの結果から、NSCLC切除後の患者の生存は手術中に評価されるリンパ節の数と関連していることが示されている。これは、病期分類における誤判定の減少、すなわちリンパ節のサンプリング数が増えるのに伴って、転移陽性リンパ節を見逃す確率が減少した結果である可能性が高いため、リンパ節の状態評価には11~16のリンパ節を含めるべきであることが示唆される。
CT画像法
CTスキャンは、主に腫瘍の大きさを判定するために用いられる。CTは、肝および副腎を含めるため下方まで延長すべきである。胸部および上腹部のMRIスキャンでは、CTスキャンを超える優位性は得られないと考えられる。[ 4 ]
証拠(CTスキャン):
- 肺がん患者における縦隔の非侵襲的な病期分類としてのCTの正確度に関して、医学文献の系統的レビューが実施されている。1991年から2006年6月に公表された35件の研究では、評価可能な患者が5,111人確認された。ほぼすべての研究で、CTは造影剤静注後に実施すること、および陽性の検査結果は短軸径で1cmを超える1つ以上のリンパ節転移の存在と定義すると明記されていた。[
5
]
- 縦隔転移の有病率中央値は28%であった(範囲、18~56%)。
- 縦隔リンパ節転移の同定で、CTスキャンの感度および特異度を併合すると、感度は51%(95%CI、47%-54%)および特異度は86%(95%CI、84%-88%)であった。相当する陽性(3.4%)および陰性(0.6%)尤度比が提供された。
- この系統的レビューによる結果は、大規模メタアナリシスの結果と同等であり、そこでは、悪性の縦隔リンパ節の同定で、CTスキャンの感度および特異度の中央値が、感度61%および特異度79%であったことが報告されている。[ 6 ]
- より早期のメタアナリシスでは、平均感度64%および特異度74%と報告された。[ 7 ]
18F-FDG PETスキャン
18F-FDG PETスキャンが広く利用可能になり、病期判定に使用されるようになって、縦隔リンパ節および遠隔転移の病期判定アプローチが変化している。
切除可能と考えられるNSCLCを対象に、18F-FDG PETスキャンの有用性を評価したランダム化試験によると、非治癒開胸術の件数における相対的な減少の点では、相反する結果が報告されている。
現時点での証拠は矛盾しているが、外科的切除可能範囲の外にあり、標準的な術前病期分類法では明確に規定されていない転移病変の証拠を有する患者を、18F-FDG PETスキャンにより同定することで、病期が初期の肺がんの転帰が改善される可能性がある。
証拠(18F-FDG PETスキャン):
- 2001年にInstitute for Clinical and Evaluative Sciencesが実施した健康技術評価を拡張した系統的レビューで、肺がんの診断および病期分類における18F-FDG PETスキャンの正確度および有用性が評価された。[ 8 ]系統的な文献調査を通して、18F-FDG PETスキャンの診断的正確度に関して、12件の証拠要約報告および15件のプロスペクティブ研究が確認された。NSCLCにおける縦隔の病期分類では、18F-FDG PETスキャンがCT画像法より優れていると考えられる。18F-FDG PETスキャンは、1cmほどの小さな病変の良性か悪性かの鑑別でも感度が高く、特異度が妥当であると考えられる。
- 肺がん患者における縦隔の非侵襲的な病期分類としての18F-FDG PETスキャンの正確度に関する医学文献の系統的レビューにより、1994年から2006年に発表された44件の研究が確認され、評価可能な患者の数は2,865人であった。[ 5 ]縦隔転移の有病率中央値は29%であった(範囲、5~64%)。縦隔転移を同定するための感度および特異度の併合推定値は、感度74%(95%CI、69%-79%)および特異度85%(95%CI、82%-88%)であった。18F-FDG PETスキャンによる縦隔の病期分類について対応する陽性(4.9%)および陰性(0.3%)の尤度比が提供された。これらの知見から、肺がん患者における縦隔の病期分類では、18F-FDG PETスキャンの方がCTスキャンより正確であることが実証されている。
18F-FDG PETスキャンの費用対効果
18F-FDG PETスキャンにより、縦隔のCTスキャンで偽陰性の患者、あるいは他の方法では検出できない転移巣がある患者を同定することで、総医療費が抑えられる可能性があることが、決定解析で実証されている。[ 9 ][ 10 ][ 11 ]縦隔病変が18F-FDG PET陽性であれば、縦隔鏡検査を実施しないことで節約される費用は、偽陽性となる結果が許容できないほど多いため、正当化されないことが研究で結論された。[ 9 ][ 10 ][ 11 ]従来の病期分類へ18F-FDG PETスキャンを追加したことに関連して、開胸術が有意に減少したことがランダム化研究により明らかになった。[ 12 ]18F-FDG PETスキャンが臨床管理に与える影響を評価した別のランダム化試験では、18F-FDG PETスキャンにより、適切な病期に関する補足情報が得られるが、開胸術の有意な減少にはつながらないことが明らかにされた。[ 13 ]
CT画像法と18F-FDG PETスキャンの併用
CT画像法と18F-FDG PETスキャンの併用は、CT画像法単独より感度および特異度が高い。[ 14 ]
証拠(CT/18F-FDG PETスキャン):
- CTスキャンで遠隔転移の証拠が認められない場合、18F-FDG PETスキャンは縦隔の病期決定を行うCTスキャンを補完する。18F-FDG PETスキャンに関する多数の非ランダム化研究では、比較のためのゴールドスタンダードとして手術(すなわち、縦隔鏡検査および/または縦隔リンパ節郭清を伴う開胸術)を用いて縦隔リンパ節が評価されている。
- 18F-FDG PETスキャンおよびCTスキャンの条件付き検査性能を評価したメタアナリシスでは、リンパ節が腫大した患者における18F-FDG PETスキャンの感度および特異度の中央値は、感度100%および特異度78%であったことが報告された。[ 6 ]リンパ節が腫大している場合の悪性リンパ節病変の同定では、18F-FDG PETスキャンはきわめて正確であると考えられる。しかしながら、18F-FDG PETスキャンでは、通常は炎症または感染の結果として、他の原因でリンパ節が腫大している患者の約1/4を誤って悪性腫瘍と同定してしまう。[ 15 ][ 16 ]
- 縦隔リンパ節が正常な大きさの患者では、18F-FDG PETスキャンの感度および特異度の中央値は、感度82%および特異度93%であった。[ 6 ]これらのデータは、リンパ節の大きさは正常であるが悪性病変を有する患者では、20%近くが18F-FDG PETスキャンの所見が偽陰性となることを示している。
臨床的に手術可能なNSCLCの患者では、縦隔リンパ節について、胸部CTスキャンで横軸断面の短径が1cmを超えることが明らかになった場合、または18F-FDG PETスキャンで陽性であることが明らかになった場合は、生検が推奨される。18F-FDG PETスキャンが陰性でも放射線学的に腫大が認められた縦隔リンパ節の生検は除外されない。縦隔リンパ節におけるがんの検出で、CTスキャンおよび18F-FDG PETスキャンの結果からお互いに裏付けが得られない場合は、縦隔鏡検査が必要である。
脳転移の評価
脳転移のリスクがある患者は、CTまたはMRIで病期が決定される。手術可能と考えられるNSCLC患者で、神経学的症状を認めない患者332人を対象に、肺の手術前に潜在性脳転移を検出するために、脳のCTまたはMRI画像法のいずれかにランダムに割り付けた研究が1件ある。MRIは、術前検出率がCTスキャンより高い傾向を示し(P = 0.069)、手術前から手術後12ヵ月までの全検出率は約7%であった。[ 17 ]I期またはII期のがん患者の検出率は4%(すなわち、患者200人中8人で検出)であった;しかしながら、III期のがん患者の検出率は11.4%(すなわち、患者132人中15人で検出)であった。脳転移巣の平均最大径は、MRI群で有意に小さかった。MRIの高い検出率により転帰が改善されるかどうかは、依然として不明である。すべての患者がMRIに耐えられるわけではなく、これらの患者に対しては造影CTが合理的な代替法である。
脳以外の遠隔転移の評価
多数のプロスペクティブおよびレトロスペクティブの非ランダム化研究から、遠隔転移病変の病期分類において、従来の画像法を超える診断的優位性が18F-FDG PETスキャンにより得られると考えられることが実証されている;しかしながら、標準的な18F-FDG PETスキャンには限界がある。18F-FDG PETスキャンは骨盤より下方には実施されないことがあり、下肢の長骨における骨転移を検出できない場合がある。18F-FDG PETスキャンに用いられる代謝トレーサーは、脳および尿路に蓄積するため、これらの部位における転移の検出では、18F-FDG PETスキャンは信頼できない。[ 17 ]
改訂国際肺がん病期分類システム
改訂国際肺がん病期分類システムは、5,000人以上の患者の臨床データベースから得た情報に基づいて、米国がん合同委員会(AJCC)およびUnion Internationale Contre le Cancerにより2010年に採択された。[ 18 ][ 19 ]これらの改訂では、患者グループの予後の特異性に重点を置いている;しかしながら、病期と予後の相関はPET画像診断が広く利用される以前のものである。
AJCCの病期分類とTNM定義
AJCCは、NSCLCを定義するためにTNM(腫瘍、リンパ節、転移)分類による病期判定を指定している。[ 19 ]
表1.TNM潜伏がんの定義a 病期 TNM 説明 aAJCCから許諾を得て転載:Lung.In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual.8th ed. New York, NY: Springer, 2017, pp 431-56. 潜伏がん TX、N0、M0 TX = 原発腫瘍が評価できない場合、あるいは喀痰または気管支洗浄液中に悪性細胞が認められることにより腫瘍が立証されるが、画像法または気管支鏡検査では視認できない場合。 N0 = 所属リンパ節に転移を認めない。 M0 = 遠隔転移を認めない。 T = 原発腫瘍;N = 所属リンパ節;M = 遠隔転移。 表2.TNM分類における0期の定義a 病期 TNM 説明 T = 原発腫瘍;N = 所属リンパ節;M = 遠隔転移。 aAJCCから許諾を得て転載:Lung.In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual.8th ed. New York, NY: Springer, 2017, pp 431-56. 0 Tis、N0、M0 Tis = 上皮内(in situ)がん;SCIS = 扁平上皮がん(squamous cell carcinoma in situ);AIS:上皮内腺がん(adenocarcinoma in situ);純粋な鱗状のパターンを有する最大径が3cm以下の腺がん。 N0 = 所属リンパ節に転移を認めない。 M0 = 遠隔転移を認めない。 参考文献- Pfister DG, Johnson DH, Azzoli CG, et al.: American Society of Clinical Oncology treatment of unresectable non-small-cell lung cancer guideline: update 2003. J Clin Oncol 22 (2): 330-53, 2004.[PUBMED Abstract]
- Albain KS, Crowley JJ, LeBlanc M, et al.: Survival determinants in extensive-stage non-small-cell lung cancer: the Southwest Oncology Group experience. J Clin Oncol 9 (9): 1618-26, 1991.[PUBMED Abstract]
- Ludwig MS, Goodman M, Miller DL, et al.: Postoperative survival and the number of lymph nodes sampled during resection of node-negative non-small cell lung cancer. Chest 128 (3): 1545-50, 2005.[PUBMED Abstract]
- Webb WR, Gatsonis C, Zerhouni EA, et al.: CT and MR imaging in staging non-small cell bronchogenic carcinoma: report of the Radiologic Diagnostic Oncology Group. Radiology 178 (3): 705-13, 1991.[PUBMED Abstract]
- Toloza EM, Harpole L, McCrory DC: Noninvasive staging of non-small cell lung cancer: a review of the current evidence. Chest 123 (1 Suppl): 137S-146S, 2003.[PUBMED Abstract]
- Gould MK, Kuschner WG, Rydzak CE, et al.: Test performance of positron emission tomography and computed tomography for mediastinal staging in patients with non-small-cell lung cancer: a meta-analysis. Ann Intern Med 139 (11): 879-92, 2003.[PUBMED Abstract]
- Dwamena BA, Sonnad SS, Angobaldo JO, et al.: Metastases from non-small cell lung cancer: mediastinal staging in the 1990s--meta-analytic comparison of PET and CT. Radiology 213 (2): 530-6, 1999.[PUBMED Abstract]
- Ung YC, Maziak DE, Vanderveen JA, et al.: 18Fluorodeoxyglucose positron emission tomography in the diagnosis and staging of lung cancer: a systematic review. J Natl Cancer Inst 99 (23): 1753-67, 2007.[PUBMED Abstract]
- Dietlein M, Weber K, Gandjour A, et al.: Cost-effectiveness of FDG-PET for the management of potentially operable non-small cell lung cancer: priority for a PET-based strategy after nodal-negative CT results. Eur J Nucl Med 27 (11): 1598-609, 2000.[PUBMED Abstract]
- Scott WJ, Shepherd J, Gambhir SS: Cost-effectiveness of FDG-PET for staging non-small cell lung cancer: a decision analysis. Ann Thorac Surg 66 (6): 1876-83; discussion 1883-5, 1998.[PUBMED Abstract]
- Gambhir SS, Hoh CK, Phelps ME, et al.: Decision tree sensitivity analysis for cost-effectiveness of FDG-PET in the staging and management of non-small-cell lung carcinoma. J Nucl Med 37 (9): 1428-36, 1996.[PUBMED Abstract]
- van Tinteren H, Hoekstra OS, Smit EF, et al.: Effectiveness of positron emission tomography in the preoperative assessment of patients with suspected non-small-cell lung cancer: the PLUS multicentre randomised trial. Lancet 359 (9315): 1388-93, 2002.[PUBMED Abstract]
- Viney RC, Boyer MJ, King MT, et al.: Randomized controlled trial of the role of positron emission tomography in the management of stage I and II non-small-cell lung cancer. J Clin Oncol 22 (12): 2357-62, 2004.[PUBMED Abstract]
- Vansteenkiste JF, Stroobants SG, De Leyn PR, et al.: Lymph node staging in non-small-cell lung cancer with FDG-PET scan: a prospective study on 690 lymph node stations from 68 patients. J Clin Oncol 16 (6): 2142-9, 1998.[PUBMED Abstract]
- Roberts PF, Follette DM, von Haag D, et al.: Factors associated with false-positive staging of lung cancer by positron emission tomography. Ann Thorac Surg 70 (4): 1154-9; discussion 1159-60, 2000.[PUBMED Abstract]
- Liewald F, Grosse S, Storck M, et al.: How useful is positron emission tomography for lymphnode staging in non-small-cell lung cancer? Thorac Cardiovasc Surg 48 (2): 93-6, 2000.[PUBMED Abstract]
- Yokoi K, Kamiya N, Matsuguma H, et al.: Detection of brain metastasis in potentially operable non-small cell lung cancer: a comparison of CT and MRI. Chest 115 (3): 714-9, 1999.[PUBMED Abstract]
- Mountain CF: Revisions in the International System for Staging Lung Cancer. Chest 111 (6): 1710-7, 1997.[PUBMED Abstract]
- Lung. In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 431–56.[PUBMED Abstract]
- NSCLCに対する治療法選択肢の概要
-
非小細胞肺がん(NSCLC)においては、大部分の限局性のがんを除いて標準治療の結果は不良である。新たに非小細胞肺がんと診断されたすべての患者は、新しい治療法を評価するための試験の潜在的候補者である。
手術は、この疾患に対する治癒の可能性が高い治療法選択肢である。術後化学療法により、切除したNSCLC患者に付加的利益がもたらされる場合がある。化学療法と併用する放射線療法はごくわずかの患者に治癒をもたらし、ほとんどの患者に症状緩和をもたらしうる。予防的頭蓋照射は脳転移の発生を低下させうるが、生存利益の証拠はなく予防的頭蓋照射の生活の質への効果は不明である。[ 1 ][ 2 ]進行期疾患の患者では、化学療法または上皮成長因子受容体(EGFR)キナーゼ阻害薬が生存期間中央値のわずかな改善をもたらすが、全生存率は不良である。[ 3 ][ 4 ]
化学療法は進行したNSCLCの患者の疾患関連症状に短期改善をもたらす。いくつかの臨床試験で、化学療法の腫瘍関連症状および生活の質への影響を評価する試みが行われている。全体として、これらの研究は、化学療法が全生活の質に悪影響を及ぼすことなく腫瘍関連症状を制御できることを示唆している[ 5 ][ 6 ];しかしながら、化学療法の生活の質への影響については、さらなる研究を要する。一般に、パフォーマンスステータスが良好で医学的に健康な高齢患者は、治療により年齢が若い患者と同様な利益が得られる。
肺がんにおける遺伝子突然変異の同定を契機として、転移病変を有する患者サブセットの生存を改善する分子標的療法の開発が行われている。[ 7 ]特に、NSCLCのサブセットにおいて、EGFR、MAPK、およびPI3Kのシグナル伝達経路で生じた遺伝子異常は、薬物感受性および原発性または後天性のキナーゼ阻害薬への耐性の機序を規定する場合がある。EGFR突然変異は、EGFR阻害薬の奏効率および無増悪生存率の改善を強力に予測する。ALK遺伝子とEML4や他の遺伝子との融合は、非選別のNSCLCにおいて3~7%の幅で発生する転座産物を形成し、クリゾチニブなどの薬剤によるALKの薬理学的阻害に反応する。METがん遺伝子は、肝細胞増殖因子受容体をコード化する。この遺伝子の増幅は、EGFRチロシンキナーゼ阻害薬への二次耐性に関連している。ROS1遺伝子を巻き込んだ頻発性融合は、NSCLCの最大2%に観察され、クリゾチニブおよびエヌトレクチニブによる治療に反応を示す。NTRK遺伝子融合は、NSCLCの最大1%に発現する可能性があり、TRK阻害薬のラロトレクチニブおよびエヌトレクチニブによる治療が可能である。
NSCLCの各病期別に、標準治療法の選択肢を表7に示す。
表7.NSCLCに対する標準治療法の選択肢 病期( 標準治療法の選択肢 ALK = 未分化リンパ腫キナーゼ;BRAF = v-raf マウス肉腫ウイルスがん遺伝子ホモログB1;EGFR = 上皮成長因子受容体;MEK = MAPKキナーゼ1;NSCLC = 非小細胞肺がん;NTRK = 神経栄養性チロシン受容体キナーゼ;PD-L1 = プログラム細胞死リガンド1;TNM = T、腫瘍の大きさおよび隣接組織へのがんの拡がり;N、隣接リンパ節へのがんの拡がり;M、転移すなわち身体の別の部位へのがんの拡がり。 潜伏NSCLC 手術 0期NSCLC 手術 気管支内療法 IA期およびIB期NSCLC 手術 放射線療法 IIA期およびIIB期NSCLC 手術 補助化学療法 術前補助化学療法 放射線療法 IIIA期NSCLC 切除後または切除可能病変 手術 術前療法 補助療法 切除不能病変 放射線療法 化学放射線療法 上溝腫瘍 放射線療法単独 手術 化学放射線療法とその後の手術 胸壁に浸潤した腫瘍 手術 手術および放射線療法 放射線療法単独 化学療法と放射線療法の同時併用および/または手術 IIIB期およびIIIC期NSCLC 化学療法と放射線療法の順次施行または同時併用 同時化学放射線療法における放射線療法の線量増加 化学療法と放射線療法の同時併用前または後の追加の全身療法 放射線療法単独 新たに診断されたIV期、再燃および再発したNSCLC 細胞毒性併用化学療法 モノクローナル抗体を併用する併用化学療法 第一選択化学療法後の維持療法(プラチナ製剤をベースにした併用化学療法を4サイクル施行後に安定または反応を示している患者に対して) EGFRチロシンキナーゼ阻害薬 ALK阻害薬(ALK転座が認められる患者に対して) BRAF V600EおよびMEK阻害薬(BRAF V600E変異を有する患者に対して) ROS1阻害薬(ROS1再構成が認められる患者に対して) NTRK阻害薬(NTRK融合が認められる患者に対して) 化学療法を併用するまたは併用しない免疫チェックポイント阻害薬 局所療法および特別な考慮事項 進行性IV期、再燃および再発したNSCLC 化学療法 EGFRを標的にした治療 ALKを標的にしたTKI BRAF V600EおよびMEK阻害薬(BRAF V600E変異を有する患者に対して) ROS1を標的にした治療 NTRK阻害薬(NTRK融合が認められる患者に対して) 免疫療法 表7に示す標準治療法の選択肢に加え、以下の臨床評価段階にある治療法の選択肢が含まれる:
- 局所治療(手術)の併用。
- 領域治療(放射線療法)。
- 全身治療(化学療法、免疫療法、および標的薬物)。
- より効果的な全身療法の開発。
経過観察
化学療法、放射線療法、または化学放射線療法後のフッ素18-フルデオキシグルコースポジトロン放射断層撮影(18F-FDG PET)における腫瘍縮小は、病理学的完全奏効および良好な予後と相関することが数件の小規模シリーズで報告されている。[ 8 ][ 9 ][ 10 ][ 11 ][ 12 ][ 13 ][ 14 ][ 15 ]これらの研究で使用している評価タイミング、18F-FDG PETのパラメータ、および18F-FDG PETの反応を判定するカットポイントは異なっている。最大標準摂取率(SUV:standardized uptake value)の80%を超える低下は病理学的完全奏効を予測し、感度90%、特異度100%、正確度96%であった。[ 16 ]切除後の生存期間中央値は、腫瘍のSUV値が4未満の患者でより長かった(56ヵ月 vs 19ヵ月)。[ 15 ]放射線療法後に完全代謝反応を認めた患者は、生存期間中央値が31ヵ月 vs 11ヵ月であったことが報告された。[ 17 ]
18F-FDG PETは、導入療法に対する反応評価で、感度および特異度がコンピュータ断層撮影(CT)スキャンより高い可能性がある。画像検査の最適なタイミングはまだ確定していない;しかしながら、画像再検査を放射線療法後30日まで延期した場合、18F-FDG PETで達成される感度および特異度がより大きくなることを示唆した研究が1件ある。[ 16 ]
ルーチンの治療後PET-CTスキャンの役割は明確ではない。[ 18 ][証拠レベル:3iiA]
証拠(化学療法を併用するまたは併用しない放射線療法後の画像検査によるサーベイランス):
- American College of Radiology Imaging Network(ACRIN)およびRadiation Therapy Oncology Group(RTOG)共同グループ(ACRIN 6668/RTOG 0235[NCT00083083])により実施された1件のプロスペクティブ多施設試験では、III期疾患の患者173人を対象に標準治療法の化学療法と放射線療法の併用後の全生存(OS)を予測するため、治療後約14週間経過時(範囲、12~14週間)のPET-CTの役割が調査された。
- 主要エンドポイントは、SUVpeakの事前に規定されたバイナリカットオフ値であるSUVpeak 3.5とOSとの関係の測定であった。
- この研究により、3.5を超えるSUVpeakと比較して、OSと3.5以下のSUVpeakとの関連は実証されなかった(2年OS率の推定値51% vs 37%;P = 0.29)。
- 探索的解析により、OSと連続変数としてのSUVpeakのほか、SUVpeak 5.0および7.0のバイナリカットオフ値との関連が示された。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Lester JF, MacBeth FR, Coles B: Prophylactic cranial irradiation for preventing brain metastases in patients undergoing radical treatment for non-small-cell lung cancer: a Cochrane Review. Int J Radiat Oncol Biol Phys 63 (3): 690-4, 2005.[PUBMED Abstract]
- Pöttgen C, Eberhardt W, Grannass A, et al.: Prophylactic cranial irradiation in operable stage IIIA non small-cell lung cancer treated with neoadjuvant chemoradiotherapy: results from a German multicenter randomized trial. J Clin Oncol 25 (31): 4987-92, 2007.[PUBMED Abstract]
- Chemotherapy for non-small cell lung cancer. Non-small Cell Lung Cancer Collaborative Group. Cochrane Database Syst Rev (2): CD002139, 2000.[PUBMED Abstract]
- Chemotherapy in non-small cell lung cancer: a meta-analysis using updated data on individual patients from 52 randomised clinical trials. Non-small Cell Lung Cancer Collaborative Group. BMJ 311 (7010): 899-909, 1995.[PUBMED Abstract]
- Spiro SG, Rudd RM, Souhami RL, et al.: Chemotherapy versus supportive care in advanced non-small cell lung cancer: improved survival without detriment to quality of life. Thorax 59 (10): 828-36, 2004.[PUBMED Abstract]
- Clegg A, Scott DA, Hewitson P, et al.: Clinical and cost effectiveness of paclitaxel, docetaxel, gemcitabine, and vinorelbine in non-small cell lung cancer: a systematic review. Thorax 57 (1): 20-8, 2002.[PUBMED Abstract]
- Pao W, Girard N: New driver mutations in non-small-cell lung cancer. Lancet Oncol 12 (2): 175-80, 2011.[PUBMED Abstract]
- Curran WJ, Paulus R, Langer CJ, et al.: Sequential vs. concurrent chemoradiation for stage III non-small cell lung cancer: randomized phase III trial RTOG 9410. J Natl Cancer Inst 103 (19): 1452-60, 2011.[PUBMED Abstract]
- Fournel P, Robinet G, Thomas P, et al.: Randomized phase III trial of sequential chemoradiotherapy compared with concurrent chemoradiotherapy in locally advanced non-small-cell lung cancer: Groupe Lyon-Saint-Etienne d'Oncologie Thoracique-Groupe Français de Pneumo-Cancérologie NPC 95-01 Study. J Clin Oncol 23 (25): 5910-7, 2005.[PUBMED Abstract]
- Zatloukal P, Petruzelka L, Zemanova M, et al.: Concurrent versus sequential chemoradiotherapy with cisplatin and vinorelbine in locally advanced non-small cell lung cancer: a randomized study. Lung Cancer 46 (1): 87-98, 2004.[PUBMED Abstract]
- Rowell NP, O'rourke NP: Concurrent chemoradiotherapy in non-small cell lung cancer. Cochrane Database Syst Rev (4): CD002140, 2004.[PUBMED Abstract]
- Cerfolio RJ, Bryant AS, Winokur TS, et al.: Repeat FDG-PET after neoadjuvant therapy is a predictor of pathologic response in patients with non-small cell lung cancer. Ann Thorac Surg 78 (6): 1903-9; discussion 1909, 2004.[PUBMED Abstract]
- Pöttgen C, Levegrün S, Theegarten D, et al.: Value of 18F-fluoro-2-deoxy-D-glucose-positron emission tomography/computed tomography in non-small-cell lung cancer for prediction of pathologic response and times to relapse after neoadjuvant chemoradiotherapy. Clin Cancer Res 12 (1): 97-106, 2006.[PUBMED Abstract]
- Eschmann SM, Friedel G, Paulsen F, et al.: 18F-FDG PET for assessment of therapy response and preoperative re-evaluation after neoadjuvant radio-chemotherapy in stage III non-small cell lung cancer. Eur J Nucl Med Mol Imaging 34 (4): 463-71, 2007.[PUBMED Abstract]
- Hellwig D, Graeter TP, Ukena D, et al.: Value of F-18-fluorodeoxyglucose positron emission tomography after induction therapy of locally advanced bronchogenic carcinoma. J Thorac Cardiovasc Surg 128 (6): 892-9, 2004.[PUBMED Abstract]
- Cerfolio RJ, Bryant AS: When is it best to repeat a 2-fluoro-2-deoxy-D-glucose positron emission tomography/computed tomography scan on patients with non-small cell lung cancer who have received neoadjuvant chemoradiotherapy? Ann Thorac Surg 84 (4): 1092-7, 2007.[PUBMED Abstract]
- Mac Manus MP, Hicks RJ, Matthews JP, et al.: Positron emission tomography is superior to computed tomography scanning for response-assessment after radical radiotherapy or chemoradiotherapy in patients with non-small-cell lung cancer. J Clin Oncol 21 (7): 1285-92, 2003.[PUBMED Abstract]
- Machtay M, Duan F, Siegel BA, et al.: Prediction of survival by [18F]fluorodeoxyglucose positron emission tomography in patients with locally advanced non-small-cell lung cancer undergoing definitive chemoradiation therapy: results of the ACRIN 6668/RTOG 0235 trial. J Clin Oncol 31 (30): 3823-30, 2013.[PUBMED Abstract]
- 潜伏NSCLCの治療
-
潜伏肺がんでは、原発腫瘍の部位および性質を判定にするために、診断的評価として、綿密な経過観察(例えば、コンピュータ断層撮影スキャン)とともに、必要に応じて胸部X線および選択的気管支鏡検査を含めることが多い;このような形で発見される腫瘍は、一般に病期が初期で、手術により治癒可能である。
原発腫瘍発見後、腫瘍の病期を確定することも治療に含まれる。治療法は、同じ病期の他の非小細胞肺がん(NSCLC)患者に推奨されるものと同じである。
潜伏NSCLCに対する標準治療法の選択肢
潜伏NSCLCSに対する標準的治療選択肢には以下を含む:
- 手術。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
- 0期NSCLCの治療
-
0期の非小細胞肺がん(NSCLC)は、浸潤がんに進行する頻度が高い。[ 1 ][ 2 ][ 3 ]患者はサーベイランスのための気管支鏡検査を提案され、病変が発見されれば治癒が期待できる治療法が提案される。
0期NSCLCに対する標準治療法の選択肢
0期NSCLCに対する標準治療法の選択肢には以下のものがある:
手術
0期NSCLC患者は二次肺がんのリスクが高いことから、正常な肺組織を最大限に温存するために区域切除術または楔状切除術が用いられる。このような腫瘍は定義上非浸潤性であり、転移能力をもたないため、外科的切除により治癒可能である;しかしながら、こうした病変が同定される場合、しばしば中心に局在しており、肺葉切除が必要である。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Woolner LB, Fontana RS, Cortese DA, et al.: Roentgenographically occult lung cancer: pathologic findings and frequency of multicentricity during a 10-year period. Mayo Clin Proc 59 (7): 453-66, 1984.[PUBMED Abstract]
- Venmans BJ, van Boxem TJ, Smit EF, et al.: Outcome of bronchial carcinoma in situ. Chest 117 (6): 1572-6, 2000.[PUBMED Abstract]
- Jeremy George P, Banerjee AK, Read CA, et al.: Surveillance for the detection of early lung cancer in patients with bronchial dysplasia. Thorax 62 (1): 43-50, 2007.[PUBMED Abstract]
- Kennedy TC, McWilliams A, Edell E, et al.: Bronchial intraepithelial neoplasia/early central airways lung cancer: ACCP evidence-based clinical practice guidelines (2nd edition). Chest 132 (3 Suppl): 221S-233S, 2007.[PUBMED Abstract]
- Corti L, Toniolo L, Boso C, et al.: Long-term survival of patients treated with photodynamic therapy for carcinoma in situ and early non-small-cell lung carcinoma. Lasers Surg Med 39 (5): 394-402, 2007.[PUBMED Abstract]
- Deygas N, Froudarakis M, Ozenne G, et al.: Cryotherapy in early superficial bronchogenic carcinoma. Chest 120 (1): 26-31, 2001.[PUBMED Abstract]
- van Boxem TJ, Venmans BJ, Schramel FM, et al.: Radiographically occult lung cancer treated with fibreoptic bronchoscopic electrocautery: a pilot study of a simple and inexpensive technique. Eur Respir J 11 (1): 169-72, 1998.[PUBMED Abstract]
- van Boxem AJ, Westerga J, Venmans BJ, et al.: Photodynamic therapy, Nd-YAG laser and electrocautery for treating early-stage intraluminal cancer: which to choose? Lung Cancer 31 (1): 31-6, 2001.[PUBMED Abstract]
- IA期およびIB期NSCLCの治療
-
IA期およびIB期NSCLCに対する標準治療法の選択肢
IA期の非小細胞肺がん(NSCLC)およびIB期のNSCLCに対する標準治療法の選択肢には以下のものがある:
化学療法または放射線療法によって、I期NSCLCを完全切除された患者の治療成績が改善されることは、明らかにされていない。
手術
外科手術が、I期のNSCLC患者に対する治療法として選択される。肺葉切除術、あるいは区域、楔状、またはスリーブ切除術を必要に応じて実施してもよい。肺機能障害がある患者は、原発腫瘍の区域切除または楔状切除の候補者である。患者の全体的な医学的状態、特に肺予備能の慎重な術前評価が、外科手術の有益性を考える上で重要である。手術直後の死亡率は年齢と関係するが、肺葉切除術では3~5%の死亡率が予測される。[ 1 ]
証拠(手術):
- Lung Cancer Study Groupは、ランダム化研究(LCSG-821)を実施し、I期の肺がん患者を対象に肺葉切除術と限局的切除術を比較した。この研究の結果から以下が示された:[
2
]
- 肺葉切除による治療を受けた患者では、限局的切除による治療を受けた患者と比べ局所再発が減少した。
- 全生存(OS)に有意差は認められない。
- 同様の結果が解剖学的区域切除と肺葉切除とを比較した非ランダム化試験で報告されている。[
3
]
- 腫瘍が3cmを超える患者では、肺葉切除により生存利益が認められたが、腫瘍が3cm未満の患者では認められなかった。
- 局所領域での再発率は、原発腫瘍の大きさとは無関係に、肺葉切除後の方が有意に低かった。
- I期の患者を対象とした研究から以下が示された:[
4
]
- 楔状または区域切除による治療を受けた患者では、完全切除であったにもかかわらず、局所再発率が50%(すなわち、患者62人中31人が再発)であった。[ 4 ]
- Cochrane Collaborationにより、早期(I-IIIA期)肺がんに対して外科的介入を受けた計1,910人の患者に関する11件のランダム化試験がレビューされた。[
5
]3件の試験のプール解析では、以下が報告された:
- 切除可能なI期、II期、およびIIIA期のNSCLC患者では、切除および完全同側縦隔リンパ節郭清(CMLND)を受けた患者の方が、切除およびリンパ節サンプリングを受けた患者と比較して4年生存率が優れていた;ハザード比(HR)は0.78(95%信頼区間[CI]、0.65-0.93、P = 0.005)と推定された。[ 5 ][証拠レベル:1iiA]
- CMLND群では、どのようながん再発(局所または遠隔)でも有意な減少(相対リスク[RR]、0.79;95%CI、0.66-0.95;P = 0.01)が認められたが、これは遠隔再発数の減少(RR = 0.78;95%CI、0.61-1.00;P = 0.05)が主な理由と考えられる。
- 手術死亡率における差は認められなかった。
- CMLNDに割り付けられた患者では、5日間を超えて継続するエアリークが有意に多く認められた(RR、2.94;95%CI、1.01-8.54;P = 0.05)。
- CMLND vs リンパ節サンプリングは、大規模なランダム化第III相試験(ACOSOG-Z0030[NCT00003831])で評価された。[
6
][
7
]
I期、II期、またはIIIA期のNSCLC患者では、CMLNDと併用した肺がん切除は、縦隔リンパ節の系統的サンプリングと併用した肺がん切除と比べ、生存の改善と関連していないことが、現時点での証拠から示唆されている。[ 7 ][証拠レベル:1iiA]
証拠の限界(手術):
局所および局所領域NSCLCを有する患者に対する手術の効力に関する結論は、現在までに研究されている参加者数が少数であること、および試験の方法論的な潜在的弱点により限定される。
補助療法
外科的治療を受けた多くの患者が、後に所属リンパ節転移または遠隔転移を来す。[ 8 ]このような患者は、化学療法または手術後の放射線療法による術後療法を評価する臨床試験への参加が勧められる。現在、化学療法または放射線療法によって、I期NSCLCを完全切除された患者の治療成績が改善されることは明らかにされていない。
補助放射線療法
術後(補助)放射線療法(PORT)の価値が評価されたが、I期NSCLCを完全切除された患者の治療成績を改善することは明らかにされていない。[ 9 ]
証拠(補助放射線療法):
- メタアナリシスでは、10件のランダム化比較試験の結果および2,232人の被験者を基に、以下が報告された:[
9
]
- PORTを受けた患者では、手術単独と比べ、死亡リスクが相対的に18%増加した(HR、1.18;P = 0.002)。これは2年間で6%の絶対的有害性(95%CI、2-9)に相当し、OSを58%から52%に低下させている。この有害な結果は、I/II期でN0~N1の患者で最も著明であるが、III期でN2の患者では有害作用の明確な証拠は認められないことが、探索的なサブグループ解析により示唆された。
- 局所(HR、1.13;P = 0.02)、遠隔(HR、1.14;P = 0.02)、および全体(HR、1.10;P = 0.06)の無再発生存の結果から、同様にPORTの有害性が示された。[ 9 ][証拠レベル:1iiA]
これらの結果が放射線照射における技術的進歩、標的体積のより的確な設定および照射ポータルにおける心臓容積の制限によって改善できるかどうかを明らかにするために、さらなる分析が必要である。
補助的近接照射療法
局所制御を改善するためI期NSCLCに対して縮小手術を受けた患者における縫合線に実施される術中の(補助的)近接照射療法の価値が評価されている;治療成績を改善することは明らかにされていない。
証拠(補助的近接照射療法):
補助化学療法
メタアナリシスに基づくと、I期NSCLCで完全切除した患者に対する術後化学療法は、臨床試験の枠外では推奨されない。[ 11 ][ 12 ][証拠レベル:1iiA].
証拠(I期NSCLCに対する補助化学療法):
- NSCLCを完全切除した患者に対するシスプラチンをベースとした化学療法について、1995年以降に実施された5件の最大規模の試験(患者4,584人)から、個々の患者の転帰に関するデータが収集され、メタアナリシスで併合された。[
13
]
- 追跡期間中央値5.2年で、全HR死亡は0.89(95%CI、0.82-0.96;P = 0.005)で、これは化学療法による5年絶対的有益性5.4%に相当した。
- 有益性は病期によってさまざまであった(傾向検定、P = 0.04;IA期に対するHR、1.40;95%CI、0.95-2.06;IB期に対するHR、0.93;95%CI、0.78-1.10;II期に対するHR、0.83;95%CI、0.73-0.95;およびIII期に対するHR、0.83;95%CI、0.72-0.94)。
- ビノレルビン(HR、0.80;95%CI、0.70-0.91)、エトポシドまたはビンカアルカロイド(HR、0.92;95%CI、0.80-1.07)、あるいは他の薬物(HR、0.97;95%CI、0.84-1.13)などの関連薬物で、化学療法の効果に有意差は認められなかった(交互作用検定、P = 0.11)。
- ビノレルビンで認められた一見より大きな有益性は、ビノレルビンとシスプラチンの併用では一般により高用量のシスプラチンの投与が必要であるため、慎重に解釈すべきである。化学療法の効果は、パフォーマンスステータスが良好な患者ほど高かった。
- 化学療法の効果と以下のいずれかの項目との相互作用は認められていない:
- 性別。
- 年齢。
- 組織像。
- 術式。
- 計画されている放射線療法。
- 計画されているシスプラチンの総用量。
- I期、II期、およびIIIA期のNSCLC患者を対象に、術後化学療法の使用を評価しているランダム化比較試験およびメタアナリシスが他にいくつかある。[ 13 ][ 14 ][ 15 ][ 16 ][ 17 ][ 18 ][ 19 ]
II期またはIIIA期のNSCLC患者では術後化学療法が有効であるという証拠は十分にあるが、IB期のNSCLC患者における有用性については、ほとんど明らかになっていない。
証拠(IB期NSCLCに対する補助化学療法):
- Cancer and Leukemia Group B研究(CALGB-9633[NCT00002852])では、IB期(すなわち、病理学的にT2、N0)のNSCLCで切除した患者344人を対象に、OSについてカルボプラチンとパクリタキセルの補助療法 vs 観察の結果が検討された。切除後4~8週間以内に、患者を術後化学療法または観察のいずれかにランダムに割り付けた。[
20
]
- 追跡期間中央値74ヵ月時点で、生存に有意差はみられなかった(HR、0.83;CI、0.64-1.08;P = 0.12)。
- グレード3~4の好中球減少が主な毒性作用であった;治療関連死はみられなかった。
- 探索的な事後解析により、腫瘍径が4cm以上の患者では術後化学療法が良好なことを示す有意な生存差が実証された(HR、0.69;CI、0.48-0.99;P = 0.043)。
観察された生存の差の大きさからすると、CALGB-9633は、わずかではあるが臨床的に意義のある生存の改善を検出するには検出力が不足していた可能性がある。また、カルボプラチン vs シスプラチンの併用が結果に影響した可能性がある。現時点では、術後化学療法によりIB期のNSCLC患者の生存が改善するという信頼できる証拠は得られていない。[ 20 ][証拠レベル:1iiA]
放射線療法
腫瘍が切除可能と考えられるが、医学的に手術禁忌の患者、またはI期で手術不能でも、残された肺機能が十分ある患者では、根治を目的とした放射線療法に適格な場合がある。
従来の放射線療法
歴史的に、従来の初回放射線療法では、超高圧放射線装置を用い、既知の腫瘍体積の中央水平面に通常分割(1.8~2.0Gy/日)で約60~70Gyが照射されていた。
予後:
従来の放射線療法に関する最大規模のレトロスペクティブ・シリーズでは、手術不能な患者の根治的放射線療法後の5年生存率はそれぞれ10~30%であった。[ 21 ][ 22 ][ 23 ]数件のシリーズで、T1、N0の腫瘍を有する患者でより良好な治療成績が得られ、このサブグループでの5年生存率は30~60%であったことが実証された。[ 21 ][ 22 ][ 24 ]しかしながら、60~65Gyの線量を照射する従来の放射線療法で治療される患者において、局所単独の失敗は50%もの患者で発生する。[ 25 ][ 26 ]
証拠(従来の放射線療法):
- 切除可能な病変が4cm未満であるが、医学的に手術できない場合、または手術を拒否した場合の70歳を過ぎた患者を対象とした単一施設の報告では、以下が報告された:[
24
]
- 治癒を目的とした放射線療法後の5年生存率は、治癒を目的として切除した同年齢層患者の歴史的対照群と同等であった。
- 対応対照を用いた小規模のケースシリーズでは、以下が報告された:[
4
]
- 気管支内近接照射療法を追加することで、外照射療法(EBRT)と比較して局所的な病勢コントロールが改善した。[ 4 ][証拠レベル:3iiiDiii]
標準の外科的切除では、共存症状に伴って周術期リスクが許容できないほど高くなるため、適格ではない患者がかなり多い。このような患者に対しては、経過観察および放射線療法を検討する場合がある。[ 27 ][ 28 ][ 29 ]非ランダム化観察研究で、切除術、放射線療法、および経過観察に伴う治療成績を比較し、経過観察のみを受けた患者で生存期間が短く、死亡率が高かったことが実証されている。[ 27 ][ 30 ]
放射線技術の改善には、腫瘍の動きを明らかにする計画立案のための技術、より原体的に照射する計画立案のための技術(例、3次元原体照射法および強度変調放射線療法)、および治療中の画像によるガイドなどがある。外照射療法を実施する最新のアプローチには、少分割放射線療法および体幹部定位放射線治療(SBRT)がある。しかしながら、どちらのアプローチによる転帰が優れているかを判定するには、比較試験による信頼できるデータが限られている。[ 28 ][ 29 ]
少分割放射線療法
少分割放射線療法では、従来の分割放射線療法と比較して短い期間でわずかに高い1日当たりの照射線量(例、2.4~4.0Gy)の放射線療法が実施される。複数のプロスペクティブ第I/II相試験では、3~4週間にわたって1日当たり2.4~4.0Gyに分割して60~70Gyの線量を照射する少分割放射線療法により中等度から重度の毒性作用の発生低下、50~60%の2年OS率、および80~90%の2年腫瘍局所制御率が得られたことが実証されている。[ 31 ][ 32 ][ 33 ][証拠レベル:3iiiA]
体幹部定位放射線治療(SBRT)
SBRTでは、1~2週間にわたってきわめて少分割のコース(例、1~5回の治療)で高精度な原体照射による高線量の放射線療法を実施する。一般的に用いられるレジメンには18Gy × 3、12~12.5Gy × 4、および10~12Gy × 5があり、歴史的な従来の放射線療法レジメンと比較してかなり高い生物学的効果線量を送達する。
複数のプロスペクティブ第I/II相試験および施設のシリーズでは、SBRTにより、肺毒性の発生低下(有症状の放射性肺炎のリスクが10%未満)、50~60%の2年OS率、および90~95%の2年腫瘍御率が得られることが実証されている。[ 34 ][ 35 ][ 36 ][ 37 ][ 38 ][ 39 ][ 40 ][証拠レベル:3iiiA]
証拠(SBRT):
- インディアナ大学の初期の第I/II相試験により、T1腫瘍に対する3分割SBRTの最大耐容線量が18Gy × 3であると確認され、このレジメンにより55%の2年OS率および95%の2年局所腫瘍制御率が得られた。
- 中心性腫瘍(気管から葉気管支レベルまで気管気管支樹の2cm以内と定義)を有する患者で観察されたグレード5の毒性作用の発生率は受け入れられないほど高かった(8.6%)。[ 35 ]
- その後の多施設試験(RTOG-0236[NCT00087438])で、末梢型T1~T2腫瘍のみを有する患者55人において18Gy × 3のレジメンが検討され、56%の3年OS率および98%の3年原発腫瘍制御率が実証された。
- 中等度から重度の毒性作用の発生率は低く、グレード3の毒性作用は患者の24%、グレード4の毒性作用は患者の4%、およびグレード5の毒性作用は認められず、グレード3の放射性肺炎の発生率は4%であった。[ 39 ]
- VU University Medical Center Amsterdamにより報告された最大規模のシリーズでは、T1~T2腫瘍を有する患者676人がリスク調整アプローチ(重要臓器への腫瘍の近接度に基づいて個別に調整された分割レジメン)を用いて3分割、5分割、および8分割のSBRTで治療された。
- 追跡期間中央値32.9ヵ月で、OS中央値は40.7ヵ月、2年局所腫瘍制御率は95%であった。[ 40 ]
- インディアナ大学の第II相研究のデータによれば中心性の位置に腫瘍がみられる場合に3分割SBRTは禁忌であるが、563個の中心性腫瘍を有する315人の患者について発表された報告のその後の系統的レビューにより、SBRTをより長期にわたって実施するレジメン(例、4~10分割)でグレード5のイベントのリスクは1~5%であったものを含めて、重度の毒性作用の発生率ははるかに低いことが実証された。[ 41 ]中心性腫瘍に対する5分割のSBRTレジメンについて最大耐容線量を確認するため、1件の多施設第I/II相試験(RTOG-0813[NCT00750269])が進行中である。
最適な放射線療法のレジメンを明らかにするため、従来の放射線療法 vs SBRT(NCT01014130)、および少分割放射線療法 vs SBRT(LUSTRE[NCT01968941])のランダム化試験が進行中であるが、医学的に切除不能なI期NSCLCの患者に対しては、体幹部定位放射線治療が広く採用されている。
臨床評価段階にある治療法の選択肢
臨床評価段階にある治療法の選択肢には以下のものがある:
- 術後化学予防(例えば、Eastern Cooperative Oncology Group[ECOG]のECOG-5597[NCT00008385]試験で証明されたような)の臨床試験。
- T1、N0、M0腫瘍を有する厳選した患者に対する光線力学療法を含む気管支内療法。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Ginsberg RJ, Hill LD, Eagan RT, et al.: Modern thirty-day operative mortality for surgical resections in lung cancer. J Thorac Cardiovasc Surg 86 (5): 654-8, 1983.[PUBMED Abstract]
- Ginsberg RJ, Rubinstein LV: Randomized trial of lobectomy versus limited resection for T1 N0 non-small cell lung cancer. Lung Cancer Study Group. Ann Thorac Surg 60 (3): 615-22; discussion 622-3, 1995.[PUBMED Abstract]
- Warren WH, Faber LP: Segmentectomy versus lobectomy in patients with stage I pulmonary carcinoma. Five-year survival and patterns of intrathoracic recurrence. J Thorac Cardiovasc Surg 107 (4): 1087-93; discussion 1093-4, 1994.[PUBMED Abstract]
- Mantz CA, Dosoretz DE, Rubenstein JH, et al.: Endobronchial brachytherapy and optimization of local disease control in medically inoperable non-small cell lung carcinoma: a matched-pair analysis. Brachytherapy 3 (4): 183-90, 2004.[PUBMED Abstract]
- Manser R, Wright G, Hart D, et al.: Surgery for early stage non-small cell lung cancer. Cochrane Database Syst Rev (1): CD004699, 2005.[PUBMED Abstract]
- Allen MS, Darling GE, Pechet TT, et al.: Morbidity and mortality of major pulmonary resections in patients with early-stage lung cancer: initial results of the randomized, prospective ACOSOG Z0030 trial. Ann Thorac Surg 81 (3): 1013-9; discussion 1019-20, 2006.[PUBMED Abstract]
- Darling GE, Allen MS, Decker PA, et al.: Randomized trial of mediastinal lymph node sampling versus complete lymphadenectomy during pulmonary resection in the patient with N0 or N1 (less than hilar) non-small cell carcinoma: results of the American College of Surgery Oncology Group Z0030 Trial. J Thorac Cardiovasc Surg 141 (3): 662-70, 2011.[PUBMED Abstract]
- Martini N, Bains MS, Burt ME, et al.: Incidence of local recurrence and second primary tumors in resected stage I lung cancer. J Thorac Cardiovasc Surg 109 (1): 120-9, 1995.[PUBMED Abstract]
- PORT Meta-analysis Trialists Group: Postoperative radiotherapy for non-small cell lung cancer. Cochrane Database Syst Rev (2): CD002142, 2005.[PUBMED Abstract]
- Fernando HC, Landreneau RJ, Mandrekar SJ, et al.: Impact of brachytherapy on local recurrence rates after sublobar resection: results from ACOSOG Z4032 (Alliance), a phase III randomized trial for high-risk operable non-small-cell lung cancer. J Clin Oncol 32 (23): 2456-62, 2014.[PUBMED Abstract]
- Deygas N, Froudarakis M, Ozenne G, et al.: Cryotherapy in early superficial bronchogenic carcinoma. Chest 120 (1): 26-31, 2001.[PUBMED Abstract]
- van Boxem TJ, Venmans BJ, Schramel FM, et al.: Radiographically occult lung cancer treated with fibreoptic bronchoscopic electrocautery: a pilot study of a simple and inexpensive technique. Eur Respir J 11 (1): 169-72, 1998.[PUBMED Abstract]
- Pignon JP, Tribodet H, Scagliotti GV, et al.: Lung adjuvant cisplatin evaluation: a pooled analysis by the LACE Collaborative Group. J Clin Oncol 26 (21): 3552-9, 2008.[PUBMED Abstract]
- Winton T, Livingston R, Johnson D, et al.: Vinorelbine plus cisplatin vs. observation in resected non-small-cell lung cancer. N Engl J Med 352 (25): 2589-97, 2005.[PUBMED Abstract]
- Arriagada R, Bergman B, Dunant A, et al.: Cisplatin-based adjuvant chemotherapy in patients with completely resected non-small-cell lung cancer. N Engl J Med 350 (4): 351-60, 2004.[PUBMED Abstract]
- Scagliotti GV, Fossati R, Torri V, et al.: Randomized study of adjuvant chemotherapy for completely resected stage I, II, or IIIA non-small-cell Lung cancer. J Natl Cancer Inst 95 (19): 1453-61, 2003.[PUBMED Abstract]
- Hotta K, Matsuo K, Ueoka H, et al.: Role of adjuvant chemotherapy in patients with resected non-small-cell lung cancer: reappraisal with a meta-analysis of randomized controlled trials. J Clin Oncol 22 (19): 3860-7, 2004.[PUBMED Abstract]
- Edell ES, Cortese DA: Photodynamic therapy in the management of early superficial squamous cell carcinoma as an alternative to surgical resection. Chest 102 (5): 1319-22, 1992.[PUBMED Abstract]
- Corti L, Toniolo L, Boso C, et al.: Long-term survival of patients treated with photodynamic therapy for carcinoma in situ and early non-small-cell lung carcinoma. Lasers Surg Med 39 (5): 394-402, 2007.[PUBMED Abstract]
- Strauss GM, Herndon JE, Maddaus MA, et al.: Adjuvant paclitaxel plus carboplatin compared with observation in stage IB non-small-cell lung cancer: CALGB 9633 with the Cancer and Leukemia Group B, Radiation Therapy Oncology Group, and North Central Cancer Treatment Group Study Groups. J Clin Oncol 26 (31): 5043-51, 2008.[PUBMED Abstract]
- Dosoretz DE, Katin MJ, Blitzer PH, et al.: Radiation therapy in the management of medically inoperable carcinoma of the lung: results and implications for future treatment strategies. Int J Radiat Oncol Biol Phys 24 (1): 3-9, 1992.[PUBMED Abstract]
- Gauden S, Ramsay J, Tripcony L: The curative treatment by radiotherapy alone of stage I non-small cell carcinoma of the lung. Chest 108 (5): 1278-82, 1995.[PUBMED Abstract]
- Sibley GS, Jamieson TA, Marks LB, et al.: Radiotherapy alone for medically inoperable stage I non-small-cell lung cancer: the Duke experience. Int J Radiat Oncol Biol Phys 40 (1): 149-54, 1998.[PUBMED Abstract]
- Noordijk EM, vd Poest Clement E, Hermans J, et al.: Radiotherapy as an alternative to surgery in elderly patients with resectable lung cancer. Radiother Oncol 13 (2): 83-9, 1988.[PUBMED Abstract]
- Dosoretz DE, Galmarini D, Rubenstein JH, et al.: Local control in medically inoperable lung cancer: an analysis of its importance in outcome and factors determining the probability of tumor eradication. Int J Radiat Oncol Biol Phys 27 (3): 507-16, 1993.[PUBMED Abstract]
- Kaskowitz L, Graham MV, Emami B, et al.: Radiation therapy alone for stage I non-small cell lung cancer. Int J Radiat Oncol Biol Phys 27 (3): 517-23, 1993.[PUBMED Abstract]
- McGarry RC, Song G, des Rosiers P, et al.: Observation-only management of early stage, medically inoperable lung cancer: poor outcome. Chest 121 (4): 1155-8, 2002.[PUBMED Abstract]
- Lanni TB, Grills IS, Kestin LL, et al.: Stereotactic radiotherapy reduces treatment cost while improving overall survival and local control over standard fractionated radiation therapy for medically inoperable non-small-cell lung cancer. Am J Clin Oncol 34 (5): 494-8, 2011.[PUBMED Abstract]
- Grutters JP, Kessels AG, Pijls-Johannesma M, et al.: Comparison of the effectiveness of radiotherapy with photons, protons and carbon-ions for non-small cell lung cancer: a meta-analysis. Radiother Oncol 95 (1): 32-40, 2010.[PUBMED Abstract]
- Raz DJ, Zell JA, Ou SH, et al.: Natural history of stage I non-small cell lung cancer: implications for early detection. Chest 132 (1): 193-9, 2007.[PUBMED Abstract]
- Bradley J, Graham MV, Winter K, et al.: Toxicity and outcome results of RTOG 9311: a phase I-II dose-escalation study using three-dimensional conformal radiotherapy in patients with inoperable non-small-cell lung carcinoma. Int J Radiat Oncol Biol Phys 61 (2): 318-28, 2005.[PUBMED Abstract]
- Bogart JA, Hodgson L, Seagren SL, et al.: Phase I study of accelerated conformal radiotherapy for stage I non-small-cell lung cancer in patients with pulmonary dysfunction: CALGB 39904. J Clin Oncol 28 (2): 202-6, 2010.[PUBMED Abstract]
- Cheung P, Faria S, Ahmed S, et al.: Phase II study of accelerated hypofractionated three-dimensional conformal radiotherapy for stage T1-3 N0 M0 non-small cell lung cancer: NCIC CTG BR.25. J Natl Cancer Inst 106 (8): , 2014.[PUBMED Abstract]
- Timmerman R, Papiez L, McGarry R, et al.: Extracranial stereotactic radioablation: results of a phase I study in medically inoperable stage I non-small cell lung cancer. Chest 124 (5): 1946-55, 2003.[PUBMED Abstract]
- Timmerman R, McGarry R, Yiannoutsos C, et al.: Excessive toxicity when treating central tumors in a phase II study of stereotactic body radiation therapy for medically inoperable early-stage lung cancer. J Clin Oncol 24 (30): 4833-9, 2006.[PUBMED Abstract]
- Lagerwaard FJ, Haasbeek CJ, Smit EF, et al.: Outcomes of risk-adapted fractionated stereotactic radiotherapy for stage I non-small-cell lung cancer. Int J Radiat Oncol Biol Phys 70 (3): 685-92, 2008.[PUBMED Abstract]
- Baumann P, Nyman J, Hoyer M, et al.: Outcome in a prospective phase II trial of medically inoperable stage I non-small-cell lung cancer patients treated with stereotactic body radiotherapy. J Clin Oncol 27 (20): 3290-6, 2009.[PUBMED Abstract]
- Fakiris AJ, McGarry RC, Yiannoutsos CT, et al.: Stereotactic body radiation therapy for early-stage non-small-cell lung carcinoma: four-year results of a prospective phase II study. Int J Radiat Oncol Biol Phys 75 (3): 677-82, 2009.[PUBMED Abstract]
- Timmerman R, Paulus R, Galvin J, et al.: Stereotactic body radiation therapy for inoperable early stage lung cancer. JAMA 303 (11): 1070-6, 2010.[PUBMED Abstract]
- Senthi S, Lagerwaard FJ, Haasbeek CJ, et al.: Patterns of disease recurrence after stereotactic ablative radiotherapy for early stage non-small-cell lung cancer: a retrospective analysis. Lancet Oncol 13 (8): 802-9, 2012.[PUBMED Abstract]
- Senthi S, Haasbeek CJ, Slotman BJ, et al.: Outcomes of stereotactic ablative radiotherapy for central lung tumours: a systematic review. Radiother Oncol 106 (3): 276-82, 2013.[PUBMED Abstract]
- Lung Cancer Study Groupは、ランダム化研究(LCSG-821)を実施し、I期の肺がん患者を対象に肺葉切除術と限局的切除術を比較した。この研究の結果から以下が示された:[
2
]
- IIA期およびIIB期NSCLCの治療
-
IIA期およびIIB期NSCLCに対する標準治療法の選択肢
IIA期の非小細胞肺がん(NSCLC)およびIIB期のNSCLCに対する標準治療法の選択肢には以下のものがある:
補助放射線療法によってII期NSCLC患者の治療成績が改善されることは、明らかにされていない。
手術
II期のNSCLC患者には、外科手術が治療法として選択される。肺葉切除術、肺全摘術、あるいは区域、楔状、またはスリーブ切除術を必要に応じて実施してもよい。患者の全体的な医学的状態、特に肺予備能の慎重な術前評価が、外科手術の有益性を考える上で重要である。手術直後の加齢に関係した死亡率の相違はあるが、肺全摘術では5~8%、肺葉切除術では3~5%の死亡率が予測される。
証拠(手術):
- Cochrane Collaborationにより、早期(I-IIIA期)肺がんに対して外科的介入を受けた計1,910人の患者に関する11件のランダム化試験がレビューされた。[
1
]3件の試験のプール解析では、以下が報告された:
- 切除可能なI期、II期、およびIIIA期のNSCLC患者では、切除および完全同側縦隔リンパ節郭清(CMLND)を受けた患者の方が、切除およびリンパ節サンプリングを受けた患者と比較して4年生存率が優れていた;ハザード比(HR)は0.78(95%信頼区間[CI]、0.65-0.93;P = 0.005)と推定された。[ 1 ][証拠レベル:1iiA]
- CMLND群では、どのようながん再発(局所または遠隔)でも有意な減少(相対リスク[RR]、0.79;95%CI、0.66-0.95;P = 0.01)が認められたが、遠隔再発数の減少(RR、0.78;95%CI、0.61-1.00;P = 0.05)が主な理由と考えられる。
- 手術死亡率における差は認められなかった。
- CMLNDに割り付けられた患者では、5日間を超えて継続するエアリークが有意に多く認められた(RR、2.94;95%CI、1.01-8.54;P = 0.05)。
- CMLND vs リンパ節サンプリングは、大規模なランダム化第III相試験(ACOSOG-Z0030[NCT00003831])で評価された。[
2
]
I期、II期、またはIIIA期のNSCLC患者では、CMLNDと併用した肺がん切除は、縦隔リンパ節の系統的サンプリングと併用した肺がん切除と比べ、生存の改善と関連していないことが、現時点での証拠から示唆されている。[ 3 ][証拠レベル:1iiA]
証拠の限界(手術):
局所および局所領域NSCLCを有する患者に対する手術の効力に関する結論は、現在までに研究されている参加者数が少数であること、および試験の方法論的な潜在的弱点により限定される。
補助化学療法
術後のシスプラチン併用化学療法により、II期の切除したNSCLC患者に有意な生存的利益がもたらされることが、圧倒的多数の証拠から示される。術前化学療法もまた、生存利益をもたらすであろう。切除可能なNSCLC患者における手術および化学療法の最適な順序、ならびに術後放射線療法の有益性とリスクについては、まだ確定していない。
手術後、多くの患者が、所属リンパ節転移または遠隔転移を来す。[ 4 ]I期、II期、およびIIIA期NSCLC患者に対する術後化学療法の使用を評価しているランダム化比較試験およびメタアナリシスがいくつかある。[ 5 ][ 6 ][ 7 ][ 8 ][ 9 ][ 10 ][ 11 ]
証拠(補助化学療法):
- NSCLCを完全切除した患者に対するシスプラチンをベースとした化学療法について、1995年以降に実施された5件の最大規模の試験(患者4,584人)から、個々の患者の転帰に関するデータが収集され、メタアナリシスで併合された。[
7
]
- 追跡期間中央値5.2年の時点で、全HR死亡は0.89(95%CI、0.82-0.96;P = 0.005)で、これは化学療法による5年絶対的有益性5.4%に相当した。
- 有益性は病期によってさまざまであった(傾向検定、P = 0.04;IA期に対するHR、1.40;95%CI、0.95-2.06;IB期に対するHR、0.93;95%CI、0.78-1.10;II期に対するHR、0.83;95%CI、0.73-0.95;およびIII期に対するHR、0.83;95%CI、0.72-0.94)。
- ビノレルビン(HR、0.80;95%CI、0.70-0.91)、エトポシドまたはビンカアルカロイド(HR、0.92;95%CI、0.80-1.07)、あるいは他の薬物(HR、0.97;95%CI、0.84-1.13)などの関連薬物で、化学療法の効果に有意差は認められなかった(交互作用検定、P = 0.11)。
- シスプラチンとビノレルビンの2剤併用により認められた生存に対する効果が他のレジメンと比較して大きかったことは、ビノレルビンによる治療を受けた患者では投与したシスプラチンの総用量が有意に高かったため、慎重に解釈すべきである。
- 術後のシスプラチンをベースにしたビノレルビンとの併用化学療法の実施は、メタアナリシス[
7
]および個々の研究[
5
][
12
]によって裏付けられている。
- Lung Adjuvant Cisplatin Evaluation(LACE)プール解析(併合HR、0.83;95%CI、0.73-0.95)、Adjuvant Navelbine International Trialist Association(ANITA)試験(HR、0.71;95%CI、0.49-1.03)、およびNational Cancer Institute of Canada Clinical Trials Group JBR.10試験(HR、0.59;95%CI、0.42-0.85)で、試験集団およびII期の患者のOSが優れていることが報告された。
- 化学療法の効果は、パフォーマンスステータス(PS)が良好な患者ほど高かった。
- 化学療法の効果と以下のいずれかの項目との相互作用は認められていない:
- 性別。
- 年齢。
- 組織像。
- 術式。
- 計画されている放射線療法。
- 計画されているシスプラチンの総用量。
- 術後のシスプラチンとビノレルビンを対象とした第III相試験のレトロスペクティブ解析では、65歳を超える患者が治療により利益を得られることが明らかになった。[
13
]
- 化学療法は高齢患者のOSを有意に延長した(HR、0.61;95%CI、0.38-0.98;P = 0.04)。
- 高齢患者が受けた治療は少ないが、毒性作用、入院、または年齢層別の治療関連死に有意差は認められなかった。[ 13 ]
- I期、II期、およびIIIA期のNSCLC患者を対象に、術後化学療法の使用を評価しているランダム化比較試験およびメタアナリシスが他にいくつかある。[ 5 ][ 6 ][ 7 ][ 8 ][ 9 ][ 10 ][ 11 ]
これらのデータに基づくと、II期の肺がんで完全切除した患者では、術後のシスプラチンをベースとした化学療法により利益が得られる可能性がある。[ 13 ][証拠レベル:1iiA]
術前補助化学療法
手術前の化学療法の役割が臨床試験で検証された。術前化学療法の提唱されている有益性は以下の通りである:
- 外科的切除を容易にしうる腫瘍サイズの減少。
- 微小転移の早期根絶。
- より良好な耐容性。
しかしながら、術前化学療法は治癒が期待できる手術を遅延させうる。
証拠(術前補助化学療法):
- 988人の患者を含み、手術単独に対して術前化学療法の手術への追加を評価した7件のランダム化比較試験を対象にした系統的レビューおよびメタアナリシスがCochrane Collaborationにより報告された。これらの試験では、I期、II期、およびIIIA期のNSCLC患者が評価された。[
14
]
- 術前化学療法により、すべての病期にわたる5年生存率で6%という絶対的有益性(14%から20%)がもたらされた(HR、0.82;95%CI、0.69-0.97;P = 0.022)。[ 14 ][証拠レベル:1iiA]
- この解析では、特定のタイプの患者が術前化学療法によってどの程度の利益を得るかといった問題は扱うことができなかった。
- 現時点で報告されている最大規模の試験では、519人の患者を、手術単独群、または3サイクルのプラチナ製剤をベースにした化学療法後に手術を施行する群のいずれかにランダムに割り付けた。臨床病期は、ほとんどの患者(61%)がI期で;31%がII期、および7%がIII期であった。[
15
]
- 生存的優位性は認められなかった。[ 15 ]
- 術後合併症は集団間でほぼ同じであり、生活の質の障害は観察されなかった。
- OSに関して有益性の証拠は認められなかった(HR、1.02;95%CI、0.80-1.31;P = 0.86)。
- 現時点での結果を追加した最新の系統的レビューでは、術前(ネオアジュバント)化学療法の追加による12%の相対的生存利益(患者1,507人;HR、0.88、95%CI、0.76-1.01、P = 0.07)が示唆され、これは5年生存率の絶対差で5%の改善と同等である。
補助放射線療法
術後(補助)放射線療法(PORT)の意義が評価されている。[ 16 ]
証拠(補助放射線療法):
- メタアナリシスでは、10件のランダム化比較試験の結果および2,232人の被験者を基に、以下が報告された:[
16
]
- PORTを受けた患者では、手術単独と比べ、死亡リスクが相対的に18%増加した(HR、1.18;P = 0.002)。これは2年間で6%の絶対的有害性(95%CI、2%-9%)に相当し、OSを58%から52%に低下させている。この有害な影響は、I/II期でN0~N1の患者で最も著明であるが、III期でN2の患者では有害作用の明確な証拠は認められないことが、探索的なサブグループ解析により示唆された。
- 局所(HR、1.13;P = 0.02)、遠隔(HR、1.14;P = 0.02)、および全体(HR、1.10;P = 0.06)の無再発生存の結果から、同様にPORTの有害性が示された。[ ][証拠レベル:1iiA]
これらの結果が放射線照射における技術的進歩、標的体積のより的確な設定および照射ポータルにおける心臓容積の制限によって改善できるかどうかを明らかにするために、さらなる分析が必要である。
放射線療法
腫瘍が切除可能と考えられるが、医学的に手術禁忌の患者、またはII期で手術不能でも残された肺機能が十分ある患者では、根治を目的とした放射線療法が勧められる。[ 17 ]初回放射線療法では、超高圧放射線装置により通常分割を用いて、既知の腫瘍容積の中央水平面に約60Gyを照射することが多い。原発腫瘍のコーンダウン(狭くなった)照射野への追加照射が、しばしば局所制御を増強するために用いられる。最善の結果を得るためには、標的体積を的確に設定し、重要な正常組織を可能な限り避けた慎重な照射計画を立てることが必要である;これには位置決め装置を使用する必要がある。
予後:
PSが優れた患者では、治癒を目的とした放射線療法を1コース完了できれば、20%の3年生存率が期待できる。
証拠(放射線療法):
臨床評価段階にある治療法の選択肢
臨床評価段階にある治療法の選択肢には以下のものがある:
- 治癒切除後の放射線療法に関する臨床試験。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Manser R, Wright G, Hart D, et al.: Surgery for early stage non-small cell lung cancer. Cochrane Database Syst Rev (1): CD004699, 2005.[PUBMED Abstract]
- Allen MS, Darling GE, Pechet TT, et al.: Morbidity and mortality of major pulmonary resections in patients with early-stage lung cancer: initial results of the randomized, prospective ACOSOG Z0030 trial. Ann Thorac Surg 81 (3): 1013-9; discussion 1019-20, 2006.[PUBMED Abstract]
- Darling GE, Allen MS, Decker PA, et al.: Randomized trial of mediastinal lymph node sampling versus complete lymphadenectomy during pulmonary resection in the patient with N0 or N1 (less than hilar) non-small cell carcinoma: results of the American College of Surgery Oncology Group Z0030 Trial. J Thorac Cardiovasc Surg 141 (3): 662-70, 2011.[PUBMED Abstract]
- Martini N, Bains MS, Burt ME, et al.: Incidence of local recurrence and second primary tumors in resected stage I lung cancer. J Thorac Cardiovasc Surg 109 (1): 120-9, 1995.[PUBMED Abstract]
- Winton T, Livingston R, Johnson D, et al.: Vinorelbine plus cisplatin vs. observation in resected non-small-cell lung cancer. N Engl J Med 352 (25): 2589-97, 2005.[PUBMED Abstract]
- Arriagada R, Bergman B, Dunant A, et al.: Cisplatin-based adjuvant chemotherapy in patients with completely resected non-small-cell lung cancer. N Engl J Med 350 (4): 351-60, 2004.[PUBMED Abstract]
- Pignon JP, Tribodet H, Scagliotti GV, et al.: Lung adjuvant cisplatin evaluation: a pooled analysis by the LACE Collaborative Group. J Clin Oncol 26 (21): 3552-9, 2008.[PUBMED Abstract]
- Scagliotti GV, Fossati R, Torri V, et al.: Randomized study of adjuvant chemotherapy for completely resected stage I, II, or IIIA non-small-cell Lung cancer. J Natl Cancer Inst 95 (19): 1453-61, 2003.[PUBMED Abstract]
- Hotta K, Matsuo K, Ueoka H, et al.: Role of adjuvant chemotherapy in patients with resected non-small-cell lung cancer: reappraisal with a meta-analysis of randomized controlled trials. J Clin Oncol 22 (19): 3860-7, 2004.[PUBMED Abstract]
- Edell ES, Cortese DA: Photodynamic therapy in the management of early superficial squamous cell carcinoma as an alternative to surgical resection. Chest 102 (5): 1319-22, 1992.[PUBMED Abstract]
- Corti L, Toniolo L, Boso C, et al.: Long-term survival of patients treated with photodynamic therapy for carcinoma in situ and early non-small-cell lung carcinoma. Lasers Surg Med 39 (5): 394-402, 2007.[PUBMED Abstract]
- Douillard JY, Rosell R, De Lena M, et al.: Adjuvant vinorelbine plus cisplatin versus observation in patients with completely resected stage IB-IIIA non-small-cell lung cancer (Adjuvant Navelbine International Trialist Association [ANITA]): a randomised controlled trial. Lancet Oncol 7 (9): 719-27, 2006.[PUBMED Abstract]
- Pepe C, Hasan B, Winton TL, et al.: Adjuvant vinorelbine and cisplatin in elderly patients: National Cancer Institute of Canada and Intergroup Study JBR.10. J Clin Oncol 25 (12): 1553-61, 2007.[PUBMED Abstract]
- Burdett SS, Stewart LA, Rydzewska L: Chemotherapy and surgery versus surgery alone in non-small cell lung cancer. Cochrane Database Syst Rev (3): CD006157, 2007.[PUBMED Abstract]
- Gilligan D, Nicolson M, Smith I, et al.: Preoperative chemotherapy in patients with resectable non-small cell lung cancer: results of the MRC LU22/NVALT 2/EORTC 08012 multicentre randomised trial and update of systematic review. Lancet 369 (9577): 1929-37, 2007.[PUBMED Abstract]
- PORT Meta-analysis Trialists Group: Postoperative radiotherapy for non-small cell lung cancer. Cochrane Database Syst Rev (2): CD002142, 2005.[PUBMED Abstract]
- Komaki R, Cox JD, Hartz AJ, et al.: Characteristics of long-term survivors after treatment for inoperable carcinoma of the lung. Am J Clin Oncol 8 (5): 362-70, 1985.[PUBMED Abstract]
- Dosoretz DE, Katin MJ, Blitzer PH, et al.: Radiation therapy in the management of medically inoperable carcinoma of the lung: results and implications for future treatment strategies. Int J Radiat Oncol Biol Phys 24 (1): 3-9, 1992.[PUBMED Abstract]
- Cochrane Collaborationにより、早期(I-IIIA期)肺がんに対して外科的介入を受けた計1,910人の患者に関する11件のランダム化試験がレビューされた。[
1
]3件の試験のプール解析では、以下が報告された:
- IIIA期NSCLCの治療
-
IIIA期の非小細胞肺がん(NSCLC)の患者は不均一な群である。同側縦隔リンパ節への転移、胸壁に浸潤した切除可能と考えられるT3腫瘍、あるいは気管支周囲または肺門のリンパ節への転移(N1)を伴う縦隔病変が患者に認められる場合がある。疾患の提示は、リンパ節への顕微鏡的転移を伴う切除可能な腫瘍から複数のリンパ節に転移した切除不能な巨大病変までさまざまである。
予後:
臨床病期がIIIA期 N2疾患患者の5年全生存(OS)率は10~15%である;しかしながら、縦隔に大きな転移(すなわち、胸部X線写真で認められるほどの)を有する患者の5年生存率は2~5%である。IIIA期のNSCLC患者に対する治療法の原理形態は、臨床環境に応じて、放射線療法、化学療法、手術、およびこれらの治療法を合わせた併用療法が考えられる。
治療選択肢は、腫瘍部位、および腫瘍が切除可能かどうかによって変わる。
切除した/切除可能なIIIA期N2のNSCLCに対する標準治療法の選択肢
術前の注意深い病期分類にもかかわらず、一部の患者は開胸術時に縦隔N2リンパ節への転移を有することが明らかになる。
切除した/切除可能な疾患に対する標準治療法の選択肢には以下のものがある:
術後のシスプラチン併用化学療法により、術中に潜伏N2病変が発見され切除したNSCLC患者に有意な生存的利益がもたらされることが、圧倒的多数の証拠から示される。切除可能なNSCLC患者における手術と化学療法の最適な順序、ならびに術後放射線療法の有益性とリスクについては、まだ確定していない。
手術
腫瘍およびリンパ節の完全切除が可能な患者では、手術に続けて術後化学療法を施行することで利益が得られる可能性がある。I期、II期、およびIIIA期のNSCLC患者において、完全同側縦隔リンパ節郭清(CMLND)と併用した肺がん切除は、縦隔リンパ節の系統的サンプリングと併用した肺がん切除と比べ、生存の改善とは関連していないことが、現時点での証拠から示唆されている。[ 1 ][証拠レベル:1iiA]
1件の第III相試験において、IIIA期NSCLC患者に対する化学放射線療法への手術の追加はOSの改善をもたらさなかったが、無増悪生存(PFS)および局所制御を改善させた。[ 2 ][証拠レベル:1iiDiii]
証拠(手術):
- Cochrane Collaborationにより、早期(I-IIIA期)肺がんに対して外科的介入を受けた計1,910人の患者に関する11件のランダム化試験がレビューされた。[
3
]3件の試験のプール解析では、以下が報告された:
- 切除可能なI期、II期、およびIIIA期のNSCLC患者では、切除および完全同側縦隔リンパ節郭清(CMLND)を受けた患者の方が、切除およびリンパ節サンプリングを受けた患者と比較して4年生存率が優れていた;ハザード比(HR)は0.78(95%信頼区間[CI]、0.65-0.93;P = 0.005)と推定された。[ 3 ][証拠レベル:1iiA]
- CMLND vs リンパ節サンプリングは、大規模なランダム化第III相試験(ACOSOG-Z0030)で評価された。手術による合併症および死亡の予備解析では、これらの手技で同等の割合が示された。[
4
]
- OS、無病生存(DFS)、局所再発、および領域内の再発における差は認められなかった。[ 1 ][証拠レベル:1iiA]
証拠の限界(手術):
局所および局所領域NSCLCを有する患者に対する手術の効力に関する結論は、現在までに研究されている参加者数が少数であること、および試験の方法論的な潜在的弱点により限定される。
術前療法
術前補助化学療法
III期 N2 NSCLC患者における手術前の化学療法の役割が臨床試験で大規模に検証されている。術前(新補助)化学療法で提唱されている有益性には以下のものがある:
- 外科的切除を容易にしうる腫瘍サイズの減少。
- 微小転移の早期根絶。
- より良好な耐容性。
証拠(術前補助化学療法):
- 988人の患者を含み、手術単独に対して術前化学療法の手術への追加を評価した7件のランダム化比較試験を対象にした系統的レビューおよびメタアナリシスがCochrane Collaborationにより報告された。[
5
]これらの試験では、I期、II期、およびIIIA期のNSCLC患者が評価された。
- 現時点で報告されている最大規模の試験では、519人の患者を、手術単独群、または3サイクルのプラチナ製剤をベースにした化学療法後に手術を施行する群のいずれかにランダムに割り付けた。[
7
]ほとんどの患者(61%)が臨床病期I期の疾患、31%がII期疾患、および7%がIII期疾患を有した。
- 術後合併症は集団間でほぼ同じであり、生活の質の障害は観察されなかった。
- OSに関して有益性の証拠は認められなかった(HR、1.02;95%CI、0.80-1.31;P = 0.86)。
- 現時点での結果を追加した最新の系統的レビューでは、術前化学療法の追加により、12%の相対的生存利益(患者1,507人、HR、0.88;95%CI、0.76-1.01;P = 0.07)が示唆されており、これは5年生存率の絶対差で5%の改善と同等である。[ 7 ]
術前化学放射線療法
手術前の術前補助化学療法および放射線療法の同時実施は治療を強化し、腫瘍負荷をダウンステージできる可能性を増加させうる。第II相試験の設定で検証されている一般的に利用されているレジメンには、シスプラチン/エトポシド(EP5050)および週1回のカルボプラチン/パクリタキセルがある。[ 8 ][ 9 ]術前化学放射線と手術 vs 同時化学放射線療法単独を比較したランダム化試験において、OSにおける差は認められなかったが、手術によりPFSと局所制御が改善した。[ 2 ][証拠レベル:1iiDiii]
証拠(術前化学放射線療法):
- Intergroup-0139[NCT00002550]試験により、IIIA期NSCLC患者396人において化学放射線療法単独と、術前化学放射線療法とその後に実施する手術とが比較された。[
2
]
- 手術はOSを改善しなかった(5年OS率、27% vs 20%;HR:0.87[0.70-1.10];P = 0.24)。
- 手術によりPFSが改善され(5年PFS率、22% vs 11%;HR 0.77[0.62-0.96];P = 0.017)、局所再発リスクが低下した(10% vs 22%;P = 0.002)。
- 特に肺切除を受けた患者のサブセットにおいて、術前化学放射線療法と手術の併用では、治療による死亡率が増加した(8% vs 2%)。
現在までのところ、現代の治療レジメンを用いた術前補助化学療法 vs 術前化学放射線療法の直接比較は実施されていない;最適な術前アプローチは不明のままである。
補助療法
補助化学療法
IIIA期NSCLC で完全切除した患者では、術後のシスプラチンをベースとした化学療法により利益が得られる可能性がある。[ 10 ][証拠レベル:1iiA]
証拠(補助化学療法):
ランダム化比較臨床試験からの証拠は、手術時にIIIA期NSCLCに予想外に遭遇した場合、完全切除後の化学療法により生存が改善することを示している。
I期、II期、およびIIIA期NSCLC患者に対する術後化学療法の使用を評価しているランダム化比較試験およびメタアナリシスがいくつかある。[ 10 ][ 11 ][ 12 ][ 13 ][ 14 ][ 15 ][ 16 ]
- NSCLCを完全切除した患者に対するシスプラチンをベースとした化学療法について、1995年以降に実施された5件の最大規模の試験(患者4,584人)から、個々の患者の転帰に関するデータが収集され、メタアナリシスで併合された。[
10
]
- 追跡期間中央値5.2年で、全HR死亡は0.89(95%CI、0.82-0.96;P = 0.005)で、これは化学療法による5年絶対的有益性5.4%に相当した。
- ビノレルビン(HR、0.80;95%CI、0.70-0.91)、エトポシドまたはビンカアルカロイド(HR、0.92;95%CI、0.80-1.07)、あるいは他の薬物(HR、0.97;95%CI、0.84-1.13)などの関連薬物で、化学療法の効果に有意差は認められなかった(交互作用検定、P = 0.11)。
- 有益性は病期により異なっていた(IIIA期のHR、0.83;95%CI、0.72-0.94)。
- 他のレジメンと比較して、シスプラチン + ビノレルビンの2剤併用療法で観察された生存へのより大きな効果は、ビノレルビンで治療された患者では投与されたシスプラチンの総用量が有意に高かったため、慎重に解釈すべきである。
- 2件の試験(FRE-IALTおよびAdjuvant Navelbine International Trialist Association [ANITA]試験)では、IIIA期における術後化学療法に関連して、有意なOSの有益性が報告されている。[
6
][
12
]
- ANITA試験(n = 325)におけるIIIA期患者のサブグループではHRが0.69(95%CI、0.53-0.90)で、FRE-IALT試験(n = 728)の結果ではHRが0.79(95%CI、0.66-0.95)であった。
- 化学療法の効果は、パフォーマンスステータス(PS)が良好な患者ほど高かった。
- 化学療法の効果と以下のいずれかの項目との相互作用は認められていない:
- 性別。
- 年齢。
- 組織像。
- 術式。
- 計画されている放射線療法。
- 計画されているシスプラチンの総用量。
- 術後のシスプラチンとビノレルビンを対象とした第III相試験のレトロスペクティブ解析では、65歳を超える患者が治療により利益を得られることが明らかになった。[
17
]
- 化学療法は高齢患者のOSを有意に延長した(HR、0.61;95%CI、0.38-0.98;P = 0.04)。
- 高齢患者が受けた治療は少ないが、毒性作用、入院、または年齢層別の治療関連死に有意差は認められなかった。
補助化学放射線療法
術前または術後に実施する併用化学療法と放射線は研究目的であり、将来、臨床試験での評価が必要であると考えるべきである。
証拠(補助化学放射線療法):
- 5件のランダム化試験で、外科的切除後の放射線療法に対して術後併用化学放射線療法の意義が評価されている。[
5
][
7
][
18
][
19
][
20
][証拠レベル:1iiA]
- DFSの改善を報告した試験は1件のみで、OSの改善を報告した試験はなかった。
- 3件の試験では、プラチナ製剤をベースにした併用化学療法とその後の手術 vs プラチナ製剤をベースにした化学療法とその後の放射線療法(60~69.6Gy)単独を評価して、手術または放射線療法が最も効力が高いかを判定している。[
20
][
21
][
22
]研究は、IIIA期 N2疾患患者の登録が73人(Radiation Therapy Oncology Group[RTOG])(RTOG 89-01)、107人(University of Texas M.D. Anderson Cancer Center)、および333人(European Organization for Research and Treatment of Cancer[EORTC-08941;NCT00002623])と小規模であったが、局所制御または生存の差を報告した試験はなかった。[
20
][
21
][
22
][証拠レベル:1iiA]
- 最大規模のシリーズ(EORTC-08941)において、組織学的または細胞学的に証明されたIIIA期 N2 NSCLCの患者579人が、3サイクルのプラチナ製剤をベースにした導入化学療法を実施された。[
22
]反応が認められた333人の患者はその後、外科的切除または放射線療法にランダムに割り付けられた。手術を受けた患者154人(92%)中、根治的切除が50%、病理学的病期後退が42%、病理学的完全奏効が5%であった;4%は手術後に死亡した。術後(補助)放射線療法(PORT)は、手術群の患者62人(40%)に施行された。放射線療法を受けた患者154人(93%)では、放射線療法の指示に対する全体のコンプライアンスは55%で、グレード3~4の急性および晩期毒性作用が、食道および肺にそれぞれ4%および7%の患者に発生した;放射線肺炎により1人の患者が死亡した。
- 切除に割り付けた患者のOS中央値が16.4ヵ月であったのに対し、放射線療法に割り付けた患者ではOS中央値が17.5ヵ月であった;切除に割り付けた患者の5年OS率が15.7%であったのに対し、放射線療法に割り付けた患者では14%であった(HR、1.06;95%CI、0.84-1.35)。[ ]
- PFS率もまた、両群でほぼ同じであった。放射線療法は罹病率および死亡率が低いことを考慮して、これらの患者に望ましい局所領域治療とみなすべきであると結論された。[ ]
- 最大規模のシリーズ(EORTC-08941)において、組織学的または細胞学的に証明されたIIIA期 N2 NSCLCの患者579人が、3サイクルのプラチナ製剤をベースにした導入化学療法を実施された。[
22
]反応が認められた333人の患者はその後、外科的切除または放射線療法にランダムに割り付けられた。手術を受けた患者154人(92%)中、根治的切除が50%、病理学的病期後退が42%、病理学的完全奏効が5%であった;4%は手術後に死亡した。術後(補助)放射線療法(PORT)は、手術群の患者62人(40%)に施行された。放射線療法を受けた患者154人(93%)では、放射線療法の指示に対する全体のコンプライアンスは55%で、グレード3~4の急性および晩期毒性作用が、食道および肺にそれぞれ4%および7%の患者に発生した;放射線肺炎により1人の患者が死亡した。
補助放射線療法
PORTの意義が評価されている。[ 18 ]一部の研究は、腫瘍切除後にリンパ節転移陽性を示す患者の局所制御がPORTにより改善されることを示唆しているが、この治療で生存が改善できるかどうかは未だ議論の余地がある。現時点では、胸部PORTの至適線量は不明である。引用した研究のほとんどが、30Gy~60Gyの範囲の線量を用い、一般に2Gy~2.5Gy分割で照射していた。[ 18 ]
National Cancer Institute of Canada (NCIC) Clinical Trials Group JBR.10の研究(NCT00002583)で述べられているように、以下のいずれかが認められる特定の患者では、局所再発のリスクを抑えるためにPORTを検討してもよい:[ 17 ]
- 複数のリンパ節における転移。
- 被膜外への腫瘍拡大。
- 切除縁が腫瘍に近いか、顕微鏡的に陽性の切除断端。
証拠(補助放射線療法):
1件の大規模なメタアナリシス、複数のランダム化試験のサブセット解析、および1件の大規模な集団研究で得られた証拠から、PORTにより局所再発が抑えられる可能性があることが示唆される。PORTのOSに対する効果を検討したこれらの研究の結果は相反している。
- PORT vs 手術単独を評価した10件のランダム化試験を対象としたメタアナリシスでは、以下が示された:
- PORT群全体でも、N2患者のサブセットでも、OSに差は認められない。[ 12 ][証拠レベル:1iiA]
- ANITA試験の非ランダム化サブアナリシスの結果では、N2患者を対象に5年OSについてPORTを受けた群と受けなかった群で比較して、以下が明らかになった:[
6
]
- 観察群(PORTを受けた患者で21% vs PORTを受けなかった患者で17%)および化学療法群(PORT併用群で47% vs PORT非併用群で34%)で放射線療法を受けた患者の方が生存率が高い;しかしながら、統計学的な比較検定は実施されなかった。[ 6 ]
- Surveillance, Epidemiology, and End Results(SEER)プログラムの結果[
19
]から、以下が示唆される:
- 大規模SEERレトロスペクティブ研究(N = 7,465)により、N2疾患において放射線療法と関連する優れた生存率(HR、0.855;95%CI、0.762-0.959)が明らかにされた。
IIIA期 N2疾患ではPORTの有益性が認められており、病期が初期のNSCLCにおけるPORTの役割は、実施中の第III相試験で明らかになるはずである。放射線照射における技術的進歩、標的体積のより的確な設定、および照射ポータルにおける心臓容積の制限によって、これらの治療成績を改善できるかどうかを明らかにするために、さらなる分析が必要である。[ 12 ]
切除不能なIIIA期N2のNSCLCに対する標準治療法の選択肢
切除不能なNSCLC患者に対する標準治療法の選択肢には以下のものがある:
放射線療法
局所的に進行した切除不能腫瘍の治療として実施する場合
放射線療法の単独実施、化学療法との逐次的照射、および化学療法との同時照射は、局所進行切除不能III期NSCLC患者に利益をもたらす場合がある。
予後:
従来の線量および分割スケジュール(6~7週間で60~70Gyに対して1.8~2.0Gy/分割/日)を用いた放射線療法により、患者の5~10%に再現性のある長期的な生存利益が得られ、有意な症状緩和がもたらされる。[ 23 ]
証拠(局所的に進行した切除不能腫瘍に対する放射線療法):
- 1件のプロスペクティブ・ランダム化研究では、以下が示された:[
24
]
- 1日3分割照射を連日(週末も含めて)施行する放射線療法(連続多分割加速放射線療法)では、1日単回照射する放射線療法と比較して、OSが改善した。[ 24 ][証拠レベル:1iiA]
- 放射線療法単独で治療された患者に対する失敗のパターンは、局所領域および遠隔の両方の失敗を含んでいた。
切除不能なIIIA期疾患の患者は放射線療法から利益が得られる場合があるが、長期治療成績は局所および全身に再燃がみられることから一般的に不良である。
緩和療法が必要な患者に対して
放射線療法は、NSCLCの局所浸潤による次のような症状の緩和に有効な場合がある:
- 気管、食道、または気管支の圧迫。
- 疼痛。
- 声帯麻痺。
- 喀血。
- 上大静脈症候群。
症例によっては、気管支内レーザー療法および/または近接照射療法が、近位の閉塞病変を改善するために使用されている。[ 25 ]
証拠(緩和療法としての放射線療法):
- 系統的レビューにより、高線量率気管支内近接照射療法(HDREB)単独、または外照射療法(EBRT)またはレーザー療法との併用に関する6件のランダム化試験が確認された。[
26
]
- EBRT単独を使用した治療を以前に受けていない患者では、より良好な全体的な症状緩和が得られ、再治療を必要とすることがより少なかった。[ 26 ][証拠レベル:1iiC]
- EBRTは症状緩和目的で頻繁に処方されるが、分割照射法をいつ使うべきかについてのコンセンサスは得られていない。
- EBRTでは多分割レジメンが異なっても、同様な症状緩和が得られると考えられる[ 27 ][ 28 ][ 29 ][ 30 ][ 31 ][ 32 ];しかしながら、NCIC Clinical Trials' Group試験(NCT00003685)で判明しているように、単回放射線療法は、少分割または標準分割レジメンと比べて、症状緩和には不十分な場合がある。[ 29 ][証拠レベル:1iiC]
- 高線量EBRTを施行した患者では、PSが良好なほど生存がわずかに延長するという証拠が得られている。[ 27 ][ 28 ][証拠レベル:1iiA]
- HDREBは、技術的に実施可能な場合に、以前にEBRTで治療されたが再発した症状を認める気管支内閉塞患者に緩和をもたらした。
化学放射線療法
放射線療法への順次化学療法および併用化学療法の追加が、プロスペクティブ・ランダム化試験およびメタアナリシスで評価されている。全体的に、併用療法は、毒性作用の増加を伴うが、生存に最も大きな利益をもたらす可能性がある。
放射線と同時のプラチナ製剤をベースにした化学療法は、局所進行NSCLC患者の生存を改善しうる。しかしながら、こうした潜在的な治療の有益性の大きさおよび化学療法の最適な投与スケジュールを正確に決定するには、利用可能なデータが不十分である。[ 33 ]
証拠(化学放射線療法):
- 11件のランダム化臨床試験による患者データを対象としたメタアナリシスでは、以下が示された:[
34
]
- シスプラチンをベースとした併用化学療法と放射線療法により、放射線療法単独と比べ死亡リスクが10%低下した。[ 34 ][証拠レベル:1iiA]
- 13件の試験を対象としたメタアナリシスでは(2,214人の評価可能患者を基に)、以下が示された:[
35
]
- 併用化学療法を根治的放射線療法へ追加することで、2年時点での死亡リスクが低下した(相対リスク[RR]、0.93;95%CI、0.88-0.98;P = 0.01)。
- プラチナ製剤をベースにした化学療法を用いた11件の試験では、RRは0.93(95%CI、0.87-0.99;P = 0.02)であった。[ 35 ]
- 1,764人の患者からの個々のデータを対象としたメタアナリシスでは、9件の試験に基づき、以下が示された:[
33
]
- 放射線療法と化学療法による治療を受けた患者におけるHR死亡は、放射線療法単独と比較して0.89(95%CI、0.81-0.98;P = 0.02)であり、化学療法による2年時点の絶対的有益性が4%であることに相当していた。
- プラチナ製剤とエトポシドの併用は、プラチナ製剤単独よりも有効と思われた。
化学放射線療法の同時併用 vs 順次施行
2件のランダム化試験(RTOG-9410[NCT01134861]を含む)および1件のメタアナリシスの結果は、化学療法と放射線療法の同時併用の方が化学療法と放射線療法の順次施行より毒性作用が大きいにもかかわらず、得られる生存利益が大きい可能性があることを示している。[ 36 ][ 37 ][ 38 ][証拠レベル:1iiA]
証拠(化学放射線療法の同時併用 vs 順次施行):
- 第一の試験では、マイトマイシンC、ビンデシン、およびシスプラチンの併用療法と、スプリットコースの連日の放射線療法を56Gyまで同時併用して、化学療法後に連日の放射線療法を56Gyまで継続する群と比較した。[
36
]
- 5年OSは同時療法の方が良好であった(27% vs 9%)。
- 骨髄抑制は同時療法群の患者で大きかったが、治療関連死亡率は両治療群で1%未満であった。[ 36 ]
- 第2の試験では、610人の患者を、シスプラチンおよびビンブラスチンによる化学療法後に63Gyの放射線療法を実施する順次施行群、同じレジメンを用いた同時化学放射線療法群、またはシスプラチンおよびエトポシドによる化学療法と1日2回の放射線療法の同時併用群のいずれかにランダムに割り付けた。[
38
]
- 生存期間中央値および5年生存率は、連日の放射線療法と化学療法の同時併用群が優れていた(順次施行レジメンとの比較で、それぞれ17ヵ月 vs 14.6ヵ月、および16% vs 10%[P = 0.046])。[ 38 ]
- 2件のより小規模な研究もまた、逐次的化学療法および放射線よりも同時化学療法および放射線を支持するOSの結果を報告したが、この結果は統計的に有意ではなかった。[ 37 ][ 39 ][証拠レベル:1iiA]
- 3件の試験を対象としたメタアナリシス(患者711人)で、同時併用と順次施行が評価された。[
35
]
- この解析では、同時併用において順次施行を超える有意な有益性が示された(RR、0.86;95%CI、0.78-0.95;P = 0.003)。すべての研究でシスプラチンをベースにしたレジメンおよび1日1回の放射線療法が用いられた。[ 35 ]
- 同時併用群では死亡が多く(OS率で3%)報告されたが、統計的有意差までには至らなかった(RR、1.60;CI、0.75-3.44;P = 0.2)。
- 急性食道炎(グレード3以上)は、同時併用群(範囲、17~26%)の方が順次施行群(範囲、0~4%;RR、6.77;P = 0.001)より多く認められた。全体で、好中球減少(グレード3以上)の発生は両群でほぼ同じであった。
同時化学放射線療法における放射線療法の線量増加
腫瘍のモーション管理や画像ガイダンスなど、1990年代における放射線療法の送達技術が改善されて、第I/II相試験では、化学療法と同時に実施する放射線療法の線量を74Gyまで増加させられることが実証された。[ 40 ][ 41 ][ 42 ]しかしながら、従来の60Gyの線量 vs 週1回のカルボプラチン/パクリタキセルを同時に実施する74Gyまでの線量増加に関する第III相試験では、局所制御またはPFSの改善は実証されず、OSは線量増加により悪化した(HR、1.38[1.09-1.76];P = 0.004)。線量増加によりグレード5のイベントの有意ではない増加(10% vs 2%)が認められ、グレード3の食道炎の発生率は増加した(21% vs 7%;P = 0.0003)。したがって、III期NSCLCに対して60Gyを超える放射線量の増加について明確な有益性は認められない。[ 43 ][証拠レベル:1iiA]
同時化学放射線療法における全身療法の選択
証拠(同時化学放射線療法における全身療法):
- 第III相ランダム化PROCLAIM研究[NCT00686959]には、新たにIIIA/B期、切除不能、非扁平上皮性のNSCLCと診断された患者598人が登録された。[
44
]患者は1:1の比率で、以下の2つの治療群のいずれかにランダムに割り付けられた:
- 治療群A:ペメトレキセド(500mg/m2)およびシスプラチン(75mg/m2)、3週間ごとに静脈内投与を3サイクル + 同時胸部放射線療法(60~66Gy)とその後のペメトレキセド地固め療法、3週間ごとを4サイクル。
- 治療群B:標準療法としてエトポシド(50mg/m2)およびシスプラチン(50mg/m2)、4週間ごとに静脈内投与を2サイクル + 同時胸部放射線療法(60~66Gy)とその後の地固め療法としてプラチナ製剤をベースにした2剤併用化学療法を2サイクル。
主目的はOSであった。この研究は、第一種過誤の確率を0.05、OSのHR、0.74を検出する検出力を80%とする優越性試験としてデザインされた。この研究では598人の患者がランダムに割り付けられ(治療群A、301人;治療群B、297人)、555人の患者(治療群A、283人;治療群B、272人)が治療された。
- 無益であったため、登録は早期に中止された。
- 治療群AのOSは、治療群Bよりも優れていなかった(HR、0.98;95%CI、0.79-1.20;中央値、26.8ヵ月 vs 25.0ヵ月;P = 0.831)。
- 治療群Aでは全治療期間中、好中球減少(24.4% vs 44.5%;P < 0.001)を含めて、薬物関連のグレード3~4の有害事象の発生が有意に低かった(64.0% vs 76.8%;P = 0.001)。
化学療法と放射線療法の同時併用前または後の追加の全身療法
化学療法と放射線療法の同時併用前の導入化学療法の追加によって、生存が改善することは示されていない。[ 45 ][証拠レベル:1iiA]
地固め免疫療法
デュルバルマブ
デュルバルマブは選択的ヒトIgG1モノクローナル抗体で、プログラム細胞死リガンド1(PD-L1)のプログラム細胞死1(PD-1)およびCD80への結合を遮断し、T細胞が腫瘍細胞を認識して殺すことができるようにする。[ 46 ]
証拠(デュルバルマブ):
- 第III相PACIFIC試験(NCT02125461)には、III期NSCLCで疾患が2サイクル以上のプラチナ製剤ベースの化学放射線療法後に増悪していない713人の患者が登録した。患者は2:1の比率で、デュルバルマブ(10mg/kg、静注)またはプラセボ(最大12ヵ月間2週間ごとに投与)を受けるようにランダムに割り付けられた。[
46
]複合主要エンドポイントは、盲検下での独立中央判定によるPFSおよびOS(中間解析時には予定されていなかった)であった。
- 中間解析時に、複合主要エンドポイントのPFSが達成された。PFS中央値は、デュルバルマブ群で16.8ヵ月であったのに対し、プラセボ群で5.6ヵ月であった(HR、0.52;95%CI、0.42-0.65;P < 0.001)。[ ][証拠レベル:1iiDiii]18ヵ月PFS率は、デュルバルマブ群で44.2% vs プラセボ群で27%であった。
- PFSの有益性は事前に規定されたすべてのサブグループで示され、化学放射線療法前のPD-L1の発現または喫煙状態とは関係がなかった。上皮成長因子受容体(EGFR)変異が6%の患者で観察された(デュルバルマブで治療された29人 vs プラセボで治療された14人)。EGFRが変異したサブグループに対する非層別化HRは、0.76(95%CI、0.35-1.64)であった。
- グレード3または4の有害事象はデュルバルマブで治療された患者の29.9%に起こり、プラセボで治療された患者では26.1%に起こった。最も一般的なグレード3または4の有害事象は、デュルバルマブを受けた患者の4.4%およびプラセボを受けた患者の3.8%に起こった肺炎であった。
- 中間解析時にOSは評価されていなかった。
上溝腫瘍(T3、N0またはN1、M0)に対する標準治療法の選択肢
上溝腫瘍に対する標準治療法の選択肢には以下のものがある:
しばしばパンコースト腫瘍と呼ばれる上溝のNSCLCは患者の5%未満に起こる。[ 50 ][ 51 ]通常、上溝腫瘍は肺尖から生じ、胸郭上口の構造物に近いために治療が困難である。この位置の腫瘍は壁側胸膜、胸壁、腕神経叢、鎖骨下血管、星状神経節、および隣接する椎体に浸潤しうる。しかしながら、パンコースト腫瘍は、特にT3、N0疾患の患者においては治癒的治療を実施可能である。
有害な予後因子として、縦隔リンパ節転移(N2病変)の存在、脊椎または鎖骨下の血管への浸潤(T4病変)、限局的切除(R1またはR2)などがある。
放射線療法単独
放射線療法はパンコースト腫瘍の治療に不可欠な部分であるが、公表されているさまざまなシリーズで用いられた線量、治療技術、および病期分類が異なるため、その有効性の確定が困難となっている。[ 50 ][ 51 ]
予後:
臨床的な病期分類のみを実施した患者を対象とした放射線療法の小規模なレトロスペクティブ・シリーズでは、T期、総照射線量、および他の予後因子にもよるが、0~40%の5年生存率が報告されている。導入放射線療法および一塊切除は、潜在的に治癒的であることが示された。
証拠(放射線療法):
化学放射線療法とその後の手術
証拠(化学放射線療法):
- 2件の第II相大規模プロスペクティブ多施設試験により、導入化学放射線療法とその後の切除が評価されている。[
53
][
54
]
- 最初の試験(NCT00002642)では、縦隔鏡検査陰性で臨床病期T3-4期、N0-1の上溝腫瘍を有する適格患者110人が登録された。[
54
]導入療法は、2サイクルのエトポシドおよびシスプラチンに45Gyの同時放射線療法の併用であった。
- 導入レジメンは十分に耐容性を示し、グレード3以上の毒性作用がみられた参加者はわずか5人であった。
- 導入化学放射線療法は、原発病変を無力化できた。導入療法は、104人(95%)の患者が完了した。手術に適格な患者95人中、88人(80%)が開胸術を受け、2人(1.8%)が術後に死亡し、完全切除されたのは83人(76%)であった。
- 病理学的完全奏効または微小顕微鏡的病変が、61人(56%)の切除標本でみられた。病理学的完全奏効では、残存病変が認められる場合よりもより良好な生存に至った(P = 0.02)。
- 5年生存率はすべての患者に対して44%および完全切除後で54%であり、T3およびT4腫瘍間で差は認められなかった。疾患進行は主に遠隔部位で発生した。
- 第2の試験では75人の患者が登録され、マイトマイシンC、ビンデシン、およびシスプラチンと併用する45Gyの放射線療法による導入療法で治療された。[
53
]57人の患者(76%)が外科的切除を受け、完全切除は51人の患者(68%)で達成された。
- 病理学的完全奏効を示した患者は12人であった。
- 乳糜胸、膿胸、肺炎、成人呼吸窮迫症候群、出血など、主要な術後合併症が8人の患者に認められた。治療関連死は3例であった。
- 3年経過時のDFS率は49%で、OS率は61%であった;5年経過時のDFS率は45%でOS率56%であった。[ ][証拠レベル:3iiiDi]
- 最初の試験(NCT00002642)では、縦隔鏡検査陰性で臨床病期T3-4期、N0-1の上溝腫瘍を有する適格患者110人が登録された。[
54
]導入療法は、2サイクルのエトポシドおよびシスプラチンに45Gyの同時放射線療法の併用であった。
同時化学放射線療法における放射線療法の線量増加
腫瘍のモーション管理や画像ガイダンスなど、1990年代における放射線療法の送達技術が改善されて、第I/II相試験では、化学療法と同時に実施する放射線療法の線量を74Gyまで増加させられることが実証された。[ 40 ][ 41 ][ 42 ]しかしながら、従来の60Gyの線量 vs 週1回のカルボプラチン/パクリタキセルを同時に実施する74Gyまでの線量増加に関する第III相試験では、局所制御またはPFSの改善は実証されず、OSは線量増加により悪化した(HR、1.38[1.09-1.76];P = 0.004)。線量増加によりグレード5のイベントの有意ではない増加(10% vs 2%)が認められ、グレード3の食道炎の発生率は増加した(21% vs 7%;P = 0.0003)。したがって、III期NSCLCに対して60Gyを超える放射線量の増加について明確な有益性は認められない。[ 43 ][証拠レベル:1iiA]
同時化学放射線療法における全身療法の選択
証拠(同時化学放射線療法における全身療法):
- 第III相ランダム化PROCLAIM研究[NCT00686959]には、新たにIIIA/B期、切除不能、非扁平上皮性のNSCLCと診断された患者598人が登録された。[
44
]患者は1:1の比率で、以下の2つの治療群のいずれかにランダムに割り付けられた:
- 治療群A:ペメトレキセド(500mg/m2)およびシスプラチン(75mg/m2)、3週間ごとに静脈内投与を3サイクル + 同時胸部放射線療法(60~66Gy)とその後のペメトレキセド地固め療法、3週間ごとを4サイクル。
- 治療群B:標準療法としてエトポシド(50mg/m2)およびシスプラチン(50mg/m2)、4週間ごとに静脈内投与を2サイクル + 同時胸部放射線療法(60~66Gy)とその後の地固め療法としてプラチナ製剤をベースにした2剤併用化学療法を2サイクル。
主目的はOSであった。この研究は、第一種過誤の確率を0.05、OSのHR、0.74を検出する検出力を80%とする優越性試験としてデザインされた。この研究では598人の患者がランダムに割り付けられ(治療群A、301人;治療群B、297人)、555人の患者(治療群A、283人;治療群B、272人)が治療された。
- 無益であったため、登録は早期に中止された。
- 治療群AのOSは、治療群Bよりも優れていなかった(HR、0.98;95%CI、0.79-1.20;中央値、26.8ヵ月 vs 25.0ヵ月;P = 0.831)。
- 治療群Aでは全治療期間中、好中球減少(24.4% vs 44.5%;P < 0.001)を含めて、薬物関連のグレード3~4の有害事象の発生が有意に低かった(64.0% vs 76.8%;P = 0.001)。
胸壁に浸潤した腫瘍(T3、N0またはN1、M0)に対する標準治療法の選択肢
胸壁に浸潤した腫瘍に対する標準治療法の選択肢には以下のものがある:
- 手術。
- 手術および放射線療法。
- 放射線療法単独。
- 放射線療法を併用する化学療法および/または手術。
胸壁に直接浸潤を認める大きな原発腫瘍のある特定の患者は、手術で腫瘍が完全に切除されれば、外科治療により長期生存が得られる。
証拠(根治的手術):
- 97人の患者を対象にした1件の小規模ケースシリーズにおいて、T3、N0、M0疾患を完全切除された患者の5年生存率は44.2%であった。T3、N1、M0疾患を完全切除された患者の5年生存率は40.0%であった。T3、N2、M0疾患を完全切除された患者の5年生存率は6.2%であった。[ 55 ][証拠レベル:3iiiDi]
- 104人の患者を対象にした1件の小規模ケースシリーズにおいて、T3、N0、M0疾患を完全切除された患者の5年生存率は67.3%であった。T3、N1、M0疾患を完全切除された患者の5年生存率は100.0%であった。T3、N2、M0疾患を完全切除された患者の5年生存率は17.9%であった。[ 56 ][証拠レベル:3iiiDi]
- 3ヵ所の施設で治療を受けた309人の患者を対象としたケースシリーズでは、一塊切除を受けた患者の方が胸膜肺切除を受けた患者と比べて治療成績が優れていた(60.3% vs 39.1%;P = 0.03)。[ 57 ][証拠レベル:3iiiDi]
補助化学療法が推奨され、放射線療法は、切除縁がはっきりしない場合にのみ使用する。切除が不完全で縦隔リンパ節に浸潤が認められた患者では、生存率が低かった。完全切除達成能力を向上させるために、集学的アプローチが評価されている。
臨床評価段階にある治療法の選択肢
臨床評価段階にある治療法の選択肢には以下のものがある:
- 化学療法、放射線療法、および手術をさまざまに組み合わせた集学的治療。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Darling GE, Allen MS, Decker PA, et al.: Randomized trial of mediastinal lymph node sampling versus complete lymphadenectomy during pulmonary resection in the patient with N0 or N1 (less than hilar) non-small cell carcinoma: results of the American College of Surgery Oncology Group Z0030 Trial. J Thorac Cardiovasc Surg 141 (3): 662-70, 2011.[PUBMED Abstract]
- Albain KS, Swann RS, Rusch VW, et al.: Radiotherapy plus chemotherapy with or without surgical resection for stage III non-small-cell lung cancer: a phase III randomised controlled trial. Lancet 374 (9687): 379-86, 2009.[PUBMED Abstract]
- Manser R, Wright G, Hart D, et al.: Surgery for early stage non-small cell lung cancer. Cochrane Database Syst Rev (1): CD004699, 2005.[PUBMED Abstract]
- Allen MS, Darling GE, Pechet TT, et al.: Morbidity and mortality of major pulmonary resections in patients with early-stage lung cancer: initial results of the randomized, prospective ACOSOG Z0030 trial. Ann Thorac Surg 81 (3): 1013-9; discussion 1019-20, 2006.[PUBMED Abstract]
- Burdett SS, Stewart LA, Rydzewska L: Chemotherapy and surgery versus surgery alone in non-small cell lung cancer. Cochrane Database Syst Rev (3): CD006157, 2007.[PUBMED Abstract]
- Douillard JY, Rosell R, De Lena M, et al.: Adjuvant vinorelbine plus cisplatin versus observation in patients with completely resected stage IB-IIIA non-small-cell lung cancer (Adjuvant Navelbine International Trialist Association [ANITA]): a randomised controlled trial. Lancet Oncol 7 (9): 719-27, 2006.[PUBMED Abstract]
- Gilligan D, Nicolson M, Smith I, et al.: Preoperative chemotherapy in patients with resectable non-small cell lung cancer: results of the MRC LU22/NVALT 2/EORTC 08012 multicentre randomised trial and update of systematic review. Lancet 369 (9577): 1929-37, 2007.[PUBMED Abstract]
- Albain KS, Rusch VW, Crowley JJ, et al.: Concurrent cisplatin/etoposide plus chest radiotherapy followed by surgery for stages IIIA (N2) and IIIB non-small-cell lung cancer: mature results of Southwest Oncology Group phase II study 8805. J Clin Oncol 13 (8): 1880-92, 1995.[PUBMED Abstract]
- Suntharalingam M, Paulus R, Edelman MJ, et al.: Radiation therapy oncology group protocol 02-29: a phase II trial of neoadjuvant therapy with concurrent chemotherapy and full-dose radiation therapy followed by surgical resection and consolidative therapy for locally advanced non-small cell carcinoma of the lung. Int J Radiat Oncol Biol Phys 84 (2): 456-63, 2012.[PUBMED Abstract]
- Pignon JP, Tribodet H, Scagliotti GV, et al.: Lung adjuvant cisplatin evaluation: a pooled analysis by the LACE Collaborative Group. J Clin Oncol 26 (21): 3552-9, 2008.[PUBMED Abstract]
- Winton T, Livingston R, Johnson D, et al.: Vinorelbine plus cisplatin vs. observation in resected non-small-cell lung cancer. N Engl J Med 352 (25): 2589-97, 2005.[PUBMED Abstract]
- Arriagada R, Bergman B, Dunant A, et al.: Cisplatin-based adjuvant chemotherapy in patients with completely resected non-small-cell lung cancer. N Engl J Med 350 (4): 351-60, 2004.[PUBMED Abstract]
- Scagliotti GV, Fossati R, Torri V, et al.: Randomized study of adjuvant chemotherapy for completely resected stage I, II, or IIIA non-small-cell Lung cancer. J Natl Cancer Inst 95 (19): 1453-61, 2003.[PUBMED Abstract]
- Hotta K, Matsuo K, Ueoka H, et al.: Role of adjuvant chemotherapy in patients with resected non-small-cell lung cancer: reappraisal with a meta-analysis of randomized controlled trials. J Clin Oncol 22 (19): 3860-7, 2004.[PUBMED Abstract]
- Edell ES, Cortese DA: Photodynamic therapy in the management of early superficial squamous cell carcinoma as an alternative to surgical resection. Chest 102 (5): 1319-22, 1992.[PUBMED Abstract]
- Corti L, Toniolo L, Boso C, et al.: Long-term survival of patients treated with photodynamic therapy for carcinoma in situ and early non-small-cell lung carcinoma. Lasers Surg Med 39 (5): 394-402, 2007.[PUBMED Abstract]
- Pepe C, Hasan B, Winton TL, et al.: Adjuvant vinorelbine and cisplatin in elderly patients: National Cancer Institute of Canada and Intergroup Study JBR.10. J Clin Oncol 25 (12): 1553-61, 2007.[PUBMED Abstract]
- PORT Meta-analysis Trialists Group: Postoperative radiotherapy for non-small cell lung cancer. Cochrane Database Syst Rev (2): CD002142, 2005.[PUBMED Abstract]
- Lally BE, Zelterman D, Colasanto JM, et al.: Postoperative radiotherapy for stage II or III non-small-cell lung cancer using the surveillance, epidemiology, and end results database. J Clin Oncol 24 (19): 2998-3006, 2006.[PUBMED Abstract]
- Johnstone DW, Byhardt RW, Ettinger D, et al.: Phase III study comparing chemotherapy and radiotherapy with preoperative chemotherapy and surgical resection in patients with non-small-cell lung cancer with spread to mediastinal lymph nodes (N2); final report of RTOG 89-01. Radiation Therapy Oncology Group. Int J Radiat Oncol Biol Phys 54 (2): 365-9, 2002.[PUBMED Abstract]
- Taylor NA, Liao ZX, Cox JD, et al.: Equivalent outcome of patients with clinical Stage IIIA non-small-cell lung cancer treated with concurrent chemoradiation compared with induction chemotherapy followed by surgical resection. Int J Radiat Oncol Biol Phys 58 (1): 204-12, 2004.[PUBMED Abstract]
- van Meerbeeck JP, Kramer GW, Van Schil PE, et al.: Randomized controlled trial of resection versus radiotherapy after induction chemotherapy in stage IIIA-N2 non-small-cell lung cancer. J Natl Cancer Inst 99 (6): 442-50, 2007.[PUBMED Abstract]
- Komaki R, Cox JD, Hartz AJ, et al.: Characteristics of long-term survivors after treatment for inoperable carcinoma of the lung. Am J Clin Oncol 8 (5): 362-70, 1985.[PUBMED Abstract]
- Saunders M, Dische S, Barrett A, et al.: Continuous hyperfractionated accelerated radiotherapy (CHART) versus conventional radiotherapy in non-small-cell lung cancer: a randomised multicentre trial. CHART Steering Committee. Lancet 350 (9072): 161-5, 1997.[PUBMED Abstract]
- Miller JI, Phillips TW: Neodymium:YAG laser and brachytherapy in the management of inoperable bronchogenic carcinoma. Ann Thorac Surg 50 (2): 190-5; discussion 195-6, 1990.[PUBMED Abstract]
- Ung YC, Yu E, Falkson C, et al.: The role of high-dose-rate brachytherapy in the palliation of symptoms in patients with non-small-cell lung cancer: a systematic review. Brachytherapy 5 (3): 189-202, 2006 Jul-Sep.[PUBMED Abstract]
- Sundstrøm S, Bremnes R, Aasebø U, et al.: Hypofractionated palliative radiotherapy (17 Gy per two fractions) in advanced non-small-cell lung carcinoma is comparable to standard fractionation for symptom control and survival: a national phase III trial. J Clin Oncol 22 (5): 801-10, 2004.[PUBMED Abstract]
- Lester JF, Macbeth FR, Toy E, et al.: Palliative radiotherapy regimens for non-small cell lung cancer. Cochrane Database Syst Rev (4): CD002143, 2006.[PUBMED Abstract]
- Bezjak A, Dixon P, Brundage M, et al.: Randomized phase III trial of single versus fractionated thoracic radiation in the palliation of patients with lung cancer (NCIC CTG SC.15). Int J Radiat Oncol Biol Phys 54 (3): 719-28, 2002.[PUBMED Abstract]
- Erridge SC, Gaze MN, Price A, et al.: Symptom control and quality of life in people with lung cancer: a randomised trial of two palliative radiotherapy fractionation schedules. Clin Oncol (R Coll Radiol) 17 (1): 61-7, 2005.[PUBMED Abstract]
- Kramer GW, Wanders SL, Noordijk EM, et al.: Results of the Dutch National study of the palliative effect of irradiation using two different treatment schemes for non-small-cell lung cancer. J Clin Oncol 23 (13): 2962-70, 2005.[PUBMED Abstract]
- Senkus-Konefka E, Dziadziuszko R, Bednaruk-Młyński E, et al.: A prospective, randomised study to compare two palliative radiotherapy schedules for non-small-cell lung cancer (NSCLC). Br J Cancer 92 (6): 1038-45, 2005.[PUBMED Abstract]
- Aupérin A, Le Péchoux C, Pignon JP, et al.: Concomitant radio-chemotherapy based on platin compounds in patients with locally advanced non-small cell lung cancer (NSCLC): a meta-analysis of individual data from 1764 patients. Ann Oncol 17 (3): 473-83, 2006.[PUBMED Abstract]
- Chemotherapy in non-small cell lung cancer: a meta-analysis using updated data on individual patients from 52 randomised clinical trials. Non-small Cell Lung Cancer Collaborative Group. BMJ 311 (7010): 899-909, 1995.[PUBMED Abstract]
- Rowell NP, O'rourke NP: Concurrent chemoradiotherapy in non-small cell lung cancer. Cochrane Database Syst Rev (4): CD002140, 2004.[PUBMED Abstract]
- Furuse K, Fukuoka M, Kawahara M, et al.: Phase III study of concurrent versus sequential thoracic radiotherapy in combination with mitomycin, vindesine, and cisplatin in unresectable stage III non-small-cell lung cancer. J Clin Oncol 17 (9): 2692-9, 1999.[PUBMED Abstract]
- Fournel P, Robinet G, Thomas P, et al.: Randomized phase III trial of sequential chemoradiotherapy compared with concurrent chemoradiotherapy in locally advanced non-small-cell lung cancer: Groupe Lyon-Saint-Etienne d'Oncologie Thoracique-Groupe Français de Pneumo-Cancérologie NPC 95-01 Study. J Clin Oncol 23 (25): 5910-7, 2005.[PUBMED Abstract]
- Curran WJ, Paulus R, Langer CJ, et al.: Sequential vs. concurrent chemoradiation for stage III non-small cell lung cancer: randomized phase III trial RTOG 9410. J Natl Cancer Inst 103 (19): 1452-60, 2011.[PUBMED Abstract]
- Zatloukal P, Petruzelka L, Zemanova M, et al.: Concurrent versus sequential chemoradiotherapy with cisplatin and vinorelbine in locally advanced non-small cell lung cancer: a randomized study. Lung Cancer 46 (1): 87-98, 2004.[PUBMED Abstract]
- Rosenman JG, Halle JS, Socinski MA, et al.: High-dose conformal radiotherapy for treatment of stage IIIA/IIIB non-small-cell lung cancer: technical issues and results of a phase I/II trial. Int J Radiat Oncol Biol Phys 54 (2): 348-56, 2002.[PUBMED Abstract]
- Socinski MA, Blackstock AW, Bogart JA, et al.: Randomized phase II trial of induction chemotherapy followed by concurrent chemotherapy and dose-escalated thoracic conformal radiotherapy (74 Gy) in stage III non-small-cell lung cancer: CALGB 30105. J Clin Oncol 26 (15): 2457-63, 2008.[PUBMED Abstract]
- Bradley JD, Bae K, Graham MV, et al.: Primary analysis of the phase II component of a phase I/II dose intensification study using three-dimensional conformal radiation therapy and concurrent chemotherapy for patients with inoperable non-small-cell lung cancer: RTOG 0117. J Clin Oncol 28 (14): 2475-80, 2010.[PUBMED Abstract]
- Bradley JD, Paulus R, Komaki R, et al.: Standard-dose versus high-dose conformal radiotherapy with concurrent and consolidation carboplatin plus paclitaxel with or without cetuximab for patients with stage IIIA or IIIB non-small-cell lung cancer (RTOG 0617): a randomised, two-by-two factorial phase 3 study. Lancet Oncol 16 (2): 187-99, 2015.[PUBMED Abstract]
- Senan S, Brade A, Wang LH, et al.: PROCLAIM: Randomized Phase III Trial of Pemetrexed-Cisplatin or Etoposide-Cisplatin Plus Thoracic Radiation Therapy Followed by Consolidation Chemotherapy in Locally Advanced Nonsquamous Non-Small-Cell Lung Cancer. J Clin Oncol 34 (9): 953-62, 2016.[PUBMED Abstract]
- Vokes EE, Herndon JE, Kelley MJ, et al.: Induction chemotherapy followed by chemoradiotherapy compared with chemoradiotherapy alone for regionally advanced unresectable stage III Non-small-cell lung cancer: Cancer and Leukemia Group B. J Clin Oncol 25 (13): 1698-704, 2007.[PUBMED Abstract]
- Antonia SJ, Villegas A, Daniel D, et al.: Durvalumab after Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. N Engl J Med 377 (20): 1919-1929, 2017.[PUBMED Abstract]
- Hanna N, Neubauer M, Yiannoutsos C, et al.: Phase III study of cisplatin, etoposide, and concurrent chest radiation with or without consolidation docetaxel in patients with inoperable stage III non-small-cell lung cancer: the Hoosier Oncology Group and U.S. Oncology. J Clin Oncol 26 (35): 5755-60, 2008.[PUBMED Abstract]
- Kelly K, Chansky K, Gaspar LE, et al.: Phase III trial of maintenance gefitinib or placebo after concurrent chemoradiotherapy and docetaxel consolidation in inoperable stage III non-small-cell lung cancer: SWOG S0023. J Clin Oncol 26 (15): 2450-6, 2008.[PUBMED Abstract]
- Butts C, Socinski MA, Mitchell PL, et al.: Tecemotide (L-BLP25) versus placebo after chemoradiotherapy for stage III non-small-cell lung cancer (START): a randomised, double-blind, phase 3 trial. Lancet Oncol 15 (1): 59-68, 2014.[PUBMED Abstract]
- Rusch VW: Management of Pancoast tumours. Lancet Oncol 7 (12): 997-1005, 2006.[PUBMED Abstract]
- Narayan S, Thomas CR: Multimodality therapy for Pancoast tumor. Nat Clin Pract Oncol 3 (9): 484-91, 2006.[PUBMED Abstract]
- Rusch VW, Parekh KR, Leon L, et al.: Factors determining outcome after surgical resection of T3 and T4 lung cancers of the superior sulcus. J Thorac Cardiovasc Surg 119 (6): 1147-53, 2000.[PUBMED Abstract]
- Kunitoh H, Kato H, Tsuboi M, et al.: Phase II trial of preoperative chemoradiotherapy followed by surgical resection in patients with superior sulcus non-small-cell lung cancers: report of Japan Clinical Oncology Group trial 9806. J Clin Oncol 26 (4): 644-9, 2008.[PUBMED Abstract]
- Rusch VW, Giroux DJ, Kraut MJ, et al.: Induction chemoradiation and surgical resection for superior sulcus non-small-cell lung carcinomas: long-term results of Southwest Oncology Group Trial 9416 (Intergroup Trial 0160). J Clin Oncol 25 (3): 313-8, 2007.[PUBMED Abstract]
- Matsuoka H, Nishio W, Okada M, et al.: Resection of chest wall invasion in patients with non-small cell lung cancer. Eur J Cardiothorac Surg 26 (6): 1200-4, 2004.[PUBMED Abstract]
- Facciolo F, Cardillo G, Lopergolo M, et al.: Chest wall invasion in non-small cell lung carcinoma: a rationale for en bloc resection. J Thorac Cardiovasc Surg 121 (4): 649-56, 2001.[PUBMED Abstract]
- Doddoli C, D'Journo B, Le Pimpec-Barthes F, et al.: Lung cancer invading the chest wall: a plea for en-bloc resection but the need for new treatment strategies. Ann Thorac Surg 80 (6): 2032-40, 2005.[PUBMED Abstract]
- Cochrane Collaborationにより、早期(I-IIIA期)肺がんに対して外科的介入を受けた計1,910人の患者に関する11件のランダム化試験がレビューされた。[
3
]3件の試験のプール解析では、以下が報告された:
- IIIB期およびIIIC期NSCLCの治療
-
Surveillance, Epidemiology, and End Results(SEER)プログラムの登録に基づくと、IIIB期の非小細胞肺がん(NSCLC)の推定発生率は17.6%である。[ 1 ]臨床病期がIIIB期のNSCLCを呈する患者の大多数に対して予想される5年生存率は、3~7%である。[ 2 ]小規模なケースシリーズによると、T4、N0~1の特定の患者では、原発肺葉内にある衛星腫瘍結節のみによる結果として、5年生存率が20%であったことが報告されている。[ 3 ][ 4 ][証拠レベル:3iiiA]
IIIB期およびIIIC期NSCLCに対する標準治療法の選択肢
IIIB期NSCLCおよびIIIC期NSCLCに対する標準治療法の選択肢には、以下のものがある:
一般に、IIIB期およびIIIC期のNSCLC患者は、手術単独では利益が得られず、初回化学療法、化学療法と放射線療法の併用、または放射線療法単独により最も良好に管理されるが、以下の条件にもよる:
- 腫瘍浸潤部位。
- 患者のパフォーマンスステータス(PS)。
PSが優れている患者のほとんどは集学的な化学療法と放射線療法に適格であるが、以下は例外である:
- T4、N0の特定の患者は、上溝腫瘍患者と同様に集学的治療および手術により治療してもよい。
化学療法と放射線療法の順次施行または同時併用
切除不能なIII期のNSCLC患者を対象とした多くのランダム化研究で、シスプラチンをベースとした化学療法と胸部放射線療法の術前または同時併用による治療に関連して、放射線療法単独を用いる治療と比べて生存が改善することが示されている。切除不能なIIIB期またはIIIC期疾患を有する患者は放射線療法により利益が得られる可能性があるが、長期的な転帰は一般に不良で、しばしば局所的および全身的に再燃する結果となる。放射線療法への逐次的および同時化学療法の追加が、複数のプロスペクティブ・ランダム化試験で評価されている。
証拠(化学療法と放射線療法の順次施行または同時併用):
- 11件のランダム化臨床試験による患者データを対象としたメタアナリシスでは、以下が示された:[
5
]
- シスプラチンをベースとした併用化学療法と放射線療法により、放射線療法単独と比べ死亡リスクが10%低下した。[ 5 ][証拠レベル:1iiA]
- 13件の試験を対象としたメタアナリシスでは(2,214人の評価可能患者を基に)、以下が示された:[
6
]
- 根治的放射線療法に加えて化学療法を同時併用することで、2年時点の死亡リスクが低下した(相対リスク[RR]、0.93;95%信頼区間[CI]、0.88-0.98;P = 0.01)。
- プラチナ製剤をベースにした化学療法を用いた11件の試験では、RRは0.93(95%CI、0.87-0.99;P = 0.02)であった。[ 6 ]
- 1,764人の患者から得られた個々のデータを対象にしたメタアナリシスで、9件の試験が評価された。[
7
]
- 放射線療法と化学療法による治療を受けた患者におけるハザード比(HR)死亡は、放射線療法単独と比較して0.89(95%CI、0.81-0.98;P = 0.02)であり、化学療法による2年時点の絶対的有益性が4%であることに相当していた。
- プラチナ製剤とエトポシドの併用は、プラチナ製剤単独よりも有効と思われた。プラチナ製剤をベースにした化学療法と放射線の同時併用により、局所的に進行したNSCLC患者の生存が改善する可能性がある。しかしながら、こうした潜在的な治療の有益性の大きさおよび化学療法の最適な投与スケジュールを正確に決定するには、利用可能なデータが不十分である。[ 7 ]
- 2件のランダム化試験(RTOG-9410[NCT01134861]を含む)および1件のメタアナリシスの結果は、化学療法と放射線療法の同時併用の方が化学療法と放射線療法の順次施行より毒性作用が大きいにもかかわらず、得られる生存利益が大きいことを示している。[
8
][
9
][
10
][証拠レベル:1iiA]
- 第一の試験では、マイトマイシンC、ビンデシン、およびシスプラチンの併用療法と、スプリットコースの連日の放射線療法を56Gyまで同時併用して、化学療法後に連日の放射線療法を56Gyまで継続する群と比較した。[
8
]
- 5年全生存率(OS)は、同時併用の方が良好であった(27% vs 9%)。
- 骨髄抑制は同時療法群の患者で大きかったが、治療関連死亡率は両治療群で1%未満であった。[ ]
- 第2の試験では、610人の患者を、シスプラチンおよびビンブラスチンによる化学療法後に63Gyの放射線療法を実施する順次施行群、同じレジメンを用いた同時化学放射線療法群、またはシスプラチンおよびエトポシドによる化学療法と1日2回の放射線療法の同時併用群のいずれかにランダムに割り付けた。[
9
][
10
]
- 生存期間中央値および5年生存率は、連日の放射線療法と化学療法の同時併用群が優れていた(順次施行レジメンとの比較で、それぞれ17ヵ月 vs 14.6ヵ月、および16% vs 10%[P = 0.046])。
- 2件のより小規模な研究もまた、順次の化学療法および放射線療法よりも同時化学療法および放射線療法を支持するOSの結果を報告したが、この結果は統計的に有意ではなかった。[ 10 ][証拠レベル:1iiA];[ 11 ]
- 第一の試験では、マイトマイシンC、ビンデシン、およびシスプラチンの併用療法と、スプリットコースの連日の放射線療法を56Gyまで同時併用して、化学療法後に連日の放射線療法を56Gyまで継続する群と比較した。[
8
]
- 3件の試験を対象としたメタアナリシス(患者711人)で、同時併用と順次施行が評価された。[
6
]
- この解析では、順次施行に対して同時併用で有意な有益性が示された(RR、0.86;95%CI、0.78-0.95;P = 0.003)。すべての研究でシスプラチンをベースにしたレジメンおよび1日1回の放射線療法が用いられた。[ 6 ]
- 同時併用群では死亡が多く(全体で3%)報告されたが、統計的有意差には至らなかった(RR、1.60;CI、0.75-3.44;P = 0.2)。
- 急性食道炎(グレード3以上)は、同時併用群(範囲、17~26%)の方が順次施行群(範囲、0~4%;RR、6.77;P = 0.001)より多く認められた。全体で、好中球減少(グレード3以上)の発生は両群でほぼ同じであった。
同時化学放射線療法における放射線療法の線量増加
腫瘍のモーション管理や画像ガイダンスなど、1990年代における放射線療法の送達技術が改善されて、第I/II相試験では、化学療法と同時に実施する放射線療法の線量を74Gyまで増加させられることが実証された。[ 12 ][ 13 ][ 14 ]しかしながら、従来の60Gyの線量 vs 週1回のカルボプラチン/パクリタキセルを同時に実施する74Gyまでの線量増加に関する第III相試験では、局所制御または無増悪生存(PFS)の改善は実証されず、OSは線量増加により悪化した(HR、1.38[1.09-1.76];P = 0.004)。線量増加によりグレード5のイベントの有意ではない増加(10% vs 2%)が認められ、グレード3の食道炎の発生率は増加した(21% vs 7%;P = 0.0003)。[ 15 ][証拠レベル:1iiA]
化学療法と放射線療法の同時併用前または後の追加の全身療法
化学療法と放射線療法の同時併用前の導入化学療法の追加によって、生存が改善することは示されていない。[ 16 ][証拠レベル:1iiA]
地固め免疫療法
デュルバルマブ
デュルバルマブは選択的ヒトIgG1モノクローナル抗体で、プログラム細胞死リガンド1(PD-L1)のプログラム細胞死1(PD-1)およびCD80への結合を遮断し、T細胞が腫瘍細胞を認識して殺すことができるようにする。[ 17 ]
証拠(デュルバルマブ):
- 第III相PACIFIC試験(NCT02125461)には、III期NSCLCで疾患が2サイクル以上のプラチナ製剤ベースの化学放射線療法後に増悪していない713人の患者が登録した。患者は2:1の比率で、デュルバルマブ(10mg/kg、静注)またはプラセボ(最大12ヵ月間2週間ごとに投与)を受けるようにランダムに割り付けられた。[
17
]複合主要エンドポイントは、盲検下での独立中央判定によるPFSおよびOS(中間解析時には予定されていなかった)であった。
- 中間解析時に、複合主要エンドポイントのPFSが達成された。PFS中央値は、デュルバルマブ群で16.8ヵ月であったのに対し、プラセボ群で5.6ヵ月であった(HR、0.52;95%CI、0.42-0.65;P < 0.001)。[ ][証拠レベル:1iiDiii]18ヵ月PFS率は、デュルバルマブ群で44.2% vs プラセボ群で27%であった。
- PFSの有益性は事前に規定されたすべてのサブグループで示され、化学放射線療法前のPD-L1の発現または喫煙状態とは関係がなかった。上皮成長因子受容体(EGFR)変異が6%の患者で観察された(デュルバルマブで治療された29人 vs プラセボで治療された14人)。EGFRが変異したサブグループに対する非層別化HRは、0.76(95%CI、0.35-1.64)であった。
- グレード3または4の有害事象はデュルバルマブで治療された患者の29.9%に起こり、プラセボで治療された患者では26.1%に起こった。最も一般的なグレード3または4の有害事象は、デュルバルマブで治療された患者の4.4%およびプラセボで治療された患者の3.8%に起こった肺炎であった。
- 中間解析時にOSは評価されていなかった。
他の全身地固め療法
ドセタキセル[ 18 ]、ゲフィチニブ[ 19 ]、およびtecemotide(MUC1抗原特異的免疫療法)[ 20 ]を含む他の地固め全身療法に関するランダム化試験では、OSの改善は示されていない。[証拠レベル:1iiA]
切除不能なNSCLCに対する化学療法と放射線療法の同時併用後の地固め全身療法の役割は、不明のままである。従来の化学療法(ドセタキセル)[ 18 ]、チロシンキナーゼ阻害薬(ゲフィチニブ)[ 19 ]、および免疫療法(tecemotide:MUC1抗原特異的免疫療法)[ 20 ]を含む地固め全身療法に関する第III相試験では、OSの改善は示されていない。[証拠レベル:1iiA]
放射線療法単独
化学療法に適さない患者における局所的に進行した切除不能な腫瘍の治療として。
放射線療法の単独実施、化学療法との逐次的照射または同時照射は、局所進行切除不能III期NSCLC患者に利益をもたらす場合がある。しかしながら、同時に実施する併用化学放射線療法は生存において最大の利益をもたらすが、毒性作用の増加を伴う。
予後:
従来の線量および分割スケジュール(6~7週間で60~70Gyに対して1.8~2.0Gy/分割/日)を用いた放射線療法により、患者の5~10%に再現性のある長期的な生存利益が得られ、有意な症状緩和がもたらされる。[ 21 ]
証拠(局所的に進行した切除不能腫瘍に対する放射線療法):
- 1件のプロスペクティブ・ランダム化臨床試験では、以下が示された:
- 1日に3分割照射する放射線療法では、1日に単回照射する放射線療法と比べ、OSが改善した。[ 22 ][証拠レベル:1iiA]
- 放射線療法単独で治療された患者に対する失敗のパターンは、局所領域および遠隔の両方の失敗を含んでいた。
緩和療法が必要な患者に対して
放射線療法は、NSCLCの局所浸潤による次のような症状の緩和に有効な場合がある:
- 気管、食道、または気管支の圧迫。
- 疼痛。
- 声帯麻痺。
- 喀血。
- 上大静脈症候群。
症例によっては、気管支内レーザー療法および/または近接照射療法が、近位の閉塞病変を改善するために使用されている。[ 23 ]
証拠(緩和療法としての放射線療法):
- 系統的レビューにより、高線量率気管支内近接照射療法(HDREB)単独、または外照射療法(EBRT)またはレーザー療法との併用に関する6件のランダム化試験が確認された。[
24
]
- EBRT単独を使用した治療を以前に受けていない患者では、より良好な全体的な症状緩和が得られ、再治療を必要とすることがより少なかった。[ 24 ][証拠レベル:1iiC]
- HDREBは、技術的に実施可能な場合に、以前にEBRTで治療されたが再発した症状を認める気管支内閉塞患者に緩和をもたらした。
- EBRTは症状緩和目的で頻繁に処方されるが、分割照射法をいつ使うべきかについてのコンセンサスは得られていない。
- 多分割のレジメンが異なっていても、同様な症状緩和が得られると考えられるが[ 25 ][ 26 ][ 27 ][ 28 ][ 29 ][ 30 ]、National Cancer Institute of Canada Clinical Trials Group試験(NCT00003685)で示されたように、単回照射療法は少分割または標準のレジメンと比べ、症状緩和には不十分な可能性がある。[ 27 ][証拠レベル:1iiC]
- 高線量放射線療法を施行した患者では、PSが良好なほど生存がわずかに長いという証拠が得られている。[ 25 ][ 26 ][証拠レベル:1iiA]
IIIB期またはIIIC期のPSが不良な患者は、肺に関連する症状(例、咳嗽、息切れ、喀血、または疼痛)を緩和するための胸部放射線療法の候補である。[ 21 ][証拠レベル:3iiiC](詳しい情報については、心肺症候群およびがん性疼痛に関するPDQ要約を参照のこと。)
臨床評価段階にある治療法の選択肢
IIIB期またはIIIC期のNSCLC患者は、全体的な治療結果が不良なため、臨床試験が勧められ、病勢コントロールの改善につながる場合がある。
臨床評価段階にある治療法の選択肢には以下のものがある:
- 新しい分割照射スケジュール。
- 放射線増感剤(NCT02186847)。
- 集学的アプローチ。
- EGFR変異またはALK転座腫瘍を有する患者において集学的治療への標的薬物の組み込み(RTOG-1306[NCT01822496];11-464[NCT01553942])。
- 治療中にポジトロン放射断層撮影に基づいて反応を評価する適応放射線治療(RTOG-1106/ACRIN-6697)。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Wisnivesky JP, Yankelevitz D, Henschke CI: Stage of lung cancer in relation to its size: part 2. Evidence. Chest 127 (4): 1136-9, 2005.[PUBMED Abstract]
- Mountain CF: Revisions in the International System for Staging Lung Cancer. Chest 111 (6): 1710-7, 1997.[PUBMED Abstract]
- Deslauriers J, Brisson J, Cartier R, et al.: Carcinoma of the lung. Evaluation of satellite nodules as a factor influencing prognosis after resection. J Thorac Cardiovasc Surg 97 (4): 504-12, 1989.[PUBMED Abstract]
- Urschel JD, Urschel DM, Anderson TM, et al.: Prognostic implications of pulmonary satellite nodules: are the 1997 staging revisions appropriate? Lung Cancer 21 (2): 83-7; discussion 89-91, 1998.[PUBMED Abstract]
- Chemotherapy in non-small cell lung cancer: a meta-analysis using updated data on individual patients from 52 randomised clinical trials. Non-small Cell Lung Cancer Collaborative Group. BMJ 311 (7010): 899-909, 1995.[PUBMED Abstract]
- Rowell NP, O'rourke NP: Concurrent chemoradiotherapy in non-small cell lung cancer. Cochrane Database Syst Rev (4): CD002140, 2004.[PUBMED Abstract]
- Aupérin A, Le Péchoux C, Pignon JP, et al.: Concomitant radio-chemotherapy based on platin compounds in patients with locally advanced non-small cell lung cancer (NSCLC): a meta-analysis of individual data from 1764 patients. Ann Oncol 17 (3): 473-83, 2006.[PUBMED Abstract]
- Furuse K, Fukuoka M, Kawahara M, et al.: Phase III study of concurrent versus sequential thoracic radiotherapy in combination with mitomycin, vindesine, and cisplatin in unresectable stage III non-small-cell lung cancer. J Clin Oncol 17 (9): 2692-9, 1999.[PUBMED Abstract]
- Curran WJ, Paulus R, Langer CJ, et al.: Sequential vs. concurrent chemoradiation for stage III non-small cell lung cancer: randomized phase III trial RTOG 9410. J Natl Cancer Inst 103 (19): 1452-60, 2011.[PUBMED Abstract]
- Fournel P, Robinet G, Thomas P, et al.: Randomized phase III trial of sequential chemoradiotherapy compared with concurrent chemoradiotherapy in locally advanced non-small-cell lung cancer: Groupe Lyon-Saint-Etienne d'Oncologie Thoracique-Groupe Français de Pneumo-Cancérologie NPC 95-01 Study. J Clin Oncol 23 (25): 5910-7, 2005.[PUBMED Abstract]
- Zatloukal P, Petruzelka L, Zemanova M, et al.: Concurrent versus sequential chemoradiotherapy with cisplatin and vinorelbine in locally advanced non-small cell lung cancer: a randomized study. Lung Cancer 46 (1): 87-98, 2004.[PUBMED Abstract]
- Rosenman JG, Halle JS, Socinski MA, et al.: High-dose conformal radiotherapy for treatment of stage IIIA/IIIB non-small-cell lung cancer: technical issues and results of a phase I/II trial. Int J Radiat Oncol Biol Phys 54 (2): 348-56, 2002.[PUBMED Abstract]
- Socinski MA, Blackstock AW, Bogart JA, et al.: Randomized phase II trial of induction chemotherapy followed by concurrent chemotherapy and dose-escalated thoracic conformal radiotherapy (74 Gy) in stage III non-small-cell lung cancer: CALGB 30105. J Clin Oncol 26 (15): 2457-63, 2008.[PUBMED Abstract]
- Bradley JD, Bae K, Graham MV, et al.: Primary analysis of the phase II component of a phase I/II dose intensification study using three-dimensional conformal radiation therapy and concurrent chemotherapy for patients with inoperable non-small-cell lung cancer: RTOG 0117. J Clin Oncol 28 (14): 2475-80, 2010.[PUBMED Abstract]
- Bradley JD, Paulus R, Komaki R, et al.: Standard-dose versus high-dose conformal radiotherapy with concurrent and consolidation carboplatin plus paclitaxel with or without cetuximab for patients with stage IIIA or IIIB non-small-cell lung cancer (RTOG 0617): a randomised, two-by-two factorial phase 3 study. Lancet Oncol 16 (2): 187-99, 2015.[PUBMED Abstract]
- Vokes EE, Herndon JE, Kelley MJ, et al.: Induction chemotherapy followed by chemoradiotherapy compared with chemoradiotherapy alone for regionally advanced unresectable stage III Non-small-cell lung cancer: Cancer and Leukemia Group B. J Clin Oncol 25 (13): 1698-704, 2007.[PUBMED Abstract]
- Antonia SJ, Villegas A, Daniel D, et al.: Durvalumab after Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. N Engl J Med 377 (20): 1919-1929, 2017.[PUBMED Abstract]
- Hanna N, Neubauer M, Yiannoutsos C, et al.: Phase III study of cisplatin, etoposide, and concurrent chest radiation with or without consolidation docetaxel in patients with inoperable stage III non-small-cell lung cancer: the Hoosier Oncology Group and U.S. Oncology. J Clin Oncol 26 (35): 5755-60, 2008.[PUBMED Abstract]
- Kelly K, Chansky K, Gaspar LE, et al.: Phase III trial of maintenance gefitinib or placebo after concurrent chemoradiotherapy and docetaxel consolidation in inoperable stage III non-small-cell lung cancer: SWOG S0023. J Clin Oncol 26 (15): 2450-6, 2008.[PUBMED Abstract]
- Butts C, Socinski MA, Mitchell PL, et al.: Tecemotide (L-BLP25) versus placebo after chemoradiotherapy for stage III non-small-cell lung cancer (START): a randomised, double-blind, phase 3 trial. Lancet Oncol 15 (1): 59-68, 2014.[PUBMED Abstract]
- Langendijk JA, ten Velde GP, Aaronson NK, et al.: Quality of life after palliative radiotherapy in non-small cell lung cancer: a prospective study. Int J Radiat Oncol Biol Phys 47 (1): 149-55, 2000.[PUBMED Abstract]
- Komaki R, Cox JD, Hartz AJ, et al.: Characteristics of long-term survivors after treatment for inoperable carcinoma of the lung. Am J Clin Oncol 8 (5): 362-70, 1985.[PUBMED Abstract]
- Miller JI, Phillips TW: Neodymium:YAG laser and brachytherapy in the management of inoperable bronchogenic carcinoma. Ann Thorac Surg 50 (2): 190-5; discussion 195-6, 1990.[PUBMED Abstract]
- Ung YC, Yu E, Falkson C, et al.: The role of high-dose-rate brachytherapy in the palliation of symptoms in patients with non-small-cell lung cancer: a systematic review. Brachytherapy 5 (3): 189-202, 2006 Jul-Sep.[PUBMED Abstract]
- Sundstrøm S, Bremnes R, Aasebø U, et al.: Hypofractionated palliative radiotherapy (17 Gy per two fractions) in advanced non-small-cell lung carcinoma is comparable to standard fractionation for symptom control and survival: a national phase III trial. J Clin Oncol 22 (5): 801-10, 2004.[PUBMED Abstract]
- Lester JF, Macbeth FR, Toy E, et al.: Palliative radiotherapy regimens for non-small cell lung cancer. Cochrane Database Syst Rev (4): CD002143, 2006.[PUBMED Abstract]
- Bezjak A, Dixon P, Brundage M, et al.: Randomized phase III trial of single versus fractionated thoracic radiation in the palliation of patients with lung cancer (NCIC CTG SC.15). Int J Radiat Oncol Biol Phys 54 (3): 719-28, 2002.[PUBMED Abstract]
- Erridge SC, Gaze MN, Price A, et al.: Symptom control and quality of life in people with lung cancer: a randomised trial of two palliative radiotherapy fractionation schedules. Clin Oncol (R Coll Radiol) 17 (1): 61-7, 2005.[PUBMED Abstract]
- Kramer GW, Wanders SL, Noordijk EM, et al.: Results of the Dutch National study of the palliative effect of irradiation using two different treatment schemes for non-small-cell lung cancer. J Clin Oncol 23 (13): 2962-70, 2005.[PUBMED Abstract]
- Senkus-Konefka E, Dziadziuszko R, Bednaruk-Młyński E, et al.: A prospective, randomised study to compare two palliative radiotherapy schedules for non-small-cell lung cancer (NSCLC). Br J Cancer 92 (6): 1038-45, 2005.[PUBMED Abstract]
- 新たに診断されたIV期、再燃および再発したNSCLCの治療
-
新たに非小細胞肺がん(NSCLC)と診断される患者の40%がIV期である。治療目標は、生存延長および疾患関連症状のコントロールである。治療法の選択肢には、細胞毒性化学療法、標的薬物、および免疫療法がある。治療選択に影響する因子には、併存疾患、パフォーマンスステータス(PS)、組織型、およびがんの分子遺伝的および免疫学的特徴が含まれる。したがって、治療を開始する前に腫瘍のゲノム変化およびプログラム死リガンド1(PD-L1)発現の評価が必須である。一般的に、症状緩和目的で放射線療法および手術が特定の症例に使用される。
治療の決定因子
IV期でPSが良好な患者を対象としたランダム化比較試験では、シスプラチンをベースとした化学療法により生存が改善し、疾患関連症状が緩和されることが示されている。[ 1 ][証拠レベル:1iiA]組織型が非扁平上皮性で、PSが良好な、喀血または他の出血の既往がない患者、あるいは心血管イベントの既往が最近ない患者では、パクリタキセルおよびカルボプラチンにベバシズマブを追加することで利益が得られる場合がある。腫瘍にEGFRのエクソン19または21において感受性を増加させる突然変異を有する患者で、特に東アジア出身の患者、喫煙歴がない患者、および腺がん患者では、第一選択または第二選択の化学療法の代替として、EGFRチロシンキナーゼ阻害薬(TKI)により利益が得られる場合がある。腫瘍に未分化リンパ腫キナーゼ(ALK)転座、ROS1再構成、または神経栄養性チロシン受容体キナーゼ(NTRK)融合が認められる患者は、第一選択または第二選択の化学療法の代替として、ALK、ROS1、またはNTRK阻害薬により利益が得られる場合がある。腫瘍がPD-L1(免疫組織化学で50%超)を発現している患者は、ペムブロリズマブにより生存が改善している。進行した非扁平上皮肺がんに対するカルボプラチン + ペメトレキセド化学療法へのペムブロリズマブの追加により、PD-L1発現に関係なく生存が改善する。[ 2 ][証拠レベル:1iiA]PSが良好な(第一選択治療の設定で次に示すものと同じまたは類似の薬物が投与されていない)患者では、PD-L1陽性腫瘍に対してニボルマブ、ドセタキセル、ペメトレキセド、またはペムブロリズマブによる第二選択全身療法でも生存が改善する。[ 1 ][証拠レベル:1iiA]
Eastern Cooperative Oncology GroupのPSが2より劣る患者における全身療法の役割は、はっきりしていない。
組織像
腺がん患者は、ペメトレキセド[ 3 ]およびベバシズマブのほか、ペムブロリズマブとの併用化学療法により利益が得られる場合がある。
年齢 vs 併存疾患
証拠は、PSが良好で併存疾患が限られた高齢患者は併用化学療法から利益が得られうるという考えを裏付けている。進行したNSCLC患者では、年齢のみで治療に関する決定を下すべきではない。PSが良好な高齢患者は、支持療法単独と比較して化学療法で治療される場合に、より長期の生存およびより良好な生活の質を享受する。臨床試験に登録されている80歳以上の患者がきわめて少数であるという理由だけで、高齢患者(70~79歳)のデータを80歳以上の患者に外挿する場合は注意すべきであり、この集団における有益性は明らかではない。[ 4 ][ 5 ]
証拠(年齢 vs 併存疾患):
- 支持療法または単剤療法と比較した場合、プラチナ製剤を含む併用化学療法レジメンは臨床的有益性をもたらす;しかしながら、一部の高齢患者においては、加齢に伴う多くの臓器の機能予備能の低下および/または合併疾患のために、こうした治療が禁忌となりうる。NSCLC患者の約3分の2が65歳以上で、約40%が70歳以上である。[ 6 ]Surveillance, Epidemiology, and End Results(SEER)データでは、70歳以上の患者が占める割合は50%に近いことが示唆される。
- 1994年から1999年のSEER Medicareデータのレビューにより、全集団に対して期待されているよりも化学療法使用の割合ははるかに低いことが明らかにされた。[ 7 ]同じデータで高齢患者は、併存疾患が多い場合、または機能不全の割合が高い場合があり、研究への参加が禁忌でなくても困難になることが示唆されている;臨床試験データがないために、標準的化学療法による個々の患者の治療決定が影響を受ける可能性がある。
- 単剤の化学療法および併用化学療法は、少なくとも一部の高齢患者に明らかに利益をもたらす。Elderly Lung Cancer Vinorelbine Italian Studyでは、70歳を過ぎた患者154人をビノレルビンまたは支持療法のいずれかにランダムに割り付けた。[
8
]
- ビノレルビンで治療された患者の1年生存率が32%であったのに対し、支持療法単独で治療された患者では14%であった。生活の質のパラメータもまた化学療法群で有意に改善され、毒性作用は受け入られる程度であった。
- 日本の試験で、PSが良好な高齢患者180人における単剤のドセタキセルとビノレルビンとが比較された。[
9
]
- 奏効率(22% vs 10%)および無増悪生存(PFS)期間(5.4ヵ月 vs 3.1ヵ月)はドセタキセルで有意に良好であったが、生存期間中央値(14.3ヵ月 vs 9.9ヵ月)および1年生存率(59% vs 37%)は統計的に有意ではなかった。
- 2剤併用療法の大規模ランダム化試験に参加した患者で、若年齢層(70歳未満)と高年齢層(70歳以上)を分析・比較したレトロスペクティブ・データでも、高年齢層の患者の方が骨髄における毒性作用のリスクが高いが、同様な生存利益が得られる可能性があることを示している。[ 4 ][ 5 ][ 10 ][ 11 ][ 12 ][ 13 ]
パフォーマンスステータス
PSは、NSCLC患者の生存に対する最も重要な予後因子の1つである。[ 14 ]この患者集団に対する治療の有益性は、レトロスペクティブ分析およびプロスペクティブ臨床試験で評価されている。
このような結果は、転移性または局所進行性の非小細胞肺がん(NSCLC)に対する化学療法アプローチのさらなる評価を支持している;しかしながら、現在のプラチナ製剤をベースにした併用化学療法の効力からは、特定のレジメンを標準療法とみなすことができないという状況である。臨床試験以外では、化学療法は、PSが良好で評価可能病変を有する患者が、予想されるリスクと限られた利益に関する十分な説明を受けた後にこのような治療を望む場合のみに行うべきである。
証拠(PS):
- カルボプラチンとパクリタキセルをパクリタキセル単剤と比較したCancer and Leukemia Group B試験(CLB-9730[NCT00003117])では、PSが2の患者99人(研究対象集団の18%)が登録された。[
12
]
- 生存期間中央値8.8ヵ月および1年生存率38%であった、PSが0~1の患者と比較して、PSが2の患者の対応する生存期間中央値は3.0ヵ月および1年生存率は14%であった;これにより、低調なPSは予後不良をもたらすことが実証されている。これらの差は統計的に有意であった。
- PSが2の患者を治療群別に分析した場合、併用化学療法を受けた患者は、単剤のパクリタキセルで治療された患者と比較して、奏効率が有意に高く(24% vs 10%)、生存期間中央値が有意に長く(4.7ヵ月 vs 2.4ヵ月)、1年生存率が有意に優れていた(18% vs 10%)。[ 12 ]
- 1件の第III相試験では、PSが2で過去に化学療法を受けたことがない患者205人においてペメトレキセド単剤とカルボプラチンおよびペメトレキセドの併用とが比較された。[
15
][証拠レベル:1iiA]
- 全生存(OS)期間中央値は、ペメトレキセド単剤群で5.3ヵ月、カルボプラチンおよびペメトレキセド併用群で9.3ヵ月であった(ハザード比[HR]、0.62;95%信頼区間[CI]、0.46-0.83;P = 0.001)。
- PFS中央値は、ペメトレキセド単剤群で2.8ヵ月、カルボプラチンおよびペメトレキセド併用群で5.8ヵ月であった(P < 0.001)。
- 奏効率は、ペメトレキセド単剤群で10.3%、カルボプラチンおよびペメトレキセド併用群で23.8%であった(P = 0.032)。
- 副作用は、予想された通り併用群で頻度が高かった。
ブラジルの8施設および米国の1施設で実施されたこの研究では、OS率およびPFS率がほとんど(ただし、すべてではない)の他の発表されている研究で歴史的に示されたものよりも高かったことが報告された。これは患者選択における差を示している可能性がある。
- 1,200人以上の患者をプラチナ製剤をベースにした4つのレジメンにランダムに割り付けた試験からPSが2の患者68人のサブセット分析が発表されている。
- 最終解析では、PSが2の患者が経験した全体の毒性作用は、5件の死亡を含め有害事象の発生率が高かったにもかからず、PSが0~1の患者が経験したものと有意差は認められなかった。
- 有効性解析では、全奏効率が14%、生存期間中央値が4.1ヵ月、1年生存率が19%であることが実証された;すべて、PSが0~1の患者の方が、大幅に劣っていた。
- シスプラチン + ゲムシタビンおよびカルボプラチン +パクリタキセルの用量を減弱した第II相ランダム化試験(E-1599[NCT00006004])では、PSが2の患者が102人含まれていた。[
16
]
- シスプラチン + ゲムシタビン群における奏効率は25%およびカルボプラチン +パクリタキセル群では16%であった;生存期間中央値はシスプラチン + ゲムシタビン群で6.8ヵ月およびカルボプラチン +パクリタキセル群で6.1ヵ月であった;1年生存率はシスプラチン + ゲムシタビン群で25%およびカルボプラチン +パクリタキセル群で19%であった。これらの差はいずれも統計的に有意ではなかったが、生存の数値は歴史的対照に基づいて予想されるものよりも長かった。
- 2件の試験の結果から、PSが2の患者は症状の改善を経験する可能性があることが示唆されている。[ 17 ][ 18 ]
新たに診断されたIV期、再燃および再発したNSCLCに対する標準治療法の選択肢(第一選択治療)
新たに診断されたIV期、再燃および再発したNSCLC患者に対する標準治療法の選択肢には以下のものがある:
- プラチナ製剤(シスプラチンまたはカルボプラチン)ならびにパクリタキセル、ゲムシタビン、ドセタキセル、ビノレルビン、イリノテカン、蛋白結合パクリタキセル、またはペメトレキセドを用いた細胞毒性併用化学療法。
- モノクローナル抗体を併用する併用化学療法。
-
第一選択化学療法後の維持療法(プラチナ製剤をベースにした併用化学療法を4サイクル施行後に安定または反応を示している患者に対して)。
- 第一選択化学療法後の維持療法。
- 第一選択のプラチナ製剤をベースにした併用化学療法後のペメトレキセド。
- プラチナ製剤をベースにした2剤併用化学療法後の維持エルロチニブ。
-
上皮成長因子受容体(EGFR)チロシンキナーゼ阻害薬(TKI)(EGFR変異を有する患者に対して)。
-
未分化リンパ腫キナーゼ(ALK)阻害薬(ALK転座が認められる患者に対して)。
- アレクチニブ。
- クリゾチニブ。
- セリチニブ。
- brigatinib。
- ロルラチニブ。
-
BRAF V600EおよびMEK阻害薬(BRAF V600E変異を有する患者に対して)。
-
ROS1阻害薬(ROS1再構成が認められる患者に対して)。
-
神経栄養チロシンキナーゼ(NTRK)阻害薬(NTRK融合を有する患者に対して)。
-
化学療法を併用するまたは併用しない免疫チェックポイント阻害薬。
-
局所療法および特別な考慮事項。
- 気管支内レーザー療法および/または近接照射療法(閉塞病変に対して)。[ 19 ]
- 外照射療法(EBRT)(主に局所症候性腫瘍の増殖を一時的に緩和するため)。[ 20 ][ 21 ][ 22 ]
- 二次原発腫瘍の治療。
- 脳転移の治療。
細胞毒性併用化学療法
併用化学療法
進行期NSCLC患者の治療に用いられる化学療法薬の種類と数がランダム化比較試験およびメタアナリシスで広範囲に評価されている。
数件のランダム化試験で、進行期NSCLCの未治療患者におけるシスプラチンまたはカルボプラチンとさまざまな薬物との併用が評価されている。これらの試験のメタアナリシスに基づくと、以下の結論を導くことができる:
- いわゆる標的薬物を追加する特定の3剤併用は、優れた生存をもたらしうる。
- EGFR阻害薬は、EGFR変異を有する特定の患者に利益をもたらす可能性がある。
- 4サイクルのプラチナ製剤併用化学療法後の維持化学療法はPFSおよびOSを改善しうる。
- ビノレルビン、パクリタキセル、ドセタキセル、ゲムシタビン、イリノテカン、蛋白結合パクリタキセル、およびペメトレキセドとプラチナ製剤との併用は、生存において類似した改善をもたらす。毒性作用の種類および頻度は異なり、これにより個々の患者に望ましいレジメンが決定される。腺がん患者は、ペメトレキセドにより利益が得られる場合がある。
- シスプラチンおよびカルボプラチンは、治療成績では同様な改善をもたらすが、毒性作用は異なる。すべてではないが一部の試験およびこれらの試験のメタアナリシスでは、シスプラチンによる治療成績の方が優れている可能性があることを示唆しているが、ただ、吐き気および嘔吐など特定の毒性リスクが高い。
- プラチナ製剤を用いない併用療法はプラチナ製剤をベースにした化学療法よりも優位性をもたらさず、一部の研究では劣性が示されている。
- 一般的に使用される化学療法薬の3剤併用は、2剤併用よりも優れた生存をもたらさず、毒性がより強い。
証拠(併用化学療法):
- Cochrane Collaborationにより、1980年1月から2006年6月までに発表された、進行期NSCLC患者において2剤レジメンと単剤レジメンを比較したか、3剤レジメンと2剤レジメンを比較したすべてのランダム化比較試験のデータがレビューされた。[
23
]65試験(13,601人の患者)が確認された。
- 2剤併用レジメンと単剤レジメンを比較した試験では、2剤併用レジメンが良好であり、有意に高い腫瘍反応(オッズ比[OR]、0.42;95%CI、0.37-0.47;P < 0.001)および1年生存率(OR、0.80;95%CI、0.70-0.91;P < 0.001)が観察された。1年生存率における絶対的有益性は5%であったが、これは1年生存率が単剤レジメンによる30%から2剤レジメンによる35%へ増加したことに相当する。2剤レジメンを原因とするグレード3および4の毒性作用の割合は、単剤レジメン療法後の割合と比較して統計的に有意に増加し、ORは1.2~6.2であった。2剤レジメンでは感染症発生率の増加は認められなかった。
- 3剤レジメン vs 2剤レジメンについては、1年生存率における増加は認められなかった(OR、1.01;95%CI、0.85-1.21;P = 0.88)。生存率中央値は1.00であった(95%CI、0.94-1.06;P = 0.97)。
- 数件のメタアナリシスにより、シスプラチンまたはカルボプラチンレジメンがさまざまな結果について優れているかどうかが評価されている。[
24
][
25
][
26
]1件のメタアナリシスにより、9件のランダム化試験に登録された患者2,968人について、個々の患者データが報告された。[
24
]
- 客観的奏効率は、シスプラチンで治療された患者(30%)の方がカルボプラチンで治療された患者(24%)よりも高かった(OR、1.37;95%CI、1.16-1.61;P < 0.001)。
- カルボプラチンによる治療は、シスプラチンによる治療よりも死亡のハザードが統計的に有意ではないものの高かった(HR、1.07;95%CI、0.99-1.15;P = 0.100)。
- 非扁平上皮性腫瘍患者および第三世代の化学療法で治療された患者におけるカルボプラチンをベースにした化学療法は、死亡の統計的に有意な増加と関連した(非扁平上皮性腫瘍患者におけるHR、1.12;95%CI、1.01-1.23および第三世代の化学療法で治療された患者におけるHR、1.11;95%CI、1.01-1.21)。
- 治療関連毒性作用もまたメタアナリシスで評価された。カルボプラチンの方がシスプラチンによる治療よりも血小板減少が多くみられたが(12% vs 6%;OR、2.27;95%CI、1.71-3.01;P < 0.001)、シスプラチンは吐き気および嘔吐(8% vs 18%;OR、0.42;95%CI、0.33-0.53;P < 0.001)および腎毒性作用(0.5% vs 1.5%;OR、0.37;95%CI、0.15-0.88;P = 0.018)をより多く引き起こした。
- 著者らは、シスプラチンによる治療は重度の毒性作用の全体的なリスクにおける実質的な増加と関連していないと結論付けた。この包括的な個々の患者のメタアナリシスは、本質的には同じ臨床試験であるが発表されたデータのみを使用した臨床試験に基づく他のメタアナリシスの結論と一致している。
- 文献に基づいた3件のメタアナリシスでは、プラチナ製剤併用療法とプラチナ製剤以外の併用療法を比較した試験を対象に解析している。[
27
][
28
][
29
]
- 最初のメタアナリシスでは、7,633人の患者を含む評価可能な37件の試験が確認された。[
27
]
- 反応に対するORの62%の増加は、プラチナ製剤をベースにした治療法によるものであった(OR、1.62;95%CI、1.46-1.8;P < 0.001)。1年生存率はプラチナ製剤をベースにしたレジメンで5%高かった(34% vs 29%;OR、1.21;95%CI、1.09-1.35;P = 0.003)。
- プラチナ製剤療法と第三世代薬をベースとした併用レジメンを比較した場合、1年生存率において統計的に有意な増加は認められなかった(OR、1.11;95%CI、0.96-1.28;P = 0.17)。
- プラチナ製剤をベースにしたレジメンの毒性作用は、血液学的毒性作用、腎毒性作用、ならびに吐き気および嘔吐について有意に高かったが、神経毒性作用、発熱性好中球減少症の発生率、または毒性による死亡率については高くなかった。これらの結果は2番目の文献に基づくメタアナリシスと一致している。
- 第2のメタアナリシスでは、4,920人の患者を含む17件の試験が確認された。[
28
]
- プラチナ製剤をベースにした2剤併用レジメンの使用に関連して、1年生存率がわずかに高く(相対リスク[RR]、1.08;95%CI、1.01-1.16;P = 0.03)、部分奏効が良好(RR、1.11、95%CI、1.02-1.21;P = 0.02)であったが、貧血、吐き気、および神経毒性作用のリスクが高かった。
- サブアナリシスでは、シスプラチンをベースとした2剤併用レジメンにより、1年生存率(RR、1.16;95%CI、1.06-1.27;P = 0.001)、完全奏効(RR、2.29;95%CI、1.08-4.88;P = 0.03)、および部分奏効(RR、1.19;95%CI、1.07-1.32;P = 0.002)が改善したが、貧血、好中球減少症、神経毒性作用、および吐き気のリスクが高かった。
- 逆に、カルボプラチンをベースにした2剤レジメンでは、1年生存率は増加しなかった(RR、0.95;95%CI、0.85-1.07;P = 0.43)。
- 第3のメタアナリシスでは、第一選択化学療法としてプラチナ製剤をベースにした vs プラチナ製剤を用いない併用にランダム化した第III相試験を対象としており、14件の試験が確認された。[
29
]実験群は、ゲムシタビンおよびビノレルビン(n = 4)、ゲムシタビンおよびタキサン(n = 7)、ゲムシタビンおよびエピルビシン(n = 1)、パクリタキセルおよびビノレルビン(n = 1)、およびゲムシタビンおよびイホスファミド(n = 1)であった。このメタアナリシスは、プラチナ製剤をベースにした2剤レジメンを用いた11件の第III相研究のセット(プラチナ製剤をベースにした治療群患者2,298人およびプラチナ製剤を用いない治療群患者2,304人)に限定された。
- プラチナ製剤をベースにしたレジメンにより治療を受けた患者は、1年時点での死亡リスクが統計的に有意に低下し(OR、0.88;95%CI、0.78-0.99;P = 0.044)、化学療法に抵抗性となるリスクが低下した(OR、0.87;CI、0.73-0.99;P = 0.049)ことにより利益が得られた。
- プラチナ製剤をベースにしたレジメンでは44例(1.9%)の毒性関連死が報告され、プラチナ製剤を用いないレジメンでは29例(1.3%)の毒性関連死が報告された(OR、1.53;CI、0.96-2.49;P = 0.08)。プラチナ製剤をベースにした化学療法を受けた患者では、グレード3~4の消化管および血液学的毒性作用のリスク増加が統計的に実証された。発熱性好中球減少のリスクにおける統計的に有意な増加は認められなかった(OR、1.23;CI、0.94-1.60;P = 0.063)。
- 最初のメタアナリシスでは、7,633人の患者を含む評価可能な37件の試験が確認された。[
27
]
薬物および投与スケジュール
活性のある併用療法の中で、非扁平上皮性腫瘍の組織型を有する患者に対するカルボプラチン、ペメトレキセド、およびペムブロリズマブは別として、薬剤の用量およびスケジュールに関して確定的な推奨は行えない。
証拠(薬剤および投与スケジュール):
- 2,867人の患者を含む7件の試験を対象とした1件のメタアナリシスにより、ドセタキセル vs ビノレルビンの有益性が評価された。[
30
]ドセタキセルは、3試験でプラチナ製剤と併用、2試験でゲムシタビンと併用、または2試験で単独療法として投与された。ビンカアルカロイド系薬物(6試験でビノレルビンおよび1試験でビンデシン)は、6試験でシスプラチンと併用または1試験で単独で投与された。
- OSに対する併合推定値から、ドセタキセルを支持する11%の改善が示された(HR、0.89;95%CI、0.82-0.96;P = 0.004)。感受性分析で、対照薬としてビノレルビンのみを検討した場合、または2剤併用レジメンのみを検討した場合は、同様な改善が示された。
- グレード3~4の好中球減少およびグレード3~4の重篤な有害事象は、ドセタキセルをベースにしたレジメン(OR、0.59;95%CI、0.38-0.89;P = 0.013)ではビンカアルカロイド系薬物をベースにしたレジメン(OR、0.68;95%CI、0.55-0.84;P < 0.001)より頻度が低かった。
- 2件のランダム化試験でパクリタキセルおよびカルボプラチンの週1回投与 vs 3週間ごとの投与が比較されており、効力に有意差は認められず、週1回投与の耐容性が良好であることが報告された。[ 31 ][ 32 ]ランダム化比較試験のメタアナリシスにより、シスプラチンの併用はカルボプラチンまたはプラチナ製剤を用いない併用よりも優れていることが示唆されているが、効力における差の臨床的関連は、予想される耐容性、投与のロジスティックス、および個々の患者に対する治療法の決定に関する医療スタッフの熟知と比較検討する必要がある。
- 大規模な非劣性第III相ランダム化研究では、IIIB期/IV期のNSCLCで、PSが0~1の化学療法未治療患者1,725人を対象にOSが比較された。[
3
]患者は、1日目にシスプラチン75mg/m2および1日目および8日目にゲムシタビン1,250mg/m2(n = 863)か、または3週間ごとの1日目にシスプラチン75mg/m2およびペメトレキセド500mg/m2(n = 862)を最大6サイクル受けた。
- シスプラチンおよびペメトレキセドに対するOS(生存期間中央値、10.3ヵ月)は、シスプラチンおよびゲムシタビン(生存期間中央値、10.3ヵ月;HR、0.94;95%CI、0.84%-1.05%)よりも劣っていなかった。
- 腺がん患者(n = 847)において、シスプラチンおよびペメトレキセドに対するOS(12.6ヵ月)は、シスプラチンおよびゲムシタビン(10.9ヵ月)よりも統計的に有意に優れていた;大細胞がんを有する患者(n = 153)では、シスプラチンおよびペメトレキセドに対するOS(10.4ヵ月)は、シスプラチンおよびゲムシタビン(6.7ヵ月)よりも統計的に有意に優れていた。
- これとは対照的に、扁平上皮性の組織像を有する患者(n = 473)では、シスプラチンおよびゲムシタビン(10.8ヵ月)の方がシスプラチンおよびペメトレキセド(9.4ヵ月)よりも生存における有意な改善が認められた。シスプラチンおよびペメトレキセドに対するグレード3または4の好中球減少、貧血、および血小板減少(P ≤ 0.001);発熱性好中球減少(P = 0.002);および脱毛(P < 0.001)の割合が有意に低かった一方で、グレード3または4の吐き気(P = 0.004)はより一般的であった。
- この研究の結果から、シスプラチンとペメトレキセドの二剤は、進行したNSCLCに対する第一選択化学療法として、別の代替的な2剤併用レジメンであることが示唆され、組織型によっては転帰が異なる可能性があることも示唆される。
モノクローナル抗体を併用する併用化学療法
ベバシズマブ
証拠(ベバシズマブ):
- 2件のランダム化試験では、血管内皮増殖因子を標的とした抗体ベバシズマブを標準的な第一選択併用化学療法に加えて評価している。
- 再発または進行したIIIB期/IV期のNSCLC患者878人を対象としたランダム化研究では、444人に対してパクリタキセルとカルボプラチンのみを投与し、434人に対してパクリタキセルとカルボプラチンにベバシズマブを加えた。[
33
]化学療法は3週間ごとに6サイクル実施され、ベバシズマブは3週間ごとに疾患進行が明らかとなるか、毒性作用が耐えられなくなるまで投与された。扁平上皮腫瘍、脳転移、臨床的に重大な喀血を認める患者、または臓器機能が不十分であるか、PSが不適切(Eastern Cooperative Oncology Group PS >1)な患者は除外された。
- 化学療法 + ベバシズマブに割り付けられた群の生存期間の中央値が12.3ヵ月であったのに対し、化学療法単独群では10.3ヵ月であった(HR死亡、0.79;P = 0.003)。
- 化学療法 + ベバシズマブに割り付けられた群のPFS中央値は6.2ヵ月(疾患増悪のHR、0.66;P < 0.001)で奏効率は35%(P < 0.001)、および化学療法単独群では4.5ヵ月(疾患増悪のHR、0.66;P < 0.001)で奏効率は15%(P < 0.001)であった。
- 臨床的に重大な出血の割合は、化学療法 + ベバシズマブに割り付けられた群で4.4%および化学療法単独群で0.7%(P < 0.001)であった。化学療法 + ベバシズマブ群では、肺出血による5例を含めて15例の治療関連死が認められた。
- NSCLC患者のこのサブグループについて、パクリタキセルおよびカルボプラチンへのベバシズマブの追加は生存利益をもたらしうる。[ ][証拠レベル:1iiA]
- 別のランダム化第III相試験では、シスプラチン-ゲムシタビン + ベバシズマブの効力および安全性が検討された。[
34
]患者は、シスプラチン(80mg/m2)およびゲムシタビン(1,250mg/m2)を最大6サイクル + 疾患増悪まで3週間ごとに低用量のベバシズマブ(7.5mg/kg)、高用量のベバシズマブ(15mg/kg)、またはプラセボを投与される群にランダムに割り付けられた。主要エンドポイントは研究過程でOSからPFSに修正された。計1,043人の患者が募集された(プラセボ群、n = 347;低用量群、n = 345;高用量群、n = 351)。
- ベバシズマブの追加によりPFSは有意に延長した;プラセボ群と比較したPFSのHRは、低用量群で0.75(PFS中央値、6.7ヵ月 vs プラセボ群の6.1ヵ月;P = 0.03)および高用量群で0.82(PFS中央値、6.5ヵ月 vs プラセボ群の6.1ヵ月;P = 0.03)であった。[ ][証拠レベル:1iiB]
- 客観的奏効率もベバシズマブの追加によって改善され、プラセボ + シスプラチン/ゲムシタビン群で20.1%、低用量ベバシズマブ + シスプラチン/ゲムシタビン群で34.1%、および高用量ベバシズマブ + シスプラチン/ゲムシタビン群で30.4%であった。
- グレード3以上の有害事象の発現率は治療群間でほぼ同じであった。
- 抗凝固治療を受けていた患者は9%であったにもかかわらず、グレード3以上の肺出血の割合は全群で1.5%以下であった。
- これらの結果は、プラチナ製剤を含む化学療法へのベバシズマブの追加を支持しているが、カルボプラチン-パクリタキセルの併用療法が使用されたときより、結果の印象ははるかに弱い。
- さらに、要約形式で報告されているこの研究では、生存における有意差は示されなかった。
- これらの知見から全体的にみて、ベバシズマブを追加する場合は化学療法の基本骨格が重要であると示唆されている。
- 再発または進行したIIIB期/IV期のNSCLC患者878人を対象としたランダム化研究では、444人に対してパクリタキセルとカルボプラチンのみを投与し、434人に対してパクリタキセルとカルボプラチンにベバシズマブを加えた。[
33
]化学療法は3週間ごとに6サイクル実施され、ベバシズマブは3週間ごとに疾患進行が明らかとなるか、毒性作用が耐えられなくなるまで投与された。扁平上皮腫瘍、脳転移、臨床的に重大な喀血を認める患者、または臓器機能が不十分であるか、PSが不適切(Eastern Cooperative Oncology Group PS >1)な患者は除外された。
セツキシマブ
証拠(セツキシマブ):
- 2件の試験で、一次併用化学療法へのセツキシマブの追加が評価されている。[
35
][
36
]
- 第一の試験では、IIIB期(胸水)またはIV期のNSCLCで化学療法未治療の患者676人を対象に、組織型またはEGFR発現による制限なしに、タキサン系(パクリタキセルまたはドセタキセルとカルボプラチン)と併用するセツキシマブまたは併用化学療法を投与した。[
35
]
- セツキシマブの追加は、本研究の主要エンドポイントであるPFSとOSについて統計的に有意な改善をもたらさなかった。
- PFS中央値は、セツキシマブ-化学療法群の患者が4.40ヵ月に対して、タキサン-カルボプラチン群の患者が4.24ヵ月であった(HR、0.902;95%CI、0.761-1.069;P = 0.236)。
- OS中央値は、セツキシマブ-化学療法群の患者が9.69ヵ月に対して、化学療法単独群の患者が8.38ヵ月であった(HR、0.890;95%CI、0.754-1.051;P = 0.169)。
- 治療群別解析では、EGFR発現、EGFR突然変異、EGFRコピー数、またはKRAS突然変異と、PFS、OS、および奏効間で有意な関連性は認められなかった。[ ]
- 第2の試験では、進行したEGFR発現を認めるIIIB期/IV期のNSCLCで化学療法未治療の患者1,125人を対象に、シスプラチン-ビノレルビンの化学療法 + セツキシマブ、または化学療法単独による治療を行った。[
36
]
- この研究の主要エンドポイントであるOSは、セツキシマブと化学療法による治療を受けた患者の方が長かった(中央値11.3ヵ月 vs 10.1ヵ月;HR死亡、0.871;95%CI、0.762-0.996;P = 0.044)。
- 生存利益はすべての組織型サブグループで認められた;しかしながら、非白人またはアジア系患者では生存利益は認められなかった。治療と民族起源との相互作用のみが有意であった(P = 0.011)。
- セツキシマブに関係する主な有害事象は、ざ瘡様発疹(グレード3、10%)であった。
- これら2研究における治療成績の差が研究集団、EGFR発現に関する腫瘍の特徴、または化学療法レジメンにおける差の結果であるかどうかは不明である。
- 第一の試験では、IIIB期(胸水)またはIV期のNSCLCで化学療法未治療の患者676人を対象に、組織型またはEGFR発現による制限なしに、タキサン系(パクリタキセルまたはドセタキセルとカルボプラチン)と併用するセツキシマブまたは併用化学療法を投与した。[
35
]
ネシツムマブ
証拠(ネシツムマブ):
- 2件の第III相試験により、進行期の非扁平上皮性および扁平上皮性NSCLC患者の第一選択治療においてプラチナ製剤を含む2剤併用化学療法への第2世代組換えヒト免疫グロブリンG1 EGFR抗体であるネシツムマブの追加が評価されている。[
38
][
39
]
-
SQUIRE(NCT00981058)試験では、進行期扁平上皮性NSCLC患者1,093人がシスプラチンおよびゲムシタビンによる第一選択化学療法またはネシツムマブ(各サイクルの1日目と8日目に800mg)を追加する同じレジメンを受ける群にランダムに割り付けられた。[
39
]
- ネシツムマブの追加により、OS中央値が延長した(11.5ヵ月 vs 9.9ヵ月;P = 0.01)。
- ネシツムマブの追加により、PFSも延長した(5.7ヵ月 vs 5.5ヵ月);しかしながら、全奏効率は両群でほぼ同じであった(31% vs 28%)。
- ネシツムマブを含む治療群ではグレード3および4の有害事象が高かった(72% vs 62%)。
- ネシツムマブでは毒性作用が高く、相対的にわずかな有益性しか得られない。
-
INSPIRE(NCT00982111)試験では、進行期非扁平上皮性NSCLC患者633人がシスプラチンおよびペメトレキセドによる第一選択化学療法またはネシツムマブ(各サイクルの1日目と8日目に800mg)を追加するシスプラチンおよびペメトレキセドを受ける群にランダムに割り付けられた。[
38
]
- この研究では、進行期非扁平上皮性NSCLCに対する標準的な第一選択化学療法へのネシツムマブの追加による有益性は示されなかった。
- OSは、ネシツムマブを含む群の患者で11.3ヵ月(95%CI、9.5-13.4) vs 化学療法単独群の患者で11.5ヵ月(95%CI、10.1-13.1)であった;P = 0.96。同様に、客観的奏効率またはPFSについて両群間で差は認められなかった。
- 重篤な有害事象およびグレード3~4の有害事象(血栓塞栓性の事象など)の割合はネシツムマブを含む群の患者で高かった;治療関連死亡率も高かった(5% vs 3%)。
- これらの結果に基づき、ネシツムマブは進行期非扁平上皮性NSCLC患者に対する標準的な第一選択化学療法との併用療法としては推奨されない。
-
SQUIRE(NCT00981058)試験では、進行期扁平上皮性NSCLC患者1,093人がシスプラチンおよびゲムシタビンによる第一選択化学療法またはネシツムマブ(各サイクルの1日目と8日目に800mg)を追加する同じレジメンを受ける群にランダムに割り付けられた。[
39
]
第一選択化学療法後の維持療法(プラチナ製剤をベースにした併用化学療法を4サイクル施行後に安定または反応を示している患者に対して)
NSCLCにおいて広範囲にわたり研究されている治療戦略の1つに、化学療法に対して初期反応が得られた後の維持療法がある。研究されている維持療法の選択肢には以下のものがある:
- 初回併用化学療法レジメンの継続。
- 単剤のみの化学療法の継続。
- 維持療法として新薬の導入。
複数のランダム化試験で、3~4サイクルを超えて継続する一次併用細胞毒性化学療法の効力が評価されている。
証拠(第一選択化学療法後の維持療法):
- 細胞毒性併用療法を継続する試験では、4サイクルを超える追加、つまり長期の治療継続によって有意なOSの優位性を示したものはなかった。非扁平上皮性のNSCLCを有する患者については、2件の研究で、切り替えのまたは継続する維持化学療法(例、初期のシスプラチンおよびゲムシタビン後の維持ペメトレキセドまたは初期のシスプラチンとペメトレキセド後の維持ペメトレキセド)によりPFSおよびOSの改善が実証されている。[ 40 ]
- 3件の試験では、化学療法の追加により、PFSまたは無増悪期間が統計的に有意に改善したことが明らかにされた。[ 41 ][ 42 ][ 43 ]
- QOLにおける一貫した改善は報告されなかった。[ 42 ][ 44 ][ 45 ]
- 化学療法関連毒性は、化学療法の延長とともに増大した。[ 44 ][ 45 ]
これらのデータは、非扁平上皮性のNSCLCを有する患者のPFSおよびOSが有効な化学療法の4サイクルを超える継続または代替化学療法の即時開始のいずれによっても、改善しうることを示唆している。しかしながら、PFSの改善は、追加の細胞毒性化学療法を含めて有害事象の増加およびQOLにおいて一貫した改善が得られないことで抑えられる。疾患が安定しているか、第一選択療法に反応する患者に関する証拠は、疾患進行までまたは疾患進行前の異なる化学療法の開始までの細胞毒性併用化学療法の継続を支持していない。総合すると、これらの試験から、第一選択の細胞毒性併用化学療法は、疾患進行時、または4サイクルの治療に対しても病状に反応が認められない患者では中止すべきであることが示唆される;6サイクルを超えて投与することはできない。[ 41 ][ 42 ][ 44 ][ 45 ]非扁平上皮性のNSCLCを有し、4~6サイクルのプラチナ製剤併用化学療法後に反応を示しているか、または安定している患者に対してペメトレキセドによる維持化学療法を検討すべきである。[ 40 ]
証拠(第一選択のプラチナ製剤をベースにした併用化学療法とその後のペメトレキセド):
- 2件のランダム化試験(NCT00102804およびNCT00789373)の知見から、標準的な第一選択のプラチナ製剤をベースにした併用化学療法後にペメトレキセドを追加した場合の治療成績の改善が示された。[
43
][
46
]
- 1つ目の試験では、4サイクルのペメトレキセド以外のプラチナ製剤をベースにした化学療法で増悪しなかったIIIB期/IV期疾患の患者663人が、疾患増悪までペメトレキセドまたはプラセボを受ける群にランダムに割り付けられた(2:1の比率)。[
46
]
- 主要エンドポイントであるPFS、および副次エンドポイントであるOSは、維持ペメトレキセドの追加により、いずれも統計的に有意に延長した(PFS中央値、4.3ヵ月 vs 2.6ヵ月;HR、0.50;95%CI、0.42-0.61;P < 0.0001;OS中央値、13.4ヵ月 vs 10.6ヵ月;HR、0.79;95%CI、0.65-0.95;P = 0.012)。
- 組織型が扁平上皮性の患者では、有益性が認められなかった。
- グレード3より高い毒性および薬物関連毒性作用による治療中止は、プラセボ群よりペメトレキセド群が多かった。
- ペメトレキセド関連死は起こらなかった。
- 治療中止後に全身療法を受けた患者は、プラセボ群よりペメトレキセド群の方が相対的に少なかった(227人 [51%] vs 149人 [67%];P = 0.0001)。
- ペメトレキセドを使用した維持療法中の生活の質はプラセボと同様であったが、Lung Cancer Symptom Scaleによる評価で食欲不振のわずかな増加と、疼痛および喀血の悪化の有意な遅延が認められた。[ ]生活の質の主要エンドポイントである症状悪化までの期間について高い割合で打ち切り(50%超)が発生したため、これらの生活の質の結果は慎重な評価を必要とする。
- 試験では、維持ペメトレキセド vs 増悪時のペメトレキセドは評価されていない。
- 2つ目の試験では、ペメトレキセドおよびシスプラチンによる治療後に増悪していない非扁平上皮性のNSCLC患者539人がペメトレキセドの継続投与群またはプラセボ群にランダムに割り付けられた。[
43
]
- 主要エンドポイントであるPFS(4.1ヵ月 vs 2.8ヵ月、HR、0.62;95%CI、0.49-0.79)および副次エンドポイントであるOS(13.9ヵ月 vs 11ヵ月、HR、0.78;95%CI、0.64-0.96)に統計的に有意な改善が認められた。[ ][ ][証拠レベル:1iDiii]
- 1つ目の試験では、4サイクルのペメトレキセド以外のプラチナ製剤をベースにした化学療法で増悪しなかったIIIB期/IV期疾患の患者663人が、疾患増悪までペメトレキセドまたはプラセボを受ける群にランダムに割り付けられた(2:1の比率)。[
46
]
証拠(プラチナ製剤をベースにした2剤併用化学療法後の維持エルロチニブ):
- 1件の試験(NCT00556712)は、プラチナ製剤をベースにした2剤併用化学療法を4サイクル施行後に安定を示している患者に対する維持エルロチニブについて、良好な治療成績を報告している。[
48
]
- この試験では、疾患の進行が認められないNSCLC患者889人を、疾患進行または許容できない毒性がみられるまでエルロチニブ投与群(150mg/日)またはプラセボ投与群にランダムに割り付けた。[
48
]
- PFS中央値は、エルロチニブ群の方がプラセボ群より有意に長かった:エルロチニブ群の患者の12.3週に対しプラセボ群の患者の11.1週(HR、0.71;95%CI、0.62-0.82;P < 0.0001)。
- 全集団では、活性化EGFR変異が認められる腫瘍を有する患者が、維持エルロチニブ治療からPFSに関する最大の利益を得ていた(n = 49;HR、0.10;P < 0.0001)。
- 野生型EGFR腫瘍を有する患者もPFS(HR、0.78)およびOS(HR、0.77)の有意な改善を得ていた。
- 疾患が安定していて活性化EGFR変異が認められない腫瘍を有する患者のサブグループ(n = 217)では、エルロチニブの投与によりPFS(HR、0.72;95%CI、0.54-0.96;P = 0.0231)およびOS(HR、0.65;95%CI、0.48-0.87;P = 0.0041)がいずれも有意に延長された。
- 活性化EGFR変異が認められる腫瘍を有する患者(n = 30)でも、OSにはエルロチニブによる改善がみられた(HR、0.48;95%CI、0.14-1.62)が、この解析では統計的に有意ではなかった。[ ]
- EGFR免疫組織化学検査、EGFR蛍光in situハイブリダイゼーション(FISH)、KRAS変異、およびイントロン1反復長状態におけるEGFR CA単純反復配列は、エルロチニブの効力を予測しなかった。[ ]KRAS突然変異状態はPFSに対する有意な負の予後因子であった。[ ][証拠レベル:1iDiii]
- この試験では、疾患の進行が認められないNSCLC患者889人を、疾患進行または許容できない毒性がみられるまでエルロチニブ投与群(150mg/日)またはプラセボ投与群にランダムに割り付けた。[
48
]
EGFRチロシンキナーゼ阻害薬
特定の患者では、単剤のEGFR TKIにより、利益が得られる場合がある。EGFR突然変異を有するNSCLCの化学療法未治療患者を対象としたランダム化比較試験では、EGFR阻害薬はPFSを改善するがOSを改善せず、併用化学療法と比較して毒性プロファイルが良好であることが示された。
オシメルチニブ
証拠(オシメルチニブ):
- 1件の第III相多施設ランダム化二重盲検比較試験(FLAURA[NCT02296125])では、米国食品医薬品局(FDA)承認済みの検査で検出された未治療のEGFR変異陽性(エクソン19欠失またはL858R)進行期NSCLCを有する患者の第一選択治療として、オシメルチニブと標準ケアのEGFR TKI(ゲフィチニブまたはエルロチニブ)が比較された。[
51
]556人の患者が1:1の比率でランダムに割り付けられた。
- 主要エンドポイントである研究者が評価したPFS期間はオシメルチニブ群の方が有意に長かった(18.9ヵ月 vs 10.2ヵ月;HR、0.46;95%CI、0.37-0.57、P < 0.0001)。[ 51 ][証拠レベル:1iDiii]
- 客観的奏効率は両群でほぼ同じであった(オシメルチニブ群で80% vs 標準のEGFR TKI群で76%)。
- 奏効期間中央値は、オシメルチニブ群で17.2ヵ月(95%CI、13.8-22.0) vs 標準のEGFR TKI群で8.5ヵ月であった(95%CI、7.3-9.8)。
- OSのデータはまだ不完全である。
- グレード3以上の有害事象の頻度は標準のTKI群(45%)よりもオシメルチニブ群(34%)の方が低かった。
オシメルチニブは、EGFR変異(エクソン19欠失またはL858R)NSCLCの第一選択治療としてFDAにより承認された。
ゲフィチニブ
証拠(ゲフィチニブ):
- 東アジアにおいて、喫煙歴がないか、または過去に軽度の喫煙者であり、臨床的に選別された進行した肺腺がんの患者に対する第一選択治療として、ゲフィチニブをカルボプラチン + パクリタキセルと比較した第III相多施設ランダム化試験がある。[
52
]
- この研究では、カルボプラチンとパクリタキセルの併用療法と比較してゲフィチニブのPFSの優位性を実証するという研究の主要目標が達成された(増悪または死亡のHR、0.74;95%CI、0.65-0.85;P < 0.001)。
- PFS中央値は、ゲフィチニブ群で5.7ヵ月、カルボプラチン-パクリタキセル群で5.8ヵ月であった。[ 52 ][証拠レベル:1iDiii]
- 化学療法が中止され、ゲフィチニブが継続された時点から、PFS曲線に明確な分離が認められゲフィチニブが良好となった。
- 12ヵ月目のPFS率は、ゲフィチニブ群で24.9%、カルボプラチン-パクリタキセル群で6.7%であった。
- この試験では、del19またはエクソン21 L858R突然変異のいずれかの突然変異を有する患者が90%を超えており、EGFR阻害薬に感受性があることが示されている。突然変異を有する患者のサブグループでは、ゲフィチニブを投与した患者でPFSが有意に長かった(HR、0.48;95%CI、0.36-0.64;P < 0.001);しかしながら、突然変異が陰性であった患者のサブグループでは、カルボプラチン-パクリタキセル併用を投与した患者でPFSが有意に長かった(ゲフィチニブ群のHR、2.85;95%CI、2.05-3.98;P < 0.001)。PFSに関して治療とEGFR突然変異間で有意な相互作用が認められた(P < 0.001)。[ 52 ]
- OSは、ゲフィチニブとカルボプラチン-パクリタキセルを投与した患者でほぼ同じであり、治療全体(HR、0.90;95%CI、0.79-1.02;P = 0.109)、またはEGFR突然変異陽性(HR、1.00;95%CI、0.76-1.33;P = 0.990)、またはEGFR突然変異陰性(HR、1.18;95%CI、0.86-1.63;P = 0.309;EGFR突然変異別の治療の相互作用P = 0.480)の各サブグループ間に有意差は認められなかった。カルボプラチン-パクリタキセルレジメンにランダムに割り付けられたEGFR突然変異陽性患者の多く(64.3%)が、その後にEGFR TKIを投与された。PFSは、EGFR遺伝子コピー数が多く、EGFR突然変異が認められる腫瘍の患者にゲフィチニブを投与した場合に有意に長かった(HR、0.48;95%CI、0.34-0.67)が、EGFR遺伝子コピー数が多いもののEGFR突然変異が伴わない場合は有意に短かった(HR、3.85;95%CI、2.09-7.09)。
- 日本で実施された2件の第III相試験は、EGFR突然変異を有するNSCLC患者に対するゲフィチニブを用いた治療で、PFSが改善しOSは改善しなかったことをプロスペクティブに確認した。[
53
][
54
]
- 1つ目の試験では、EGFR突然変異を有する転移性NSCLCの化学療法未治療患者230人が、ゲフィチニブまたはカルボプラチン-パクリタキセルの投与を受ける群にランダムに割り付けられた。[
53
]
- 最初の200人の患者データを対象として予定されていた中間解析が行われ、ゲフィチニブ群のPFSが標準化学療法群より有意に長かった(ゲフィチニブのHR死亡または増悪のハザード比、0.36;P < 0.001)ため、研究は早期に終了された。
- ゲフィチニブ群のPFS中央値は有意に長かった(10.8ヵ月 vs 化学療法群の5.4ヵ月;HR、0.30;95%CI、0.22-0.41;P < 0.001)。[ ][証拠レベル:1iiDiii]OS中央値は、ゲフィチニブ群で30.5ヵ月、標準化学療法群で23.6ヵ月であった(P = 0.31)。
- 2つ目の試験は、西日本がん研究機構(West Japanese Oncology Group)が、75歳以下で化学療法未治療のEGFR変異(エクソン19欠失またはL858R点変異)を有するIIIB/IV期または術後再発のNSCLCを診断された患者177人を対象として実施した第III相試験(WJTOG3405)である。[
54
]
- 患者はゲフィチニブ投与群またはシスプラチン + ドセタキセル投与群(21日ごとを3~6サイクル投与)のいずれかにランダムに割り付けられた。主要エンドポイントはPFSであった。
- ゲフィチニブ群のPFSはシスプラチン + ドセタキセル群よりも有意に長く、PFS中央値は9.2ヵ月(95%CI、8.0-13.9) vs 6.3ヵ月(範囲、5.8-7.8ヵ月;HR、0.489;95%CI、0.336-0.710、ログランク検定;P < 0.0001)であった。[ ][証拠レベル:1iiDiii]
- 1つ目の試験では、EGFR突然変異を有する転移性NSCLCの化学療法未治療患者230人が、ゲフィチニブまたはカルボプラチン-パクリタキセルの投与を受ける群にランダムに割り付けられた。[
53
]
エルロチニブ
証拠(エルロチニブ):
- 中国で実施されたオープンラベルのランダム化第III相試験(NCT00874419)では、組織学的にIIIB期/IV期NSCLCが確認され、かつEGFRの活性化突然変異(すなわち、エクソン19欠失またはエクソン21 L858R点突然変異)が認められた18歳以上の患者165人が、疾患進行または許容できない毒性作用がみられるまでエルロチニブ(150mg/日)を経口投与する治療か、またはゲムシタビン + カルボプラチンを最大4サイクル投与する治療を受けた。[
55
]
- PFS中央値は、エルロチニブ投与群の患者の方が化学療法群の患者よりも有意に長かった(13.1ヵ月[95%CI、10.58-16.53] vs 4.6ヵ月[範囲、4.21-5.42ヵ月];HR、0.16;95%CI、0.10-0.26;P < 0.0001)。[ 55 ][証拠レベル:1iiDiii]
- ヨーロッパの研究(EURTAC[NCT00446225])で、進行したNSCLC患者1,227人がEGFR突然変異のスクリーニングを受けた。そのうちのEGFR突然変異を有する患者174人が、エルロチニブ投与群またはプラチナ製剤をベースにした化学療法群にランダムに割り付けられた。[
56
]主要エンドポイントはPFSであった。
- 最初の153人の患者を対象とした中間解析では、化学療法群のPFSは5.2ヵ月(95%CI、4.5-5.8)で、対するエルロチニブ投与群は9.7ヵ月(95%CI、8.4-12.3)であった(HR、0.37;P < 0.0001)。生存期間中央値は、化学療法群の患者で19.3ヵ月、エルロチニブ投与群の患者で19.5ヵ月であった(HR、0.80;P = 0.42)。[ 57 ][証拠レベル:1iiDiii]
アファチニブ
証拠(アファチニブ):
- 1件のオープンラベルのランダム化第III相研究(LUX-Lung 3 [NCT00949650])では、IIIB/IV期NSCLCでEGFR変異(すなわち、エクソン19欠失、L858Rなど[345人中38人の患者は他のあまり一般的でない変異を有した])が確認されたアジア系(72%)と白人(26%)の患者345人がスクリーニングを受け、340人の患者が研究薬の投与(第一選択治療として、不可逆性EGFR/ヒト上皮成長因子受容体TKIであるアファチニブ40mgの1日1回経口投与またはシスプラチンおよびペメトレキセドの最大6サイクル投与のいずれか)を少なくとも1回受けた。[
58
]
- 主要エンドポイントはPFSであった。この研究では、アファチニブ群のPFSはシスプラチン + ペメトレキセド群よりも有意に長く、アファチニブ群のPFS中央値は11.1ヵ月、化学療法群では6.9ヵ月であった(HR、0.58;95%CI、0.43-0.78;P = 0.001)。[ 58 ][証拠レベル:1iiDiii]
- OSの評価は副次エンドポイントであり、別に報告された。[
59
]PFSの解析と同様に、OSはEGFR変異のタイプおよび民族起源に基づいて層別化された。
- 追跡期間中央値41ヵ月で、OS中央値は両群の患者で28.2ヵ月であった(HR、0.88;95%CI、0.66-1.17;P = 0.39)。
- 一般的なEGFR変異(すなわち、エクソン19欠失およびL858R)を有する患者の生存については、治療群間で有意差は認められなかった(HR、0.78;95%CI、0.58-1.06;P = 0.11)。しかしながら、事前に規定されたサブグループ解析により、EGFR del19突然変異を有する腫瘍の患者では化学療法と比較してアファチニブによる生存優位が実証された(OS中央値、33.3ヵ月 vs 21.1ヵ月;HR、0.54;95%CI、0.36-0.79;P = 0.0015)が、L858R突然変異を有する腫瘍の患者では治療群間で有意差は実証されなかった(OS中央値、27.6ヵ月 vs 40.3ヵ月;HR、1.30;95%CI、0.80-2.11;P = 0.29)。
- EGFR del19変異を有するNSCLC患者において、第一選択治療でのアファチニブは化学療法と比較して有意な生存優位に関連したが、EGFR L858R変異を有する患者またはEGFR変異陽性患者集団全体では生存優位に関連しなかった。[ ][証拠レベル:1iiA]
- 1件のオープンラベルのランダム化第III相研究(LUX-Lung 6[NCT01121393])では、IIIB/IV期NSCLCでEGFR変異(すなわち、エクソン19欠失、L858Rなど)が確認された東アジア系の患者364人が、第一選択治療として毎日40mgのアファチニブまたは最大6サイクルのゲムシタビンおよびシスプラチンに(2:1の比率)ランダムに割り付けられた。[
60
]
- 主要エンドポイントはPFSであった。PFS中央値は、アファチニブ投与群の患者の方(11.0ヵ月;95%CI、9.7-13.7)がゲムシタビンおよびシスプラチン群の患者(5.6ヵ月[範囲、5.1-6.7ヵ月];HR、0.28;95%CI、0.20-0.39;P < 0.0001)よりも有意に長かった。[ 60 ][証拠レベル:1iiDiii]
- OSの評価は事前に規定された副次エンドポイントであり、別に報告された。[
59
]PFSの解析と同様に、OSはEGFR変異のタイプおよび民族起源に基づいて層別化された。
- 追跡期間中央値33ヵ月で、OS中央値はアファチニブ群の患者で23.1ヵ月および化学療法群の患者で23.5ヵ月であった(HR、0.93;95%CI、0.72-1.22;P = 0.61)。
- 一般的なEGFR変異(すなわち、エクソン19欠失およびL858R)を有する患者の生存については、治療群間で有意差は認められなかった(HR、0.83;95%CI、0.62-1.09;P = 0.18)。しかしながら、事前に規定されたサブグループ解析により、EGFR del19変異を有する腫瘍の患者では化学療法と比較してアファチニブによる生存優位が実証された(OS中央値、31.4ヵ月 vs 18.4ヵ月;HR、0.64;95%CI、0.44-0.94;P = 0.023)が、L858R変異を有する腫瘍の患者では治療群間で有意差は示されなかった(OS中央値、19.6ヵ月 vs 24.3ヵ月;HR、1.22;95%CI、0.81-1.83;P = 0.34)。
- EGFR del19変異を有するNSCLC患者において、第一選択治療でのアファチニブは化学療法と比較して有意な生存優位に関連したが、EGFR L858R変異を有する患者またはEGFR変異陽性患者集団全体では生存優位に関連しなかった。[ ][証拠レベル:1iiA]
ALK阻害薬(ALK転座が認められる患者に対して)
アレクチニブ
証拠(アレクチニブ):
- 1件の第III相ランダム化オープンラベル研究(ALEX試験[NCT02075840])では、未治療の進行期ALK再構成NSCLC患者303人が、アレクチニブ(600mg、1日2回)またはクリゾチニブ(250mg、1日2回)のいずれかを受けた。[
61
]主要エンドポイントは研究者が評価したPFSであった。
- PFS率はクリゾチニブよりもアレクチニブで有意に高かった;12ヵ月イベントフリー生存率は、アレクチニブ群で68.4%(95%CI、61.0-75.9)であったのに対し、クリゾチニブ群で48.7%(95%CI、40.4-56.9)(HR、0.47;95%CI、0.34-0.65;P < 0.001)であった。アレクチニブ群ではPFS中央値に達していなかった。独立判定委員会により評価されたPFSの結果も一致していた。[ 61 ][証拠レベル:1iiDiii]
- 中枢神経系(CNS)の増悪イベントの頻度はアレクチニブ群(12%)の方がクリゾチニブ群(45%)よりも低かった(HR、0.16;95%CI、0.10-0.28;P < 0.001)。
- 奏効率は両群でほぼ同じであり、アレクチニブ群で82.9%であったのに対し、クリゾチニブ群で75.5%であった(P = 0.09)。
- グレード3~5の有害事象の頻度はアレクチニブ群(41%)の方がクリゾチニブ群(50%)よりも低かった。
- 2件目の第III相ランダム化オープンラベル試験(J-ALEX)では、ALK陽性NSCLCで化学療法未治療または以前に1つしか化学療法レジメンを受けておらず、ALK阻害薬未治療の日本人患者207人が募集された。患者は1:1の比率で、アレクチニブ(300mg、1日2回;日本で承認されている用量であり、他の国で承認されている600mg、1日2回の用量よりも低い) vs クリゾチニブ(250mg、1日2回)を受けるようにランダムに割り付けられた。[
62
]主要エンドポイントは独立判定委員会によって評価されたPFSであった。
- 2回目の主要エンドポイント中間解析のデータカットオフ時点で、独立データ監視委員会は主要エンドポイントが達成されている(HR、0.34;99.7%CI、0.17-0.71;P < 0.0001)と判定し、データの即時公開を推奨した。PFS中央値はアレクチニブ群で到達していなかったが、クリゾチニブ群では10.2ヵ月で到達していた。
- グレード3または4の有害事象の発生頻度はアレクチニブ群(26%の発生率)の方がクリゾチニブ群(52%の発生率)よりも低かった。
クリゾチニブ
証拠(クリゾチニブ):
- 1件のオープンラベルのランダム化第III相研究では、IIIB/IV期NSCLCでALKに転座を有する患者343人が、250mgのクリゾチニブ、1日2回経口投与、またはペメトレキセドおよびシスプラチンまたはカルボプラチンの併用を最大6サイクル実施のいずれかを受けた。[
63
]疾患増悪時には、化学療法群の患者はクリゾチニブへのクロスオーバーが許可されていた;その後、化学療法群の患者の60%がクリゾチニブを投与された。この研究の主要エンドポイントはPFSであった。
- 研究は主要エンドポイントを満たし、クリゾチニブはPFS期間の延長において化学療法よりも優れていることが実証された(中央値、10.9ヵ月 vs 7.0ヵ月;HR、0.454;95%CI、0.346-0.596;P < 0.0001)。[ 64 ][証拠レベル:1iiDiii]
セリチニブ
証拠(セリチニブ):
- 1件のオープンラベルのランダム化第III相研究では、IIIB/IV期非扁平上皮性NSCLCでALKが再構成された患者376人が、750mgのセリチニブ、毎日経口投与、またはプラチナ製剤をベースにした3週間ごとの化学療法(シスプラチンまたはカルボプラチンとペメトレキセドの併用)を4サイクル実施後、維持ペメトレキセドのいずれかを受けた。[
65
]主要エンドポイントはPFSであり、進行が明らかになった時点で化学療法からセリチニブへのクロスオーバーが許可されていた。
- 盲検化された独自のレビューにより評価されたPFS中央値は、セリチニブ群で16.6ヵ月および化学療法群で8.1ヵ月であった(HR、0.55;95%CI、0.42-0.73;P < 0.00001)。
- OS中央値は、セリチニブ群では未到達、化学療法群で26.2ヵ月であった(HR、0.73;95%CI、0.50-1.08;P = 0.056)。[ 65 ][証拠レベル:1iiDiii]
brigatinib
証拠(brigatinib):
- 1件の第II相オープンラベル試験(NCT02094573)では、ALK転座局所進行または転移性NSCLCを有し、クリゾチニブ治療後に疾患が増悪した患者222人が登録した。患者は90mg、1日1回投与(n = 112;109人が治療された)または90mg、1日1回、7日間の導入を経て180mg、1日1回投与(n = 110)を受けるようにランダムに割り付けられた。[
66
]
- 主要エンドポイントは客観的奏効率であり、研究者らにより評価された。客観的奏効率は、90mgの投与を受けた患者で45%(97.5%CI、34-56)、180mgの投与を受けた患者で54%(97.5%CI、43-65)であった。
- PFS中央値は、90mgの投与を受けた患者で9.2ヵ月(95%CI、7.4-15.6)、180mgの投与を受けた患者で12.9ヵ月(95%CI、11.1-未到達)であった。
- データカットオフ時点での奏効期間中央値は、90mgの投与を受けた患者で13.8ヵ月(95%CI、5.6-13.8)、180mgの投与を受けた患者で11.1ヵ月(95%CI、9.2-13.8)であった。[ 66 ][証拠レベル:1iiDiv]
- 測定可能なCNS病変が認められた患者におけるCNSの客観的奏効率は、90mgの1日1回投与を受けた患者(n = 26)で42%、180mgの1日1回投与を受けた患者(n = 18)で67%であった。
- 一般的な有害事象(主にグレード1または2で、高用量群患者の27~38%に発生した)は、吐き気、下痢、頭痛、および咳嗽であった。早期に発症した(発生中央値、2日目)肺の有害事象のサブセットは、治療を受けた219人の患者のうち14人に発生した(すべてのグレード、6%;グレード3以上、3%);180mgに増量後の発生は認められなかった。有害事象には、呼吸困難、低酸素、咳嗽、肺炎、または肺臓炎が含まれた。これらは投与を中断して管理された。14人の患者のうち7人では、brigatinibによる再治療が成功した。
- FDAにより承認されたbrigatinibの用量は、90mg、1日1回、7日間であった;耐えられた場合は、用量が180mg、1日1回に増量された。
ロルラチニブ
証拠(ロルラチニブ):
- 1件の現在実施中の複数のコホートによるオープンラベル第II相研究では、転移性ALK再構成NSCLC患者が、ALKの状態および治療歴に基づいて6つのALK拡大(EXP)コホートに登録された。[
67
]患者はロルラチニブ100mg、1日1回を21日サイクルで持続的に投与された。主要エンドポイントは、独立中央レビューによる全体および頭蓋内の腫瘍反応で、併合した主要サブグループで評価された。[
67
][証拠レベル:3iiiDiv]
- 各コホートまたは併合コホートで、治療を受けた患者数、客観的奏効率、および頭蓋内奏効率は、以下の通りである:
- EXP1(n = 30、未治療)。
- 客観的奏効率 = 90.0%;95%CI、73.5‒97.9。
- 頭蓋内奏効率(n = 3)、66.7%;95%CI、9.4‒99.2。
- EXP2(n = 27、前治療はクリゾチニブのみ)およびEXP3A(n = 32、前治療はクリゾチニブと化学療法)。
- 客観的奏効率 = 69.5%;95%CI、56.1‒80.8。
- 頭蓋内奏効率(n = 23)、87.0%;95%CI、66.4‒97.2。
- EXP3B(n = 28、前治療は1種類の第2世代ALK阻害薬単独または化学療法との併用)。
- 客観的奏効率 = 32.1%;95%CI、15.9‒52.4。
- 頭蓋内奏効率(n = 9)、55.6%;95%CI、21.2‒86.3。
- EXP4(n = 65、前治療は2種類のALK阻害薬単独または化学療法との併用)およびEXP5(n = 46、前治療は3種類のALK阻害薬単独または化学療法との併用)。
- 客観的奏効率 = 38.7%;95%CI、29.6‒48.5。
- 頭蓋内奏効率(n = 49)、53.1%;95%CI、38.3‒67.5。
- EXP1(n = 30、未治療)。
- 奏効期間中央値はいずれの併合コホートについても未達である。
- 最も一般的な有害事象は高コレステロール血症(16% グレード3~4)であり、3%の患者が有害事象のために治療を中止した。
- 各コホートまたは併合コホートで、治療を受けた患者数、客観的奏効率、および頭蓋内奏効率は、以下の通りである:
BRAF V600EおよびMEK阻害薬(BRAF V600E変異を有する患者に対して)。
BRAF V600E変異は、肺腺がんの1~2%に発生する。
ダブラフェニブおよびトラメチニブ
証拠(ダブラフェニブおよびトラメチニブ):
- 第II相多施設非ランダム化オープンラベル研究(NCT01336634)において、未治療の転移性NSCLCでBRAF V600E変異に対する検査が陽性となった患者36人がダブラフェニブ(BRAF阻害薬)、150mg、1日2回およびトラメチニブ(MEK阻害薬)、2mg、1日1回で治療された。[
68
]BRAF V600E変異はOncomine Dx Target Test(ThermoFisher Scientific)により同定された。主要エンドポイントは研究者が評価した全奏効率であった。
- 全奏効率は64%(95%CI、46-79)であった。6%の患者で完全奏効、58%の患者で部分奏効が得られた。
- 研究者が評価したPFS中央値は10.9ヵ月(95%CI、7.0-16.6ヵ月)であった。奏効期間中央値は10.4ヵ月(95%CI、8.3-17.9)と推定された。データカットオフ時点で、47%の患者が死亡しており、OS中央値は24.6ヵ月(95%CI、12.3-推定不可能)であった。
- 69%の患者にグレード3または4の有害事象が少なくとも1回以上発生し、このうち最も一般的なものは、発熱、アラニンアミノトランスフェラーゼ増加、高血圧、または嘔吐であった。有害事象により22%の患者で投与が永久的に中止され、75%の患者では投与が中断または延期され、39%の患者では用量が減量された。[ 68 ][証拠レベル:3iiiDiv]
ダブラフェニブおよびトラメチニブの併用は、FDA承認の検査により検出されBRAF V600E変異が腫瘍に認められたNSCLC患者の治療において承認された。
ROS1阻害薬(ROS1再構成が認められる患者に対して)
ROS1再構成はNSCLC患者の約1%に発生する。[ 69 ]クリゾチニブおよびエヌトレクチニブは、ROS1再構成を有するNSCLC患者への使用に対してFDAにより承認されており、後者は頭蓋内病変に対する活性がより大きいとみられる。
エヌトレクチニブ
エヌトレクチニブは、以前に受けた全身療法の数に関係なく、腫瘍がROS1陽性である転移性NSCLC患者の治療に対してFDA承認を受けている。
証拠(エヌトレクチニブ):
- ROS1融合陽性の転移性NSCLCにおけるエヌトレクチニブの安全性および臨床活性は、3件の多施設共同単群オープンラベル臨床試験(ALKA-372-001/EudraCT、2012-000148-88、STARTRK-1 [NCT02097810]、およびSTARTRK-2 [NCT02568267])の統合解析により決定された。[
70
]エヌトレクチニブは、600mg以上の用量で1日1回経口投与された。主要エンドポイントは、盲検下の独立中央レビューにより決定された客観的奏効率および奏効期間(DOR)であった。注意すべき点として、無イベント期間(time-to-event)のエンドポイントは、対照群がない場合に解釈が困難である。検査室で開発した検査としてのFISHまたは次世代塩基配列決定法(NGS)のいずれかを用いた施設内検査室で、ROS1遺伝子融合に対する腫瘍検体の評価がプロスペクティブに実施された。
17人(32%)の患者は以前に全身治療を受けておらず、23人(43%)の患者は以前に1つの治療を受けており、13人(25%)の患者は以前に2ライン以上の治療を受けていた。CNS病変は、ベースライン時に23人(43%)の患者で認められた。31人(59%)の患者は喫煙したことがなく、52人(98%)の患者の組織型が腺がんであった。
- 有効性評価可能患者53人における客観的奏効率は、77%(95%CI、64-88)であった。患者の6%で完全奏効が得られ、72%で部分奏効が得られた。ベースライン時にCNS病変を有していた患者では、客観的奏効率が74%(95%CI、52-90)であり、すべての患者が部分奏効であった。ベースライン時にCNS病変を有していなかった患者では、客観的奏効率が80%(95%CI、61-92)であった(10%が完全奏効、70%が部分奏効)。[ 70 ][証拠レベル:3iiiDiv]
- 有効性評価可能患者におけるDOR中央値は24.6ヵ月(95%CI、11.4-34.8)であった;ベースライン時にCNS病変を有していた患者では12.6ヵ月(95%CI、6.5-推定不能)、ベースライン時にCNS病変を有していなかった患者では24.6ヵ月(95%CI、11.4-34.8)であった。
- 安全性評価可能集団の患者134人で治療関連有害事象(TRAE)が評価された。グレード1または2のTRAEは、79人(59%)の患者で観察された。グレード3または4のTRAEは、46人(34%)の患者で観察された。15人(11%)の患者が重篤なTRAEであった。治療関連死はみられなかった。
- 有効性評価可能患者におけるPFS中央値は、19ヵ月(95%CI、12.2-36.6)であった;ベースライン時にCNS病変を有していた患者では13.6ヵ月(95%CI、4.5-推定不能)、ベースライン時にCNS病変を有していなかった患者では26.3ヵ月(95%CI、15.7-36.6)であった。
クリゾチニブ
クリゾチニブは、以前に受けた全身療法の数に関係なく、転移性NSCLCで腫瘍がROS1陽性である患者に対して承認された。
証拠(クリゾチニブ):
- クリゾチニブに関する第I相研究の拡大コホートにおいて、進行期NSCLCでROS1再構成に対する検査が陽性となった患者50人が、クリゾチニブ、250mg、1日2回経口投与で治療された。[
71
]ROS1再構成は、分離プローブを用いたFISHまたは逆転写ポリメラーゼ連鎖反応測定により同定された。7人の患者(14%)は進行期疾患に対して以前に治療を受けておらず、21人の患者(42%)が以前に1つの治療を受けており、22人の患者(44%)は以前に2つ以上の治療を受けていた。主要エンドポイントは奏効率であった。
- 全奏効率は72%(95%CI、58-84)であった。6%の患者に完全奏効、66%に部分奏効、および18%に最良反応として疾患の安定が得られた。
- PFS中央値は19.2ヵ月(95%CI、14.4-未到達)であった。奏効期間は、17.6ヵ月(95%CI、14.5-未到達)と推定された。[ 71 ][証拠レベル:3iiiDiv]
- 1件の第II相オープンラベル単一群試験において、ROS1陽性NSCLCの東アジアの患者127人が、クリゾチニブ、250mg、1日2回で治療された。[
72
]24人の患者(18.9%)は進行期疾患に対して以前に治療を受けておらず、53人の患者(41.7%)が以前に1つの治療を受けており、50人の患者(39%)は以前に2つまたは3つの治療を受けていた。主要エンドポイントは独立判定による客観的奏効率であった。
- 客観的奏効率は71.7%(95%CI、63.0-79.3)であった。奏効率は、以前の治療の数に関係なくほぼ同じであった。13.4%の患者に完全奏効、58.3%の患者に部分奏効、および16.5%の患者に最良反応として疾患の安定が得られた。[ 72 ][証拠レベル:3iiiDiv]
- PFS中央値は15.9ヵ月(95%CI、12.9-24)であった。奏効期間は、19.7ヵ月(95%CI、14.1-未到達)であった。
- OS期間は32.5ヵ月(95%CI、32.5-未到達)であった。
NTRK阻害薬(NTRK融合が認められる患者に対して)
NTRKにおける体細胞遺伝子融合は、NSCLC腫瘍の0.5%未満を含めて一定範囲の固形腫瘍に発生する。[ 73 ][ 74 ]これらの融合は、肺腺がんの非喫煙者においてより頻繁に発生するようである。
ラロトレクチニブ
証拠(ラロトレクチニブ):
- ラロトレクチニブが3つのプロトコル:成人の第I相研究、小児の第I相/II相研究、および青年および成人の第II相研究で検討された。[
75
]腫瘍における融合は、FISHまたはNGS法を用いて確認された。併合解析に対する主要エンドポイントは独立したレビューによる客観的奏効率であり、奏効率について30%未満の下方限界を除外することを目標に調節因子からの情報を用いて実施された。全体では、年齢中央値45歳(範囲、生後4ヵ月~76歳)の55人の患者が、NTRK融合陽性の17の異なる腫瘍タイプについて登録された。患者はすべて、転移性疾患(82%)または局所進行切除不能疾患(18%)のいずれかを有した。登録された患者は以前に中央値で2つの全身療法を受けていた。
- 客観的奏効率は75%(95%CI、61%-75%)で、これらの反応の73%が6ヵ月以上持続した。[ 75 ][証拠レベル:3iiiDiv]
- 有害事象の93%がグレード1~2で、治療は十分に耐えられた;最も一般的なグレード3~4の有害事象は貧血(11%の患者)、高トランスアミナーゼ血症(7%)、および好中球減少(7%)であった。
既知の後天性の抵抗性変異が認められず、NTRK遺伝子融合が認められる局所進行または転移性腫瘍を有し、満足の行く代替療法がないか、治療後にがんが進行した患者の治療としてFDAはラロトレクチニブを承認した。
エヌトレクチニブ
既知の後天性の抵抗性変異が認められず、NTRK遺伝子融合が認められるか、転移性であるか、治療後にがんが進行したか、満足の行く代替療法がない固形腫瘍の治療、または外科的切除により重度の障害を来す可能性が高い症例に対して、エヌトレクチニブはFDAから加速承認を受けた。
証拠(エヌトレクチニブ):
- NTRK1、NTRK2、またはNTRK3遺伝子融合を有する転移性または局所進行固形腫瘍(NSCLCを含む)でNTRK阻害薬による治療歴のない患者におけるエヌトレクチニブの安全性および臨床活性は、初期段階の3件の多施設共同単群オープンラベル臨床試験(ALKA-372-001/EudraCT、2012-000148-88、STARTRK-1 [NCT02097810]、およびSTARTRK-2 [NCT02568267])の統合解析により決定された。[
76
]エヌトレクチニブからなる治療では、600mg以上の用量が1日1回経口投与された。主要エンドポイントは客観的奏効率およびDOR中央値で、盲検下の独立中央レビューにより評価された。注意すべき点として、無イベント期間(time-to-event)のエンドポイントは、対照群がない場合に解釈が困難である。NTRK遺伝子融合の陽性状態の同定は、施設内検査室または中央検査室で各種の核酸ベースの検査を用いてプロスペクティブに実施された。
NTRK遺伝子融合陽性の有効性評価可能集団の患者54人のうち、20人(37%)は以前に全身治療を受けておらず、11人(20%)は1つの全身治療を受けており、23人(43%)は2つ以上の全身治療を受けていた。べースライン時に12人(22%)の患者でCNS病変が認められていた。10人(19%)の患者がNSCLCであった。52人(96%)の患者では、NGSによりNTRK遺伝子融合が検出されており、2人(4%)の患者では、他の核酸ベースの検査によりNTRK遺伝子融合が検出されていた。
- 54人の患者における客観的奏効率は57%(95%CI、43.2-70.8)であった。患者の7%で完全奏効が得られ、50%で部分奏効が得られた。ベースライン時にCNS病変を有していた患者では、50%が奏効(すべて部分奏効)に達したのに対して、ベースライン時にCNS病変を有していなかった患者では、60%が奏効(10%が完全奏効;50%が部分奏効)に達した。[ 76 ][証拠レベル:3iiiDiv]
- 有効性評価可能患者におけるDOR中央値は、10.4ヵ月(95%CI、7.1-推定不能)であった。ベースライン時にCNS病変を有していた患者におけるDORは推定不能であり、ベースライン時にCNS病変を有していなかった患者では12.9ヵ月(95%CI、7.1-推定不能)であった。
- NSCLC患者10人では、奏効率が70%(95%CI、35-93)、DORが1.9ヵ月~20.1ヵ月の範囲であった。(詳しい情報については、処方情報を参照のこと。)
- 安全性評価可能集団は、腫瘍がNTRK融合陽性の患者68人から構成された。ほとんどのTRAEがグレード1または2であり、可逆性であった。特に頻度の高いグレード3または4のTRAEは、体重増加(10%)および貧血(12%)であった。重篤なTRAEは、7人(10%)の患者で報告された。TRAEのために、3人(4%)の患者が投与を中断し、27人(40%)の患者が用量を減量した。治療関連死はみられなかった。
- PFS中央値は11.2ヵ月(95%CI、8.0-14.9)であった。ベースライン時にCNS病変を有していた患者におけるPFS中央値は7.7ヵ月(95%CI、4.7-推定不能)であり、ベースライン時にCNS病変を有していなかった患者では12ヵ月(95%CI、8.7-15.7)であった。
化学療法を併用するまたは併用しない免疫チェックポイント阻害薬
ペムブロリズマブはヒト化モノクローナル抗体で、腫瘍細胞および腫瘍浸潤免疫細胞に発現するプログラム細胞死タンパク質1(PD1)共抑制免疫チェックポイントとそのリガンドであるプログラム細胞死リガンド1(PD-L1)および2(PD-L2)間の相互作用を阻害する。[ 77 ]
ペムブロリズマブ + 化学療法
証拠(ペムブロリズマブ + 化学療法):
- 1件の第III相二重盲検試験(KEYNOTE-189[NCT02578680])では、EGFR感作変異またはALK再構成を伴わない非扁平上皮性の転移性NSCLCで、転移性疾患に対して以前に治療を受けていない患者616人が2:1の比率でランダムに割り付けられた。患者はペメトレキセドとプラチナ製剤ベースの薬物 + 200mgのペムブロリズマブまたはプラセボを3週間ごとに4サイクル投与された後、最大で計35サイクルのペムブロリズマブまたはプラセボと維持ペメトレキセドを投与された。[
2
]プラセボを含む併用群の患者では増悪が確認された後に、ペムブロリズマブ単剤療法へのクロスオーバーが許可されていた。主要エンドポイントは盲検下での独立中央委員会の画像診断により評価されたOSおよびPFSであった。
- 追跡期間中央値23.1ヵ月後、ペムブロリズマブ併用群におけるOS中央値は22.0ヵ月(95%CI、19.5-25.2)であったのに対し、プラセボ併用群では10.7ヵ月(95%CI、8.7-13.6)であった(HR、0.56;95%CI、0.45−0.70)。[ 78 ][証拠レベル:1iA]
- ペムブロリズマブ併用群におけるPFS中央値は9.0ヵ月(95%CI、8.1-9.9)であったのに対し、プラセボ併用群では4.9ヵ月(4.7-5.5)であった(HR、0.48;95%CI、0.40-0.58)。
- すべてのPD-L1カテゴリーにわたり、また肝転移/脳転移が存在する状況で、生存期間の改善が示された。
- グレード3以上の有害事象の発生頻度は両治療群でほぼ同じであった(ペムブロリズマブ併用群で71.9% vs プラセボ併用群で66.8%)。
- Research and Treatment of Cancer Quality-of-Life Questionnaire-Core 30(QLQ-C30)およびLung Cancer 13(QLQ-LC13)により測定された全般的健康状態/生活の質スコアは、ペムブロリズマブ化学療法群でより良好に維持されていた(群間差;5.3ポイント[1.1-9.5];P = 0.014)。咳嗽、胸痛、または呼吸困難の悪化までの時間の中央値は、ペムブロリズマブ化学療法群が未到達(95%CI、10.2ヵ月-未到達)で、プラセボ + ペメトレキセド-プラチナ製剤群が7.0ヵ月(4.8ヵ月-未到達)であった(HR、0.81 [95%CI、0.60-1.09];P = 0.16)。[ 79 ]
ペムブロリズマブ単独
証拠(ペムブロリズマブ単独):
- 第III相オープンラベル研究(KEYNOTE-024)では、未治療の進行期NSCLCで、腫瘍細胞の50%以上にPD-L1が発現しているが、感受性を増加させるEGFR変異またはALK転座は認められない305人の患者が、ペムブロリズマブ静注(200mgを3週間ごとに最大35サイクル)またはプラチナ製剤をベースにした化学療法(研究者の選択で4~6サイクル;非扁平上皮性腫瘍にはペメトレキセド維持療法が許可された)のいずれかにランダムに割り付けられた。[
77
]主要エンドポイントはPFSであった。
- PD-L1発現は、PD-L1免疫組織化学22C3 pharmDxアッセイ(Dako North America)を用いて集中的に評価された。腫瘍細胞の50%以上におけるPD-L1発現は、調査された患者サンプル1,653人の30.2%で明らかにされた。
- ペムブロリズマブでは、PFS中央値における有意な改善が実証された(10.3ヵ月 vs 6.0ヵ月;HR、0.50;95%CI、0.37-0.68;P < 0.001)。全奏効率(44.8% vs 27.8%)、奏効期間中央値(未到達、[範囲、1.9+~14.5+ヵ月] vs 6.3ヵ月[範囲、2.1+~12.6+ヵ月])、および6ヵ月経過時の推定OS率(80.2% vs 72.4%;HR、0.60;95%CI、0.41-0.89;P = 0.005)はいずれも、化学療法よりもペムブロリズマブの方が高かった。
- この研究をさらに追跡したところ、ペムブロリズマブを支持するOSの優位性が確認された;OS中央値はペムブロリズマブを受けた患者で30ヵ月(95%CI、18.3ヵ月-未到達)であったのに対し、化学療法を受けた患者では14.2ヵ月で、後に75%が免疫療法にクロスオーバーしていたが、クロスオーバーは生存に影響しないことが示唆された。[ 80 ]
- 有害事象(すべてのグレード)の頻度は化学療法よりもペムブロリズマブの方が低かった(73.4% vs 90.0%)。
- グレード3~5の有害事象は、ペムブロリズマブで治療された患者の26.6%にみられ、化学療法で治療された患者では53.3%にみられた。
- グレード3~4の免疫関連イベントはペムブロリズマブで治療された患者の9.7%に起こり、化学療法で治療された患者では0.7%に起こった。
- ペムブロリズマブに関連した最も一般的なグレード3または4の免疫関連イベントは、重度の皮膚反応(3.9%)、肺炎(2.6%)、および結腸炎(1.3%)であった。
- グレード5の免疫関連イベントはみられなかった。
- ペムブロリズマブ治療により、化学療法と比較してPFS、OS、および奏効期間が有意に改善し、有害事象の頻度が低かったことが実証された。[ 77 ][証拠レベル:1iiDiii]
ペメトレキセドおよびカルボプラチンと併用するペムブロリズマブは、PD-L1発現に関係なく非扁平上皮性の転移性NSCLC患者に対する第一選択治療としてFDAの承認を受けた。ペムブロリズマブはまた、NSCLCで腫瘍にPD-L1が発現している(FDA承認の検査で50%以上の染色と定められた)患者に対する第一選択単剤治療としての承認も受けた。患者はEGFRまたはALKにゲノム異常がみられる腫瘍を有し、ペムブロリズマブを投与される前にFDAにより承認された治療法で疾患が進行している必要がある(ペムブロリズマブのFDAラベルを参照のこと)。
局所療法および特別な考慮事項
気管支内レーザー療法および/または近接照射療法(閉塞病変に対して)
放射線療法は、NSCLCの局所病変による症候性患者で、以下のいずれかの症状の緩和に有効な可能性がある:
- 気管、食道、または気管支の圧迫。
- 疼痛。
- 声帯麻痺。
- 喀血。
- 上大静脈症候群。
症例によっては、気管支内レーザー療法および/または近接照射療法が、中枢寄りの閉塞病変を改善するために使用されている。[ 19 ]
EBRT(主に局所症候性腫瘍の増殖を一時的に緩和するため)
EBRTは症状緩和目的で頻繁に処方されるが、どの分割照射法を使うべきかについてのコンセンサスは得られていない。さまざまな多分割レジメンで同様の症状緩和が得られるようであるが[ 81 ][ 82 ][ 83 ][ 84 ][ 85 ][ 86 ]、NCT00003685試験で証明されている通り、単回照射療法は少分割照射法または標準分割レジメンと比べ、症状緩和のためには不十分であろう。[ 20 ][証拠レベル:1iiC]高線量の放射線療法を施行した患者では、PSが良好なほど生存がわずかに延長するという証拠が得られている。[ 22 ][ 87 ][証拠レベル:1iiA]綿密に観察される症状のない患者では、症状または腫瘍の成長の徴候を認めるまで、しばしば治療は適宜延期される。
証拠(放射線療法):
二次原発腫瘍の治療
最初に切除した気管支がんからの単一の肺転移はまれである。肺は頻繁に、原発肺がん患者の二次原発悪性腫瘍の発生部位となる。新たな病変が新しい原発肺がんであるか転移であるかを見極めるのは難しい。ほとんどの患者で、新たな病変は二次原発腫瘍であり、切除後に長期生存を達成する患者もいることが研究により示されている。このため、最初の原発腫瘍が制御されている場合には、できれば二次原発腫瘍を切除すべきである。[ 89 ][ 90 ]
脳転移の治療
原発性非小細胞肺がん病変の切除後に単一の脳転移を来し、頭蓋外腫瘍の証拠を認めない患者は、脳転移の外科的切除と術後の全脳照射により無病生存率の延長を達成できる。[ 91 ][ 92 ]このような条件下において切除不能な脳転移には定位放射線手術による治療を行う。[ 93 ]
切除および術後放射線療法を行った患者の約50%は脳に再発を招く;これらの患者の中には追加治療がふさわしい患者もいる。[ 94 ]PSが良好で、脳以外に転移の進行を認めない特定の患者では、再手術または定位放射線手術が、治療法選択肢に含まれる。[ 93 ][ 94 ]ほとんどの患者には、追加放射線療法が考えられる;しかしながら、この治療による症状緩和の利益は限られている。[ 95 ][証拠レベル:3iiiDiii]
新たに診断されたIV期、再燃および再発したNSCLCに対して臨床評価段階にある治療法の選択肢(第一選択治療)
新たに診断されたIV期、再発および再燃したNSCLCに対して臨床評価段階にある治療法の選択肢(第一選択治療)には以下のものがある:
- 臨床試験は第一選択治療として考えることができる。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Weick JK, Crowley J, Natale RB, et al.: A randomized trial of five cisplatin-containing treatments in patients with metastatic non-small-cell lung cancer: a Southwest Oncology Group study. J Clin Oncol 9 (7): 1157-62, 1991.[PUBMED Abstract]
- Gandhi L, Rodríguez-Abreu D, Gadgeel S, et al.: Pembrolizumab plus Chemotherapy in Metastatic Non-Small-Cell Lung Cancer. N Engl J Med 378 (22): 2078-2092, 2018.[PUBMED Abstract]
- Scagliotti GV, Parikh P, von Pawel J, et al.: Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced-stage non-small-cell lung cancer. J Clin Oncol 26 (21): 3543-51, 2008.[PUBMED Abstract]
- Langer CJ, Vangel M, Schiller J, et al.: Age-specific subanalysis of ECOG 1594: fit elderly patients (70-80 YRS) with NSCLC do as well as younger pts (<70). [Abstract] Proceedings of the American Society of Clinical Oncology 22: A-2571, 2003.[PUBMED Abstract]
- Langer CJ, Manola J, Bernardo P, et al.: Cisplatin-based therapy for elderly patients with advanced non-small-cell lung cancer: implications of Eastern Cooperative Oncology Group 5592, a randomized trial. J Natl Cancer Inst 94 (3): 173-81, 2002.[PUBMED Abstract]
- Ries LA: Influence of extent of disease, histology, and demographic factors on lung cancer survival in the SEER population-based data. Semin Surg Oncol 10 (1): 21-30, 1994 Jan-Feb.[PUBMED Abstract]
- Ramsey SD, Howlader N, Etzioni RD, et al.: Chemotherapy use, outcomes, and costs for older persons with advanced non-small-cell lung cancer: evidence from surveillance, epidemiology and end results-Medicare. J Clin Oncol 22 (24): 4971-8, 2004.[PUBMED Abstract]
- Effects of vinorelbine on quality of life and survival of elderly patients with advanced non-small-cell lung cancer. The Elderly Lung Cancer Vinorelbine Italian Study Group. J Natl Cancer Inst 91 (1): 66-72, 1999.[PUBMED Abstract]
- Takeda K, Kudoh S, Nakagawa K, et al.: Randomized phase III study of docetaxel (D) versus vinorelbine (V) for elderly patients (pts) with advanced non-small cell lung cancer (NSCLC): Results of a West Japan Thoracic Oncology Group trial (WJTOG9904). [Abstract] J Clin Oncol 23 (Suppl 16): A-7009, 2005.[PUBMED Abstract]
- Schiller JH, Harrington D, Belani CP, et al.: Comparison of four chemotherapy regimens for advanced non-small-cell lung cancer. N Engl J Med 346 (2): 92-8, 2002.[PUBMED Abstract]
- Belani CP, Fossella F: Elderly subgroup analysis of a randomized phase III study of docetaxel plus platinum combinations versus vinorelbine plus cisplatin for first-line treatment of advanced nonsmall cell lung carcinoma (TAX 326). Cancer 104 (12): 2766-74, 2005.[PUBMED Abstract]
- Lilenbaum RC, Herndon JE, List MA, et al.: Single-agent versus combination chemotherapy in advanced non-small-cell lung cancer: the cancer and leukemia group B (study 9730). J Clin Oncol 23 (1): 190-6, 2005.[PUBMED Abstract]
- Hensing TA, Peterman AH, Schell MJ, et al.: The impact of age on toxicity, response rate, quality of life, and survival in patients with advanced, Stage IIIB or IV nonsmall cell lung carcinoma treated with carboplatin and paclitaxel. Cancer 98 (4): 779-88, 2003.[PUBMED Abstract]
- Sweeney CJ, Zhu J, Sandler AB, et al.: Outcome of patients with a performance status of 2 in Eastern Cooperative Oncology Group Study E1594: a Phase II trial in patients with metastatic nonsmall cell lung carcinoma . Cancer 92 (10): 2639-47, 2001.[PUBMED Abstract]
- Zukin M, Barrios CH, Pereira JR, et al.: Randomized phase III trial of single-agent pemetrexed versus carboplatin and pemetrexed in patients with advanced non-small-cell lung cancer and Eastern Cooperative Oncology Group performance status of 2. J Clin Oncol 31 (23): 2849-53, 2013.[PUBMED Abstract]
- Tester WJ, Stephenson P, Langer CJ, et al.: ECOG 1599: randomized phase II study of paclitaxel/carboplatin or gemcitabine/cisplatin in performance status (PS) 2 patients with advanced non-small cell lung cancer (NSCLC). [Abstract] J Clin Oncol 22 (Suppl 14): A-7055, 630s, 2004.[PUBMED Abstract]
- Vansteenkiste JF, Vandebroek JE, Nackaerts KL, et al.: Clinical-benefit response in advanced non-small-cell lung cancer: A multicentre prospective randomised phase III study of single agent gemcitabine versus cisplatin-vindesine. Ann Oncol 12 (9): 1221-30, 2001.[PUBMED Abstract]
- Hickish TF, Smith IE, O'Brien ME, et al.: Clinical benefit from palliative chemotherapy in non-small-cell lung cancer extends to the elderly and those with poor prognostic factors. Br J Cancer 78 (1): 28-33, 1998.[PUBMED Abstract]
- Miller JI, Phillips TW: Neodymium:YAG laser and brachytherapy in the management of inoperable bronchogenic carcinoma. Ann Thorac Surg 50 (2): 190-5; discussion 195-6, 1990.[PUBMED Abstract]
- Bezjak A, Dixon P, Brundage M, et al.: Randomized phase III trial of single versus fractionated thoracic radiation in the palliation of patients with lung cancer (NCIC CTG SC.15). Int J Radiat Oncol Biol Phys 54 (3): 719-28, 2002.[PUBMED Abstract]
- Macbeth F, Toy E, Coles B, et al.: Palliative radiotherapy regimens for non-small cell lung cancer. Cochrane Database Syst Rev (3): CD002143, 2001.[PUBMED Abstract]
- Sundstrøm S, Bremnes R, Aasebø U, et al.: Hypofractionated palliative radiotherapy (17 Gy per two fractions) in advanced non-small-cell lung carcinoma is comparable to standard fractionation for symptom control and survival: a national phase III trial. J Clin Oncol 22 (5): 801-10, 2004.[PUBMED Abstract]
- Delbaldo C, Michiels S, Rolland E, et al.: Second or third additional chemotherapy drug for non-small cell lung cancer in patients with advanced disease. Cochrane Database Syst Rev (4): CD004569, 2007.[PUBMED Abstract]
- Ardizzoni A, Boni L, Tiseo M, et al.: Cisplatin- versus carboplatin-based chemotherapy in first-line treatment of advanced non-small-cell lung cancer: an individual patient data meta-analysis. J Natl Cancer Inst 99 (11): 847-57, 2007.[PUBMED Abstract]
- Jiang J, Liang X, Zhou X, et al.: A meta-analysis of randomized controlled trials comparing carboplatin-based to cisplatin-based chemotherapy in advanced non-small cell lung cancer. Lung Cancer 57 (3): 348-58, 2007.[PUBMED Abstract]
- Hotta K, Matsuo K, Ueoka H, et al.: Meta-analysis of randomized clinical trials comparing Cisplatin to Carboplatin in patients with advanced non-small-cell lung cancer. J Clin Oncol 22 (19): 3852-9, 2004.[PUBMED Abstract]
- D'Addario G, Pintilie M, Leighl NB, et al.: Platinum-based versus non-platinum-based chemotherapy in advanced non-small-cell lung cancer: a meta-analysis of the published literature. J Clin Oncol 23 (13): 2926-36, 2005.[PUBMED Abstract]
- Rajeswaran A, Trojan A, Burnand B, et al.: Efficacy and side effects of cisplatin- and carboplatin-based doublet chemotherapeutic regimens versus non-platinum-based doublet chemotherapeutic regimens as first line treatment of metastatic non-small cell lung carcinoma: a systematic review of randomized controlled trials. Lung Cancer 59 (1): 1-11, 2008.[PUBMED Abstract]
- Pujol JL, Barlesi F, Daurès JP: Should chemotherapy combinations for advanced non-small cell lung cancer be platinum-based? A meta-analysis of phase III randomized trials. Lung Cancer 51 (3): 335-45, 2006.[PUBMED Abstract]
- Douillard JY, Laporte S, Fossella F, et al.: Comparison of docetaxel- and vinca alkaloid-based chemotherapy in the first-line treatment of advanced non-small cell lung cancer: a meta-analysis of seven randomized clinical trials. J Thorac Oncol 2 (10): 939-46, 2007.[PUBMED Abstract]
- Belani CP, Ramalingam S, Perry MC, et al.: Randomized, phase III study of weekly paclitaxel in combination with carboplatin versus standard every-3-weeks administration of carboplatin and paclitaxel for patients with previously untreated advanced non-small-cell lung cancer. J Clin Oncol 26 (3): 468-73, 2008.[PUBMED Abstract]
- Schuette W, Blankenburg T, Guschall W, et al.: Multicenter randomized trial for stage IIIB/IV non-small-cell lung cancer using every-3-week versus weekly paclitaxel/carboplatin. Clin Lung Cancer 7 (5): 338-43, 2006.[PUBMED Abstract]
- Sandler A, Gray R, Perry MC, et al.: Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer. N Engl J Med 355 (24): 2542-50, 2006.[PUBMED Abstract]
- Reck M, von Pawel J, Zatloukal P, et al.: Phase III trial of cisplatin plus gemcitabine with either placebo or bevacizumab as first-line therapy for nonsquamous non-small-cell lung cancer: AVAil. J Clin Oncol 27 (8): 1227-34, 2009.[PUBMED Abstract]
- Lynch TJ, Patel T, Dreisbach L, et al.: Cetuximab and first-line taxane/carboplatin chemotherapy in advanced non-small-cell lung cancer: results of the randomized multicenter phase III trial BMS099. J Clin Oncol 28 (6): 911-7, 2010.[PUBMED Abstract]
- Pirker R, Pereira JR, Szczesna A, et al.: Cetuximab plus chemotherapy in patients with advanced non-small-cell lung cancer (FLEX): an open-label randomised phase III trial. Lancet 373 (9674): 1525-31, 2009.[PUBMED Abstract]
- Khambata-Ford S, Harbison CT, Hart LL, et al.: Analysis of potential predictive markers of cetuximab benefit in BMS099, a phase III study of cetuximab and first-line taxane/carboplatin in advanced non-small-cell lung cancer. J Clin Oncol 28 (6): 918-27, 2010.[PUBMED Abstract]
- Paz-Ares L, Mezger J, Ciuleanu TE, et al.: Necitumumab plus pemetrexed and cisplatin as first-line therapy in patients with stage IV non-squamous non-small-cell lung cancer (INSPIRE): an open-label, randomised, controlled phase 3 study. Lancet Oncol 16 (3): 328-37, 2015.[PUBMED Abstract]
- Thatcher N, Hirsch FR, Luft AV, et al.: Necitumumab plus gemcitabine and cisplatin versus gemcitabine and cisplatin alone as first-line therapy in patients with stage IV squamous non-small-cell lung cancer (SQUIRE): an open-label, randomised, controlled phase 3 trial. Lancet Oncol 16 (7): 763-74, 2015.[PUBMED Abstract]
- Paz-Ares LG, de Marinis F, Dediu M, et al.: PARAMOUNT: Final overall survival results of the phase III study of maintenance pemetrexed versus placebo immediately after induction treatment with pemetrexed plus cisplatin for advanced nonsquamous non-small-cell lung cancer. J Clin Oncol 31 (23): 2895-902, 2013.[PUBMED Abstract]
- Brodowicz T, Krzakowski M, Zwitter M, et al.: Cisplatin and gemcitabine first-line chemotherapy followed by maintenance gemcitabine or best supportive care in advanced non-small cell lung cancer: a phase III trial. Lung Cancer 52 (2): 155-63, 2006.[PUBMED Abstract]
- Park JO, Kim SW, Ahn JS, et al.: Phase III trial of two versus four additional cycles in patients who are nonprogressive after two cycles of platinum-based chemotherapy in non small-cell lung cancer. J Clin Oncol 25 (33): 5233-9, 2007.[PUBMED Abstract]
- Paz-Ares L, de Marinis F, Dediu M, et al.: Maintenance therapy with pemetrexed plus best supportive care versus placebo plus best supportive care after induction therapy with pemetrexed plus cisplatin for advanced non-squamous non-small-cell lung cancer (PARAMOUNT): a double-blind, phase 3, randomised controlled trial. Lancet Oncol 13 (3): 247-55, 2012.[PUBMED Abstract]
- Socinski MA, Schell MJ, Peterman A, et al.: Phase III trial comparing a defined duration of therapy versus continuous therapy followed by second-line therapy in advanced-stage IIIB/IV non-small-cell lung cancer. J Clin Oncol 20 (5): 1335-43, 2002.[PUBMED Abstract]
- von Plessen C, Bergman B, Andresen O, et al.: Palliative chemotherapy beyond three courses conveys no survival or consistent quality-of-life benefits in advanced non-small-cell lung cancer. Br J Cancer 95 (8): 966-73, 2006.[PUBMED Abstract]
- Ciuleanu T, Brodowicz T, Zielinski C, et al.: Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer: a randomised, double-blind, phase 3 study. Lancet 374 (9699): 1432-40, 2009.[PUBMED Abstract]
- Belani CP, Brodowicz T, Ciuleanu TE, et al.: Quality of life in patients with advanced non-small-cell lung cancer given maintenance treatment with pemetrexed versus placebo (H3E-MC-JMEN): results from a randomised, double-blind, phase 3 study. Lancet Oncol 13 (3): 292-9, 2012.[PUBMED Abstract]
- Cappuzzo F, Ciuleanu T, Stelmakh L, et al.: Erlotinib as maintenance treatment in advanced non-small-cell lung cancer: a multicentre, randomised, placebo-controlled phase 3 study. Lancet Oncol 11 (6): 521-9, 2010.[PUBMED Abstract]
- Coudert B, Ciuleanu T, Park K, et al.: Survival benefit with erlotinib maintenance therapy in patients with advanced non-small-cell lung cancer (NSCLC) according to response to first-line chemotherapy. Ann Oncol 23 (2): 388-94, 2012.[PUBMED Abstract]
- Brugger W, Triller N, Blasinska-Morawiec M, et al.: Prospective molecular marker analyses of EGFR and KRAS from a randomized, placebo-controlled study of erlotinib maintenance therapy in advanced non-small-cell lung cancer. J Clin Oncol 29 (31): 4113-20, 2011.[PUBMED Abstract]
- Soria JC, Ohe Y, Vansteenkiste J, et al.: Osimertinib in Untreated EGFR-Mutated Advanced Non-Small-Cell Lung Cancer. N Engl J Med 378 (2): 113-125, 2018.[PUBMED Abstract]
- Mok TS, Wu YL, Thongprasert S, et al.: Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma. N Engl J Med 361 (10): 947-57, 2009.[PUBMED Abstract]
- Maemondo M, Inoue A, Kobayashi K, et al.: Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR. N Engl J Med 362 (25): 2380-8, 2010.[PUBMED Abstract]
- Mitsudomi T, Morita S, Yatabe Y, et al.: Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor (WJTOG3405): an open label, randomised phase 3 trial. Lancet Oncol 11 (2): 121-8, 2010.[PUBMED Abstract]
- Zhou C, Wu YL, Chen G, et al.: Erlotinib versus chemotherapy as first-line treatment for patients with advanced EGFR mutation-positive non-small-cell lung cancer (OPTIMAL, CTONG-0802): a multicentre, open-label, randomised, phase 3 study. Lancet Oncol 12 (8): 735-42, 2011.[PUBMED Abstract]
- Rosell R, Gervais R, Vergnenegre A, et al.: Erlotinib versus chemotherapy (CT) in advanced non-small cell lung cancer (NSCLC) patients (p) with epidermal growth factor receptor (EGFR) mutations: Interim results of the European Erlotinib Versus Chemotherapy (EURTAC) phase III randomized trial. [Abstract] J Clin Oncol 29 (Suppl 15): A-7503, 2011.[PUBMED Abstract]
- Rosell R, Carcereny E, Gervais R, et al.: Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer (EURTAC): a multicentre, open-label, randomised phase 3 trial. Lancet Oncol 13 (3): 239-46, 2012.[PUBMED Abstract]
- Sequist LV, Yang JC, Yamamoto N, et al.: Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations. J Clin Oncol 31 (27): 3327-34, 2013.[PUBMED Abstract]
- Yang JC, Wu YL, Schuler M, et al.: Afatinib versus cisplatin-based chemotherapy for EGFR mutation-positive lung adenocarcinoma (LUX-Lung 3 and LUX-Lung 6): analysis of overall survival data from two randomised, phase 3 trials. Lancet Oncol 16 (2): 141-51, 2015.[PUBMED Abstract]
- Wu YL, Zhou C, Hu CP, et al.: Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations (LUX-Lung 6): an open-label, randomised phase 3 trial. Lancet Oncol 15 (2): 213-22, 2014.[PUBMED Abstract]
- Peters S, Camidge DR, Shaw AT, et al.: Alectinib versus Crizotinib in Untreated ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med 377 (9): 829-838, 2017.[PUBMED Abstract]
- Hida T, Nokihara H, Kondo M, et al.: Alectinib versus crizotinib in patients with ALK-positive non-small-cell lung cancer (J-ALEX): an open-label, randomised phase 3 trial. Lancet 390 (10089): 29-39, 2017.[PUBMED Abstract]
- Solomon BJ, Mok T, Kim DW, et al.: First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med 371 (23): 2167-77, 2014.[PUBMED Abstract]
- Mok T, Kim D, Wu Y, et al.: First-line crizotinib versus pemetrexed-cisplatin or pemetrexed-carboplatin in patients (pts) with advanced ALK-positive non-squamous non-small cell lung cancer (NSCLC): results of a phase III study (PROFILE 1014). [Abstract] J Clin Oncol 32 (Suppl 15): A-8002, 2014.[PUBMED Abstract]
- Soria JC, Tan DSW, Chiari R, et al.: First-line ceritinib versus platinum-based chemotherapy in advanced ALK-rearranged non-small-cell lung cancer (ASCEND-4): a randomised, open-label, phase 3 study. Lancet 389 (10072): 917-929, 2017.[PUBMED Abstract]
- Kim DW, Tiseo M, Ahn MJ, et al.: Brigatinib in Patients With Crizotinib-Refractory Anaplastic Lymphoma Kinase-Positive Non-Small-Cell Lung Cancer: A Randomized, Multicenter Phase II Trial. J Clin Oncol 35 (22): 2490-2498, 2017.[PUBMED Abstract]
- Solomon BJ, Besse B, Bauer TM, et al.: Lorlatinib in patients with ALK-positive non-small-cell lung cancer: results from a global phase 2 study. Lancet Oncol 19 (12): 1654-1667, 2018.[PUBMED Abstract]
- Planchard D, Smit EF, Groen HJM, et al.: Dabrafenib plus trametinib in patients with previously untreated BRAF(V600E)-mutant metastatic non-small-cell lung cancer: an open-label, phase 2 trial. Lancet Oncol 18 (10): 1307-1316, 2017.[PUBMED Abstract]
- Gainor JF, Shaw AT: Novel targets in non-small cell lung cancer: ROS1 and RET fusions. Oncologist 18 (7): 865-75, 2013.[PUBMED Abstract]
- Drilon A, Siena S, Dziadziuszko R, et al.: Entrectinib in ROS1 fusion-positive non-small-cell lung cancer: integrated analysis of three phase 1-2 trials. Lancet Oncol 21 (2): 261-270, 2020.[PUBMED Abstract]
- Shaw AT, Ou SH, Bang YJ, et al.: Crizotinib in ROS1-rearranged non-small-cell lung cancer. N Engl J Med 371 (21): 1963-71, 2014.[PUBMED Abstract]
- Wu YL, Yang JC, Kim DW, et al.: Phase II Study of Crizotinib in East Asian Patients With ROS1-Positive Advanced Non-Small-Cell Lung Cancer. J Clin Oncol 36 (14): 1405-1411, 2018.[PUBMED Abstract]
- Farago AF, Le LP, Zheng Z, et al.: Durable Clinical Response to Entrectinib in NTRK1-Rearranged Non-Small Cell Lung Cancer. J Thorac Oncol 10 (12): 1670-4, 2015.[PUBMED Abstract]
- Gatalica Z, Xiu J, Swensen J, et al.: Molecular characterization of cancers with NTRK gene fusions. Mod Pathol 32 (1): 147-153, 2019.[PUBMED Abstract]
- Drilon A, Laetsch TW, Kummar S, et al.: Efficacy of Larotrectinib in TRK Fusion-Positive Cancers in Adults and Children. N Engl J Med 378 (8): 731-739, 2018.[PUBMED Abstract]
- Doebele RC, Drilon A, Paz-Ares L, et al.: Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol 21 (2): 271-282, 2020.[PUBMED Abstract]
- Reck M, Rodríguez-Abreu D, Robinson AG, et al.: Pembrolizumab versus Chemotherapy for PD-L1-Positive Non-Small-Cell Lung Cancer. N Engl J Med 375 (19): 1823-1833, 2016.[PUBMED Abstract]
- Gadgeel S, Rodríguez-Abreu D, Speranza G, et al.: Updated Analysis From KEYNOTE-189: Pembrolizumab or Placebo Plus Pemetrexed and Platinum for Previously Untreated Metastatic Nonsquamous Non-Small-Cell Lung Cancer. J Clin Oncol : JCO1903136, 2020.[PUBMED Abstract]
- Garassino MC, Gadgeel S, Esteban E, et al.: Patient-reported outcomes following pembrolizumab or placebo plus pemetrexed and platinum in patients with previously untreated, metastatic, non-squamous non-small-cell lung cancer (KEYNOTE-189): a multicentre, double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 21 (3): 387-397, 2020.[PUBMED Abstract]
- Reck M, Rodríguez-Abreu D, Robinson AG, et al.: Updated Analysis of KEYNOTE-024: Pembrolizumab Versus Platinum-Based Chemotherapy for Advanced Non-Small-Cell Lung Cancer With PD-L1 Tumor Proportion Score of 50% or Greater. J Clin Oncol 37 (7): 537-546, 2019.[PUBMED Abstract]
- Danson S, Middleton MR, O'Byrne KJ, et al.: Phase III trial of gemcitabine and carboplatin versus mitomycin, ifosfamide, and cisplatin or mitomycin, vinblastine, and cisplatin in patients with advanced nonsmall cell lung carcinoma. Cancer 98 (3): 542-53, 2003.[PUBMED Abstract]
- Pfister DG, Johnson DH, Azzoli CG, et al.: American Society of Clinical Oncology treatment of unresectable non-small-cell lung cancer guideline: update 2003. J Clin Oncol 22 (2): 330-53, 2004.[PUBMED Abstract]
- Smit EF, van Meerbeeck JP, Lianes P, et al.: Three-arm randomized study of two cisplatin-based regimens and paclitaxel plus gemcitabine in advanced non-small-cell lung cancer: a phase III trial of the European Organization for Research and Treatment of Cancer Lung Cancer Group--EORTC 08975. J Clin Oncol 21 (21): 3909-17, 2003.[PUBMED Abstract]
- Kubota K, Watanabe K, Kunitoh H, et al.: Phase III randomized trial of docetaxel plus cisplatin versus vindesine plus cisplatin in patients with stage IV non-small-cell lung cancer: the Japanese Taxotere Lung Cancer Study Group. J Clin Oncol 22 (2): 254-61, 2004.[PUBMED Abstract]
- Georgoulias V, Ardavanis A, Agelidou A, et al.: Docetaxel versus docetaxel plus cisplatin as front-line treatment of patients with advanced non-small-cell lung cancer: a randomized, multicenter phase III trial. J Clin Oncol 22 (13): 2602-9, 2004.[PUBMED Abstract]
- Sandler AB, Nemunaitis J, Denham C, et al.: Phase III trial of gemcitabine plus cisplatin versus cisplatin alone in patients with locally advanced or metastatic non-small-cell lung cancer. J Clin Oncol 18 (1): 122-30, 2000.[PUBMED Abstract]
- Lester JF, Macbeth FR, Toy E, et al.: Palliative radiotherapy regimens for non-small cell lung cancer. Cochrane Database Syst Rev (4): CD002143, 2006.[PUBMED Abstract]
- Ung YC, Yu E, Falkson C, et al.: The role of high-dose-rate brachytherapy in the palliation of symptoms in patients with non-small-cell lung cancer: a systematic review. Brachytherapy 5 (3): 189-202, 2006 Jul-Sep.[PUBMED Abstract]
- Salerno TA, Munro DD, Blundell PE, et al.: Second primary bronchogenic carcinoma: life-table analysis of surgical treatment. Ann Thorac Surg 27 (1): 3-6, 1979.[PUBMED Abstract]
- Yellin A, Hill LR, Benfield JR: Bronchogenic carcinoma associated with upper aerodigestive cancers. J Thorac Cardiovasc Surg 91 (5): 674-83, 1986.[PUBMED Abstract]
- Patchell RA, Tibbs PA, Walsh JW, et al.: A randomized trial of surgery in the treatment of single metastases to the brain. N Engl J Med 322 (8): 494-500, 1990.[PUBMED Abstract]
- Mandell L, Hilaris B, Sullivan M, et al.: The treatment of single brain metastasis from non-oat cell lung carcinoma. Surgery and radiation versus radiation therapy alone. Cancer 58 (3): 641-9, 1986.[PUBMED Abstract]
- Loeffler JS, Kooy HM, Wen PY, et al.: The treatment of recurrent brain metastases with stereotactic radiosurgery. J Clin Oncol 8 (4): 576-82, 1990.[PUBMED Abstract]
- Arbit E, Wroński M, Burt M, et al.: The treatment of patients with recurrent brain metastases. A retrospective analysis of 109 patients with nonsmall cell lung cancer. Cancer 76 (5): 765-73, 1995.[PUBMED Abstract]
- Hazuka MB, Kinzie JJ: Brain metastases: results and effects of re-irradiation. Int J Radiat Oncol Biol Phys 15 (2): 433-7, 1988.[PUBMED Abstract]
- 進行性IV期、再燃および再発したNSCLCの治療
-
進行性IV期、再燃および再発したNSCLCに対する標準治療法の選択肢(第二選択治療)
進行性IV期、再燃および再発した非小細胞肺がん(NSCLC)患者に対する標準治療法の選択肢(第二選択以降の治療)には以下のものがある:
-
化学療法。
-
上皮成長因子受容体(EGFR)を標的にした治療。
-
第一選択化学療法後のEGFRを標的にした治療。
- 以前のEGFRを標的にした治療後の後天性EGFR T790M変異に対するEGFRを標的にした治療。
-
第一選択化学療法後のEGFRを標的にした治療。
- 未分化リンパ腫キナーゼ(ALK)を標的にしたチロシンキナーゼ阻害薬(TKI)。
-
BRAF V600EおよびMEK阻害薬(BRAF V600E変異を有する患者に対して)。
-
ROS1を標的にした治療。
-
神経栄養チロシンキナーゼ(NTRK)阻害薬(NTRK融合を有する患者に対して)。
-
免疫療法。
化学療法
化学療法の施行は、転移病変を有する患者に客観的反応と、わずかな生存の改善をもたらしている。[ 1 ][証拠レベル:1iiA]症状に関する反応を調べた複数の研究では、自覚的な症状の改善が客観的反応よりも頻繁に起こると報告されている。[ 2 ][ 3 ]パフォーマンスステータス(PS)が良好で症候的再発のある同意の得られた患者には、症状緩和のためにプラチナ製剤をベースにした化学療法レジメンによる治療が勧められる。プラチナ製剤をベースにした化学療法後に再燃した患者には、二次治療を考える。
ドセタキセル
証拠(ドセタキセル):
- 2件のプロスペクティブ・ランダム化試験では、ビノレルビン、イホスファミド、または最適な支持療法と比較して、ドセタキセルの投与による生存の改善を明らかにしている[ 4 ][ 5 ];しかし、二次治療法の対象となる患者の選択基準は十分に定義されていない。[ 6 ]
- 865人の患者を対象とし、毎週または3週間ごとに投与するドセタキセルの効力および安全性を評価する5件の試験のメタアナリシスが報告されている。[
7
]この解析では、以下が示された:
- 生存期間中央値は、3週間ごとに治療した患者で27.4週間、毎週治療した患者で26.1週間であった(P = 0.24、ログランク検定)。
- ドセタキセルの週1回投与では、好中球減少症および発熱性好中球減少症の重症度が有意に低いことが報告された(両者に対して、P < 0.001);しかしながら、貧血、血小板減少症、および非血液学的毒性作用では、有意差は認められなかった。
ドセタキセル + ラムシルマブ
証拠(ドセタキセル + ラムシルマブ):
- 1件の二重盲検プラセボ対照第III相研究では、Eastern Cooperative Oncology Group(ECOG)のPSが0~1で第一選択化学療法後に疾患が進行した1,253人の患者がドセタキセル + プラセボまたはドセタキセル + ラムシルマブを受ける群にランダムに割り付けられた。[
8
][証拠レベル:1iiA]ラムシルマブは血管内皮増殖因子受容体2の細胞外ドメインを標的にしたヒト免疫グロブリンG1モノクローナル抗体である。この研究の主要エンドポイントは全生存(OS)であり、副次エンドポイントは無増悪生存(PFS)および客観的奏効率であった。研究に登録した患者は非扁平上皮性または扁平上皮性NSCLCのいずれかを有した;ただし、高血圧をうまく制御できない患者、消化管穿孔または瘻孔、(ランダム化前の)6ヵ月以内に動脈血栓塞栓イベント、2ヵ月以内に大量の喀血、または3ヵ月以内にグレード3~4の消化管出血が認められた患者は除外された。さらに、試験には主要血管に転移しているまたは腫瘍内の空洞化が認められる腫瘍の患者は含められなかった。
- ドセタキセルへのラムシルマブの追加により、プラセボ + ドセタキセルと比較して、OS中央値(10.5ヵ月 vs 9.1ヵ月;ハザード比[HR]、0.86;95%信頼区間[CI]、0.75-0.98)、客観的奏効率(23% vs 14%)、およびPFS(4.5ヵ月 vs 3ヵ月)が増加した。ラムシルマブの追加によるOSの改善は、扁平上皮性および非扁平上皮性の組織型を有するサブグループで一貫しているようであった。
- グレード3~4の治療関連有害事象(TRAE)は、ドセタキセルおよびラムシルマブを受けた患者の79%にみられたのに対し、ドセタキセル + プラセボを受けた患者では71%にみられた。発熱性好中球減少、疲労、および高血圧はドセタキセルへのラムシルマブの追加によって一般的にみられた毒性作用であった。治療群間でグレード3~4の出血の発生率における有意差は認められなかった。
- この研究に基づいて、ドセタキセル化学療法へのラムシルマブの追加は、PSが良好な進行期NSCLCで、第一選択化学療法後に疾患が進行した患者に対して検討できる。
上皮成長因子受容体(EGFR)を標的にした治療
第一選択化学療法後のEGFRを標的にした治療
エルロチニブ
証拠(エルロチニブ):
- 2件のランダム化プラセボ対照試験では、第一選択または第二選択の化学療法後のNSCLC患者では、プラセボ群と比較して、エルロチニブにより生存期間および症状悪化までの時間が延長するが[
11
][
12
]、ドセタキセルまたはペメトレキセドを投与する標準的な第二選択の化学療法と比較すると、生存は改善されないことが示された。[
13
]
- 731人の患者を対象として、エルロチニブと最適な支持療法とを比較する試験が実施された;患者の49%が以前に2つの化学療法レジメンを受け、93%がプラチナ製剤をベースにした化学療法を受けていた。
- 過去に2種類の化学療法レジメンを受けていた患者では、OSが6.7ヵ月で、プラチナ製剤をベースにした化学療法を受けていた患者では4.7ヵ月であった。HRは0.70(P < 0.001)で、エルロチニブの方が良好であった。[ ][証拠レベル:1iiA]
- 第一選択のプラチナ製剤併用療法での疾患増悪後にエルロチニブと標準の第二選択化学療法とを比較し優位性を明らかにするようデザインされた試験(NCT00556322)において、424人の患者が各群にランダムに割り付けられた。
- 主要エンドポイントであるOSには差がみられなかった(OS中央値、5.3ヵ月 vs 5.5ヵ月;HR、0.96;95%CI、0.78-1.19)。[ ][証拠レベル:1iiA]
- 731人の患者を対象として、エルロチニブと最適な支持療法とを比較する試験が実施された;患者の49%が以前に2つの化学療法レジメンを受け、93%がプラチナ製剤をベースにした化学療法を受けていた。
ゲフィチニブ
証拠(ゲフィチニブ):
- ランダム化第III相試験で以前に治療を受けたNSCLC患者1,692人を対象にゲフィチニブ vs プラセボが評価され、以下が示された:
- ゲフィチニブによりOSは改善しない。
- 生存期間中央値では、全集団(ゲフィチニブ群で5.6ヵ月、プラセボ群で5.1ヵ月;HR、0.89;95%CI、0.77-1.02;P = 0.087)、または腺がん患者812人(6.3ヵ月 vs 5.4ヵ月;HR、0.84;CI、0.68-1.03;P = 0.089)の治療群間に有意差は認められなかった。
- 予め計画されたゲフィチニブ群とプラセボ群のサブグループの解析により、非喫煙者(n = 375;95%CI、0.67[0.49-0.92];P = 0.012;生存期間中央値8.9ヵ月 vs 6.1ヵ月)およびアジア系の患者(n = 342;95%CI、0.66[0.48-0.91];P = 0.01;生存期間中央値9.5ヵ月 vs 5.5ヵ月)についてゲフィチニブ群の方がプラセボ群よりも有意に長い生存期間が示された。[ ][証拠レベル:1iiA]
- 1件の大規模ランダム化試験では、局所進行または転移性NSCLCを有し、プラチナ製剤をベースにした化学療法で前処置された患者において、ゲフィチニブがドセタキセルと比較された。[
15
]この試験の主要目的は、複合主要解析により治療群間のOSを比較して、全集団を対象に非劣性を評価すること、およびintention-to-treat集団を対象にEGFR遺伝子コピー数が多い患者における優位性を評価することであった。1,466人の患者がゲフィチニブ投与(経口投与で250mg/日;n = 733)またはドセタキセル投与(静脈内投与で75mg/m2、3週間ごと;n = 733)にランダムに割り付けられた。
- OSに関してドセタキセルと比較したゲフィチニブの非劣性が確認された(HR、1.020;95%CI、0.905-1.150)。しかしながら、EGFR遺伝子コピー数が多い患者(患者85人 vs 89人)におけるゲフィチニブの優位性は証明されなかった(HR、1.09;95%CI、0.78-1.51;P = 0.62)。
- ゲフィチニブ群における最も一般的な有害事象は発疹またはざ瘡(49% vs 10%)および下痢(35% vs 25%)であった。ドセタキセル群では、好中球減少(5% vs 74%)、無力症(25% vs 47%)、および脱毛症(3% vs 36%)が最も一般的であった。
- この試験では、ドセタキセルと比較してゲフィチニブによる治療を受けた患者の生存の非劣性が確定したことから、ゲフィチニブは既に治療を受けた進行NSCLC患者に対する有効な治療法であることが示唆される。
エルロチニブおよびゲフィチニブに対する客観的奏効率は、非喫煙者、女性、東アジア系、腺がんおよび細気管支肺胞上皮がんの患者においてより高い。[ 16 ][ 17 ][ 18 ][ 19 ][ 20 ][ 21 ][ 22 ]反応は、EGFR-のチロシンキナーゼドメインにおいて感受性を増加させる変異の存在[ 17 ][ 18 ][ 19 ][ 21 ][ 22 ]、およびKRAS変異がないこと[ 20 ][ 21 ][ 22 ]と関連している可能性がある。[証拠レベル:3iiiDiii]免疫組織化学によりEGFR蛋白発現を認めるか、蛍光in situハイブリダイゼーション検査によりEGFR遺伝子コピー数の増加を示す患者では生存利益がより大きいと可能性がある[ 21 ][ 22 ]が、免疫組織化学によるEGFR検査の臨床的有用性については異議が唱えられている。[ 23 ]
アファチニブ
証拠(アファチニブ):
- 進行した扁平上皮がん患者における第二選択治療として、ErbBファミリー受容体に対する不可逆的阻害薬であるアファチニブがエルロチニブと比較されている。1件の第III相ランダム化比較試験(LUX-Lung 8[NCT01523587])では、IIIB/IV期扁平上皮性NSCLCで第一選択のプラチナ製剤ベースの化学療法後に疾患が進行した患者が、1:1の比率でアファチニブ(398人の患者、40mg、1日1回、経口投与)またはエルロチニブ(397人の患者、150mg、1日1回、経口投与)を受ける群にランダムに割り付けられた。[
24
][証拠レベル:1iiDiii]主要エンドポイントはPFSであった。副次エンドポイントには、OSと奏効率が含められた。
- 追跡期間中央値6.7ヵ月後、PFSは2.4ヵ月 vs 1.9ヵ月であった(HR、0.82;95%CI、0.68-1.00)。
- 追跡期間中央値18.4ヵ月後、OS中央値はアファチニブ群で有意に長かった(7.9ヵ月 vs 6.8ヵ月;HR、0.81;95%CI、0.69-0.95;P = 0.007)。6ヵ月生存率(63.6% vs 54.6%;P = 0.009)、12ヵ月生存率(36.4% vs 28.2%;P = 0.015)、および18ヵ月生存率(22% vs 14.4%;P = 0.013)はいずれも、アファチニブを投与された患者において有意に良好であった。
- 2群間で奏効率における有意差は認められなかった(6% vs 3%;P = 0.551)。
- 有害事象の頻度は2群間でほぼ同じであり、57%の患者がグレード3以上の有害事象を経験した。アファチニブではグレード3の治療による下痢および口内炎がより頻繁に発生した;しかしながら、グレード3の発疹またはざ瘡はエルロチニブを投与された患者においてより一般的にみられた。
- アファチニブは、エルロチニブと比較してIV期扁平上皮性NSCLC患者に対する第二選択治療として、別の選択肢である。
以前のEGFRを標的にした治療後の後天性EGFR T790M変異に対するEGFRを標的にした治療
オシメルチニブ
証拠(オシメルチニブ):
- 1件のオープンラベル第III相試験(AURA 3[NCT02151981])では、EGFR感作変異を有し、疾患が第一選択EGFR阻害薬後に進行し、Cobas® EGFR Mutation Testで定義されたT790M EGFR抵抗性変異を有したNSCLC患者においてオシメルチニブが研究された。[
25
]この試験では、419人の患者が(2:1の比率で)オシメルチニブ、80mg、1日1回、経口投与、またはペメトレキセド + カルボプラチンあるいはシスプラチン静注、3週間ごと、最大6サイクルのいずれかを受けるようにランダムに割り付けられた;化学療法群では維持ペメトレキセドが許可されていた。主要エンドポイントはPFSであった。
- オシメルチニブでは、PFS中央値の延長において化学療法より優れていた(10.1ヵ月 vs 4.4ヵ月;HR、0.30;95%CI、0.23-0.41;P < 0.001)。
- 客観的奏効率は、オシメルチニブで71%であったのに対し、プラチナ製剤による治療では31%であった(客観的奏効に対するオッズ比、5.39;95%CI、3.47-8.48;P < 0.001)。
- 中枢神経系(CNS)転移を来した144人の患者におけるPFS中央値は、オシメルチニブで8.5ヵ月であったのに対し、プラチナ製剤の治療法では4.2ヵ月(HR、0.32;95%CI、0.21-0.49)であった。
- グレード3以上の有害事象はオシメルチニブで治療された患者の23%に起こったのに対し、プラチナ製剤で治療された患者では47%に起こった。[ ][証拠レベル:1iiDiii]
ALKを標的にしたチロシンキナーゼ阻害薬(TKI)
第一選択化学療法後のALKを標的にしたTKI
クリゾチニブ
証拠(クリゾチニブ):
- 1件の研究(NCT00585195)では、ALK再構成が認められるNSCLC患者1,500人を対象としたスクリーニングにより、進行したALK陽性疾患の患者82人を同定し、それらの患者を、拡大コホート研究を行う臨床試験に登録し、第I相用量漸増試験でMETおよびALKのデュアル阻害薬であるクリゾチニブ250mgを28日サイクルで1日2回投与という推奨用量を確立した後、このコホート研究を開始した。[
26
]大半の患者は以前に治療を受けていた。
- 6.4ヵ月の平均治療期間で、全奏効率は57%(患者82人中47人、うち46人は部分奏効、1人は完全奏効が確認された);27人(33%)は疾患が安定していた。[ ][証拠レベル:3iiiD]
- 6ヵ月時のPFSの推定確率は72%であった。
- 1年OSは74%(95%CI、63-82)で、2年OSは54%(40-66)であった。
- 第二選択または第三選択治療としてクリゾチニブを投与されたALK陽性の患者30人の生存期間は、クリゾチニブ以外の第二選択療法が実施された別のコホートから同定されたALK陽性の対照群患者23人よりも有意に長かった(OS中央値、未到達[95%CI、14ヵ月-未到達] vs 6ヵ月[95%CI、4-17]、1年OS率、70%[95%CI、50-83] vs 44%[95%CI、23-64]、および2年OS率、55%[33-72] vs 12%[2-30];HR、0.36;95%CI、0.17-0.75;P = 0.004)。[ ][証拠レベル:3iiiD]
- 一般的にみられた毒性はグレード1または2(軽度)の消化管の副作用であった。
- ALK再構成が認められる患者は、再構成が認められない患者よりも若い傾向がみられた;大半の患者はタバコにほとんどまたは全く曝露していなかった;こうした患者腺がんを患っていた。
- 1件のオープンラベルのランダム化第III相研究では、IIIB/IV期NSCLCでALKに転座を有し、以前に1回プラチナ製剤をベースにした化学療法レジメンを受けたことのある患者347人が、クリゾチニブ(250mg、1日2回経口投与)または化学療法(ペメトレキセド未投与の場合はペメトレキセド、500mg/m2またはドセタキセル、75mg/m2を21日ごとに静脈内投与)を受けた。[
28
]
- 主要エンドポイントはPFSであった。PFS中央値は、クリゾチニブを支持して有意に長かった(7.7ヵ月 vs 3.0ヵ月、P < 0.001)。[ ][証拠レベル:1iiDiii]
- 副次エンドポイントのOSに有意差は認められなかったが、研究デザインにおいてかなりのクロスオーバーが実施された。
以前のALK TKI療法後のALKを標的にしたTKI
セリチニブ
証拠(セリチニブ):
- 1件の単一治療群のオープンラベル試験に、ALK転座IIIB/IV期NSCLCを有し、クリゾチニブ治療中に疾患が増悪したか、クリゾチニブに不耐性の患者163人が登録された。[
29
]
- 主要エンドポイントはResponse Evaluation Criteria In Solid Tumors(RECIST、バージョン1.0)に基づく客観的奏効率で、副次エンドポイントは奏効期間(DOR)であった。盲検下の独立レビューによる客観的奏効率は43.6%(95%CI、36-52)で、DOR中央値は7.1ヵ月(範囲、5.6~推定不能)であった。[ ][証拠レベル:3iiiDiv]
- 注目すべきこととして、患者の38%は消化管毒性のために用量の変更が必要であった;正常値の上限の5倍を超えるアラニントランスアミナーゼ上昇が27%の患者に認められた。
アレクチニブ
証拠(アレクチニブ):
- 1件の第II相オープンラベル試験(NCT01871805)では、ALK転座IIIB/IV期NSCLCを有し、クリゾチニブ治療後に疾患が増悪した患者87人が登録した。[
30
]
- 主要エンドポイントはRECIST(version 1.1)に基づく客観的奏効であった。この進行中の研究の主要エンドポイントを解析した時点で、48%の患者(95%CI、36-60)で部分奏効が確認され、32%で盲検化された独自のレビューによる疾患の安定が示された。DOR中央値は、13.5ヵ月(95%CI、6.7-推定不可能)であった。PFS中央値は、8.1ヵ月(95%CI、6.2-12.6)と推定された。[ ][証拠レベル:3iiiDiv]
- 16人の患者ではベースライン時に測定可能なCNS病変が認められ、このうち11人が以前に放射線療法を受けていた。CNSの全奏効率は75%(95%CI、48-93)で、25%の患者が完全奏効を達成し、50%の患者が部分奏効を達成した。
- 最も一般的な副作用は、重症度のグレードが1または2であった;23~36%の患者に発生した最も頻度の高い有害事象は、便秘、疲労、筋肉痛、および末梢浮腫であった。36%の患者では投与の中断が必要となり、16%では用量が減量された。
- 2件目の第II相オープンラベル試験に、ALK陽性IIIB/IV期NSCLCを有し、クリゾチニブ治療中に疾患が増悪した患者138人が登録した。[
31
]
- 主要エンドポイントは独立中央レビューによる客観的奏効率であった。客観的奏効率は50%(95%CI、41-59)であった。DOR中央値は11.2ヵ月(95%CI、9.6-未到達)であった。PFS中央値は、8.9ヵ月(95%CI、5.6-11.3)であった。[ ][証拠レベル:3iiiDiv]
- 測定可能なCNS病変が認められた35人の患者におけるCNSの客観的奏効率は57%(95%CI、39-74)であった。
- 主にグレード1または2で、25~33%の患者に発生した一般的な有害事象は、便秘、疲労、および末梢浮腫であった。
brigatinib
証拠(brigatinib):
- 1件の第II相オープンラベル試験(NCT02094573)では、ALK転座局所進行または転移性NSCLCを有し、クリゾチニブ治療後に疾患が増悪した患者222人が登録した。患者は90mg、1日1回投与(n = 112;109人が治療された)または90mg、1日1回、7日間の導入を経て180mg、1日1回投与(n = 110)を受けるようにランダムに割り付けられた。[
32
]
- 主要エンドポイントは客観的奏効率であり、研究者らにより評価された。客観的奏効率は、90mgが投与された患者で45%(97.5%CI、34-56)、180mgが投与された患者で54%(97.5%CI、43-65)であった。
- PFS中央値は、90mgの投与を受けた患者で9.2ヵ月(95%CI、7.4-15.6)で、180mgの投与を受けた患者で12.9ヵ月(95%CI、11.1-未到達)であった。
- データカットオフ時点でのDOR中央値は、90mgの投与を受けた患者で13.8ヵ月(95%CI、5.6-13.8)で、180mgの投与を受けた患者で11.1ヵ月(95%CI、9.2-13.8)であった。[ ][証拠レベル:1iiDiv]
- 測定可能なCNS病変が認められた患者におけるCNSの客観的奏効率は、90mgが1日1回投与された患者(n = 26)で42%、180mgが1日1回投与された患者(n = 18)で67%であった。
- 一般的な有害事象(主にグレード1または2で、高用量群患者の27~38%に発生した)は、吐き気、下痢、頭痛、および咳嗽であった。早期に発症した(発生中央値、2日目)肺の有害事象のサブセットは、治療を受けた219人の患者のうち14人に発生した(すべてのグレード、6%;グレード3以上、3%);180mgに増量後の発生は認められなかった。有害事象には、呼吸困難、低酸素、咳嗽、肺炎、または肺臓炎が含まれた。これらは投与を中断して管理された。14人の患者のうち7人では、brigatinibによる再治療が成功した。
- 米国食品医薬品局(FDA)により承認されたbrigatinibの用量は、90mg、1日1回、7日間であった;耐えられた場合は、用量が180mg、1日1回に増量された。
BRAF V600EおよびMEK阻害薬(BRAF V600E変異を有する患者に対して)。
BRAF V600E変異は、肺腺がんの1~2%に発生する。
ダブラフェニブおよびトラメチニブ
証拠(ダブラフェニブおよびトラメチニブ):
- 第II相多施設非ランダム化オープンラベル研究(NCT01336634)において、BRAF V600E変異の検査が陽性の転移性NSCLCに対する治療としてプラチナ製剤を含むレジメンを以前に少なくとも1~3つ以上受けた後に進行した患者57人がダブラフェニブ(BRAF阻害薬)、150mg、1日2回およびトラメチニブ(MEK阻害薬)、2mg、1日1回で治療された。[
33
]BRAF V600E変異は地域の検査で確認された。主要エンドポイントは研究者が評価した全奏効率であった。
- 全奏効率は63.2%(95%CI、49.3-75.6)であり、研究者と独立判定委員会による評価によって独自に算出された。研究者による評価では完全奏効は36例中2例であった;独立判定委員会ではすべての反応が部分奏効であったと考えられた。
- 研究者が評価したPFS中央値は9.7ヵ月(95%CI、6.9-19.6ヵ月)であった。DOR中央値は9.0ヵ月(95%CI、6.9-18.3)と推定された。OSデータはまだ不完全である。
- 49%の患者にグレード3または4の有害事象が少なくとも1回以上発生し、このうち最も一般的なものは、好中球減少、低ナトリウム血症、および貧血であった。[ 33 ][証拠レベル:3iiiDiv]
ダブラフェニブおよびトラメチニブの併用は、FDA承認の検査により検出されたBRAF V600E変異が腫瘍に認められたNSCLC患者の治療において承認された。
ROS1を標的にした治療
ROS1再構成はNSCLC患者の約1%に発生する。[ 34 ]クリゾチニブおよびエヌトレクチニブは、ROS1再構成を有するNSCLC患者への使用に対して承認されており、後者は頭蓋内病変に対する活性がより大きいとみられる。
エヌトレクチニブ
エヌトレクチニブは、以前に受けた全身療法の数に関係なく、腫瘍がROS1陽性である転移性NSCLC患者の治療に対してFDA承認を受けている。
証拠(エヌトレクチニブ):
- ROS1融合陽性の転移性NSCLCにおけるエヌトレクチニブの安全性および臨床活性は、3件の多施設共同単群オープンラベル臨床試験(ALKA-372-001/EudraCT、2012-000148-88、STARTRK-1 [NCT02097810]、およびSTARTRK-2 [NCT02568267])の統合解析により決定された。[
35
]エヌトレクチニブは、600mg以上の用量で1日1回経口投与された。主要エンドポイントは、盲検下の独立中央レビューにより決定された全奏効率およびDORであった。注意すべき点として、無イベント期間(time-to-event)のエンドポイントは、対照群がない場合に解釈が困難である。検査室で開発した検査として蛍光in situハイブリダイゼーション(FISH)または次世代塩基配列決定法(NGS)のいずれかを用いた施設内検査室で、ROS1遺伝子融合に対する腫瘍検体の評価がプロスペクティブに実施された。
17人(32%)の患者は以前に全身治療を受けておらず、23人(43%)の患者は以前に1つの治療を受けており、13人(25%)の患者は以前に2ライン以上の治療を受けていた。ベースライン時にCNS病変が23人(43%)の患者に認められた。31人(59%)の患者は喫煙したことがなく、52人(98%)の患者は組織型が腺がんであった。
- 有効性評価可能患者53人における全奏効率は、77%(95%CI、64-88)であった。患者の6%で完全奏効が得られ、72%で部分奏効が得られた。ベースライン時にCNS病変を有していた患者では、全奏効率が74%であり、すべての患者が部分奏効であった。ベースライン時にCNS病変を有していなかった患者では、全奏効率が80%(10%が完全奏効;70%が部分奏効)であった。[ 35 ][証拠レベル:3iiiDiv]
- DOR中央値は24.6ヵ月(95%CI、11.4-34.8)であった;ベースライン時にCNS病変を有していた患者では12.6ヵ月(95%CI、6.5-推定不能)、ベースライン時にCNS病変を有していなかった患者では24.6ヵ月(95%CI、11.4-34.8)であった。
- TRAEは、安全性評価可能集団の患者134人で評価された。グレード1または2のTRAEは、79人(59%)の患者で観察された。グレード3または4のTRAEは、46人(34%)の患者で観察された。15人(11%)の患者が重篤なTRAEであった。治療関連死はみられなかった。
- PFS中央値は、19ヵ月(95%CI、12.2-36.6)であった;ベースライン時にCNS病変を有していた患者では13.6ヵ月(95%CI、4.5-推定不能)、ベースライン時にCNS病変を有していなかった患者では26.3ヵ月(95%CI、15.7-36.6)であった。
クリゾチニブ
クリゾチニブは、以前に受けた全身療法の数に関係なく、転移性NSCLCで腫瘍がROS1陽性である患者に対して承認された。
証拠(クリゾチニブ):
- クリゾチニブに関する第I相研究の拡大コホートにおいて、進行期NSCLCでROS1再構成に対する検査が陽性となった患者50人が、クリゾチニブ、250mg、1日2回経口投与で治療された。[
36
]ROS1再構成は、分離プローブを用いたFISHまたは逆転写ポリメラーゼ連鎖反応測定により同定された。7人(14%)の患者は進行期疾患に対して以前に治療を受けておらず、21人(42%)の患者が以前に1つの治療を受けており、22人(44%)の患者は以前に2つ以上の治療を受けていた。主要エンドポイントは奏効率であった。
- 全奏効率は72%(95%CI、58-84)であった。6%の患者に完全奏効、66%に部分奏効、および18%に最良反応として疾患の安定が得られた。
- PFS中央値は19.2ヵ月(95%CI、14.4-未到達)であった。DORは、17.6ヵ月(95%CI、14.5-未到達)と推定された。[ 36 ][証拠レベル:3iiiDiv]
- 1件の第II相オープンラベル単一群試験において、ROS1陽性NSCLCの東アジアの患者127人が、クリゾチニブ、250mg、1日2回で治療された。[
37
]24人の患者(18.9%)は進行期疾患に対して以前に治療を受けておらず、53人の患者(41.7%)が以前に1つの治療を受けており、50人の患者(39%)は以前に2つまたは3つの治療を受けていた。主要エンドポイントは独立判定による客観的奏効率であった。
- 客観的奏効率は71.7%(95%CI、63.0-79.3)であった。奏効率は、以前の治療の数に関係なくほぼ同じであった。13.4%の患者に完全奏効、58.3%の患者に部分奏効、および16.5%の患者に最良反応として疾患の安定が得られた。[ 37 ][証拠レベル:3iiiDiv]
- PFS中央値は15.9ヵ月(95%CI、12.9-24)であった。奏効期間は、19.7ヵ月(95%CI、14.1-未到達)であった。
- OS期間は32.5ヵ月(95%CI、32.5-未到達)であった。
NTRK阻害薬(NTRK融合が認められる患者に対して)
NTRKにおける体細胞遺伝子融合は、NSCLC腫瘍の0.5%未満を含めて一定範囲の固形腫瘍に発生する。[ 38 ][ 39 ]これらの融合は、肺腺がんの非喫煙者においてより頻繁に発生するようである。
ラロトレクチニブ
証拠(ラロトレクチニブ):
- ラロトレクチニブが3つのプロトコル:成人の第I相研究、小児の第I相/II相研究、および青年および成人の第II相研究で検討された。[
40
]腫瘍における融合は、FISHまたはNGS法を用いて確認された。併合解析に対する主要エンドポイントは独立したレビューによる客観的奏効率であり、奏効率について30%未満の下方限界を除外することを目標に調節因子からの情報を用いて実施された。全体では、年齢中央値45歳(範囲、生後4ヵ月~76歳)の55人の患者が、NTRK融合陽性の17の異なる腫瘍タイプについて登録された。患者はすべて、転移性疾患(82%)または局所進行切除不能疾患(18%)のいずれかを有した。登録された患者は以前に中央値で2つの全身療法を受けていた。
- 客観的奏効率は75%(95%CI、61%-75%)で、これらの反応の73%が6ヵ月以上持続した。[ 40 ][証拠レベル:3iiiDiv]
- 有害事象の93%がグレード1~2で、治療は十分に耐えられた;最も一般的なグレード3~4の有害事象は貧血(11%の患者)、高トランスアミナーゼ血症(7%)、および好中球減少(7%)であった。
既知の後天性の抵抗性変異が認められず、NTRK遺伝子融合が認められる局所進行または転移性腫瘍を有し、満足の行く代替療法がないか、治療後にがんが進行した患者の治療としてFDAはラロトレクチニブを承認した。
エヌトレクチニブ
既知の後天性の抵抗性変異が認められず、NTRK遺伝子融合が認められるか、転移性であるか、治療後にがんが進行したか、満足の行く代替療法がない固形腫瘍の治療、または外科的切除により重度の障害を来す可能性が高い症例に対して、エヌトレクチニブはFDAから加速承認を受けた。
証拠(エヌトレクチニブ):
-
NTRK1、NTRK2、またはNTRK3遺伝子融合を有する転移性または局所進行固形腫瘍(NSCLCを含む)でNTRK阻害薬による治療歴のない患者におけるエヌトレクチニブの安全性および臨床活性は、初期段階の3件の多施設共同単群オープンラベル臨床試験(ALKA-372-001/EudraCT、2012-000148-88、STARTRK-1 [NCT02097810]、およびSTARTRK-2 [NCT02568267])の統合解析により決定された。[
41
]エヌトレクチニブからなる治療では、600mg以上の用量が1日1回経口投与された。主要エンドポイントは客観的奏効率およびDOR中央値で、盲検下の独立中央レビューにより評価された。注意すべき点として、無イベント期間(time-to-event)のエンドポイントは、対照群がない場合に解釈が困難である。NTRK遺伝子融合の陽性状態の同定は、施設内検査室または中央検査室で各種の核酸ベースの検査を用いてプロスペクティブに実施された。
NTRK遺伝子融合陽性の有効性評価可能集団の患者54人のうち、20人(37%)は以前に全身治療を受けておらず、11人(20%)は1つの全身治療を受けており、23人(43%)は2つ以上の全身治療を受けていた。べースライン時にCNS病変が12人(22%)の患者に認められた。10人(19%)の患者がNSCLCであった。52人(96%)の患者では、NGSによりNTRK遺伝子融合が検出されており、2人(4%)の患者では、他の核酸ベースの検査によりNTRK遺伝子融合が検出されていた。
- 54人の患者における客観的奏効率は57%(95%CI、43.2-70.8)であった。患者の7%で完全奏効が得られ、50%で部分奏効が得られた。ベースライン時にCNS病変を有していた患者では、全奏効率が50%(すべて部分奏効)であったのに対して、ベースライン時にCNS病変を有していなかった患者では、全奏効率が60%(10%が完全奏効;50%が部分奏効)であった。[ 41 ][証拠レベル:3iiiDiv]
- DOR中央値は、10.4ヵ月(95%CI、7.1-推定不能)であった。ベースライン時にCNS病変を有していた患者におけるDORは推定不能であったが、ベースライン時にCNS病変を有していなかった患者では12.9ヵ月(95%CI、7.1-推定不能)であった。
- NSCLC患者10人で、全奏効率が70%(95%CI、35-93)、DORが1.9ヵ月~20.1ヵ月の範囲であった。(詳しい情報については、処方情報を参照のこと。)
- 安全性評価可能集団は、腫瘍がNTRK融合陽性の患者68人から構成された。ほとんどのTRAEがグレード1または2であり、可逆性であった。特に頻度の高いグレード3または4のTRAEは、体重増加(10%)および貧血(12%)であった。重篤なTRAEは、7人(10%)の患者で報告された。TRAEのために、3人(4%)の患者が投与を中断し、27人(40%)の患者が用量を減量した。治療関連死はみられなかった。
- PFS中央値は11.2ヵ月(95%CI、8.0-14.9)であった。ベースライン時にCNS病変を有していた患者におけるPFS中央値は7.7ヵ月(95%CI、4.7-推定不能)であり、ベースライン時にCNS病変を有していなかった患者では12ヵ月(95%CI、8.7-15.7)であった。
免疫療法
ニボルマブは、腫瘍細胞および腫瘍浸潤免疫細胞に発現するプログラム死1(PD-1)共抑制免疫チェックポイントを阻害する完全ヒトモノクローナル抗体である。[ 42 ][ 43 ]ペムブロリズマブはヒト化モノクローナル抗体で、腫瘍細胞および腫瘍浸潤免疫細胞に発現するプログラム細胞死リガンド1(PD-L1)共抑制免疫チェックポイントとそのリガンドであるPD-L1およびPD-L2間の相互作用を阻害する。[ 44 ]アテゾリズマブはPD-L1遮断抗体である。
ニボルマブ
証拠(ニボルマブ):
- 2件の第III相臨床試験(プラチナ製剤により以前に治療された進行期扁平上皮性NSCLCを有する患者に実施された1件と、非扁平上皮性NSCLCを有する患者に実施された1件)において、以前に標準治療法であったドセタキセル化学療法と比較して、ニボルマブはOSの有意な改善を実証した。[
42
][
43
][証拠レベル:1iiA]さらに、両試験でグレード3または4の治療関連毒性の割合は、ドセタキセルと比較してニボルマブでは有意に低かった。注目すべきこととして、ニボルマブの第III相研究に登録した患者はすべてECOGのPSが0または1であった;自己免疫疾患、症状が認められる間質性肺疾患を有する患者、または全身免疫抑制を受けている患者は登録から除外された。
- 1件のランダム化オープンラベル第III相試験では、進行期扁平上皮性NSCLCで、プラチナ製剤を含む化学療法レジメンを一度受けていた患者272人が、ニボルマブ(3mg/kg、2週間ごと)またはドセタキセル(75mg/m2、3週間ごと)を疾患が進行するまで投与する群にランダムに割り付けられた。[
42
]この研究の主要エンドポイントはOSであった。
- ニボルマブは、ドセタキセルと比較してOS中央値の有意な改善を実証した(9.2ヵ月 vs 6ヵ月;P < 0.001)。さらに、奏効率(20% vs 9%;P = 0.008)およびPFS中央値(3.5ヵ月 vs 2.8ヵ月;P < 0.001)は、ニボルマブの方が良好であった。
- 治療関連毒性の割合は、ニボルマブの方がドセタキセルよりも有意に低かった(すべてのグレードについて、ニボルマブで58% vs ドセタキセルで86%;グレード3~4について、ニボルマブで7% vs ドセタキセルで55%)。
- 1件のランダム化オープンラベル第III相試験では、進行期非扁平上皮性NSCLCで、プラチナ製剤を含む化学療法レジメンを一度受けていた患者582人が、ニボルマブ(3mg/kg、2週間ごと)またはドセタキセル(75mg/m2、3週間ごと)を疾患が進行するまで投与する群にランダムに割り付けられた。[
43
]第一選択のプラチナ製剤を含む2剤併用療法後は先の維持化学療法が許可された;EGFR突然変異またはALK転座を有する患者は、TKIによる追加の治療レジメンを受けることが許可された。この研究の主要エンドポイントはOSであった。
- ニボルマブは、ドセタキセルと比較して患者のOS中央値の有意な改善を実証した(12.2ヵ月 vs 9.4ヵ月;HR、0.73;96%信頼区間[CI]、0.59-0.89;P = 0.002)。この研究における奏効率(19% vs 12%;P = 0.02)は、ニボルマブの方が良好であったが、PFS中央値(ニボルマブで2.3ヵ月 vs ドセタキセルで4.2ヵ月)では変わらなかった。DOR中央値はニボルマブで17.2ヵ月およびドセタキセルで5.6ヵ月であった。
- 治療関連毒性の割合は、ニボルマブの方がドセタキセルよりも有意に低かった(すべてのグレードについて、ニボルマブで69% vs ドセタキセルで88%;グレード3~4について、ニボルマブで10% vs ドセタキセルで54%)。
- これらの両試験により、2年経過時の治療成績の長期臨床的有益性が実証された。扁平上皮性NSCLCにおけるドセタキセルと比較したニボルマブに対する2年経過時のOS率は23%(95%CI、16-30) vs 8%(95%CI、4-13)で、非扁平上皮性NSCLCにおけるOS率は29%(95%CI、24-34) vs 16%(95%CI、12-20)であった。[ 45 ]扁平上皮性NSCLCでの奏効者10人(37%)および非扁平上皮性NSCLCでの奏効者56人中19人(34%)で確認された反応は、2年経過時にも持続して観察された。両研究のドセタキセルで治療された患者で反応が持続していた者はなかった。
- 1件のランダム化オープンラベル第III相試験では、進行期扁平上皮性NSCLCで、プラチナ製剤を含む化学療法レジメンを一度受けていた患者272人が、ニボルマブ(3mg/kg、2週間ごと)またはドセタキセル(75mg/m2、3週間ごと)を疾患が進行するまで投与する群にランダムに割り付けられた。[
42
]この研究の主要エンドポイントはOSであった。
ニボルマブは現在では、プラチナ製剤をベースにした第一選択化学療法中または療法後に進行した転移性NSCLCを有する患者に対する標準の第二選択療法であると考えられており、ドセタキセルよりも生存を改善し、毒性作用の発生率が低い。しかしながら、現在までのニボルマブに関する臨床試験では自己免疫疾患の病歴、間質性肺疾患、またはECOGのPSが1を超える患者は登録されていない。自己免疫疾患の動きが活発な患者はニボルマブによる治療を行えない。治療による自己免疫毒性について、すべての患者を注意深く監視する必要がある。FDAのニボルマブのラベルには、自己免疫毒性を管理するための特殊なアルゴリズムが含まれる。
ペムブロリズマブ
証拠(ペムブロリズマブ):
- 複数の拡大コホートを用いた第I相研究において、ペムブロリズマブは、奏効率およびDORについて有意な活性を実証した。[
44
][証拠レベル:3iiiDiv]
- この研究では、495人の患者がペムブロリズマブ 2mg/kgの3週間ごと、10mg/kgの3週間ごと、または10mg/kgの2週間ごとのいずれかを投与された。異なる治療スケジュール間で有意差はみられなかった。主要な除外基準は、自己免疫疾患、肺炎の既往、全身免疫抑制療法の必要性、および1を超えるPSであった。客観的奏効率は19.4%(95%CI、16.0-23.2)で、これには治療歴のある患者394人における18.0%(95%CI、14.4-22.2)および治療歴のない患者101人における24.8%(95%CI、16.7-34.3)の奏効率を含んでいた。PFS中央値は、すべての患者について3.7ヵ月(95%CI、2.9-4.1)、治療歴のある患者で3.0ヵ月(95%CI、2.2-4.0)、および治療歴のない患者で6.0ヵ月(95%CI、4.1-8.6)であった。すべての患者におけるDOR中央値は、12.5ヵ月(範囲、1.0-23.3ヵ月)であった。
- この研究では、PD-L1レベルが高い患者におけるペムブロリズマブの効力が、抗PD-L1抗体クローン22C3による査定で評価された。妥当性検証群の患者73人における腫瘍細胞の50%以上における膜染色というカットオフ値を用いたところ、奏効率は45.2%(95%CI、33.5-57.3)、この群のPFS中央値は6.3ヵ月(95%CI、2.9-12.5)であった。発表の時点ではOS中央値に達していなかった。
- スクリーニングを受けた患者1,143人(このうち824人の標本が評価可能であった)について、PD-L1腫瘍細胞染色の推定割合は次の通りである:23.2%で腫瘍細胞の50%以上が染色した;37.6%では腫瘍細胞の1~49%が染色した;39.2%では腫瘍細胞の染色が1%未満であった。
- 最も一般的な有害事象は、疲労、そう痒症、および食欲減退であった。9.5%の患者でグレード3以上の有害事象が報告された。2%を超える患者に発生した炎症性および免疫介在性の有害事象は、注入に伴う反応(3.0%)、甲状腺機能低下症(6.9%)、および肺炎(3.6%)であった。
- 1件の第II/III相ランダム化臨床試験では、NSCLCを以前に治療され、腫瘍細胞の少なくとも1%以上でPD-L1発現が認められた患者がペムブロリズマブ(2mg/kg)、ペムブロリズマブ(10mg/kg)、またはドセタキセル(75mg/m2)を3週間ごとに投与される群(1:1:1)にランダムに割り付けられた。[
46
][証拠レベル:1iiA]主要エンドポイントは、全集団および腫瘍細胞の少なくとも50%以上でPD-L1発現が認められた患者におけるOSとPFSであった。この研究には1,034人の患者が登録された;このうち345人がペムブロリズマブ(2mg/kg)に割り付けられ;346人がペムブロリズマブ(10mg/kg)に割り付けられ;343人がドセタキセルに割り付けられた。
- 全集団におけるOS中央値は、ペムブロリズマブ(2mg/kg)で10.4ヵ月、ペムブロリズマブ(10mg/kg)で12.7ヵ月、およびドセタキセルで8.5ヵ月であった。OS期間は、ドセタキセルと比較したペムブロリズマブ(2mg/kg)(HR、0.71;95%CI、0.58-0.88;P = 0.0008)およびドセタキセルと比較したペムブロリズマブ(10mg/kg)(HR、0.61;CI、0.49-0.75;P < 0.0001)で有意に長かった。
- 全集団におけるPFSは、ドセタキセル群と比較したペムブロリズマブ群で延長されなかった。
- 腫瘍細胞の少なくとも50%以上でPD-L1発現が認められた患者におけるOSは、ドセタキセルよりもペムブロリズマブ(2mg/kg)(中央値、14.9ヵ月 vs 8.2ヵ月;HR、0.54;95%CI、0.38-0.77;P = 0.0002)およびドセタキセルよりもペムブロリズマブ(10mg/kg)(中央値、17.3ヵ月 vs 8.2ヵ月;HR、0.50;CI、0.36-0.70;P < 0.0001)で有意に長かった。
- 腫瘍細胞の少なくとも50%以上でPD-L1発現が認められた患者集団におけるPFSは、ドセタキセルよりもペムブロリズマブ(2mg/kg)(中央値、5.0ヵ月 vs 4.1ヵ月;HR、0.59、95%CI、0.44-0.78;P = 0.0001)およびドセタキセルよりもペムブロリズマブ(10mg/kg)(中央値、5.2ヵ月 vs 4.1ヵ月;HR、0.59;CI、0.45-0.78;P< 0.0001)で有意に長かった。
- グレード3~5の治療関連有害事象はドセタキセルよりもペムブロリズマブの方が低頻度であった(ペムブロリズマブ(2mg/kg)投与患者339人中43人[13%]、ペムブロリズマブ(10mg/kg)投与患者343人中55人[16%]、およびドセタキセル投与患者309人中109人[35%])。
ペムブロリズマブは、第一選択化学療法中または後に進行したNSCLC患者で腫瘍にPD-L1が発現している(FDA承認の検査で50%を超える染色と定められた)場合の第二選択療法として迅速承認を受けた。患者はEGFRまたはALKにゲノム異常がみられる腫瘍を有し、ペムブロリズマブを投与される前にFDAにより承認された治療法で疾患が進行している必要がある(ペムブロリズマブのFDAラベルを参照のこと)。
アテゾリズマブ
証拠(アテゾリズマブ):
- 2件の国際ランダム化オープンラベル臨床試験(OAK[NCT02008227]およびPOPLAR[NCT01903993])により、以前にプラチナ製剤による化学療法を受けた計1,137人のNSCLC患者における効力および安全性が実証された。[
47
][
48
][証拠レベル:1iiA]ドセタキセルと比較して、適応患者集団におけるアテゾリズマブによる治療により、OS期間がOAK研究では4.2ヵ月およびPOPLAR研究では2.9ヵ月改善した。
- OAK試験におけるアテゾリズマブ群のOS中央値は13.8ヵ月(95%CI、11.8-15.7)であったのに対し、ドセタキセル群では9.6ヵ月(95%CI、8.6-11.2)であった(HR = 0.74;95%CI、0.63-0.87;P = 0.0004)。
- POPLAR試験におけるアテゾリズマブ群のOS中央値は12.6ヵ月(95%CI、9.7-16.0)で、ドセタキセル群では9.7ヵ月(95%CI、8.6-12.0)であった(HR、0.69;95%CI、0.52-0.92)。
- 改善の大きさは腫瘍細胞および腫瘍浸潤免疫細胞でのPD-L1の免疫組織化学的発現と相関していたが、アテゾリズマブによる生存利益は腫瘍にPD-L1発現が認められる患者と認められない患者の双方で示された。
- POPLAR試験における最も一般的な(20%以上)有害反応はアテゾリズマブで治療された患者に認められ、疲労、食欲減退、呼吸困難、咳嗽、吐き気、筋骨格痛、および便秘がみられた。
- アテゾリズマブで治療された患者において最も一般的な(2%以上)グレード3~4の有害事象は、呼吸困難、肺炎、低酸素症、低ナトリウム血症、疲労、貧血、筋骨格痛、アスパラギン酸アミノトランスフェラーゼ増加、アラニンアミノトランスフェラーゼ増加、嚥下困難、および関節痛であった。
- アテゾリズマブを投与されている患者に対する臨床的に意義のある免疫関連有害事象として、肺炎、肝炎、結腸炎、および甲状腺疾患がみられた。
進行性IV期、再燃および再発したNSCLCに対して臨床評価段階にある治療法の選択肢(第二選択治療)
進行性IV期、再燃および再発したNSCLCに対して臨床評価段階にある治療法の選択肢(第二選択治療)には以下のものがある:
- 臨床試験は第二選択治療として考えることができる。
最新の臨床試験
NCIが支援しているがん臨床試験で現在患者登録中の試験を検索するには、臨床試験アドバンスト・サーチを使用のこと(なお、このサイトは日本語検索に対応していない。)。このサーチでは、試験の場所、治療の種類、薬物名やその他の基準による絞り込みが可能である。臨床試験に関する一般情報も入手することができる。
参考文献- Souquet PJ, Chauvin F, Boissel JP, et al.: Polychemotherapy in advanced non small cell lung cancer: a meta-analysis. Lancet 342 (8862): 19-21, 1993.[PUBMED Abstract]
- Ellis PA, Smith IE, Hardy JR, et al.: Symptom relief with MVP (mitomycin C, vinblastine and cisplatin) chemotherapy in advanced non-small-cell lung cancer. Br J Cancer 71 (2): 366-70, 1995.[PUBMED Abstract]
- Girling DJ, et al.: Randomized trial of etoposide cyclophosphamide methotrexate and vincristine versus etoposide and vincristine in the palliative treatment of patients with small-cell lung cancer and poor prognosis. Br J Cancer 67 (Suppl 20): A-4;2, 14, 1993.[PUBMED Abstract]
- Fossella FV, DeVore R, Kerr RN, et al.: Randomized phase III trial of docetaxel versus vinorelbine or ifosfamide in patients with advanced non-small-cell lung cancer previously treated with platinum-containing chemotherapy regimens. The TAX 320 Non-Small Cell Lung Cancer Study Group. J Clin Oncol 18 (12): 2354-62, 2000.[PUBMED Abstract]
- Shepherd FA, Dancey J, Ramlau R, et al.: Prospective randomized trial of docetaxel versus best supportive care in patients with non-small-cell lung cancer previously treated with platinum-based chemotherapy. J Clin Oncol 18 (10): 2095-103, 2000.[PUBMED Abstract]
- Huisman C, Smit EF, Giaccone G, et al.: Second-line chemotherapy in relapsing or refractory non-small-cell lung cancer: a review. J Clin Oncol 18 (21): 3722-30, 2000.[PUBMED Abstract]
- Di Maio M, Perrone F, Chiodini P, et al.: Individual patient data meta-analysis of docetaxel administered once every 3 weeks compared with once every week second-line treatment of advanced non-small-cell lung cancer. J Clin Oncol 25 (11): 1377-82, 2007.[PUBMED Abstract]
- Garon EB, Ciuleanu TE, Arrieta O, et al.: Ramucirumab plus docetaxel versus placebo plus docetaxel for second-line treatment of stage IV non-small-cell lung cancer after disease progression on platinum-based therapy (REVEL): a multicentre, double-blind, randomised phase 3 trial. Lancet 384 (9944): 665-73, 2014.[PUBMED Abstract]
- Hanna N, Shepherd FA, Fossella FV, et al.: Randomized phase III trial of pemetrexed versus docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy. J Clin Oncol 22 (9): 1589-97, 2004.[PUBMED Abstract]
- Scagliotti G, Hanna N, Fossella F, et al.: The differential efficacy of pemetrexed according to NSCLC histology: a review of two Phase III studies. Oncologist 14 (3): 253-63, 2009.[PUBMED Abstract]
- Shepherd FA, Rodrigues Pereira J, Ciuleanu T, et al.: Erlotinib in previously treated non-small-cell lung cancer. N Engl J Med 353 (2): 123-32, 2005.[PUBMED Abstract]
- Bezjak A, Tu D, Seymour L, et al.: Symptom improvement in lung cancer patients treated with erlotinib: quality of life analysis of the National Cancer Institute of Canada Clinical Trials Group Study BR.21. J Clin Oncol 24 (24): 3831-7, 2006.[PUBMED Abstract]
- Ciuleanu T, Stelmakh L, Cicenas S, et al.: Efficacy and safety of erlotinib versus chemotherapy in second-line treatment of patients with advanced, non-small-cell lung cancer with poor prognosis (TITAN): a randomised multicentre, open-label, phase 3 study. Lancet Oncol 13 (3): 300-8, 2012.[PUBMED Abstract]
- Thatcher N, Chang A, Parikh P, et al.: Gefitinib plus best supportive care in previously treated patients with refractory advanced non-small-cell lung cancer: results from a randomised, placebo-controlled, multicentre study (Iressa Survival Evaluation in Lung Cancer). Lancet 366 (9496): 1527-37, 2005 Oct 29-Nov 4.[PUBMED Abstract]
- Kim ES, Hirsh V, Mok T, et al.: Gefitinib versus docetaxel in previously treated non-small-cell lung cancer (INTEREST): a randomised phase III trial. Lancet 372 (9652): 1809-18, 2008.[PUBMED Abstract]
- Miller VA, Kris MG, Shah N, et al.: Bronchioloalveolar pathologic subtype and smoking history predict sensitivity to gefitinib in advanced non-small-cell lung cancer. J Clin Oncol 22 (6): 1103-9, 2004.[PUBMED Abstract]
- Paez JG, Jänne PA, Lee JC, et al.: EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy. Science 304 (5676): 1497-500, 2004.[PUBMED Abstract]
- Lynch TJ, Bell DW, Sordella R, et al.: Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib. N Engl J Med 350 (21): 2129-39, 2004.[PUBMED Abstract]
- Pao W, Miller V, Zakowski M, et al.: EGF receptor gene mutations are common in lung cancers from "never smokers" and are associated with sensitivity of tumors to gefitinib and erlotinib. Proc Natl Acad Sci U S A 101 (36): 13306-11, 2004.[PUBMED Abstract]
- Pao W, Wang TY, Riely GJ, et al.: KRAS mutations and primary resistance of lung adenocarcinomas to gefitinib or erlotinib. PLoS Med 2 (1): e17, 2005.[PUBMED Abstract]
- Tsao MS, Sakurada A, Cutz JC, et al.: Erlotinib in lung cancer - molecular and clinical predictors of outcome. N Engl J Med 353 (2): 133-44, 2005.[PUBMED Abstract]
- Hirsch FR, Varella-Garcia M, Bunn PA, et al.: Molecular predictors of outcome with gefitinib in a phase III placebo-controlled study in advanced non-small-cell lung cancer. J Clin Oncol 24 (31): 5034-42, 2006.[PUBMED Abstract]
- Clark GM, Zborowski DM, Culbertson JL, et al.: Clinical utility of epidermal growth factor receptor expression for selecting patients with advanced non-small cell lung cancer for treatment with erlotinib. J Thorac Oncol 1 (8): 837-46, 2006.[PUBMED Abstract]
- Soria JC, Felip E, Cobo M, et al.: Afatinib versus erlotinib as second-line treatment of patients with advanced squamous cell carcinoma of the lung (LUX-Lung 8): an open-label randomised controlled phase 3 trial. Lancet Oncol 16 (8): 897-907, 2015.[PUBMED Abstract]
- Mok TS, Wu Y-L, Ahn M-J, et al.: Osimertinib or Platinum-Pemetrexed in EGFR T790M-Positive Lung Cancer. N Engl J Med 376 (7): 629-640, 2017.[PUBMED Abstract]
- Kwak EL, Bang YJ, Camidge DR, et al.: Anaplastic lymphoma kinase inhibition in non-small-cell lung cancer. N Engl J Med 363 (18): 1693-703, 2010.[PUBMED Abstract]
- Shaw AT, Yeap BY, Solomon BJ, et al.: Effect of crizotinib on overall survival in patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement: a retrospective analysis. Lancet Oncol 12 (11): 1004-12, 2011.[PUBMED Abstract]
- Shaw AT, Kim DW, Nakagawa K, et al.: Crizotinib versus chemotherapy in advanced ALK-positive lung cancer. N Engl J Med 368 (25): 2385-94, 2013.[PUBMED Abstract]
- Shaw AT, Kim DW, Mehra R, et al.: Ceritinib in ALK-rearranged non-small-cell lung cancer. N Engl J Med 370 (13): 1189-97, 2014.[PUBMED Abstract]
- Shaw AT, Gandhi L, Gadgeel S, et al.: Alectinib in ALK-positive, crizotinib-resistant, non-small-cell lung cancer: a single-group, multicentre, phase 2 trial. Lancet Oncol 17 (2): 234-42, 2016.[PUBMED Abstract]
- Ou SH, Ahn JS, De Petris L, et al.: Alectinib in Crizotinib-Refractory ALK-Rearranged Non-Small-Cell Lung Cancer: A Phase II Global Study. J Clin Oncol 34 (7): 661-8, 2016.[PUBMED Abstract]
- Kim DW, Tiseo M, Ahn MJ, et al.: Brigatinib in Patients With Crizotinib-Refractory Anaplastic Lymphoma Kinase-Positive Non-Small-Cell Lung Cancer: A Randomized, Multicenter Phase II Trial. J Clin Oncol 35 (22): 2490-2498, 2017.[PUBMED Abstract]
- Planchard D, Besse B, Groen HJM, et al.: Dabrafenib plus trametinib in patients with previously treated BRAF(V600E)-mutant metastatic non-small cell lung cancer: an open-label, multicentre phase 2 trial. Lancet Oncol 17 (7): 984-993, 2016.[PUBMED Abstract]
- Gainor JF, Shaw AT: Novel targets in non-small cell lung cancer: ROS1 and RET fusions. Oncologist 18 (7): 865-75, 2013.[PUBMED Abstract]
- Drilon A, Siena S, Dziadziuszko R, et al.: Entrectinib in ROS1 fusion-positive non-small-cell lung cancer: integrated analysis of three phase 1-2 trials. Lancet Oncol 21 (2): 261-270, 2020.[PUBMED Abstract]
- Shaw AT, Ou SH, Bang YJ, et al.: Crizotinib in ROS1-rearranged non-small-cell lung cancer. N Engl J Med 371 (21): 1963-71, 2014.[PUBMED Abstract]
- Wu YL, Yang JC, Kim DW, et al.: Phase II Study of Crizotinib in East Asian Patients With ROS1-Positive Advanced Non-Small-Cell Lung Cancer. J Clin Oncol 36 (14): 1405-1411, 2018.[PUBMED Abstract]
- Farago AF, Le LP, Zheng Z, et al.: Durable Clinical Response to Entrectinib in NTRK1-Rearranged Non-Small Cell Lung Cancer. J Thorac Oncol 10 (12): 1670-4, 2015.[PUBMED Abstract]
- Gatalica Z, Xiu J, Swensen J, et al.: Molecular characterization of cancers with NTRK gene fusions. Mod Pathol 32 (1): 147-153, 2019.[PUBMED Abstract]
- Drilon A, Laetsch TW, Kummar S, et al.: Efficacy of Larotrectinib in TRK Fusion-Positive Cancers in Adults and Children. N Engl J Med 378 (8): 731-739, 2018.[PUBMED Abstract]
- Doebele RC, Drilon A, Paz-Ares L, et al.: Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol 21 (2): 271-282, 2020.[PUBMED Abstract]
- Brahmer J, Reckamp KL, Baas P, et al.: Nivolumab versus Docetaxel in Advanced Squamous-Cell Non-Small-Cell Lung Cancer. N Engl J Med 373 (2): 123-35, 2015.[PUBMED Abstract]
- Borghaei H, Paz-Ares L, Horn L, et al.: Nivolumab versus Docetaxel in Advanced Nonsquamous Non-Small-Cell Lung Cancer. N Engl J Med 373 (17): 1627-39, 2015.[PUBMED Abstract]
- Garon EB, Rizvi NA, Hui R, et al.: Pembrolizumab for the treatment of non-small-cell lung cancer. N Engl J Med 372 (21): 2018-28, 2015.[PUBMED Abstract]
- Horn L, Spigel DR, Vokes EE, et al.: Nivolumab Versus Docetaxel in Previously Treated Patients With Advanced Non-Small-Cell Lung Cancer: Two-Year Outcomes From Two Randomized, Open-Label, Phase III Trials (CheckMate 017 and CheckMate 057). J Clin Oncol 35 (35): 3924-3933, 2017.[PUBMED Abstract]
- Herbst RS, Baas P, Kim DW, et al.: Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial. Lancet 387 (10027): 1540-50, 2016.[PUBMED Abstract]
- Rittmeyer A, Barlesi F, Waterkamp D, et al.: Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK): a phase 3, open-label, multicentre randomised controlled trial. Lancet 389 (10066): 255-265, 2017.[PUBMED Abstract]
- Fehrenbacher L, Spira A, Ballinger M, et al.: Atezolizumab versus docetaxel for patients with previously treated non-small-cell lung cancer (POPLAR): a multicentre, open-label, phase 2 randomised controlled trial. Lancet 387 (10030): 1837-46, 2016.[PUBMED Abstract]
-
化学療法。
- 本要約の変更点(05/07/2020)
-
PDQがん情報要約は定期的に見直され、新情報が利用可能になり次第更新される。本セクションでは、上記の日付における本要約最新変更点を記述する。
新たに診断されたIV期、再燃および再発したNSCLCの治療
本文で、以下の第III相二重盲検KEYNOTE-189試験に関する記述が更新された;追跡期間中央値23.1ヵ月後、ペムブロリズマブ併用群における全生存期間中央値は22.0ヵ月であったのに対し、プラセボ併用群では10.7ヵ月であった;無増悪生存期間中央値は、ペムブロリズマブ併用群が9.0ヵ月、プラセボ併用群が4.9ヵ月であった;すべてのプログラム細胞死リガンド1カテゴリーにわたり、また肝転移/脳転移が存在する状況で、生存期間の改善がみられた;全般的健康状態/生活の質スコアは、ペムブロリズマブ併用群で良好に維持された(引用、参考文献78としてGadgeel et al.および証拠レベル:1iA、ならびに参考文献79としてGarassino et al.)。
本要約はPDQ Adult Treatment Editorial Boardが作成と内容の更新を行っており、編集に関してはNCIから独立している。本要約は独自の文献レビューを反映しており、NCIまたはNIHの方針声明を示すものではない。PDQ要約の更新におけるPDQ編集委員会の役割および要約の方針に関する詳しい情報については、本PDQ要約についておよびPDQ® - NCI's Comprehensive Cancer Databaseを参照のこと。
- 本PDQ要約について
-
本要約の目的
医療専門家向けの本PDQがん情報要約では、非小細胞肺がんの治療について、包括的な、専門家の査読を経た、そして証拠に基づいた情報を提供する。本要約は、がん患者を治療する臨床家に情報を与え支援するための情報資源として作成されている。これは医療における意思決定のための公式なガイドラインまたは推奨事項を提供しているわけではない。
査読者および更新情報
本要約は編集作業において米国国立がん研究所(NCI)とは独立したPDQ Adult Treatment Editorial Boardにより定期的に見直され、随時更新される。本要約は独自の文献レビューを反映しており、NCIまたは米国国立衛生研究所(NIH)の方針声明を示すものではない。
委員会のメンバーは毎月、最近発表された記事を見直し、記事に対して以下を行うべきか決定する:
- 会議での議論、
- 本文の引用、または
- 既に引用されている既存の記事との入れ替え、または既存の記事の更新。
要約の変更は、発表された記事の証拠の強さを委員会のメンバーが評価し、記事を本要約にどのように組み入れるべきかを決定するコンセンサス過程を経て行われる。
- Janet Dancey, MD, FRCPC (Ontario Institute for Cancer Research & NCIC Clinical Trials Group)
- Raymond Mak, MD (Harvard Medical School)
- Arun Rajan, MD (National Cancer Institute)
- Eva Szabo, MD (National Cancer Institute)
本要約の内容に関するコメントまたは質問は、NCIウェブサイトのEmail UsからCancer.gov まで送信のこと。要約に関する質問またはコメントについて委員会のメンバー個人に連絡することを禁じる。委員会のメンバーは個別の問い合わせには対応しない。
証拠レベル
本要約で引用される文献の中には証拠レベルの指定が記載されているものがある。これらの指定は、特定の介入やアプローチの使用を支持する証拠の強さを読者が査定する際、助けとなるよう意図されている。PDQ Adult Treatment Editorial Boardは、証拠レベルの指定を展開する際に公式順位分類を使用している。
本要約の使用許可
PDQは登録商標である。PDQ文書の内容は本文として自由に使用できるが、完全な形で記し定期的に更新しなければ、NCI PDQがん情報要約とすることはできない。しかし、著者は“NCI's PDQ cancer information summary about breast cancer prevention states the risks succinctly: 【本要約からの抜粋を含める】.”のような一文を記述してもよい。
本PDQ要約の好ましい引用は以下の通りである:
PDQ® Adult Treatment Editorial Board.PDQ Non-Small Cell Lung Cancer Treatment.Bethesda, MD: National Cancer Institute.Updated <MM/DD/YYYY>.Available at: https://www.cancer.gov/types/lung/hp/non-small-cell-lung-treatment-pdq.Accessed <MM/DD/YYYY>.[PMID: 26389304]
本要約内の画像は、PDQ要約内での使用に限って著者、イラストレーター、および/または出版社の許可を得て使用されている。PDQ情報以外での画像の使用許可は、所有者から得る必要があり、米国国立がん研究所(National Cancer Institute)が付与できるものではない。本要約内のイラストの使用に関する情報は、多くの他のがん関連画像とともにVisuals Online(2,000以上の科学画像を収蔵)で入手できる。
免責条項
入手可能な証拠の強さに基づき、治療選択肢は「標準」または「臨床評価段階にある」のいずれかで記載される場合がある。これらの分類は、保険払い戻しの決定基準として使用されるべきものではない。保険の適用範囲に関する詳しい情報については、Cancer.govのManaging Cancer Careページで入手できる。
お問い合わせ
Cancer.govウェブサイトについての問い合わせまたはヘルプの利用に関する詳しい情報は、Contact Us for Helpページに掲載されている。質問はウェブサイトのEmail UsからもCancer.govに送信可能である。

 画像を拡大する
画像を拡大する