ご利用について
医療専門家向けの本PDQがん情報要約では、乳がんおよび婦人科がんの遺伝学について、包括的な、専門家の査読を経た、そして証拠に基づいた情報を提供する。本要約は、がん患者を治療する臨床家に情報を与え支援するための情報資源として作成されている。これは医療における意思決定のための公式なガイドラインまたは推奨事項を提供しているわけではない。
本要約は編集作業において米国国立がん研究所(NCI)とは独立したPDQ Cancer Genetics Editorial Boardにより定期的に見直され、随時更新される。本要約は独自の文献レビューを反映しており、NCIまたは米国国立衛生研究所(NIH)の方針声明を示すものではない。
CONTENTS
- 要旨
-
この要旨では、本PDQ要約で扱う乳がんおよび婦人科がんの遺伝学の話題について概要を示すとともに、各話題に関するエビデンスを記述した以下の詳細セクションへのハイパーリンクを提供する。
- 序
-
一般情報
[注: 本要約で用いられている多くの医学および科学用語についての解説がNCI Dictionary of Genetics Termsに用意されている。リンクが張られた用語をクリックすれば、別のウインドウにその定義が表示される。]
[注: 現在、遺伝学的多様性を記載するための用語体系を変化させるべく、遺伝学のコミュニティにおいて協調的な取り組みが進められている。その変化とは、研究対象の個人または集団と参照配列との間に存在する遺伝学的な差異、特に生殖細胞系に存在する差異を記述する際に、従来の「mutation(突然変異ないし変異)」ではなく、「variant(多様体ないしバリアント)」という用語を使用するというものである。多様体はさらに、良性(無害)(benign [harmless])、おそらく良性(likely benign)、意義不明(of uncertain significance)、おそらく病原性(likely pathogenic)、病原性(疾患を引き起こす)(pathogenic [disease causing])のいずれかに分類することができる。本要約では、全体を通じて、疾患を引き起こす突然変異に対して病原性多様体(pathogenic variant)という用語を使用する。多様体の分類に関する詳しい情報については、がん遺伝学の概要の要約を参照のこと。]
[注: 本要約に記載されている多くの遺伝子および病態については、Online Mendelian Inheritance in Man(OMIM)カタログに掲載されている。(詳しい情報については、OMIMを参照のこと。)]
乳がんは、非メラノーマ性皮膚がんに続いて米国における女性に最も一般的に診断されるがんであり、肺がんに続いてがんによる死亡原因の2番目となっている。2020年には、279,100人(2,620人の男性症例を含む)が新たに乳がんと診断され、乳がんによる死亡は42,690人(男性の520人を含む)になると推定される。[ 1 ]乳がんの発生率は、特に50歳を過ぎて発生するエストロゲン受容体(ER)陽性のがんで低下しており、2003年以降はさらに急速な割合で低下している;これは、時期的にみてWomen's Health Initiative(WHI)による初期の報告後にホルモン補充療法(HRT)が減少したことに関係している可能性がある。[ 2 ]2020年には、米国において推定21,750人の新たな卵巣がん症例が予想され、推定13,940人が死亡する。卵巣がんは、女性において5番目に致死的ながんである。[ 1 ]2020年には、米国において推定65,620人の新たな子宮内膜がん症例が予想され、推定12,590人が死亡する。[ 1 ](乳がん、卵巣がん、および子宮内膜がんの割合、診断、および管理に関する詳しい情報については、乳がんの治療[成人];上皮性卵巣がん、卵管がん、原発性腹膜がんの治療;および子宮内膜がん(子宮体がん)の治療に関するPDQ要約を参照のこと。)
乳がんおよび卵巣がんリスクに対して考えられる遺伝的寄与は、家族歴(詳しい情報については、以下の乳がんの危険因子、卵巣がんの危険因子、および子宮内膜がんの危険因子のセクションを参照のこと)を有する女性の間でこれらのがんの発生増大があること、およびがん感受性について常染色体優性パターンで遺伝する乳がんおよび/または卵巣がんに多数の家系員が罹患している一部の家系を観察することによって示される。引き続いて家系の正式な研究(連鎖解析)が乳がんおよび卵巣がんに対する常染色体優性素因の存在を明らかにし、多くの家系における遺伝性発がんリスクの原因として複数の浸透度の高い遺伝子を同定するに至った。(連鎖解析に関する詳しい情報については、がん遺伝学の概要に関するPDQ要約を参照のこと。)これらの遺伝子における病原性多様体は一般集団においてはまれであり、全乳がんおよび卵巣がん例の5~10%に過ぎないと推定される。他の遺伝因子がこれらのがんの病因に寄与している可能性が高い。
乳がんの危険因子
一般集団における乳がんの危険因子に関する情報については、乳がんの予防に関するPDQ要約を参照のこと。
年齢
乳がんの累積リスクは年齢とともに増大し、大半の乳がんは、50歳以降に発症する。[ 3 ]遺伝的感受性を有する女性では、散発例よりも乳がん(および程度は低いが卵巣がん)を若い年齢で発症する傾向にある。
遺伝性がん遺伝子を含む家族歴
成人を調査対象とする横断研究では、調査対象となった女性の5~10%は母親または姉妹が乳がんに罹患しており、約2倍の数の女性が、第一度近親者(FDR)か第二度近親者のどちらかに乳がんの罹患者がいた。[ 4 ][ 5 ][ 6 ][ 7 ]乳がん家族歴によってもたらされるリスクは、ボランティアおよび集団ベースのサンプルを用いて、ケースコントロール研究およびコホート研究で評価され、おおむね一致した結果が得られている。[ 8 ]38件の研究のプール解析では、乳がんに罹患しているFDRによってもたらされる乳がんの相対リスク(RR)は、2.1であった(95%信頼区間[CI]、2.0-2.2)。[ 8 ]リスクは罹患している近親者の数、診断時年齢、家系員における両側性乳がんまたは同側における複数の乳がんの発生、および罹患している男性近親者の数に伴い増加する。[ 5 ][ 6 ][ 8 ][ 9 ][ 10 ]スウェーデンのFamily Cancer Databaseからの大規模集団ベース研究により、乳がんの母親または姉妹がいる女性では乳がんのリスクが有意に高いという知見が確認された。家系において1人の乳がんを有する女性のハザード比(HR)は1.8(95%CI、1.8-1.9)、複数の乳がんの家族歴を有する女性では2.7(95%CI、2.6-2.9)であった。家系に複数の乳がんを有し、1人が40歳前に発症している女性のHRは3.8(95%CI、3.1-4.8)であった。しかしながら、この研究ではまた、近親者が60歳以上であった場合に乳がんリスクが有意に増加することが明らかにされ、家系における乳がんは年齢に関係なくリスクをある程度増加させることが示唆されている。[ 10 ]片側 vs 対側乳がん(CBC)女性における別の研究で、家系員における乳がんリスクが評価された。[ 11 ]結果から、罹患したFDRがいる女性の対側乳がんリスクは10年経過時に8.1%であったことが示された。このリスクは40歳前に診断されるか、対側乳がんが認められた近親者で比較的高く、BRCAキャリアにおける低いリスク推定値に近かった。(この集団におけるがんリスク推定値に関する情報については、本要約の高浸透度の乳がんおよび/または婦人科がん感受性遺伝子のセクションにあるBRCA病原性多様体キャリアにおける対側乳がんのセクションを参照のこと。)これらのリスク推定値は、BRCA1/BRCA2、ATM、CHEK2、およびPALB2における有害な多様体に対する検査が陰性であった女性に解析を限定した場合に、変化が認められないままであった。
双生児を対象にかつて実施された中で最大規模の研究の1つでは、一卵性双生児80,309組、二卵性双生児123,382組において、乳がんの遺伝可能性の推定値が31%(95%CI、11%-51%)と報告された。[ 12 ]女児の双生児で、一卵性双生児が乳がんになった場合に一方の双生児が乳がんになる確率は28.1%(95%CI、23.9%-32.8%)で、二卵性双生児が乳がんになった場合に一方の双生児が乳がんになる確率は19.9%(95%CI、17%-23.2%)であった。これらの推定値から、一卵性双生児では乳がんリスクが二卵性双生児より10%高いことが示唆される。しかしながら、一卵性双生児間でも不一致の割合が高いことから、乳がんリスクの差に環境因子も関与していることが示唆される。
(BRCA1/BRCA2病原性多様体を有する家系出身であるが、自身は家族性病原性多様体の検査が陰性である女性における家系的リスクの考察については、本要約のBRCA病原性多様体の浸透度のセクションを参照のこと。)
出産歴
一般的に、乳がんのリスクは、初潮が早い人および閉経が遅い人ほど高く、低年齢で第1子を満期出産すると低下する。比較的若年(30歳前)で妊娠するBRCA1およびBRCA2病原性多様体キャリアでは乳がんリスクが高い可能性があり、BRCA1病原性多様体キャリアにはより有意な影響がみられる。[ 13 ][ 14 ][ 15 ]同様に、授乳はBRCA1(ただし、BRCA2ではない)病原性多様体キャリアにおける乳がんリスクを低下させうる。[ 16 ]妊娠が乳がんの転帰に及ぼす影響については、妊娠中の乳がんの診断も乳がん後の妊娠もBRCA1またはBRCA2病原性多様体を保有する女性における不良な生存転帰とは関連していないようである。[ 17 ]出産歴はBRCA1およびBRCA2病原性多様体キャリアにとって予防的であるようであり、さらに40歳以前の生児出生には追加の予防効果があると考えられる。[ 18 ]
出産歴は卵巣がんおよび子宮内膜がんのリスクにも影響しうる。(詳しい情報については、本要約の卵巣がんの危険因子および子宮内膜がんの危険因子のセクションにある出産歴のセクションを参照のこと。)
経口避妊薬
経口避妊薬(OC)は、長期服用者に乳がんリスクのわずかな増大をもたらすが、これは短期的な作用のようである。54件の研究から得られたデータのメタアナリシスによれば、経口避妊薬服用に関連する乳がんリスクは、乳がんの家族歴に関係して変化することはなかった。[ 19 ]
BRCA1およびBRCA2の病原性多様体キャリアを対象にした卵巣がん予防に、経口避妊薬が推奨されることがある。(詳しい情報については、本要約の卵巣がんの危険因子のセクションにある経口避妊薬のセクションを参照のこと。)データが完全に一貫しているわけではないが、メタアナリシスの結論では、BRCA1/BRCA2病原性多様体キャリアにおいて経口避妊薬を使用しても、乳がんリスクに有意な増加は認められなかった。[ 20 ]しかしながら、1975年より前に製剤化された経口避妊薬の使用は、乳がんのリスク増加と関係していた(要約相対リスク[SRR]、1.47;95%CI、1.06-2.04)。[ 20 ](詳しい情報については、本要約のBRCA病原性多様体キャリアの臨床管理のセクションにある生殖因子のセクションを参照のこと。)
ホルモン補充療法
閉経後HRTと乳がんとの関連性に関して、観察研究とランダム化臨床試験の両方からデータが得られている。51件の観察研究から得られたデータのメタアナリシスにより、閉経後に5年以上HRTを受けた女性における乳がんのRRが1.35(95%CI、1.21-1.49)と示された。[ 21 ]WHIによる閉経後の女性約160,000人を対象にしたランダム化比較試験(NCT00000611)では、HRTのリスクと有益性が調査された。16,000人以上の女性を併用HRTかプラセボ投与のいずれかにランダムに割り付けたこの研究で、エストロゲン + プロゲスチン群は、健康上のリスクが有益性を上回ったために早期に打ち切られた。[ 22 ][ 23 ]中止を促した有害な転帰は、全乳がん(245 vs 185症例)および浸潤性乳がん(199 vs 150症例)のいずれにも有意な増加(RR、1.24;95%CI、1.02-1.5、P < 0.001)が認められたこと、冠動脈心疾患、脳卒中、および肺塞栓症のリスクが増加したことなどであった。英国のプロスペクティブ観察研究、Million Women's Studyのエストロゲン-プロゲスチン群で同様の所見がみられた。[ 24 ]しかしながら、WHI研究ではエストロゲン単独 vs プラセボにランダムに割り付けられた女性における乳がんリスクの増加は認められなかった(RR、0.77;95%CI、0.59-1.01)。この研究のエストロゲン単独群の適格性には子宮摘出術が求められ、これらの患者の40%はまた卵巣摘出術も受けていたが、このことが乳がんリスクに影響を及ぼした可能性がある。[ 25 ]
乳がんの家族歴をもつ女性におけるHRTと乳がんリスクとの関連には一貫性がなく;家族歴がある女性で特にリスクの増加を報告する研究がある一方で、これらの要因間に相互作用の証拠が見出せないとする研究もある。[ 26 ][ 27 ][ 28 ][ 29 ][ 30 ][ 21 ] 大規模なメタアナリシスにおいてHRTの使用と関連していた乳がんリスクの増加は、家族歴がある被験者とない被験者の間では有意に異ならなかった。[ 30 ] WHI研究では、乳がんの家族歴に関して層別化した解析が報告されておらず、被験者はBRCA1/BRCA2病原性多様体について系統的に検査されていなかった。[ 23 ]更年期症状の治療を目的とした短期間のホルモン剤服用は、乳がんリスクに対してほとんどまたは全く影響を及ぼさないようである。[ 21 ][ 31 ]BRCA1またはBRCA2の病原性多様体キャリアにおけるHRTの乳がんリスクへの影響は、リスク低減のための両側卵巣摘出術の状況でのみ研究されており、短期間の補充療法は、乳がんリスクに対する卵巣摘出術の予防効果を減じないようである。[ 32 ](詳しい情報については、本要約のBRCA1/BRCA2病原性多様体キャリアにおけるホルモン補充療法のセクションを参照のこと。)
ホルモン使用は子宮内膜がんの発症リスクにも影響しうる。(詳しい情報については、本要約の子宮内膜がんの危険因子のセクションにあるホルモンのセクションを参照のこと。)
放射線曝露
広島および長崎の原爆生存者と胸部および上半身への放射線照射治療を受けた女性の観察から、放射線曝露を受けるとその結果として乳がんリスクが増大することが実証された。乳がんの遺伝的感受性を有する女性におけるこの危険因子の意義は明らかにされていない。
予備的データからは、放射線に対する感受性の増大は、BRCA1またはBRCA2病原性多様体のキャリアにおいて[ 33 ][ 34 ][ 35 ][ 36 ]、またATMおよびTP53生殖細胞多様体との関連においてがん感受性の原因となりうるということが示唆されている。[ 37 ][ 38 ]
乳がんの遺伝的感受性が、放射線感受性の機序を介して起こるという可能性は、放射線曝露について問題を提起する。マンモグラフィを含め診断的放射線曝露は、平均リスクの女性よりも遺伝的感受性のある女性のリスクを増大させる可能性がある。治療的放射線照射によっても発がんリスクが増大する可能性がある。しかしながら、乳房温存療法による治療を受けたBRCA1およびBRCA2病原性多様体キャリアを対象にしたコホート研究では、キャリアの乳房、肺または骨髄における放射線感受性の増大または後遺症の証拠は示されていない。[ 39 ]この知見は、BRCA1/BRCA2関連乳がんの患者691人を中央値で8.6年間にわたり追跡したレトロスペクティブ・コホート研究で確認された。最初の乳がん診断時に40歳未満であった患者サブセットを含め、いずれのコホートでも補助放射線療法の実施と対側乳がんのリスク増加との関係は観察されなかった。[ 40 ]逆に、放射線感受性は、乳がんに対する遺伝的感受性を有する女性の腫瘍を、放射線による治療に対してより敏感にさせうる。BRCA1およびBRCA2の病原性多様体キャリアを対象に、マンモグラフィを含むが、これだけに限らず放射線曝露の影響を調査した研究では、一貫した結果は得られていない。[ 41 ][ 42 ][ 43 ][ 44 ][ 45 ][ 46 ]大規模な欧州の研究では、放射線総曝露量とともにリスクが上昇する線量対反応関係が示されたが、これは主に20歳前のマンモグラフィ以外の放射線曝露によって算出されたものである。[ 45 ]その後、研究参加時点で乳がんの診断を受けていないBRCA1キャリア1,844人とBRCA2キャリア502人を対象としたプロスペクティブ研究によると、平均追跡期間が5.3年で、マンモグラフィの受診歴と乳がんリスクとの間に有意な関連性は観察されなかった。[ 46 ](放射線に関する詳しい情報については、本要約のBRCA病原性多様体キャリアの臨床管理のセクションにあるマンモグラフィのセクションを参照のこと。)
アルコール摂取
一般集団では、毎日のアルコール摂取量が10g(アルコール飲料約1杯以内)増えるごとに、乳がんのリスクが約10%高まる。[ 47 ][ 48 ]BRCA1/BRCA2病原性多様体キャリアを対象にした先行研究では、アルコール摂取量と関連したリスク増加はみられなかった。[ 49 ][ 50 ][ 51 ]
身体的活動と人体計測的特徴
ほとんどの疫学的研究で、身体活動の増加と乳がんリスクの低下との関連が認められている。BRCA1またはBRCA2病原性多様体を有する女性の研究でも、リスク低下が確認されている。例えば、ある研究で、中程度の身体活動により、閉経前乳がんリスクの38%低下が報告された(身体活動の下位4分の1と比較した上位4分の1でのオッズ比[OR]、0.62;95%CI、0.40-0.96)。[ 52 ]乳がんリスク低下は、広範な乳がんの絶対リスクでも確認されており、これには、乳がん家族歴を基に乳がんリスクが高いものの、既知のBRCA1またはBRCA2病原性多様体が認められない女性におけるリスク低下が含まれる。[ 53 ]
卵巣がんの危険因子
一般集団における卵巣がんの危険因子に関する情報については、卵巣がん、卵管がん、原発性腹膜がんの予防に関するPDQ要約を参照のこと。
年齢
卵巣がん発生率は、年齢30歳から50歳まで直線的に上昇し、その後もペースは落とすものの上昇を続ける。30歳未満では、遺伝性がんの家系でも上皮性卵巣がんの発症リスクはごくわずかである。[ 63 ]
遺伝性がん遺伝子を含む家族歴
生殖因子、人口統計学的因子および生活様式因子は、卵巣がんのリスクを増大させるが、最も大きな卵巣がんの危険因子は、疾患の家族歴である。公表された15件の研究の大規模なメタアナリシスによれば、卵巣がんのFDRを少なくとも1人もつ場合の卵巣がんリスクに対するオッズ比は3.1と推定された。[ 64 ]
出産歴
出産経験がないことは、BRCA1/BRCA2病原性多様体キャリアを含めて、卵巣がんリスクの増加と一貫して関連しているが、1件のメタアナリシスでリスクの低下が確認されたのは4人以上の生児出生が得られた女性のみであった。[ 15 ]リスクは、排卵誘発剤を使用している女性でも高く、特に妊娠経験のない女性で顕著であった。[ 65 ][ 66 ]数件の研究で、BRCA1/BRCA2病原性多様体キャリアにおける経口避妊薬の使用後、卵巣がんのリスク低下が報告されている[ 67 ][ 68 ][ 69 ];リスク低下はまた、BRCA1キャリアにおける卵管結紮術後にも示されており、この手技の実施後、22~80%という統計的に有意なリスク低下が得られている。[ 69 ][ 70 ]12ヵ月超の授乳もまた、BRCA1/BRCA2病原性多様体キャリアにおいて、卵巣がんの低下と関連している可能性がある。[ 71 ]これに対して、閉経期のホルモン補充療法(HRT)の使用が、卵巣がんのリスクの増大と関連しているという証拠はますます高まり、特に長期使用者やエストロゲン-プロゲステロンの連続投与を受けている者で顕著である。[ 72 ][ 73 ][ 74 ][ 75 ]
手術歴
両側卵管結紮術および子宮全摘出術は、BRCA1/BRCA2病原性多様体キャリアを含めて、卵巣がんリスクの低下[ 65 ][ 76 ][ 77 ]と関連している。[ 78 ]BRCA1またはBRCA2の病原性多様体を有することが証明され、リスク低減のための卵管-卵巣摘出術(RRSO)を選択した女性では、卵巣がんのリスク低下が90%を超えている。この同じ集団において、リスク低減のための卵巣摘出術は続発性乳がんのリスクもほぼ50%低下させるという結果をもたらした。[ 79 ][ 80 ]BRCA2病原性多様体を有する患者では、BRCA1病原性多様体を有する患者よりも乳がん減量の恩恵が大きいことを示している研究がいくつかある一方で、BRCA1キャリアでは恩恵が得られないことを示している研究もある。さらに、これらの研究の多くは、有益性を実証する検出力が依然として不足している。[ 81 ](これらの研究に関する詳しい情報については、本要約のRRSOのセクションを参照のこと。)
経口避妊薬
4年間以上の経口避妊薬の使用は、一般集団における卵巣がんリスクの約50%の低下と関連している。[ 65 ][ 82 ]すべてではないものの、大部分の研究もまた、BRCA1/BRCA2病原性多様体キャリアにおける経口避妊薬の保護的な役割を支持している。[ 70 ][ 83 ][ 84 ][ 85 ][ 86 ]BRCA病原性多様体キャリア13,627人を含む18件の研究を対象としたメタアナリシスでは、経口避妊薬使用に関連して、卵巣がんリスクの有意な低下(SRR、0.50;95%CI、0.33-0.75)が報告された。[ 20 ](詳しい情報については、本要約の化学予防のセクションにある経口避妊薬のセクションを参照のこと。)
子宮内膜がんの危険因子
一般集団における子宮内膜がんの危険因子に関する情報については、子宮内膜がんの予防に関するPDQ要約を参照のこと。
年齢
年齢は子宮内膜がんの重要な危険因子である。子宮内膜がん女性のほとんどが閉経後に診断される。50歳前に子宮内膜がんを診断される女性はわずか15%であり、40歳前に診断されるのは5%未満である。[ 87 ]リンチ症候群の女性は比較的早い年齢で子宮内膜がんを発症する傾向があり、診断時年齢中央値は48歳である。[ 88 ]
遺伝性がん遺伝子を含む家族歴
高エストロゲン状態は子宮内膜がんの最も一般的な素因であるが、家族歴もまた、女性の疾患リスクにおいて重要な役割を果たしている。子宮がん症例の約3~5%は遺伝的原因によるものであり[ 89 ]、主要な遺伝性子宮内膜がん症候群は、集団の有病率が300人に1人から1,000人に1人の常染色体優性遺伝疾患であるリンチ症候群である。[ 90 ][ 91 ](詳しい情報については、大腸がんの遺伝学に関するPDQ要約のリンチ症候群のセクションを参照のこと。)
非リンチ症候群遺伝子も子宮内膜がんリスクの一因となっている可能性がある。多重遺伝子パネル検査を受けた非選択の子宮内膜がんコホートで、CHEK2、APC、ATM、BARD1、BRCA1、BRCA2、BRIP1、NBN、PTEN、およびRAD51Cを含む非リンチ症候群遺伝子における生殖細胞病原性多様体について、検査結果が陽性であった患者は約3%であった。[ 92 ]注目すべきことに、非リンチ症候群遺伝子に病原性多様体を認める患者は、腫瘍が漿液性組織型である可能性が病原性多様体を認めない患者よりも高かった。さらに、RRSO後の子宮内膜がん全体のリスクは、BRCA1病原性多様体のキャリアで増加しなかったが、これらの患者は漿液性および漿液性類似の子宮内膜がんのリスクが高いとみなされた。[ 93 ]
ホルモン
I型子宮内膜がんのリスクを増加させるホルモン因子の解明が進んでいる。すべての子宮内膜がんに共通して、プロゲステロンよりもエストロゲンが優勢にみられる。エストロゲンへの長期曝露または拮抗されないエストロゲン療法は子宮内膜がんのリスクを増加させる。エストロゲンへの内因性曝露は肥満、多嚢胞性卵巣症候群、および未経産の結果として起こる一方、外因性エストロゲンは拮抗されないエストロゲンまたはタモキシフェン投与の結果として起こる。拮抗されないエストロゲン療法はその使用期間に比例して、子宮内膜がんの発症リスクを2~20倍増加させる。[ 96 ][ 97 ]選択的エストロゲン受容体モジュレータのタモキシフェンは乳房組織においてはエストロゲンアンタゴニストとして作用する一方、子宮内膜に対してはエストロゲンアゴニストとして作用することで、子宮内膜がんリスクを増加させる。[ 98 ]これとは対照的に、経口避妊薬、レボノルゲストレル放出子宮内避妊システム、およびエストロゲン-プロゲステロンの併用ホルモン補充療法はいずれも、子宮内膜に対するプロゲステロンの抗増殖性効果により、子宮内膜がんリスクを低下させる。[ 99 ][ 100 ][ 101 ][ 102 ]
乳がんおよび婦人科がんの素因の常染色体優性遺伝
乳がんおよび婦人科がんの常染色体優性遺伝は、家族の母系または父系を通じて世代から世代へとがん素因を伝達することで特徴づけられ、以下の特性を有する:
乳がんおよび卵巣がんは、いくつかの常染色体優性遺伝がん症候群の構成要素である。両方のがんと最も強く関連する常染色体優性遺伝がん症候群はBRCA1またはBRCA2病原性多様体を伴う症候群である。乳がんはまた、TP53病原性多様体によるリー-フラウメニ症候群およびPTEN病原性多様体によるコーデン症候群の一般的な特徴である。[ 103 ]随伴する特徴として乳がんを含むことがある他の遺伝症候群には、毛細血管拡張性失調症遺伝子のヘテロ接合体キャリアおよびポイツ・ジェガース症候群がある。卵巣がんでは、リンチ症候群、基底細胞母斑(ゴーリン)症候群、および多発性内分泌腫瘍1型との関連も認められている。[ 103 ]リンチ症候群は主に大腸がんおよび子宮内膜がんに関連しているが、数件の研究により、リンチ症候群の患者はまた尿管および腎盂の移行上皮がん;胃、小腸、肝臓と胆管、脳、乳房、前立腺、および副腎皮質のがん;さらに皮膚皮脂腺腫瘍(ムア-トレ症候群)を発症するリスクも存在することが実証されている。[ 104 ][ 105 ][ 106 ][ 107 ][ 108 ][ 109 ][ 110 ]
これらの常染色体優性遺伝がん症候群の原因となっている遺伝子における生殖細胞系病原性多様体により、特徴的な悪性腫瘍の臨床的に異なった表現型を生じ、場合によっては、関連した非悪性異常が生じることもある。
遺伝性のがん素因が疑われる家族特性には以下のものがある:
図1および図2は、それぞれBRCA1およびBRCA2の病原性多様体の古典的な遺伝的特徴の一部を示している。図3は古典的なリンチ症候群家系を示している。(これらの家系図で用いられる標準的なシンボルの定義については、がんの遺伝学的リスク評価とカウンセリングに関するPDQ要約の標準的な家系図命名法の図を参照のこと。)
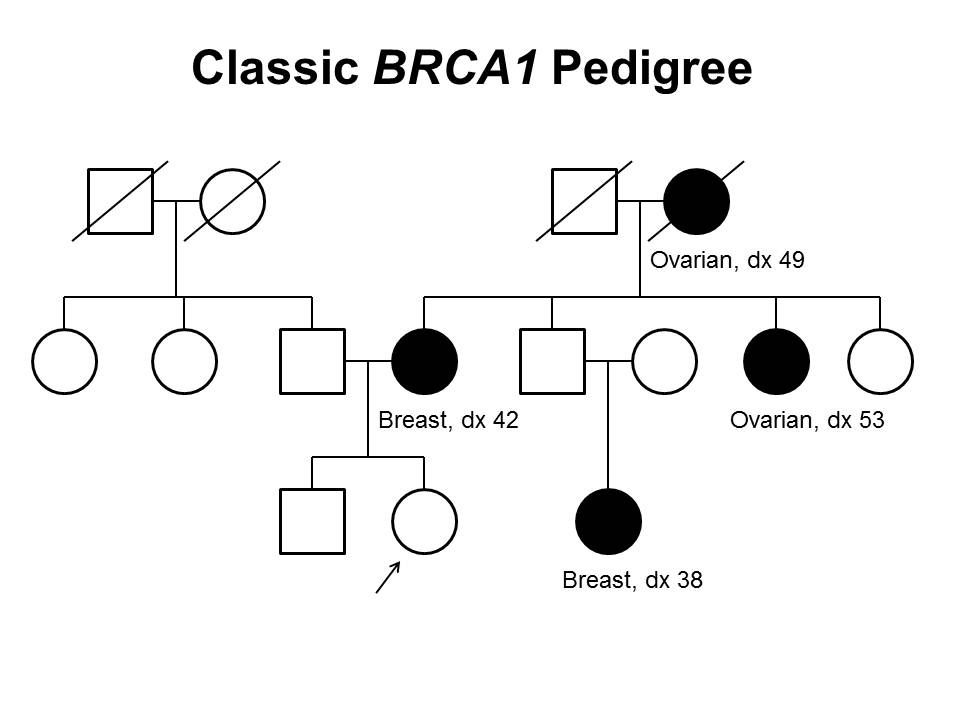
図1.BRCA1家系図。この家系図は、乳がんまたは卵巣がんを若い年齢で発症した罹患家系員など、3世代にわたってBRCA1の病原性多様体を有する家系の古典的な特徴の一部を示す。BRCA1家系は、これらの特徴の一部またはすべてを示す可能性がある。図に示しているように母系または父系を通して、常染色体優性症候群としてBRCA1病原性多様体が伝播する可能性がある。 
図2.BRCA2家系図。この家系図は、乳がん(男性乳がんも含む)、卵巣がん、膵がん、または前立腺がんを比較的若い年齢で発症した罹患家系員など、3世代にわたってBRCA2の病原性多様体を有する家系の古典的な特徴の一部を示す。BRCA2家系は、これらの特徴の一部またはすべてを示す可能性がある。図に示しているように母系または父系を通して、常染色体優性症候群としてBRCA2病原性多様体が伝播する可能性がある。 
図3.リンチ症候群家系図。この家系図は、結腸がんまたは子宮内膜がんを(一部の個人では若い年齢で)発症した罹患家系員や不完全浸透など、リンチ症候群を有する家系の古典的な特徴の一部を示す。リンチ症候群家系は、これらの特徴の一部またはすべてを示す可能性がある。リンチ症候群家系には、このほか消化管がん、婦人科がん、泌尿生殖器がん、または他の結腸外のがんの個人が存在する場合もある。図に示しているように母系または父系を通して、常染色体優性症候群としてリンチ症候群が伝播する可能性がある。がんのリスクは100%ではないため、例えばこの家系の37歳で結腸がんと診断された女性の母親のように、リンチ症候群の個人ががんに罹患しない場合もある(不完全浸透と呼ばれる)。 BRCA1またはBRCA2病原性多様体キャリアに発生する乳がんおよび卵巣がんと非キャリアに発生する乳がんおよび卵巣がんとを区別する疾病特徴的な特性はない。BRCA1病原性多様体キャリアに発生する乳がんは、ER陰性、プロゲステロン受容体陰性、HER2/neu受容体陰性(すなわち、トリプルネガティブ乳がん[TNBC])であり、基底細胞表現型(basal phenotype)を有する傾向がより高い。BRCA1関連卵巣がんは、高悪性度で病理組織学的に漿液性である可能性が高い。(詳しい情報については、本要約の乳がんの病理学および卵巣がんの病理学のセクションを参照のこと。)
一部の病理学的特徴によってリンチ症候群関連病原性多様体キャリアと非キャリアを区別できる。リンチ症候群において発生する子宮内膜がんの顕著な特徴は、マイクロサテライト不安定性(MSI)の存在および特異的なミスマッチ修復(MMR)蛋白の欠如といったMMRの欠損である。これらの分子的変化に加えて、腫瘍浸潤リンパ球、腫瘍周囲リンパ球、組織像が未分化型腫瘍、子宮下部起源であること、同時性腫瘍といった組織学的変化も見られる。
乳がんおよび卵巣がんのリスク評価とリスクに関する家族歴の確認における考慮事項
リスクを評価するために家族歴を用いる場合、家族歴の正確性および完全性を考慮に入れる必要がある。既報の家族歴に誤りがあるか、がんに罹患している近親者に気付かない場合もある。さらに、小家族および若年死は、家族歴から得られる情報を限定する。通常母系よりも父系の乳がんおよび卵巣がんの方が遠い血縁者まで含むので、情報を取得するのがより困難である。別個に検証した症例と自己報告型の情報を比較した場合、乳がんの家族歴の感度は比較的高く83~97%であるが、卵巣がんでは低く60%である。[ 111 ][ 112 ]家族歴に依拠する場合のこの他の制限としては、養子縁組;女性が少数の家族;家族歴情報の入手の制限;がん以外の適応により、子宮、卵巣、および/または卵管が偶発的に切除されていることが挙げられる。家族歴は進化するため、時間の経過とともに両方の親の家族歴を更新することが重要である。(詳しい情報については、がんの遺伝学的リスク評価とカウンセリングのPDQ要約の家族歴の正確度のセクションを参照のこと。)
乳がんおよび婦人科がんリスクの予測モデル
乳がんおよび/または婦人科がんに罹患する個人の生涯リスクを予測するモデルが利用可能である。[ 113 ][ 114 ][ 115 ][ 116 ]加えて、個人がBRCA1、BRCA2、またはリンチ症候群に関連するいずれかのMMR遺伝子に病原性多様体を有する確率を予測するモデルも存在する。(これらのモデルの一部に関する詳しい情報については、本要約のBRCA1またはBRCA2病原性多様体の確率を予測するためのモデルのセクションを参照のこと。)すべてのモデルがすべての患者に対し適切に使用できるわけではない。各モデルは患者の特性や家族歴がそのモデルの元になる研究集団の特性や家族歴と類似している場合にのみ適切である。モデルが異なれば、同じ臨床シナリオに対して大幅に異なるリスク推定値が得られる可能性があるが、これらの推定値の検証は、多くのモデルで実施されていない。[ 114 ][ 117 ][ 118 ]
乳がんのリスク評価モデル
一般に、乳がんリスク評価モデルは次の2種類の集団を想定して設計されている:1)病原性多様体または乳がんあるいは卵巣がんの強力な家族歴のない女性;2)乳がんまたは卵巣がんの個人歴または家族歴を有するために高リスクである女性。[ 118 ]第一のタイプの女性集団向けモデル(例、Breast Cancer Risk Assessment Tool [BCRAT]の基礎となっているゲイルモデル[ 119 ]、およびColditz and Rosnerモデル[ 120 ])は、限られた家族歴に関する情報(例、乳がんに罹患した第一度近親者の数)のみを必要とする。一方、高リスク女性集団向けのモデルには、がんの発症時年齢および/または特定の乳がん感受性アレルに関するキャリア状態など、乳がんおよび卵巣がんの個人歴と家族歴についてより詳細な情報が必要となる。後者のモデルで用いられる遺伝因子は多様であり、1つのリスク遺伝子座を想定するモデル(例、クラウスモデル[ 121 ])もあれば、2つの遺伝子座を想定するモデル(例、International Breast Cancer Intervention Study [IBIS]モデル[ 122 ]やBRCAPROモデル[ 123 ])もあり、さらには複数の遺伝子座に加えて多遺伝子性の要素も想定するモデル(例、Breast and Ovarian Analysis of Disease Incidence and Carrier Estimation Algorithm [BOADICEA]モデル[ 124 ][ 125 ][ 126 ])もある。また、モデル間には、非遺伝的な危険因子に関する情報を用いるか否かに関する相違もある。3つのモデル(ゲイル/BCRAT、Pfeiffer[ 116 ]、IBIS)は非遺伝的な危険因子を考慮するが、それぞれが対象とする危険因子は異なる(例、Pfeifferモデルは飲酒量を用いるが、ゲイル/BCRATでは用いない)。これらのモデルが有する、がんに罹患する個人と罹患しない個人との識別能は限定的であり、これが高いモデルほど識別能が1に近く、低いモデルほど0.5に近いとすると、現行のモデルの識別能は0.56~0.63の範囲に収まる。[ 127 ]既存のモデルが将来のがんを予測する精度は一般に、プロスペクティブ研究においてより高いと評価されている。[ 118 ][ 128 ][ 129 ][ 130 ]BOADICEA、BRCAPRO、BCRAT、およびIBISモデルの10年間の性能を比較した解析で、家系選択がより詳細なモデル、特にBOADICEAおよびIBISの優越性が実証された。[ 131 ]
米国では、BRCAPRO、クラウスモデル、[ 121 ][ 132 ]およびゲイル/BCRATモデル[ 119 ]が臨床的カウンセリングにおいて広く用いられている。これらのモデルから得られるリスク推定値は、患者によって異なる。より詳細な家族歴情報を含む他のいくつかのモデルも用いられており、以下で考察する。
乳がんリスク評価モデルの臨床使用に関する他の留意事項
ゲイルモデルは、BCRATというコンピュータプログラムの基礎になっており、この評価ツールは1-800-4-CANCER(1-800-422-6237)のCancer Information Serviceへ電話することで米国国立がん研究所(NCI)から入手可能である。ゲイルモデルのこのバージョンは、浸潤性乳がんリスクのみを推定するものである。ゲイル/BCRATモデルは、マンモグラフィによるスクリーニングを毎年受けている白人女性の大規模集団において、乳がんリスクの予測で適度な正確度を有することが明らかになっている;しかしながら、試験対象のコホートにより信頼性はさまざまである。[ 133 ][ 134 ][ 135 ][ 136 ][ 137 ][ 138 ]リスクは以下の集団で過大評価されることがある:
ゲイル/BCRATモデルは35歳以上の女性に対して妥当である。このモデルは本来、白人女性を対象に開発された。[ 137 ]その後、浸潤性乳がんのアフリカ系米国人女性1,600人以上と対照1,600人以上から得られたデータでリスク推定を較正し、アフリカ系米国人女性用の拡張ゲイルモデルが開発された。[ 139 ]さらに、高リスクの一塩基多型と病原性多様体が拡張ゲイルモデルに組み込まれている;しかしながら、現在、これらの拡張モデルでリスクを計算するソフトウェアは存在しない。[ 140 ][ 141 ]乳房組織密度を組み入れている他のリスク評価モデルが開発されているが、臨床での使用には時期尚早である。[ 142 ][ 143 ]
一般的に、以下の特性の1つ以上に該当する家系には、ゲイル/BCRATモデルを単独で用いるべきではない:
家族歴を組み入れている一般的なモデルには、IBIS、BOADICEA、BRCAPROの各モデルがある。IBIS/Tyrer-Cuzickモデルは遺伝的要因と非遺伝的要因の両方を組み入れている。[ 122 ]3世代にわたる家系を用いて、ある人がBRCA1/BRCA2病原性多様体または浸透度が低いと想定される遺伝子のいずれかを保有している可能性が推定される。さらに、このモデルでは、出産歴、肥満指数(BMI)、身長、初潮年齢、第1子出産年齢、閉経年齢、HRT開始年齢などの個人的な危険因子も組み入れている。遺伝的要因と非遺伝的要因の両方を組み合わせてリスクが推定される。BOADICEAモデルは家族歴を調査して乳がんリスクを推定し、BRCA1/BRCA2とBRCA1/BRCA2以外の遺伝的危険因子の両方を組み込んでいる。[ 125 ]BOADICEAモデルとBRCA1/BRCA2に関する情報を使用する他のモデルとの最も重要な相違は、BOADICEAが乳がんの基礎的な遺伝学に関する知見により適合するように、複数の遺伝子座だけでなく多遺伝子性の要素を考慮に入れていることである。[ 124 ][ 125 ][ 126 ]BOADICEAモデルはまた、CHEK2、ATM、PALB2など、追加の病原性多様体を含めるように拡張されている。[ 144 ]しかし、これらのモデルの識別能と較正は、独立したサンプルで比較した場合に大きく異なる;[ 128 ]IBISモデルとBOADICEAモデルでは、残りの生涯リスクを推定する場合に比べ、より短い一定期間(例、10年)のリスクを推定する場合に、より類似した結果が得られる。[ 128 ]通常、あらゆるがんのリスク推定モデルは、より短期間(例、5年または10年)について検証されているため、残りの生涯リスクの推定よりも一定期間のリスク推定の方が正確で、臨床状況における有用な手法となりうる。
加えて、容易に利用でき、当人の危険因子に基づいて集団レベルのリスクとの関係から女性個人のリスクに関する情報を提供するモデルも、臨床状況では有用となるであろう(例、Your Disease Risk)。こうしたツールは、平均リスクの女性に関する情報を使用して開発されており、絶対リスク推定値は算出しないが、それでもなお予防に関するカウンセリングを受ける女性には役立ちうる。いくつかのリスク評価モデルに対して、大規模コホートを用いた開発と検証により、遺伝的データと非遺伝的データ、乳腺密度、その他のバイオマーカーの組み込みが進められている。
ほとんどの乳がんリスクモデルは、全体として適切に調整されていることが示されているが、女性のサブグループごとにモデルの能力が異なる可能性がある。特に、BRCA1またはBRCA2病原性多様体の検査が陰性の女性に対するリスクモデルについて、独立したプロスペクティブな検証により、最も一般的に使用される臨床リスクモデルでは、このグループの女性のリスクが過小予測されることが裏付けられた。[ 145 ]血縁者の検査結果が知られているかどうかによっても、その能力は異なる。本モデルでは、検査結果が陰性であったが、血縁者が検査を受けていない女性でも、リスクが26.3~56.7%過少予測された。
卵巣がんリスク評価モデル
卵巣がんに関しては、2つのリスク予測モデルが開発されている。[ 115 ][ 116 ]Rosnerモデル[ 115 ]では、閉経年齢、初潮年齢、経口避妊薬の使用、卵管結紮が用いられた;C統計量は0.60であった(0.57-0.62)。Pfeifferモデル[ 116 ]では経口避妊薬の使用、閉経期のホルモン療法、乳がんまたは卵巣がんの家族歴が用いられ、識別能は0.59と同等であった(0.56-0.62)。いずれのモデルも十分に較正されたが、双方とも識別能はそれほど高くなく、スクリーニングにおける有用性は限定的であった。
子宮内膜がんリスク評価モデル
Pfeifferモデルは一般集団における子宮内膜がんの予測に使用されている。[ 116 ]この相対リスクモデルでは、子宮内膜がんに関して、BMI、閉経期のホルモン療法の使用、閉経状態、閉経年齢、喫煙状態、経口避妊薬の使用状況が含まれた。同モデルの識別能は0.68であった(0.66-0.70);このモデルは、ほとんどのサブグループで子宮内膜がんの発生を過大評価したが、最もBMIが高い層の女性、閉経前女性、閉経期に10年以上ホルモン療法を受けている女性では、がんを過小評価した。
対照的に、MMRpredict、PREMM5(PREdiction Model for gene Mutations)、MMRproの3つは、リンチ症候群に罹患しうる個人の識別に用いられる定量的予測モデルである。[ 146 ][ 147 ][ 148 ]MMRpredictが対象とするのは大腸がんのみであるが、MSIと免疫組織化学(IHC)腫瘍検査の結果が考慮される。PREMM5はPREMM(1,2,6)が更新されたものであり、PMS2およびEPCAMなど、リンチ症候群に関連する5つの遺伝子のそれぞれを検討に含める。他のリンチ症候群関連腫瘍も検討に含めるが、腫瘍検査の結果は考慮しない。[ 147 ]MMRproは、腫瘍検査ならびに生殖細胞検査の結果を取り入れるが、罹患した個人と罹患していない個人をリスク定量化プロセスに含めるため、より多くの時間を要する。これら3種類の予測モデルはいずれも、MMR遺伝子の病原性多様体を有する大腸がん患者の特定において、従来のアムステルダムおよびBethesda基準と同等である。[ 149 ]しかし、これらのモデルは大腸がん患者を対象に開発、検証されたため、結腸がん患者を対象とした場合に比べて、子宮内膜がん患者のリンチ症候群に対する識別能が低い。[ 150 ]実際に、病原性多様体キャリアの識別に関するMSIおよびIHCの感度と特異度はこれらの予測モデルよりもかなり高く、子宮内膜がん女性のリンチ症候群スクリーニングにおける分子的な腫瘍検査の実施が支持される。
表1に、臨床状況で広く用いられている乳がんおよび婦人科がんのリスク評価モデルについて、それぞれの特色をまとめた。これらのモデルは、検討される家族歴の範囲、非遺伝的な危険因子を含むか否か、キャリアの状態および多遺伝子リスクを考慮するか否かという点(モデルへの入力)に相違がある。さらに、生成されるリスク推定の種類(モデルの出力)も異なる。これらの因子は、特定の個人に最適なモデルを選択する際に必要な情報となりうる。
表1.乳がんおよび婦人科がんの年齢別絶対リスク算出に用いられる予測モデルの概要 モデル 家族歴(入力) 病原性多様体(入力) 危険因子(入力) 生成されるリスク推定値(出力) BCRAT = Breast Cancer Risk Assessment Tool(乳がんリスク評価ツール);BOADICEA = Breast and Ovarian Analysis of Disease Incidence and Carrier Estimation Algorithm(乳がんおよび卵巣がん発生およびキャリア推定に関する解析アルゴリズム);IBIS = International Breast Cancer Intervention Study(国際乳がん介入研究);PREMM = PREdiction Model for gene Mutations(遺伝子変異に対する予測モデル)。 a高リスクは、指定されたがんの種類の個人歴または家族歴を有する人と定義される。 bモデルの基礎的な想定としてポリジーンを考慮する。 乳がんのリスク評価モデル 平均リスクの女性のモデル ゲイル/BCRAT 第一度近親者(乳がん) いいえ はい 乳がん Pfeiffer (乳房)[ 116 ] 第一度近親者(乳がん、卵巣がん) いいえ はい 乳がん Colditz and Rosner [ 120 ] なし いいえ はい 乳がん 高リスク女性のモデルa クラウス[ 121 ] 数世代にわたる(乳がん) いいえ いいえ 乳がん BRCAPRO 数世代にわたる(乳がん、卵巣がん) BRCA1/BRCA2 いいえ 乳がん;BRCA1/BRCA2病原性多様体を有するリスク(%) IBIS 数世代にわたる(卵巣がん) BRCA1/BRCA2 はい 乳がん;BRCA1/BRCA2病原性多様体を有するリスク(%) BOADICEAb 数世代にわたる(膵がん、乳がん、卵巣がん) BRCA1/BRCA2 いいえ 乳がんおよび卵巣がん;BRCA1/BRCA2病原性多様体を有するリスク(%) 卵巣がんのリスク評価モデル 平均リスクの女性のモデル Rosner [ 115 ] なし いいえ はい 卵巣がん Pfeiffer (卵巣)[ 116 ] 第一度近親者(乳がん、卵巣がん) いいえ はい 乳がん 高リスク女性のモデルa BOADICEAb 数世代にわたる(膵がん、乳がん、卵巣がん) BRCA1/BRCA2 いいえ 乳がんおよび卵巣がん;BRCA1/BRCA2病原性多様体を有するリスク(%) 子宮内膜がんのリスク評価モデル 平均リスクの女性のモデル Pfeiffer (子宮内膜)[ 116 ] なし いいえ はい 子宮内膜がん 高リスク女性のモデルa PREMM5 数世代にわたる(結腸がん、子宮内膜がん、その他のリンチ症候群関連がんおよびポリープ) いいえ いいえ MLH1、MSH2、MSH6病原性多様体を有するリスク(%) MMRpro 数世代にわたる(結腸がん、子宮内膜がん) いいえ いいえ MLH1、MSH2、MSH6病原性多様体を有するリスク(%) MMRpredict [ 146 ] 数世代にわたる(結腸がん、子宮内膜がん) いいえ いいえ MLH1、MSH2、MSH6病原性多様体を有するリスク(%) 遺伝子検査を実施する場合の考慮事項
遺伝子検査の適応
いくつかの専門家組織および専門家委員会-米国臨床腫瘍学会[ 151 ]、National Comprehensive Cancer Network(NCCN)[ 152 ]、米国人類遺伝学会[ 153 ]、American College of Medical Genetics and Genomics[ 154 ]、米国遺伝カウンセラー学会(National Society of Genetic Counselors)[ 154 ]、米国予防サービス作業部会(U.S. Preventive Services Task Force)[ 155 ]、およびSociety of Gynecologic Oncologists[ 156 ]など-は、医療提供者がBRCA1またはBRCA2病原性多様体を有する可能性のある個人を同定する際に有用な臨床基準および診療ガイドラインを開発している。
2019年にAmerican Society of Breast Surgeonsは、「臨床シナリオおよび家族歴に適切な他の遺伝子とともに、BRCA1/BRCA2およびPALB2」の遺伝子検査をすべての乳がん患者に対して利用可能にする勧告を公表した。[ 157 ]この勧告は、乳がん患者が遺伝子検査に関するNCCNガイドラインを満たすかどうかにかかわらず、拡大多重遺伝子パネルを通して同定された病原性多様体の保有率が同程度であることを示した研究に基づいていた。[ 158 ]この研究は、考慮する必要がある重要な方法論的問題をかかえており、その中には、検査をすでに受けた参加者の除外、研究参加者で報告されたリスク基準の精度が不明確、管理ガイドラインが不明確な遺伝子の組み入れ、および病原性多様体または病原性の可能性が高い多様体が同定された具体的な遺伝子における2つのグループ間での相違がある。例えば、NCCN基準を満たした参加者と満たさなかった参加者の間では、BRCA1/BRCA2多様体の検出に統計的な有意差が認められた。他の研究でも、BRCA1/BRCA2多様体を予測する際に、NCCN基準が良好な感度を有していることが明らかにされている。例えば、NCCN基準によりBRCA1/BRCA2病原性多様体キャリアの88.9%が検出できることを示した研究[ 159 ]が1つあり、複数のNCCN基準を満たす場合は、陽性適中率が10%の閾値を超える(例、2つを超えるNCCN基準を満たす場合は12%)ことを明らかにした研究もある。[ 160 ]遺伝子検査の費用が継続的に減少していくにつれて、バイアスのない証拠が利用可能になった時点で、スクリーニング、予防、および検査に対する費用対効果の影響を含め、検査の適応が拡大する可能性がある。
がん診断時に遺伝子検査を提案する有益性
新たながんの診断時に、遺伝性がん素因に対する遺伝子検査は、手術、化学療法および他の生物学的製剤、放射線療法の決定を含めて患者のケアの指針となる可能性がある。[ 161 ][ 162 ]高リスク患者では、遺伝子検査の選択肢は、診断時のがん治療に関して共有される意思決定過程において重要な部分である。この状況において、遺伝子検査に関する意思決定を容易にするツールが利用可能である。[ 163 ]
乳がんの診断
乳がん診断時に遺伝子検査を提供する有益性には以下のものがあるが、これだけに限定されない:
- 手術:乳がんに対する遺伝的感受性の確認は、外科的治療の決定に影響しうる。一例として、BRCA病原性多様体キャリア、特に若年で診断されたキャリアにおける2番目の原発性乳がんのリスク増加は、乳がんの外科的治療として(腫瘤摘出術または片側乳房切除術/乳房亜全摘手術よりも)両側乳房切除術を選択する決定に影響しうる。[ 164 ](2番目の原発性乳がんのリスクに関する詳しい情報については、本要約のBRCA病原性多様体キャリアにおける対側乳がんのセクションを参照のこと。)リスク低減のための卵管卵巣摘出術の話し合いが適応となり[ 165 ]、婦人科への紹介が検討されることがある。
- 化学療法および他の生物学的製剤:遺伝性がん素因遺伝子における病原性多様体の同定により、内科的治療が誘導される場合がある。一例として、BRCA病原性多様体キャリアでは、乳がんの治療にプラチナベースの薬物が含まれる場合がある。[ 166 ]さらに、ポリ(ADPリボース)ポリメラーゼ(PARP)阻害薬などの新たな薬物が転移性乳がんの治療に用いられる場合がある。[ 167 ]
- 放射線療法:遺伝性乳がん感受性遺伝子における病原性多様体の存在により、放射線療法の使用に関する決定が誘導される場合がある。特に、照射された乳房における創傷治癒の不良は、再建術を併用するリスク低減のための乳房切除術を検討しているキャリアにとっては重要な考慮事項である。一例として、TP53に病原性多様体を有する個人は、後の新たながんに対するリスク増加など、放射線によるリスクが高くなることがある。[ 168 ][ 169 ]したがって、乳がんが診断されている状況でのTP53キャリアの同定は、放射線療法の決定および再建術の選択肢に影響しうる。
卵巣がんの診断
卵巣がん診断時に遺伝子検査を提供する有益性には以下のものがあるが、これだけに限定されない:
- 手術:ほとんどの症例では、卵巣がん手術に対する決定は、付属器腫瘤または腹部症状に基づいてなされる。可能な場合は、診断時に遺伝性の遺伝子多様体の可能性を検討することで、手術の意思決定の価値が高まる可能性がある。卵巣/卵管がんに対する遺伝的感受性の確認は、外科的治療の決定に影響しうる。浸透度の高い卵巣がん遺伝子の病原性多様体を保有するリスクが高い比較的若年の女性における疑わしい付属器腫瘤について、この情報の認識はリスク低減のための、または治療のための手術の決定の指針として役立つことがある。[ 170 ][ 171 ]妊孕性温存手術を検討している女性には、遺伝学的知識は両側卵管卵巣摘出術を検討する動機になり、BRCA1病原性多様体キャリアの場合は、侵攻性の子宮がんリスクに関してより詳細な話し合いの動機になる。
- 化学療法および生物学的製剤:卵巣がんに対する第一選択化学療法は依然として、プラチナ製剤およびタキサン系の化学療法の基本骨格に依存している。最適に切除されたIII期卵巣がんに対する現在の治療法の選択肢には、静脈内(IV)化学療法、投与間隔を狭めた(dose-dense)IV化学療法、IVパクリタキセル + 腹腔内(IP)シスプラチンの併用とその1週間後のIPパクリタキセルが挙げられる。BRCA1およびBRCA2病原性多様体のキャリアはプラチナ製剤感受性で、BRCA1およびBRCA2野生型患者と比較して無増悪生存期間が長いと考えられるため[ 172 ][ 173 ]、特定の治療戦略が抗血管新生効果、腹膜の用量強度、またはプラチナ製剤の用量強度によって推進されるかどうかは不明である。生物学的標的として(化学療法と併用するか、維持療法としての)PARPの登場もまた、登録を完了した臨床試験の結果を待つ間、卵巣がんの第一選択治療という武器庫を増加させうる。(卵巣がん治療におけるPARP阻害薬に関する詳しい情報については、本要約の卵巣がんのセクションにある卵巣がんの治療における全身療法のセクションを参照のこと。)
子宮内膜がんの診断
子宮内膜がん診断時に遺伝子検査を提供する有益性には以下のものがあるが、これだけに限定されない:
- 手術:新たに診断された子宮内膜がんに対する最も一般的な治療として、卵巣および卵管の切除のほか、リンパ節の評価を伴う子宮摘出が挙げられる。[ 174 ]この実施に対する例外は、妊孕性の維持または付属器の維持を希望する比較的若年の女性に当てはまる場合がある。子宮内膜サンプリングの免疫組織化学検査により、診断時に遺伝性の遺伝子多様体の可能性を評価でき、手術の意思決定過程の価値が高まる可能性がある。リンチ症候群であることが明らかになった若年の女性について、この情報の認識は、将来の出産が可能となるようなホルモンによる子宮内膜がんの管理か、または特定の遺伝子多様体に基づいて卵巣がんリスクが十分に高いと考えられる場合は卵管卵巣摘除術を決定する指針として役立つ可能性がある。BRCA1/BRCA2における病原性多様体、または卵巣がんリスクを増大させる他の相同組換え欠損の1つを保有することが明らかになった若年の女性は、卵管卵巣摘除術または、少なくとも卵管切除術のどちらかを選びたいと希望する場合がある。
- 化学療法および他の生物学的製剤:免疫チェックポイント阻害薬は、MSIまたはMMR欠損が認められる子宮内膜がんにおける使用が現在承認されている。[ 175 ]MSIおよびMMR状態が診断時または疾患再発時に評価される一方で、診断時の腫瘍検査とともに初回の病理組織判定(通常は子宮摘出時)を実施することは有益であろう。
多重遺伝子(パネル)検査
次世代の塩基配列決定法が利用可能になり、米国の最高裁判所がヒト遺伝子に特許権を設定することはできないと判決したことから、現在ではいくつかの臨床検査施設から、単一遺伝子検査と同程度の費用で多重遺伝子パネルを用いた遺伝子検査が提供されている。BRCA1とBRCA2の検査でさえ、2つの遺伝子に限定したパネル検査である。卵巣/卵管/腹膜がん全体の約25%が遺伝性の遺伝子疾患により引き起こされる。これらのうち約4分の1(卵巣/卵管/腹膜がん全体の6%)は、ファンコニー貧血経路と関係している多くの遺伝子を含むBRCA1とBRCA2以外の遺伝子か、そうでなくとも相同的組換えが関与している遺伝子に起因している。[ 176 ] BRCA1とBRCA2の病原性多様体が陰性の卵巣がん患者集団では、多重遺伝子パネル検査によりアクション可能な病原性多様体が明らかにされることがある。[ 177 ][ 178 ][ 179 ]
一般に、多重遺伝子パネル検査により、さまざまな集団にわたりBRCA以外の病原性多様体の検出率が増加する。[ 162 ][ 180 ][ 181 ][ 182 ]選択されていない乳がん患者集団におけるBRCA1とBRCA2の病原性多様体の保有率は6.1%であったが、他の乳がん/卵巣がん素因遺伝子における病原性多様体の保有率は4.6%であった。[ 183 ]選択されていない子宮内膜がん患者集団におけるリンチ症候群の病原性多様体(MLH1、MSH2、EPCAM-MSH2、MSH6、およびPMS2)の保有率は5.8%であった;他のアクション可能な遺伝子における病原性多様体の保有率は3.4%であった。[ 92 ]同様に、Myriad社の25遺伝子パネルを用いて検査した乳がんの女性35,409人を対象にした1件の研究では、9.3%の女性に病原性多様体が見つかった。[ 184 ]この9.3%のうち、48.5%の女性がBRCA1またはBRCA2に病原性多様体を保有した。病原性多様体が同定された他の乳がん遺伝子の大多数には、CHEK2(11.7%)、ATM(9.7%)、およびPALB2(9.3%)が含まれた。このパネル上の他の乳がん遺伝子における病原性多様体の保有率は、0.05~0.31%に及んだ。リンチ症候群遺伝子における病原性多様体は、同定された多様体の7.0%を占めた;3.7%がこのパネルに含まれた他の遺伝子において発見された。病原性多様体の割合は、40歳前に診断されたTNBCの女性で比較的高かった。男性の乳がん患者におけるBRCA以外の感受性遺伝子において病原性多様体が同定される同様の傾向も報告されている。[ 185 ]BRCA1/BRCA2について以前の検査で陰性であった女性を対象にした2件の研究において、多重遺伝子パネルを用いた反射検査により、8~11%の症例で追加の遺伝子における病原性多様体が同定された。[ 186 ][ 187 ]乳がん患者77,085人および卵巣がん患者6,001人を対象とした研究で、それぞれ24.1%および30.9%が遺伝子検査を受けた。検査を受けた患者のうち、乳がん患者の7.8%および卵巣がん患者の14.5%で病原性多様体または病原性の可能性が高い多様体が同定された。乳がん患者において、BRCA以外で多く同定された病原性多様体には、CHEK2(1.6%)、PALB2(1.0%)、ATM (0.7%)、およびNBN(0.4%)が含まれていた。卵巣がん患者において、BRCA以外の病原性多様体には、CHEK2(1.4%)、BRIP1(0.9%)、MSH2(0.8%)、およびATM(0.6%)が含まれていた。[ 188 ]
TNBCと診断された年齢が60歳未満の女性は現在、治療決定の指針とするために、BRCA1/BRCA2検査を受けるように推奨されている。[ 152 ]多重遺伝子(パネル)検査を用いて2つの個別コホートを比較した大規模研究では、BRCA1/BRCA2遺伝子に加えて、他の6つの乳がん感受性遺伝子もより高いTNBCリスクと関連していることが報告された。特に、BRCA1およびBRCA2に加えて、BARD1、PALB2、およびRAD51Dにおける病原性多様体は、それぞれ5倍を超える乳がん増加と関連していた。[ 189 ]他の3つの遺伝子、BRIP1、RAD51C、およびTP53における病原性多様体は、それぞれ2倍を超えるTNBCリスク増加と関連していた。これらの8つの遺伝子における病原性多様体は、TNBC症例の12%(BRCA1/BRCA2で8.3%、BRCA1/BRCA2以外で3.7%)で報告された。この研究は、21遺伝子パネルを用いる遺伝子検査を受けた140,449人の個人(8,753人がTNBC症例)からなる臨床検証コホート(サンプルA)を対象に実施された。さらに、二番目のサンプル(サンプルB)では、17遺伝子パネルを用いて2,143人の個人からなる併合コンソーシアムを対象に遺伝子頻度の比率が検討された。サンプルAで検討された21遺伝子における病原性多様体全体の頻度は14.4%(BRCA1/BRCA2が8.4%、BRCA1/BRCA2以外が6.0%)であった。この2つのサンプルでは、年齢、人種/民族、およびがん家族歴に差があり、サンプルAの方が若く、人種的および民族的により多様で、がん家族歴を有する傾向が高かったにもかかわらず、リスク推定値に関して非常に一貫した結果が得られた。これらの21遺伝子における病原性多様体の検出頻度は、白人(全体で14%、BRCA1/BRCA2で7.8%、BRCA1/BRCA2以外で6.2%)とアフリカ系米国人(全体で14.6%、BRCA1/BRCA2で9.0%、BRCA1/BRCA2以外で5.6%)でも類似していたことから、白人に対してアフリカ系米国人で高いTNBC発生率は、環境要因によりもたらされることが裏付けられる。
多重遺伝子検査には留意すべき点がある。多重遺伝子パネル検査の一環として同定された遺伝子は、多様な乳がんリスクと関連していることもあれば、既知のリスクを与えないこともある。[ 179 ]意義不明の多様体の所見が得られる可能性もある。ある1つの遺伝子内でも、特異的な病原性多様体に基づいてリスクに差がある可能性がある。[ 190 ]遺伝性乳がんおよび卵巣がん以外の症候群で懸念される家族歴がある場合、またはより重要な点として、特に保険上の制約がある場合に、1つの検査によって可能な限り多くの遺伝子情報を得るために、現在では多くのセンターが単なるBRCA1とBRCA2の検査の代わりに多重遺伝子パネル検査を提供している。
(遺伝学教育およびカウンセリングの考慮、ならびに多重遺伝子検査の使用を検討している研究を含む多重遺伝子検査に関する詳しい情報については、がんの遺伝学的リスク評価とカウンセリングのPDQ要約の多重遺伝子(パネル)検査のセクションを参照のこと。)
参考文献- American Cancer Society: Cancer Facts and Figures 2020. Atlanta, Ga: American Cancer Society, 2020. Available online. Last accessed May 12, 2020.[PUBMED Abstract]
- Ravdin PM, Cronin KA, Howlader N, et al.: The decrease in breast-cancer incidence in 2003 in the United States. N Engl J Med 356 (16): 1670-4, 2007.[PUBMED Abstract]
- Feuer EJ, Wun LM, Boring CC, et al.: The lifetime risk of developing breast cancer. J Natl Cancer Inst 85 (11): 892-7, 1993.[PUBMED Abstract]
- Yang Q, Khoury MJ, Rodriguez C, et al.: Family history score as a predictor of breast cancer mortality: prospective data from the Cancer Prevention Study II, United States, 1982-1991. Am J Epidemiol 147 (7): 652-9, 1998.[PUBMED Abstract]
- Colditz GA, Willett WC, Hunter DJ, et al.: Family history, age, and risk of breast cancer. Prospective data from the Nurses' Health Study. JAMA 270 (3): 338-43, 1993.[PUBMED Abstract]
- Slattery ML, Kerber RA: A comprehensive evaluation of family history and breast cancer risk. The Utah Population Database. JAMA 270 (13): 1563-8, 1993.[PUBMED Abstract]
- Johnson N, Lancaster T, Fuller A, et al.: The prevalence of a family history of cancer in general practice. Fam Pract 12 (3): 287-9, 1995.[PUBMED Abstract]
- Pharoah PD, Day NE, Duffy S, et al.: Family history and the risk of breast cancer: a systematic review and meta-analysis. Int J Cancer 71 (5): 800-9, 1997.[PUBMED Abstract]
- Bevier M, Sundquist K, Hemminki K: Risk of breast cancer in families of multiple affected women and men. Breast Cancer Res Treat 132 (2): 723-8, 2012.[PUBMED Abstract]
- Kharazmi E, Chen T, Narod S, et al.: Effect of multiplicity, laterality, and age at onset of breast cancer on familial risk of breast cancer: a nationwide prospective cohort study. Breast Cancer Res Treat 144 (1): 185-92, 2014.[PUBMED Abstract]
- Reiner AS, Sisti J, John EM, et al.: Breast Cancer Family History and Contralateral Breast Cancer Risk in Young Women: An Update From the Women's Environmental Cancer and Radiation Epidemiology Study. J Clin Oncol 36 (15): 1513-1520, 2018.[PUBMED Abstract]
- Mucci LA, Hjelmborg JB, Harris JR, et al.: Familial Risk and Heritability of Cancer Among Twins in Nordic Countries. JAMA 315 (1): 68-76, 2016.[PUBMED Abstract]
- Johannsson O, Loman N, Borg A, et al.: Pregnancy-associated breast cancer in BRCA1 and BRCA2 germline mutation carriers. Lancet 352 (9137): 1359-60, 1998.[PUBMED Abstract]
- Jernström H, Lerman C, Ghadirian P, et al.: Pregnancy and risk of early breast cancer in carriers of BRCA1 and BRCA2. Lancet 354 (9193): 1846-50, 1999.[PUBMED Abstract]
- Friebel TM, Domchek SM, Rebbeck TR: Modifiers of cancer risk in BRCA1 and BRCA2 mutation carriers: systematic review and meta-analysis. J Natl Cancer Inst 106 (6): dju091, 2014.[PUBMED Abstract]
- Jernström H, Lubinski J, Lynch HT, et al.: Breast-feeding and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 96 (14): 1094-8, 2004.[PUBMED Abstract]
- Valentini A, Lubinski J, Byrski T, et al.: The impact of pregnancy on breast cancer survival in women who carry a BRCA1 or BRCA2 mutation. Breast Cancer Res Treat 142 (1): 177-85, 2013.[PUBMED Abstract]
- Milne RL, Osorio A, Ramón y Cajal T, et al.: Parity and the risk of breast and ovarian cancer in BRCA1 and BRCA2 mutation carriers. Breast Cancer Res Treat 119 (1): 221-32, 2010.[PUBMED Abstract]
- Breast cancer and hormonal contraceptives: collaborative reanalysis of individual data on 53 297 women with breast cancer and 100 239 women without breast cancer from 54 epidemiological studies. Collaborative Group on Hormonal Factors in Breast Cancer. Lancet 347 (9017): 1713-27, 1996.[PUBMED Abstract]
- Iodice S, Barile M, Rotmensz N, et al.: Oral contraceptive use and breast or ovarian cancer risk in BRCA1/2 carriers: a meta-analysis. Eur J Cancer 46 (12): 2275-84, 2010.[PUBMED Abstract]
- Breast cancer and hormone replacement therapy: collaborative reanalysis of data from 51 epidemiological studies of 52,705 women with breast cancer and 108,411 women without breast cancer. Collaborative Group on Hormonal Factors in Breast Cancer. Lancet 350 (9084): 1047-59, 1997.[PUBMED Abstract]
- Writing Group for the Women's Health Initiative Investigators: Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women's Health Initiative randomized controlled trial. JAMA 288 (3): 321-33, 2002.[PUBMED Abstract]
- Chlebowski RT, Hendrix SL, Langer RD, et al.: Influence of estrogen plus progestin on breast cancer and mammography in healthy postmenopausal women: the Women's Health Initiative Randomized Trial. JAMA 289 (24): 3243-53, 2003.[PUBMED Abstract]
- Beral V; Million Women Study Collaborators: Breast cancer and hormone-replacement therapy in the Million Women Study. Lancet 362 (9382): 419-27, 2003.[PUBMED Abstract]
- Anderson GL, Limacher M, Assaf AR, et al.: Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: the Women's Health Initiative randomized controlled trial. JAMA 291 (14): 1701-12, 2004.[PUBMED Abstract]
- Schuurman AG, van den Brandt PA, Goldbohm RA: Exogenous hormone use and the risk of postmenopausal breast cancer: results from The Netherlands Cohort Study. Cancer Causes Control 6 (5): 416-24, 1995.[PUBMED Abstract]
- Steinberg KK, Thacker SB, Smith SJ, et al.: A meta-analysis of the effect of estrogen replacement therapy on the risk of breast cancer. JAMA 265 (15): 1985-90, 1991.[PUBMED Abstract]
- Sellers TA, Mink PJ, Cerhan JR, et al.: The role of hormone replacement therapy in the risk for breast cancer and total mortality in women with a family history of breast cancer. Ann Intern Med 127 (11): 973-80, 1997.[PUBMED Abstract]
- Stanford JL, Weiss NS, Voigt LF, et al.: Combined estrogen and progestin hormone replacement therapy in relation to risk of breast cancer in middle-aged women. JAMA 274 (2): 137-42, 1995.[PUBMED Abstract]
- Colditz GA, Egan KM, Stampfer MJ: Hormone replacement therapy and risk of breast cancer: results from epidemiologic studies. Am J Obstet Gynecol 168 (5): 1473-80, 1993.[PUBMED Abstract]
- Gorsky RD, Koplan JP, Peterson HB, et al.: Relative risks and benefits of long-term estrogen replacement therapy: a decision analysis. Obstet Gynecol 83 (2): 161-6, 1994.[PUBMED Abstract]
- Rebbeck TR, Friebel T, Wagner T, et al.: Effect of short-term hormone replacement therapy on breast cancer risk reduction after bilateral prophylactic oophorectomy in BRCA1 and BRCA2 mutation carriers: the PROSE Study Group. J Clin Oncol 23 (31): 7804-10, 2005.[PUBMED Abstract]
- Helzlsouer KJ, Harris EL, Parshad R, et al.: Familial clustering of breast cancer: possible interaction between DNA repair proficiency and radiation exposure in the development of breast cancer. Int J Cancer 64 (1): 14-7, 1995.[PUBMED Abstract]
- Helzlsouer KJ, Harris EL, Parshad R, et al.: DNA repair proficiency: potential susceptiblity factor for breast cancer. J Natl Cancer Inst 88 (11): 754-5, 1996.[PUBMED Abstract]
- Abbott DW, Thompson ME, Robinson-Benion C, et al.: BRCA1 expression restores radiation resistance in BRCA1-defective cancer cells through enhancement of transcription-coupled DNA repair. J Biol Chem 274 (26): 18808-12, 1999.[PUBMED Abstract]
- Abbott DW, Freeman ML, Holt JT: Double-strand break repair deficiency and radiation sensitivity in BRCA2 mutant cancer cells. J Natl Cancer Inst 90 (13): 978-85, 1998.[PUBMED Abstract]
- Easton DF: Cancer risks in A-T heterozygotes. Int J Radiat Biol 66 (6 Suppl): S177-82, 1994.[PUBMED Abstract]
- Kleihues P, Schäuble B, zur Hausen A, et al.: Tumors associated with p53 germline mutations: a synopsis of 91 families. Am J Pathol 150 (1): 1-13, 1997.[PUBMED Abstract]
- Pierce LJ, Strawderman M, Narod SA, et al.: Effect of radiotherapy after breast-conserving treatment in women with breast cancer and germline BRCA1/2 mutations. J Clin Oncol 18 (19): 3360-9, 2000.[PUBMED Abstract]
- Drooger J, Akdeniz D, Pignol JP, et al.: Adjuvant radiotherapy for primary breast cancer in BRCA1 and BRCA2 mutation carriers and risk of contralateral breast cancer with special attention to patients irradiated at younger age. Breast Cancer Res Treat 154 (1): 171-80, 2015.[PUBMED Abstract]
- Narod SA, Lubinski J, Ghadirian P, et al.: Screening mammography and risk of breast cancer in BRCA1 and BRCA2 mutation carriers: a case-control study. Lancet Oncol 7 (5): 402-6, 2006.[PUBMED Abstract]
- Andrieu N, Easton DF, Chang-Claude J, et al.: Effect of chest X-rays on the risk of breast cancer among BRCA1/2 mutation carriers in the international BRCA1/2 carrier cohort study: a report from the EMBRACE, GENEPSO, GEO-HEBON, and IBCCS Collaborators' Group. J Clin Oncol 24 (21): 3361-6, 2006.[PUBMED Abstract]
- Goldfrank D, Chuai S, Bernstein JL, et al.: Effect of mammography on breast cancer risk in women with mutations in BRCA1 or BRCA2. Cancer Epidemiol Biomarkers Prev 15 (11): 2311-3, 2006.[PUBMED Abstract]
- Gronwald J, Pijpe A, Byrski T, et al.: Early radiation exposures and BRCA1-associated breast cancer in young women from Poland. Breast Cancer Res Treat 112 (3): 581-4, 2008.[PUBMED Abstract]
- Pijpe A, Andrieu N, Easton DF, et al.: Exposure to diagnostic radiation and risk of breast cancer among carriers of BRCA1/2 mutations: retrospective cohort study (GENE-RAD-RISK). BMJ 345: e5660, 2012.[PUBMED Abstract]
- Giannakeas V, Lubinski J, Gronwald J, et al.: Mammography screening and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers: a prospective study. Breast Cancer Res Treat 147 (1): 113-8, 2014.[PUBMED Abstract]
- Smith-Warner SA, Spiegelman D, Yaun SS, et al.: Alcohol and breast cancer in women: a pooled analysis of cohort studies. JAMA 279 (7): 535-40, 1998.[PUBMED Abstract]
- Hamajima N, Hirose K, Tajima K, et al.: Alcohol, tobacco and breast cancer--collaborative reanalysis of individual data from 53 epidemiological studies, including 58,515 women with breast cancer and 95,067 women without the disease. Br J Cancer 87 (11): 1234-45, 2002.[PUBMED Abstract]
- McGuire V, John EM, Felberg A, et al.: No increased risk of breast cancer associated with alcohol consumption among carriers of BRCA1 and BRCA2 mutations ages <50 years. Cancer Epidemiol Biomarkers Prev 15 (8): 1565-7, 2006.[PUBMED Abstract]
- Dennis J, Ghadirian P, Little J, et al.: Alcohol consumption and the risk of breast cancer among BRCA1 and BRCA2 mutation carriers. Breast 19 (6): 479-83, 2010.[PUBMED Abstract]
- Cybulski C, Lubinski J, Huzarski T, et al.: Prospective evaluation of alcohol consumption and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. Breast Cancer Res Treat 151 (2): 435-41, 2015.[PUBMED Abstract]
- Lammert J, Lubinski J, Gronwald J, et al.: Physical activity during adolescence and young adulthood and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. Breast Cancer Res Treat 169 (3): 561-571, 2018.[PUBMED Abstract]
- Kehm RD, Genkinger JM, MacInnis RJ, et al.: Recreational Physical Activity Is Associated with Reduced Breast Cancer Risk in Adult Women at High Risk for Breast Cancer: A Cohort Study of Women Selected for Familial and Genetic Risk. Cancer Res 80 (1): 116-125, 2020.[PUBMED Abstract]
- Chen J, Pee D, Ayyagari R, et al.: Projecting absolute invasive breast cancer risk in white women with a model that includes mammographic density. J Natl Cancer Inst 98 (17): 1215-26, 2006.[PUBMED Abstract]
- Dupont WD, Page DL, Parl FF, et al.: Long-term risk of breast cancer in women with fibroadenoma. N Engl J Med 331 (1): 10-5, 1994.[PUBMED Abstract]
- Boyd NF, Byng JW, Jong RA, et al.: Quantitative classification of mammographic densities and breast cancer risk: results from the Canadian National Breast Screening Study. J Natl Cancer Inst 87 (9): 670-5, 1995.[PUBMED Abstract]
- Byrne C, Schairer C, Wolfe J, et al.: Mammographic features and breast cancer risk: effects with time, age, and menopause status. J Natl Cancer Inst 87 (21): 1622-9, 1995.[PUBMED Abstract]
- Pankow JS, Vachon CM, Kuni CC, et al.: Genetic analysis of mammographic breast density in adult women: evidence of a gene effect. J Natl Cancer Inst 89 (8): 549-56, 1997.[PUBMED Abstract]
- Boyd NF, Lockwood GA, Martin LJ, et al.: Mammographic densities and risk of breast cancer among subjects with a family history of this disease. J Natl Cancer Inst 91 (16): 1404-8, 1999.[PUBMED Abstract]
- Vachon CM, King RA, Atwood LD, et al.: Preliminary sibpair linkage analysis of percent mammographic density. J Natl Cancer Inst 91 (20): 1778-9, 1999.[PUBMED Abstract]
- Brunet JS, Ghadirian P, Rebbeck TR, et al.: Effect of smoking on breast cancer in carriers of mutant BRCA1 or BRCA2 genes. J Natl Cancer Inst 90 (10): 761-6, 1998.[PUBMED Abstract]
- Ghadirian P, Lubinski J, Lynch H, et al.: Smoking and the risk of breast cancer among carriers of BRCA mutations. Int J Cancer 110 (3): 413-6, 2004.[PUBMED Abstract]
- Amos CI, Struewing JP: Genetic epidemiology of epithelial ovarian cancer. Cancer 71 (2 Suppl): 566-72, 1993.[PUBMED Abstract]
- Stratton JF, Pharoah P, Smith SK, et al.: A systematic review and meta-analysis of family history and risk of ovarian cancer. Br J Obstet Gynaecol 105 (5): 493-9, 1998.[PUBMED Abstract]
- Whittemore AS, Harris R, Itnyre J: Characteristics relating to ovarian cancer risk: collaborative analysis of 12 US case-control studies. II. Invasive epithelial ovarian cancers in white women. Collaborative Ovarian Cancer Group. Am J Epidemiol 136 (10): 1184-203, 1992.[PUBMED Abstract]
- Brinton LA, Lamb EJ, Moghissi KS, et al.: Ovarian cancer risk after the use of ovulation-stimulating drugs. Obstet Gynecol 103 (6): 1194-203, 2004.[PUBMED Abstract]
- Gronwald J, Byrski T, Huzarski T, et al.: Influence of selected lifestyle factors on breast and ovarian cancer risk in BRCA1 mutation carriers from Poland. Breast Cancer Res Treat 95 (2): 105-9, 2006.[PUBMED Abstract]
- McLaughlin JR, Risch HA, Lubinski J, et al.: Reproductive risk factors for ovarian cancer in carriers of BRCA1 or BRCA2 mutations: a case-control study. Lancet Oncol 8 (1): 26-34, 2007.[PUBMED Abstract]
- Antoniou AC, Rookus M, Andrieu N, et al.: Reproductive and hormonal factors, and ovarian cancer risk for BRCA1 and BRCA2 mutation carriers: results from the International BRCA1/2 Carrier Cohort Study. Cancer Epidemiol Biomarkers Prev 18 (2): 601-10, 2009.[PUBMED Abstract]
- Narod SA, Sun P, Ghadirian P, et al.: Tubal ligation and risk of ovarian cancer in carriers of BRCA1 or BRCA2 mutations: a case-control study. Lancet 357 (9267): 1467-70, 2001.[PUBMED Abstract]
- Kotsopoulos J, Lubinski J, Gronwald J, et al.: Factors influencing ovulation and the risk of ovarian cancer in BRCA1 and BRCA2 mutation carriers. Int J Cancer 137 (5): 1136-46, 2015.[PUBMED Abstract]
- Rodriguez C, Patel AV, Calle EE, et al.: Estrogen replacement therapy and ovarian cancer mortality in a large prospective study of US women. JAMA 285 (11): 1460-5, 2001.[PUBMED Abstract]
- Riman T, Dickman PW, Nilsson S, et al.: Hormone replacement therapy and the risk of invasive epithelial ovarian cancer in Swedish women. J Natl Cancer Inst 94 (7): 497-504, 2002.[PUBMED Abstract]
- Lacey JV, Mink PJ, Lubin JH, et al.: Menopausal hormone replacement therapy and risk of ovarian cancer. JAMA 288 (3): 334-41, 2002.[PUBMED Abstract]
- Anderson GL, Judd HL, Kaunitz AM, et al.: Effects of estrogen plus progestin on gynecologic cancers and associated diagnostic procedures: the Women's Health Initiative randomized trial. JAMA 290 (13): 1739-48, 2003.[PUBMED Abstract]
- Tortolero-Luna G, Mitchell MF: The epidemiology of ovarian cancer. J Cell Biochem Suppl 23: 200-7, 1995.[PUBMED Abstract]
- Hankinson SE, Hunter DJ, Colditz GA, et al.: Tubal ligation, hysterectomy, and risk of ovarian cancer. A prospective study. JAMA 270 (23): 2813-8, 1993.[PUBMED Abstract]
- Rutter JL, Wacholder S, Chetrit A, et al.: Gynecologic surgeries and risk of ovarian cancer in women with BRCA1 and BRCA2 Ashkenazi founder mutations: an Israeli population-based case-control study. J Natl Cancer Inst 95 (14): 1072-8, 2003.[PUBMED Abstract]
- Kauff ND, Satagopan JM, Robson ME, et al.: Risk-reducing salpingo-oophorectomy in women with a BRCA1 or BRCA2 mutation. N Engl J Med 346 (21): 1609-15, 2002.[PUBMED Abstract]
- Rebbeck TR, Lynch HT, Neuhausen SL, et al.: Prophylactic oophorectomy in carriers of BRCA1 or BRCA2 mutations. N Engl J Med 346 (21): 1616-22, 2002.[PUBMED Abstract]
- Kotsopoulos J, Huzarski T, Gronwald J, et al.: Bilateral Oophorectomy and Breast Cancer Risk in BRCA1 and BRCA2 Mutation Carriers. J Natl Cancer Inst 109 (1): , 2017.[PUBMED Abstract]
- John EM, Whittemore AS, Harris R, et al.: Characteristics relating to ovarian cancer risk: collaborative analysis of seven U.S. case-control studies. Epithelial ovarian cancer in black women. Collaborative Ovarian Cancer Group. J Natl Cancer Inst 85 (2): 142-7, 1993.[PUBMED Abstract]
- Narod SA, Risch H, Moslehi R, et al.: Oral contraceptives and the risk of hereditary ovarian cancer. Hereditary Ovarian Cancer Clinical Study Group. N Engl J Med 339 (7): 424-8, 1998.[PUBMED Abstract]
- Whittemore AS, Balise RR, Pharoah PD, et al.: Oral contraceptive use and ovarian cancer risk among carriers of BRCA1 or BRCA2 mutations. Br J Cancer 91 (11): 1911-5, 2004.[PUBMED Abstract]
- McGuire V, Felberg A, Mills M, et al.: Relation of contraceptive and reproductive history to ovarian cancer risk in carriers and noncarriers of BRCA1 gene mutations. Am J Epidemiol 160 (7): 613-8, 2004.[PUBMED Abstract]
- Modan B, Hartge P, Hirsh-Yechezkel G, et al.: Parity, oral contraceptives, and the risk of ovarian cancer among carriers and noncarriers of a BRCA1 or BRCA2 mutation. N Engl J Med 345 (4): 235-40, 2001.[PUBMED Abstract]
- Soliman PT, Oh JC, Schmeler KM, et al.: Risk factors for young premenopausal women with endometrial cancer. Obstet Gynecol 105 (3): 575-80, 2005.[PUBMED Abstract]
- Vasen HF, Stormorken A, Menko FH, et al.: MSH2 mutation carriers are at higher risk of cancer than MLH1 mutation carriers: a study of hereditary nonpolyposis colorectal cancer families. J Clin Oncol 19 (20): 4074-80, 2001.[PUBMED Abstract]
- Daniels MS: Genetic testing by cancer site: uterus. Cancer J 18 (4): 338-42, 2012 Jul-Aug.[PUBMED Abstract]
- Dunlop MG, Farrington SM, Nicholl I, et al.: Population carrier frequency of hMSH2 and hMLH1 mutations. Br J Cancer 83 (12): 1643-5, 2000.[PUBMED Abstract]
- de la Chapelle A: The incidence of Lynch syndrome. Fam Cancer 4 (3): 233-7, 2005.[PUBMED Abstract]
- Ring KL, Bruegl AS, Allen BA, et al.: Germline multi-gene hereditary cancer panel testing in an unselected endometrial cancer cohort. Mod Pathol 29 (11): 1381-1389, 2016.[PUBMED Abstract]
- Shu CA, Pike MC, Jotwani AR, et al.: Uterine Cancer After Risk-Reducing Salpingo-oophorectomy Without Hysterectomy in Women With BRCA Mutations. JAMA Oncol 2 (11): 1434-1440, 2016.[PUBMED Abstract]
- McPherson CP, Sellers TA, Potter JD, et al.: Reproductive factors and risk of endometrial cancer. The Iowa Women's Health Study. Am J Epidemiol 143 (12): 1195-202, 1996.[PUBMED Abstract]
- Dossus L, Allen N, Kaaks R, et al.: Reproductive risk factors and endometrial cancer: the European Prospective Investigation into Cancer and Nutrition. Int J Cancer 127 (2): 442-51, 2010.[PUBMED Abstract]
- Shapiro S, Kelly JP, Rosenberg L, et al.: Risk of localized and widespread endometrial cancer in relation to recent and discontinued use of conjugated estrogens. N Engl J Med 313 (16): 969-72, 1985.[PUBMED Abstract]
- Ziel HK, Finkle WD: Increased risk of endometrial carcinoma among users of conjugated estrogens. N Engl J Med 293 (23): 1167-70, 1975.[PUBMED Abstract]
- Fisher B, Costantino JP, Redmond CK, et al.: Endometrial cancer in tamoxifen-treated breast cancer patients: findings from the National Surgical Adjuvant Breast and Bowel Project (NSABP) B-14. J Natl Cancer Inst 86 (7): 527-37, 1994.[PUBMED Abstract]
- Pike MC, Peters RK, Cozen W, et al.: Estrogen-progestin replacement therapy and endometrial cancer. J Natl Cancer Inst 89 (15): 1110-6, 1997.[PUBMED Abstract]
- Fournier A, Dossus L, Mesrine S, et al.: Risks of endometrial cancer associated with different hormone replacement therapies in the E3N cohort, 1992-2008. Am J Epidemiol 180 (5): 508-17, 2014.[PUBMED Abstract]
- Weiss NS, Sayvetz TA: Incidence of endometrial cancer in relation to the use of oral contraceptives. N Engl J Med 302 (10): 551-4, 1980.[PUBMED Abstract]
- Soini T, Hurskainen R, Grénman S, et al.: Cancer risk in women using the levonorgestrel-releasing intrauterine system in Finland. Obstet Gynecol 124 (2 Pt 1): 292-9, 2014.[PUBMED Abstract]
- Lindor NM, McMaster ML, Lindor CJ, et al.: Concise handbook of familial cancer susceptibility syndromes - second edition. J Natl Cancer Inst Monogr (38): 1-93, 2008.[PUBMED Abstract]
- Vasen HF, Offerhaus GJ, den Hartog Jager FC, et al.: The tumour spectrum in hereditary non-polyposis colorectal cancer: a study of 24 kindreds in the Netherlands. Int J Cancer 46 (1): 31-4, 1990.[PUBMED Abstract]
- Watson P, Lynch HT: Extracolonic cancer in hereditary nonpolyposis colorectal cancer. Cancer 71 (3): 677-85, 1993.[PUBMED Abstract]
- Watson P, Vasen HF, Mecklin JP, et al.: The risk of endometrial cancer in hereditary nonpolyposis colorectal cancer. Am J Med 96 (6): 516-20, 1994.[PUBMED Abstract]
- Aarnio M, Mecklin JP, Aaltonen LA, et al.: Life-time risk of different cancers in hereditary non-polyposis colorectal cancer (HNPCC) syndrome. Int J Cancer 64 (6): 430-3, 1995.[PUBMED Abstract]
- Raymond VM, Everett JN, Furtado LV, et al.: Adrenocortical carcinoma is a lynch syndrome-associated cancer. J Clin Oncol 31 (24): 3012-8, 2013.[PUBMED Abstract]
- Raymond VM, Mukherjee B, Wang F, et al.: Elevated risk of prostate cancer among men with Lynch syndrome. J Clin Oncol 31 (14): 1713-8, 2013.[PUBMED Abstract]
- Suspiro A, Fidalgo P, Cravo M, et al.: The Muir-Torre syndrome: a rare variant of hereditary nonpolyposis colorectal cancer associated with hMSH2 mutation. Am J Gastroenterol 93 (9): 1572-4, 1998.[PUBMED Abstract]
- Kerber RA, Slattery ML: Comparison of self-reported and database-linked family history of cancer data in a case-control study. Am J Epidemiol 146 (3): 244-8, 1997.[PUBMED Abstract]
- Parent ME, Ghadirian P, Lacroix A, et al.: The reliability of recollections of family history: implications for the medical provider. J Cancer Educ 12 (2): 114-20, 1997 Summer.[PUBMED Abstract]
- Ready K, Litton JK, Arun BK: Clinical application of breast cancer risk assessment models. Future Oncol 6 (3): 355-65, 2010.[PUBMED Abstract]
- Amir E, Freedman OC, Seruga B, et al.: Assessing women at high risk of breast cancer: a review of risk assessment models. J Natl Cancer Inst 102 (10): 680-91, 2010.[PUBMED Abstract]
- Rosner BA, Colditz GA, Webb PM, et al.: Mathematical models of ovarian cancer incidence. Epidemiology 16 (4): 508-15, 2005.[PUBMED Abstract]
- Pfeiffer RM, Park Y, Kreimer AR, et al.: Risk prediction for breast, endometrial, and ovarian cancer in white women aged 50 y or older: derivation and validation from population-based cohort studies. PLoS Med 10 (7): e1001492, 2013.[PUBMED Abstract]
- Gail MH, Mai PL: Comparing breast cancer risk assessment models. J Natl Cancer Inst 102 (10): 665-8, 2010.[PUBMED Abstract]
- Quante AS, Whittemore AS, Shriver T, et al.: Breast cancer risk assessment across the risk continuum: genetic and nongenetic risk factors contributing to differential model performance. Breast Cancer Res 14 (6): R144, 2012.[PUBMED Abstract]
- Gail MH, Brinton LA, Byar DP, et al.: Projecting individualized probabilities of developing breast cancer for white females who are being examined annually. J Natl Cancer Inst 81 (24): 1879-86, 1989.[PUBMED Abstract]
- Colditz GA, Rosner B: Cumulative risk of breast cancer to age 70 years according to risk factor status: data from the Nurses' Health Study. Am J Epidemiol 152 (10): 950-64, 2000.[PUBMED Abstract]
- Claus EB, Risch N, Thompson WD: Autosomal dominant inheritance of early-onset breast cancer. Implications for risk prediction. Cancer 73 (3): 643-51, 1994.[PUBMED Abstract]
- Tyrer J, Duffy SW, Cuzick J: A breast cancer prediction model incorporating familial and personal risk factors. Stat Med 23 (7): 1111-30, 2004.[PUBMED Abstract]
- Parmigiani G, Berry D, Aguilar O: Determining carrier probabilities for breast cancer-susceptibility genes BRCA1 and BRCA2. Am J Hum Genet 62 (1): 145-58, 1998.[PUBMED Abstract]
- Antoniou AC, Pharoah PD, McMullan G, et al.: A comprehensive model for familial breast cancer incorporating BRCA1, BRCA2 and other genes. Br J Cancer 86 (1): 76-83, 2002.[PUBMED Abstract]
- Antoniou AC, Pharoah PP, Smith P, et al.: The BOADICEA model of genetic susceptibility to breast and ovarian cancer. Br J Cancer 91 (8): 1580-90, 2004.[PUBMED Abstract]
- Antoniou AC, Cunningham AP, Peto J, et al.: The BOADICEA model of genetic susceptibility to breast and ovarian cancers: updates and extensions. Br J Cancer 98 (8): 1457-66, 2008.[PUBMED Abstract]
- Anothaisintawee T, Teerawattananon Y, Wiratkapun C, et al.: Risk prediction models of breast cancer: a systematic review of model performances. Breast Cancer Res Treat 133 (1): 1-10, 2012.[PUBMED Abstract]
- Amir E, Evans DG, Shenton A, et al.: Evaluation of breast cancer risk assessment packages in the family history evaluation and screening programme. J Med Genet 40 (11): 807-14, 2003.[PUBMED Abstract]
- Laitman Y, Simeonov M, Keinan-Boker L, et al.: Breast cancer risk prediction accuracy in Jewish Israeli high-risk women using the BOADICEA and IBIS risk models. Genet Res (Camb) 95 (6): 174-7, 2013.[PUBMED Abstract]
- MacInnis RJ, Bickerstaffe A, Apicella C, et al.: Prospective validation of the breast cancer risk prediction model BOADICEA and a batch-mode version BOADICEACentre. Br J Cancer 109 (5): 1296-301, 2013.[PUBMED Abstract]
- Terry MB, Liao Y, Whittemore AS, et al.: 10-year performance of four models of breast cancer risk: a validation study. Lancet Oncol 20 (4): 504-517, 2019.[PUBMED Abstract]
- Claus EB, Risch N, Thompson WD: The calculation of breast cancer risk for women with a first degree family history of ovarian cancer. Breast Cancer Res Treat 28 (2): 115-20, 1993.[PUBMED Abstract]
- Bondy ML, Lustbader ED, Halabi S, et al.: Validation of a breast cancer risk assessment model in women with a positive family history. J Natl Cancer Inst 86 (8): 620-5, 1994.[PUBMED Abstract]
- Spiegelman D, Colditz GA, Hunter D, et al.: Validation of the Gail et al. model for predicting individual breast cancer risk. J Natl Cancer Inst 86 (8): 600-7, 1994.[PUBMED Abstract]
- Rockhill B, Spiegelman D, Byrne C, et al.: Validation of the Gail et al. model of breast cancer risk prediction and implications for chemoprevention. J Natl Cancer Inst 93 (5): 358-66, 2001.[PUBMED Abstract]
- Costantino JP, Gail MH, Pee D, et al.: Validation studies for models projecting the risk of invasive and total breast cancer incidence. J Natl Cancer Inst 91 (18): 1541-8, 1999.[PUBMED Abstract]
- Bondy ML, Newman LA: Breast cancer risk assessment models: applicability to African-American women. Cancer 97 (1 Suppl): 230-5, 2003.[PUBMED Abstract]
- Schonfeld SJ, Pee D, Greenlee RT, et al.: Effect of changing breast cancer incidence rates on the calibration of the Gail model. J Clin Oncol 28 (14): 2411-7, 2010.[PUBMED Abstract]
- Gail MH, Costantino JP, Pee D, et al.: Projecting individualized absolute invasive breast cancer risk in African American women. J Natl Cancer Inst 99 (23): 1782-92, 2007.[PUBMED Abstract]
- Gail MH: Discriminatory accuracy from single-nucleotide polymorphisms in models to predict breast cancer risk. J Natl Cancer Inst 100 (14): 1037-41, 2008.[PUBMED Abstract]
- Gail MH: Value of adding single-nucleotide polymorphism genotypes to a breast cancer risk model. J Natl Cancer Inst 101 (13): 959-63, 2009.[PUBMED Abstract]
- Barlow WE, White E, Ballard-Barbash R, et al.: Prospective breast cancer risk prediction model for women undergoing screening mammography. J Natl Cancer Inst 98 (17): 1204-14, 2006.[PUBMED Abstract]
- Tice JA, Cummings SR, Ziv E, et al.: Mammographic breast density and the Gail model for breast cancer risk prediction in a screening population. Breast Cancer Res Treat 94 (2): 115-22, 2005.[PUBMED Abstract]
- Lee AJ, Cunningham AP, Tischkowitz M, et al.: Incorporating truncating variants in PALB2, CHEK2, and ATM into the BOADICEA breast cancer risk model. Genet Med 18 (12): 1190-1198, 2016.[PUBMED Abstract]
- MacInnis RJ, Liao Y, Knight JA, et al.: Considerations When Using Breast Cancer Risk Models for Women with Negative BRCA1/BRCA2 Mutation Results. J Natl Cancer Inst 112 (4): 418-422, 2020.[PUBMED Abstract]
- Barnetson RA, Tenesa A, Farrington SM, et al.: Identification and survival of carriers of mutations in DNA mismatch-repair genes in colon cancer. N Engl J Med 354 (26): 2751-63, 2006.[PUBMED Abstract]
- Kastrinos F, Uno H, Ukaegbu C, et al.: Development and Validation of the PREMM5 Model for Comprehensive Risk Assessment of Lynch Syndrome. J Clin Oncol 35 (19): 2165-2172, 2017.[PUBMED Abstract]
- Chen S, Wang W, Lee S, et al.: Prediction of germline mutations and cancer risk in the Lynch syndrome. JAMA 296 (12): 1479-87, 2006.[PUBMED Abstract]
- Khan O, Blanco A, Conrad P, et al.: Performance of Lynch syndrome predictive models in a multi-center US referral population. Am J Gastroenterol 106 (10): 1822-7; quiz 1828, 2011.[PUBMED Abstract]
- Mercado RC, Hampel H, Kastrinos F, et al.: Performance of PREMM(1,2,6), MMRpredict, and MMRpro in detecting Lynch syndrome among endometrial cancer cases. Genet Med 14 (7): 670-80, 2012.[PUBMED Abstract]
- Robson ME, Storm CD, Weitzel J, et al.: American Society of Clinical Oncology policy statement update: genetic and genomic testing for cancer susceptibility. J Clin Oncol 28 (5): 893-901, 2010.[PUBMED Abstract]
- National Comprehensive Cancer Network: NCCN Clinical Practice Guidelines in Oncology: Genetic/Familial High-Risk Assessment: Breast, Ovarian, and Pancreatic. Version 1.2020. Plymouth Meeting, Pa: National Comprehensive Cancer Network, 2019. Available online with free registration. Last accessed December 23, 2019.[PUBMED Abstract]
- Statement of the American Society of Human Genetics on genetic testing for breast and ovarian cancer predisposition. Am J Hum Genet 55 (5): i-iv, 1994.[PUBMED Abstract]
- Hampel H, Bennett RL, Buchanan A, et al.: A practice guideline from the American College of Medical Genetics and Genomics and the National Society of Genetic Counselors: referral indications for cancer predisposition assessment. Genet Med 17 (1): 70-87, 2015.[PUBMED Abstract]
- Owens DK, Davidson KW, Krist AH, et al.: Risk Assessment, Genetic Counseling, and Genetic Testing for BRCA-Related Cancer: US Preventive Services Task Force Recommendation Statement. JAMA 322 (7): 652-665, 2019.[PUBMED Abstract]
- Lancaster JM, Powell CB, Kauff ND, et al.: Society of Gynecologic Oncologists Education Committee statement on risk assessment for inherited gynecologic cancer predispositions. Gynecol Oncol 107 (2): 159-62, 2007.[PUBMED Abstract]
- Manahan ER, Kuerer HM, Sebastian M, et al.: Consensus Guidelines on Genetic` Testing for Hereditary Breast Cancer from the American Society of Breast Surgeons. Ann Surg Oncol 26 (10): 3025-3031, 2019.[PUBMED Abstract]
- Beitsch PD, Whitworth PW, Hughes K, et al.: Underdiagnosis of Hereditary Breast Cancer: Are Genetic Testing Guidelines a Tool or an Obstacle? J Clin Oncol 37 (6): 453-460, 2019.[PUBMED Abstract]
- Cropper C, Woodson A, Arun B, et al.: Evaluating the NCCN Clinical Criteria for Recommending BRCA1 and BRCA2 Genetic Testing in Patients With Breast Cancer. J Natl Compr Canc Netw 15 (6): 797-803, 2017.[PUBMED Abstract]
- Grindedal EM, Heramb C, Karsrud I, et al.: Current guidelines for BRCA testing of breast cancer patients are insufficient to detect all mutation carriers. BMC Cancer 17 (1): 438, 2017.[PUBMED Abstract]
- Couch FJ, Nathanson KL, Offit K: Two decades after BRCA: setting paradigms in personalized cancer care and prevention. Science 343 (6178): 1466-70, 2014.[PUBMED Abstract]
- Theobald KA, Susswein LR, Marshall ML, et al.: Utility of Expedited Hereditary Cancer Testing in the Surgical Management of Patients with a New Breast Cancer Diagnosis. Ann Surg Oncol 25 (12): 3556-3562, 2018.[PUBMED Abstract]
- Gornick MC, Kurian AW, An LC, et al.: Knowledge regarding and patterns of genetic testing in patients newly diagnosed with breast cancer participating in the iCanDecide trial. Cancer 124 (20): 4000-4009, 2018.[PUBMED Abstract]
- Chiba A, Hoskin TL, Hallberg EJ, et al.: Impact that Timing of Genetic Mutation Diagnosis has on Surgical Decision Making and Outcome for BRCA1/BRCA2 Mutation Carriers with Breast Cancer. Ann Surg Oncol 23 (10): 3232-8, 2016.[PUBMED Abstract]
- Obermair A, Youlden DR, Baade PD, et al.: The impact of risk-reducing hysterectomy and bilateral salpingo-oophorectomy on survival in patients with a history of breast cancer--a population-based data linkage study. Int J Cancer 134 (9): 2211-22, 2014.[PUBMED Abstract]
- Byrski T, Dent R, Blecharz P, et al.: Results of a phase II open-label, non-randomized trial of cisplatin chemotherapy in patients with BRCA1-positive metastatic breast cancer. Breast Cancer Res 14 (4): R110, 2012.[PUBMED Abstract]
- Robson M, Im SA, Senkus E, et al.: Olaparib for Metastatic Breast Cancer in Patients with a Germline BRCA Mutation. N Engl J Med 377 (6): 523-533, 2017.[PUBMED Abstract]
- Heymann S, Delaloge S, Rahal A, et al.: Radio-induced malignancies after breast cancer postoperative radiotherapy in patients with Li-Fraumeni syndrome. Radiat Oncol 5: 104, 2010.[PUBMED Abstract]
- Bougeard G, Renaux-Petel M, Flaman JM, et al.: Revisiting Li-Fraumeni Syndrome From TP53 Mutation Carriers. J Clin Oncol 33 (21): 2345-52, 2015.[PUBMED Abstract]
- Rebbeck TR, Kauff ND, Domchek SM: Meta-analysis of risk reduction estimates associated with risk-reducing salpingo-oophorectomy in BRCA1 or BRCA2 mutation carriers. J Natl Cancer Inst 101 (2): 80-7, 2009.[PUBMED Abstract]
- Kotsopoulos J, Lubinski J, Lynch HT, et al.: Oophorectomy after menopause and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. Cancer Epidemiol Biomarkers Prev 21 (7): 1089-96, 2012.[PUBMED Abstract]
- Cass I, Baldwin RL, Varkey T, et al.: Improved survival in women with BRCA-associated ovarian carcinoma. Cancer 97 (9): 2187-95, 2003.[PUBMED Abstract]
- Tan DS, Rothermundt C, Thomas K, et al.: "BRCAness" syndrome in ovarian cancer: a case-control study describing the clinical features and outcome of patients with epithelial ovarian cancer associated with BRCA1 and BRCA2 mutations. J Clin Oncol 26 (34): 5530-6, 2008.[PUBMED Abstract]
- Practice Bulletin No. 149: Endometrial cancer. Obstet Gynecol 125 (4): 1006-26, 2015.[PUBMED Abstract]
- Ott PA, Bang YJ, Berton-Rigaud D, et al.: Safety and Antitumor Activity of Pembrolizumab in Advanced Programmed Death Ligand 1-Positive Endometrial Cancer: Results From the KEYNOTE-028 Study. J Clin Oncol 35 (22): 2535-2541, 2017.[PUBMED Abstract]
- Walsh T, Casadei S, Lee MK, et al.: Mutations in 12 genes for inherited ovarian, fallopian tube, and peritoneal carcinoma identified by massively parallel sequencing. Proc Natl Acad Sci U S A 108 (44): 18032-7, 2011.[PUBMED Abstract]
- Frey MK, Kim SH, Bassett RY, et al.: Rescreening for genetic mutations using multi-gene panel testing in patients who previously underwent non-informative genetic screening. Gynecol Oncol 139 (2): 211-5, 2015.[PUBMED Abstract]
- Desmond A, Kurian AW, Gabree M, et al.: Clinical Actionability of Multigene Panel Testing for Hereditary Breast and Ovarian Cancer Risk Assessment. JAMA Oncol 1 (7): 943-51, 2015.[PUBMED Abstract]
- Couch FJ, Shimelis H, Hu C, et al.: Associations Between Cancer Predisposition Testing Panel Genes and Breast Cancer. JAMA Oncol 3 (9): 1190-1196, 2017.[PUBMED Abstract]
- Weitzel JN, Neuhausen SL, Adamson A, et al.: Pathogenic and likely pathogenic variants in PALB2, CHEK2, and other known breast cancer susceptibility genes among 1054 BRCA-negative Hispanics with breast cancer. Cancer 125 (16): 2829-2836, 2019.[PUBMED Abstract]
- Frey MK, Kopparam RV, Ni Zhou Z, et al.: Prevalence of nonfounder BRCA1/2 mutations in Ashkenazi Jewish patients presenting for genetic testing at a hereditary breast and ovarian cancer center. Cancer 125 (5): 690-697, 2019.[PUBMED Abstract]
- Eoh KJ, Kim JE, Park HS, et al.: Detection of Germline Mutations in Patients with Epithelial Ovarian Cancer Using Multi-gene Panels: Beyond BRCA1/2. Cancer Res Treat 50 (3): 917-925, 2018.[PUBMED Abstract]
- Tung N, Lin NU, Kidd J, et al.: Frequency of Germline Mutations in 25 Cancer Susceptibility Genes in a Sequential Series of Patients With Breast Cancer. J Clin Oncol 34 (13): 1460-8, 2016.[PUBMED Abstract]
- Buys SS, Sandbach JF, Gammon A, et al.: A study of over 35,000 women with breast cancer tested with a 25-gene panel of hereditary cancer genes. Cancer 123 (10): 1721-1730, 2017.[PUBMED Abstract]
- Pritzlaff M, Summerour P, McFarland R, et al.: Male breast cancer in a multi-gene panel testing cohort: insights and unexpected results. Breast Cancer Res Treat 161 (3): 575-586, 2017.[PUBMED Abstract]
- Yadav S, Reeves A, Campian S, et al.: Outcomes of retesting BRCA negative patients using multigene panels. Fam Cancer 16 (3): 319-328, 2017.[PUBMED Abstract]
- Crawford B, Adams SB, Sittler T, et al.: Multi-gene panel testing for hereditary cancer predisposition in unsolved high-risk breast and ovarian cancer patients. Breast Cancer Res Treat 163 (2): 383-390, 2017.[PUBMED Abstract]
- Kurian AW, Ward KC, Howlader N, et al.: Genetic Testing and Results in a Population-Based Cohort of Breast Cancer Patients and Ovarian Cancer Patients. J Clin Oncol 37 (15): 1305-1315, 2019.[PUBMED Abstract]
- Shimelis H, LaDuca H, Hu C, et al.: Triple-Negative Breast Cancer Risk Genes Identified by Multigene Hereditary Cancer Panel Testing. J Natl Cancer Inst 110 (8): 855-862, 2018.[PUBMED Abstract]
- Southey MC, Goldgar DE, Winqvist R, et al.: PALB2, CHEK2 and ATM rare variants and cancer risk: data from COGS. J Med Genet 53 (12): 800-811, 2016.[PUBMED Abstract]
- 遺伝性乳がんおよび/または婦人科がんに対する遺伝的感受性の浸透度
-
病原性多様体を有する人にある疾患が発症する割合を浸透度と呼ぶ。一般に、がん感受性に関連する遺伝子多様体で高頻度のものは、まれな遺伝子多様体より浸透度が低い。図4は、このことを示している。成人発症型疾患では、浸透度は通常、個々のキャリアの年齢、性別、および臓器の部位で記述される。例えば、女性のBRCA1病原性多様体キャリアにおける乳がんの浸透度はしばしば、50歳までおよび70歳までで示される。浸透度を推定する方法は多くあるが、バイアスの可能性のないものはなく、個々のキャリアのがんリスクの測定にはある程度の不確かさが存在する。
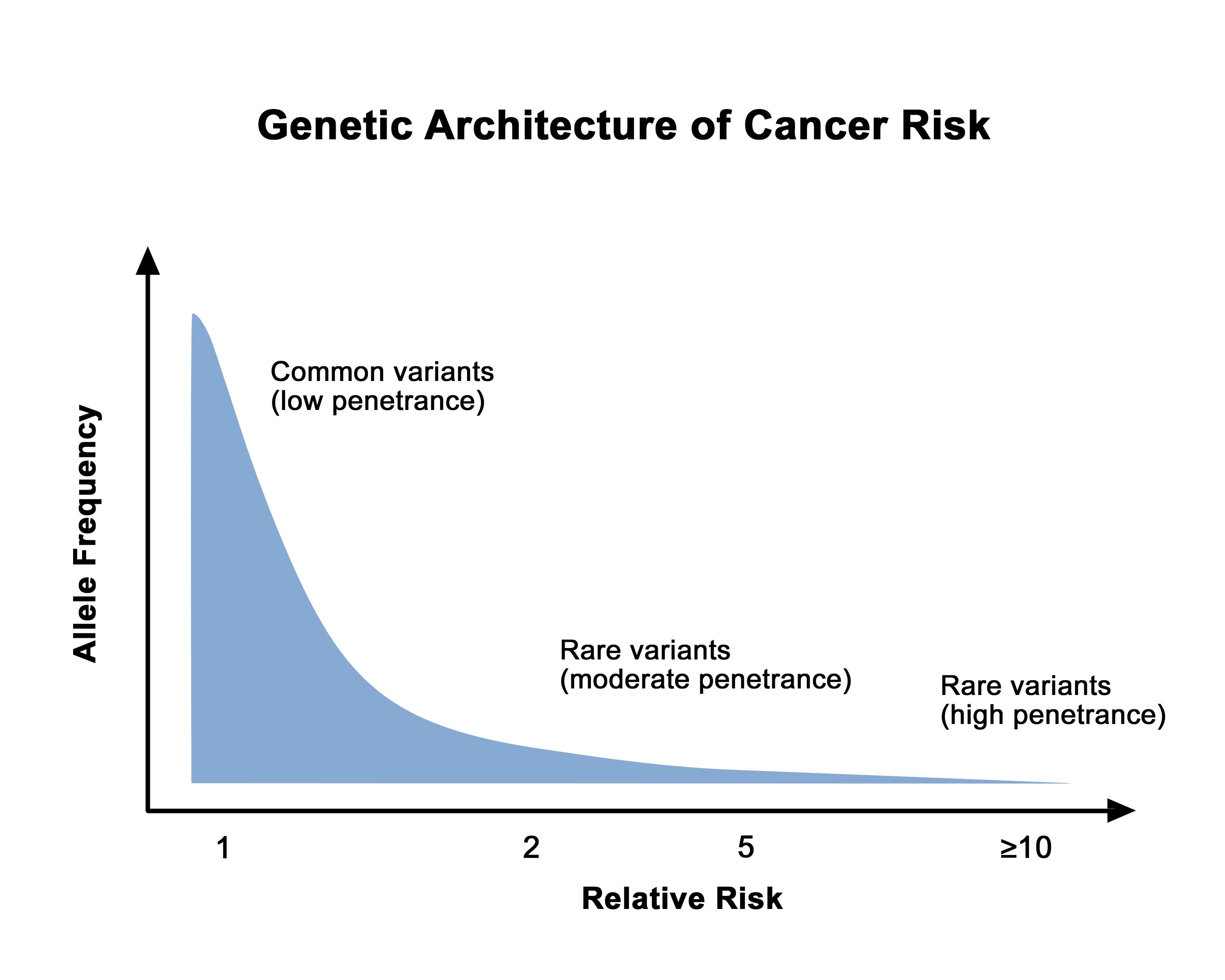
図4.がんリスクの遺伝子構成。このグラフでは、低い相対リスクはゲノムワイド関連解析で同定された一塩基多型などの高頻度で低浸透度の遺伝子多様体に関連し、高い相対リスクは遺伝性乳がんや卵巣がんに関連するBRCA1/BRCA2遺伝子やリンチ症候群に関連するミスマッチ修復遺伝子の病原性多様体などのまれな高浸透度の遺伝子多様体に関連しているという全般的な知見が示されている。 本要約全体を通して、相対リスクおよび絶対リスクについて報告している研究が考察されている。これらは重要であるが異なる2つの概念である。相対リスク(RR)とは、別のグループに対する相対的なリスクの推定値を示す(例、ある危険因子に曝されていない女性における乳がんなどのアウトカムのリスクに対する、同じ危険因子に曝された女性における乳がんリスク)。1を超えるRRの測定値は、分子に入れられた人(すなわち、曝されている人)のリスクが分母に入れられた人(すなわち、曝されていない人)のリスクよりも高いことを意味する。1未満のRRの測定値は、分子に入れられた人(すなわち、曝されている人)のリスクが分母に入れられた人(すなわち、曝されていない人)のリスクよりも低いことを意味する。同様の相対的な解釈を伴う測定値には、オッズ比(OR)、ハザード比、およびリスク比がある。
絶対リスクの測定値には、特定のアウトカムを有する人の数、集団においてそのアウトカムを有する可能性のある人の数、および人-時間(ある人がそのアウトカムを有するリスクのある期間)が考慮され、集団内でのアウトカムの絶対負荷を反映している。絶対的な測定値にはリスクおよび割合があり、特定の時間の枠組み(例、1年、5年)または全生涯で表現される。累積リスクは、ある一定の期間に発生するリスクの測定値である。例えば、全生涯リスクは所定の平均余命(例、80または90歳)に基づいて通常計算される累積リスクの一種である。累積リスクはまた他の時間の枠組み(例、50歳まで)で表される場合がある。
疾患のアウトカムがかなりまれな可能性があるため、相対リスクの測定値が大きいからといって集団レベルで個人の実際の数に大きな影響があることにはならない。例えば、喫煙に対する相対リスクは心疾患よりも肺がんではるかに高いが、喫煙者と非喫煙者間の絶対差は比較的まれなアウトカムの肺がんよりも一般的なアウトカムである心疾患の方が大きくなる。
したがって、曝露および生物学的マーカーが連続した期間において疾患の予防に及ぼす影響を評価する場合、所定の危険因子の全体的な影響を比較検討する際に相対的影響と絶対的影響間の差を認識することが重要である。例えば、乳がんの多くの危険因子に対する影響の大きさは30%(例、ORまたはRRが1.3)程度であるが、これはある危険因子(例、飲酒、初産年齢が高齢、経口避妊薬の使用、閉経後の身体のサイズ)を有する女性では、その危険因子を有していない場合と比較して、乳がんが相対的に30%増加することを意味している。ただし、リスクの絶対的増加は疾患の基礎にある絶対リスクに基づいている。図5および表2は、1.3程度の相対危険因子が絶対リスクに及ぼす影響を示している。(これらの家系図で用いられる標準的なシンボルの定義については、がんの遺伝学的リスク評価とカウンセリングに関するPDQ要約の標準的な家系図命名法の図を参照のこと。)示されているように、乳がんの家族歴を有する女性は、危険因子の低減により絶対スケールではるかに高い便益を得る。[ 1 ]
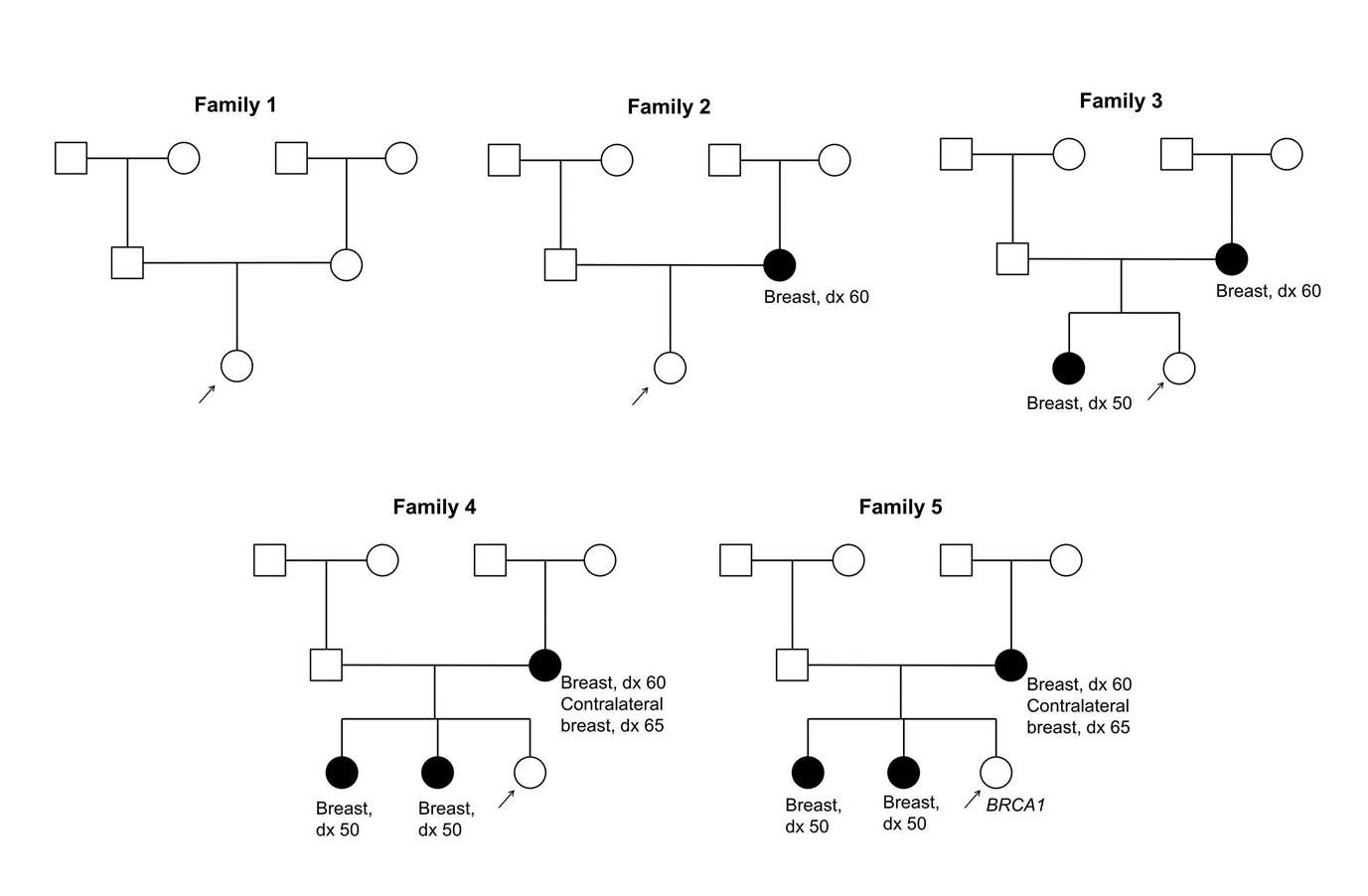
図5.これら5つの家系では家族歴の程度が異なる発端者が描かれている。表2がこの図に添えられている。 表2.乳がん家族歴が異なる女性における相対リスク1.3の危険因子を変更した場合の効果a 家族歴 生涯リスク(%) 危険因子修正後の生涯リスク(%) 絶対リスク差(%) 相対リスク aこの表に添えられている図5を参照のこと。 低い(家系1) 10.9 8.4 2.50 1.29(29%のリスク増加) 中等度(家系2) 21.6 16.8 4.80 1.28(28%のリスク増加) 中等度/高い(家系3) 27.1 21.3 5.80 1.27(27%のリスク増加) 高い(家系4) 32.0 25.3 6.70 1.26(26%のリスク増加) BRCA1病原性多様体(家系5) 53.7 44.2 9.50 1.21(21%のリスク増加) 多重遺伝子パネル検査の使用が増加するにつれ、新たな遺伝子に病原性多様体が発見された個人におけるがんリスクを管理するために、年齢別の、生涯の、および絶対的ながんリスクに関するデータを組み込んだ枠組みが記述されている。[ 2 ]この枠組みでは、これらの個人におけるスクリーニング開始年齢を、この集団のがんの5年リスクが、一般集団の女性においてスクリーニングがルーチンに開始される年齢(米国における乳がんについて約1%)に近づいたときとするように提唱されている。結果として、スクリーニング開始年齢は遺伝子によって異なることになる。(多重遺伝子パネル検査に関する詳しい情報については、本要約の序のセクションの多重遺伝子[パネル]検査のセクションを参照のこと。)
参考文献- Quante AS, Herz J, Whittemore AS, et al.: Assessing absolute changes in breast cancer risk due to modifiable risk factors. Breast Cancer Res Treat 152 (1): 193-7, 2015.[PUBMED Abstract]
- Tung N, Domchek SM, Stadler Z, et al.: Counselling framework for moderate-penetrance cancer-susceptibility mutations. Nat Rev Clin Oncol 13 (9): 581-8, 2016.[PUBMED Abstract]
- 乳がんおよび/または婦人科がん感受性に関連する遺伝子
-
いくつかの遺伝子が乳がんおよび/または婦人科がんの発生に関連していることが明らかにされている。これらの遺伝子は、本要約内では高浸透度、中浸透度、および低浸透度に分類されている。高浸透度および中浸透度の遺伝子を表3に要約する。低浸透度の遺伝子および遺伝子座は、主にがん感受性に関連している多型を含む。(詳しい情報については、本要約の高浸透度の乳がんおよび/または婦人科がん感受性遺伝子、乳がんおよび/または婦人科がんに関連する中浸透度の遺伝子、および低浸透度の遺伝子および遺伝子座のセクションを参照のこと。)
表3.乳がんおよび/または婦人科がん感受性に関連する遺伝子 がん感受性 中浸透度の遺伝子 高浸透度の遺伝子 a他のがんが本表内の遺伝子に関連している可能性がある。 b本要約の乳がんおよび/または婦人科がんに関連する中浸透度の遺伝子のセクションで考察されているが、浸透度は不明である他の遺伝子には、CASP8、TGFB1、Abraxas、RECQL、およびSMARCA4がある。 乳がん ATM、BRIP1、CHEK2、FANCD2、RAD51C BRCA1、BRCA2、CDH1、PALB2、PTEN、STK11、TP53 卵巣がん ATM、BRIP1、EPCAM、MLH1、MSH2、MSH6、RAD51C BRCA1、BRCA2 子宮内膜がん EPCAM、MLH1、MSH2、MSH6、PMS2、PTEN - 高浸透度の乳がんおよび/または婦人科がん感受性遺伝子
-
BRCA1とBRCA2
序
疫学研究は、乳がんおよび卵巣がんの重要な危険因子としての家族歴の役割を明確に確立した。性別や年齢に次いで、陽性家族歴は乳がんの最も強力な既知の予測危険因子である。しかしながら、一部の家系において、(母系と父系の両方の家系を通して)常染色体優性と思われる伝達パターンで、ときに他の臓器、特に卵巣および前立腺の腫瘍を含めて若年での発症、両側性、複数世代での乳がんの存在を特徴とする遺伝性乳がんが存在することが長い間認識されている。[ 1 ][ 2 ]現在では、これらの家系の一部にみられるがんは、1つのがん感受性遺伝子における特異的病原性多様体によって説明できることが分かっている。変異が生じた場合には、乳がん/卵巣がんリスクの有意な増大と関連する数種の遺伝子の単離は、リスクのある人の同定を可能にする。このようながん感受性遺伝子は非常に重要であるが、浸透度の高い生殖細胞病原性多様体は乳がん全体の5~10%に過ぎないと推定される。
1988年のある研究で、一部の家系における常染色体優性遺伝特性として乳がんを分離したという初の定量的証拠が報告された。[ 3 ]乳がんの遺伝的感受性に関連する遺伝子の探索は、がん罹患者が多数存在する大規模家系を対象とした研究によって促進され、その結果BRCA1やBRCA2、TP53、PTEN/MMAC1、STK11などのいくつかの感受性遺伝子が同定された。ミスマッチ修復遺伝子であるMLH1、MSH2、MSH6、PMS2など他の遺伝子は卵巣がんリスクの増加と関連しているが、乳がんとの関連は一貫していない。
BRCA1
1990年のことであるが、17番染色体の長腕(interval 17q12-21)に、乳がんの感受性遺伝子が遺伝子連鎖を基にマップされた。[ 4 ]その後すぐに、他の研究によって乳がんと染色体17q上の複数の遺伝子マーカーとの連鎖が確認され、さらに連鎖の認められる家系において、乳がんおよび卵巣がんの両がんの感受性の同時伝達を示す証拠が観察された。[ 5 ]その後ポジショナルクローニング法によってBRCA1遺伝子が同定され、その遺伝子は1,863個のアミノ酸からなる蛋白をコードする24個のエクソンを含むことが明らかにされている。BRCA1における生殖細胞病原性多様体は早期発症型乳がん、卵巣がん、および卵管がんと関連している。(詳しい情報については、本要約のBRCA病原性多様体の浸透度のセクションを参照のこと。)男性の乳がん、膵がん、精巣腫瘍、および早期発症型前立腺がんもまたBRCA1における病原性多様体と関連している[ 6 ][ 7 ][ 8 ][ 9 ];しかしながら、男性の乳がん、膵がん、および前立腺がんはBRCA2における病原性多様体とより強く関連している。
BRCA2
BRCA1と連鎖がなかった乳がんの複数症例を含む15の家系を対象に行った連鎖研究により、第二の乳がん感受性遺伝子であるBRCA2が、13番染色体長腕に存在することが明らかにされた。BRCA2の病原性多様体は多発乳がん家系と関連しており、また、男性の乳がん、卵巣がん、前立腺がん、悪性黒色腫、および膵がんとも関連している。[ 8 ][ 9 ][ 10 ][ 11 ][ 12 ][ 13 ][ 14 ](詳しい情報については、本要約のBRCA病原性多様体の浸透度のセクションを参照のこと。)BRCA2は、3,418個のアミノ酸からなる蛋白をコードする27個のエクソンを有する巨大遺伝子である。[ 15 ]BRCA1とBRCA2は相同遺伝子ではないが、両遺伝子とも通常大きなエクソン11を有し、エクソン2に翻訳開始部位が存在する。BRCA1と同様にBRCA2は、腫瘍抑制遺伝子のように振る舞う。BRCA1とBRCA2の両方の病原性多様体と関連する腫瘍では、しばしば野生型アレルが欠失している。
乳がんの症例のみが多数存在する家系の45%および乳がんと卵巣がんの両方が存在する家系の最高90%においては、BRCA1およびBRCA2の病原性多様体が疾患の原因とみられる。[ 16 ]
BRCA1とBRCA2の機能
ほとんどのBRCA1およびBRCA2病原性多様体は、切断されているが故に蛋白の機能を失った蛋白産物を産生すると予測されているが、切断を伴わずに機能喪失を起こすミスセンス病原性多様体もある。遺伝性乳がん/卵巣がんは常染色体優性の病態であるため、17番または13番染色体の片方のコピー上にBRCA1またはBRCA2病原性多様体が存在する個人であっても、対の染色体の他方には正常アレルが保有されている。病原性多様体のキャリアで研究されてきたほとんどの乳がんおよび卵巣がんでは、正常アレルの欠失が認められ、その結果すべての機能が失われていたことから、BRCA1およびBRCA2は腫瘍抑制遺伝子として分類されることになった。BRCA1およびBRCA2は、腫瘍抑制遺伝子としての役割に加えて、またその一部として、相同DNA修復、ゲノム安定性、転写調節、蛋白ユビキチン化、クロマチン再構築、および細胞周期制御といった細胞内での無数の機能に関与している。[ 17 ][ 18 ]
BRCA1とBRCA2の病原性多様体
BRCA1およびBRCA2における配列の変化ならびに約2,000の異なる多様体が既に記述されている。[ 19 ]一般集団では、400~800人中約1人がBRCA1またはBRCA2に生殖細胞病原性多様体を保有しうる。[ 20 ][ 21 ]がんリスク増大に関連する多様体によって、蛋白の欠如や、機能しない蛋白が生じることは、BRCA1およびBRCA2が腫瘍抑制遺伝子であるという仮説を裏付ける。このような病原性多様体のうちの少数は非血縁家系で繰り返し認められるのに対し、ほとんどの病原性多様体は少数の家系でしか報告されていない。
多様体スクリーニング法は、それぞれ感度が異なる。一本鎖DNA高次構造多型解析やコンフォメーション高感度ゲル電気泳動などの研究施設で広く用いられている方法では、DNA塩基配列決定法により検出される多様体のほぼ1/3が見逃される。[ 22 ]さらに、DNAの直接塩基配列決定法を含むほとんどの技法では、転座、逆位、大規模な欠失または挿入など、広範なゲノムの変化は見逃されるが、これらについての検査は市販されている。BRCA1の不活性化多様体の12~18%は、このような再構成が原因であると考えられるが、BRCA2およびアシュケナージユダヤ人(AJ)の子孫では頻度がより低い。[ 23 ][ 24 ][ 25 ][ 26 ][ 27 ][ 28 ][ 29 ]さらに、諸研究でこれらの再構成がヒスパニック系およびカリブ人集団ではより頻繁に見られることが示唆されている。[ 27 ][ 29 ][ 30 ]
意義不明の多様体
BRCA1/BRCA2遺伝子における生殖細胞病原性多様体は、約60%の乳がん生涯リスクおよび15~40%の卵巣がん生涯リスクと関連する。BRCA1やBRCA2では確実な機能検査の方法は存在しない;したがって、機能的影響が有害であるか良性であるかを予測するためにヌクレオチド変化を分類する場合には、不完全なデータを基にしなければならない。病原性多様体として認められている大多数は、蛋白の切断および/または重要な機能ドメインの欠失を引き起こすものである。しかしながら、BRCA1およびBRCA2の全塩基配列の遺伝子検査を受けた全個人の10~15%では、明らかな病原性多様体は検出されず、意義不明の多様体(variant of uncertain significance[VUS])のみが検出される。VUSが検出されると、カウンセリングで問題が生じることがあり、特にがんリスクの推定やリスク管理という面では大きな問題となってくる。こうした患者の臨床管理は、高度に個別化される必要があり、そのVUSが良性であるか有害であるかの特徴付けに役立つ情報源に加えて、患者および家族のがん病歴などの因子を考慮に入れなければならない。そのため、改善された分類および報告システムは臨床的に有用な可能性がある。[ 31 ]
Myriad Genetic Laboratories, Inc.により実施された連続する7,461件の全遺伝子配列解析の包括的分析により、3年間にわたるVUSの頻度が示された。[ 32 ]明らかな病原性多様体が検出されなかった被験者のうち、13%で「臨床的意義が不確定のミスセンス突然変異およびイントロン領域に発見される突然変異、BRCA1およびBRCA2のそれぞれ1,853番目および3,308番目のアミノ酸で蛋白を切断するペプチド鎖終結変異、ならびにこれらの蛋白の正常な終止コドンが除去される突然変異」と定義されたVUSが検出された。塩基配列多様体のVUSへの分類は時間の経過とともに変化していく場合がある。明らかな病原性多様体が検出されなかった被験者のうち別の6.8%は、当初VUSと考えられていたが、多型またはときに病原性多様体として再分類された塩基配列変異を有していた。
米国の集団内では、VUSの頻度は民族性により異なる。アフリカ系米国人のVUS発生率が最も高いようである。[ 33 ]Myriad社からのデータの2009年の研究において、アフリカ系の個人は、全民族で最も高い割合である16.5%がVUSを有した。アジア系、中東系、ヒスパニック系の各集団におけるVUSの頻度は10~14%であったが、この数値は限られた規模の標本に基づいている。時間の経過とともに、VUSに分類される変化の割合はすべての民族で減少しているが、これは主として多様体分類アルゴリズムが向上しているためである。[ 34 ]追加の情報が選別および解釈されるにつれて、VUSの再分類が行われている。[ 35 ][ 36 ]このような情報は、罹患者に現在行われているケアに影響しうる。
中立的なVUSから有害なものを弁別するための方法が数多く用意されており、統合された方法(下述参照)[ 41 ]を含めて新たな方法の開発も進行している。[ 37 ][ 38 ][ 39 ][ 40 ]VUSの解釈は、家系内のがんとこうしたVUSが共分離していないかどうかを明らかにするために、家系内に認められるこのようなVUSを追跡するためのあらゆる努力によって大いに助けられている。一般的に、病原性多様体を有する個人で観察されたVUSは、そのVUSが別の病原性多様体とともに同定された場合は特に、それ自体は有害である可能性は低いが、まれに例外がみられる。臨床情報の補助として、VUSを解釈するためのモデルが、塩基配列の保存、アミノ酸変化の生化学的性質[ 37 ][ 42 ][ 43 ][ 44 ][ 45 ][ 46 ]、BRCA1およびBRCA2関連腫瘍の病理学的特徴に関する情報(例、BRCA1関連乳がんは通常エストロゲン受容体[ER]陰性である)の組み入れ[ 47 ]、および特定の塩基配列変異がBRCA1またはBRCA2蛋白の活性に及ぼす影響を調べる機能検査[ 48 ][ 49 ]に基づいて開発されている。VUSを解釈しようとする場合には、利用可能な情報のすべてを検討するべきである。
BRCA1またはBRCA2病原性多様体を有する可能性の集団推定値
家族歴を問わないさまざまながん罹患歴を有する女性および男性の標本集団において、BRCA病原性多様体キャリアであると判明した個人の割合に関する統計が以下に提供されている。これらのデータは、がん遺伝カウンセリングへの紹介および遺伝子検査の検討により最も恩恵が得られる可能性がある人を判別するのに役立つが、個々のリスク評価に置き換えることはできず、別の個人歴および家族歴の特徴に基づけば、これにより病原性多様体の可能性が高いか低いか分かる可能性がある。
同じ病原性多様体が、見る限り関係のない複数の家系において見出される場合がある。この観察は創始者効果と一致しており、現在のある集団において同定された病原性多様体が、地理的、文化的、または他の要因により隔離された1つの小規模な創始者グループに追跡できる。特に顕著なものとして、2つの特定のBRCA1病原性多様体(185delAGおよび5382insC)および1つのBRCA2病原性多様体(6174delT)が、AJに共通していると報告されている。しかしながら、アフリカ系米国人およびヒスパニック系では他の創始者病原性多様体が同定されている。[ 30 ][ 50 ][ 51 ]これらの創始者病原性多様体の存在は、遺伝子検査にとって実際的な意味がある。多くの施設では、民族特異的なアレルに対して特異的な指示検査を実施している。これにより、検査の技術的な面は大きく簡素化しているが、制限がないわけではない。AJ集団における非創始者のBRCA病原性多様体は、3~15%と報告されている。[ 32 ][ 52 ][ 53 ]
一般集団において何らかのBRCA病原性多様体がみられる可能性は以下の通りである:
AJの個人おいて何らかのBRCA病原性多様体がみられる可能性は以下の通りである:
65歳未満の乳がん患者を対象にした米国の集団ベースの大規模研究2件では、さまざまな民族におけるBRCA1[ 57 ][ 73 ]およびBRCA2[ 57 ]病原性多様体の保有率が調査された。乳がん患者における民族ごとのBRCA1病原性多様体の保有率は、ヒスパニック系で3.5%、アフリカ系米国人で1.3~1.4%、アジア系米国人で0.5%、非アシュケナージユダヤ系白人で2.2~2.9%、およびアシュケナージユダヤ人で8.3~10.2%であった。[ 57 ][ 73 ]民族ごとのBRCA2病原性多様体の保有率は、アフリカ系米国人で2.6%および白人で2.1%であった。[ 57 ]
乳がんおよび/または卵巣がんの個人歴または家族歴を有し、米国南西部の複数のクリニックを通じて登録されたヒスパニック系の患者を対象にした研究で、BRCA1およびBRCA2病原性多様体の保有率が調査された。BRCA病原性多様体が患者746人中189人(25%)に同定された(BRCA1が124人、BRCA2が65人)[ 74 ];同定された189のBRCA病原性多様体のうち21の多様体(11%)が大規模な遺伝子再構成で、そのうち13の多様体(62%)がBRCA1 exon 9-12の欠失であった。メキシコ系の乳がん女性810人の非選択的コホートが検査された;4.3%がBRCA病原性多様体を有した。同定された35の病原性多様体のうち8つの多様体もまた、BRCA1 exon 9-12の欠失であった。[ 75 ]ヒスパニック系の乳がん女性492人を対象にした別の集団ベースのコホートでは、BRCA1 exon 9-12の欠失が3人の患者で明らかにされたことから、この多様体はメキシコ人の創始者病原性多様体の可能性があり、米国の同様のクリニックおよび集団ベースのコホートにおけるBRCA1の全病原性多様体のうち、10~12%を占めると示唆されている。クリニックベースのコホート内で、9つの反復性病原性多様体がみられ、このコホートで観察された全多様体の53%を占めたことから、この集団における追加の創始者病原性多様体の存在が示唆されている。
AJの原発卵管がん患者29人に関するレトロスペクティブ・レビューでは、17%に生殖細胞系BRCA病原性多様体が特定された。[ 72 ]卵管がん女性108人を対象にした別の研究では、ユダヤ人女性の55.6%および非ユダヤ人女性の26.4%(全体で30.6%)に病原性多様体が同定された。[ 76 ]BRCA病原性多様体キャリアにおける卵管がんの発生頻度の推定は、高悪性度で転移性の漿液性がん腫の原発部位を初発時に決定する精度の不足により制限される。[ 6 ][ 72 ][ 76 ][ 77 ]
集団スクリーニング
集団スクリーニングでは、家族ベース検査の基準に適合しなかったであろうAJ集団の多くでキャリアが同定されている。[ 64 ][ 78 ][ 79 ][ 80 ]これにより、予防戦略から利益が得られると考えられる個人の数が拡大する可能性がある。1件の研究により、(個人歴/家族歴ベースの検査と比較した)AJ創始者多様体に対する集団スクリーニングは、米国および英国のデータに基づいて費用効果的であることが示唆されている。[ 81 ]著者らは、費用対効果を評価するため生涯コストと遺伝子検査の効果を推定する意思決定解析モデルを用いた;このモデルには、検査前の遺伝カウンセリングと遺伝子検査の費用と心血管系転帰の予想されるリスクが含められた。同じグループにより実施された追加の解析で、検査をBRCA1、BRCA2、RAD51C、RAD51D、およびPALB2におけるすべての病原性多様体を含めるように拡張された場合でも費用対効果が示唆された。[ 82 ]これらの研究はさまざまな想定に基づいており、その一部には不正確なものがある(例、一部の遺伝子に対する集団の保有率の推定値)。さらに、著者らが認めているように、病原性多様体を有することが確認された患者がこの情報から利益を得るようにするため、このような取り組みには一連のケアを通して臨床でのサポートが必要である。したがって、集団スクリーニングの取り組みを検討する際は依然としてかなりの資源が必要であり、進行中の研究の取り組みの焦点となる。検出率は集団における病原性多様体の保有率に強く依存しているため、このアプローチを他の創始者病原性多様体集団を含む他の集団にどのように適用するかは明らかではない。その他の未解決の問題は、全集団に対して適切な遺伝カウンセリングを提供できるかどうかである。
BRCA1またはBRCA2病原性多様体の確率に関する臨床基準および予測モデル
複数の研究で、乳がんまたは卵巣がんに罹患している女性のBRCA1またはBRCA2病原性多様体の頻度が評価されている。[ 57 ][ 58 ][ 73 ][ 83 ][ 84 ][ 85 ][ 86 ][ 87 ][ 88 ][ 89 ][ 90 ][ 91 ]BRCA1および/またはBRCA2病原性多様体の可能性が高いという関係がある個人的特徴には以下のものがある:
BRCA1および/またはBRCA2病原性多様体を保有する確率の増大に関連する家族歴の特徴には以下のものがある:
BRCA1またはBRCA2病原性多様体を有しうる個人を同定するための臨床基準および診療ガイドライン
米国臨床腫瘍学会[ 96 ]、National Comprehensive Cancer Network(NCCN)[ 97 ]、米国人類遺伝学会[ 98 ]、American College of Medical Genetics and Genomics[ 99 ]、米国遺伝カウンセラー学会(National Society of Genetic Counselors)[ 99 ]、米国予防サービス作業部会(U.S. Preventive Services Task Force)[ 100 ]、およびSociety of Gynecologic Oncologists[ 101 ]など、いくつかの専門家組織および専門家委員会は、医療提供者がBRCA1またはBRCA2病原性多様体を有する可能性のある個人を同定する際に有用な臨床基準および診療ガイドラインを開発している。
BRCA1またはBRCA2病原性多様体の確率を予測するためのモデル
個人または家系において生殖細胞系BRCA1/BRCA2病原性多様体が同定される確率を予測するために、多くのモデルが開発されている。これらのモデルには、ロジスティック回帰を用いるモデル[ 32 ][ 83 ][ 84 ][ 86 ][ 89 ][ 102 ][ 103 ]、ベイズの解析を用いる遺伝子モデル(BRCAPROおよびBreast and Ovarian Analysis of Disease Incidence and Carrier Estimation Algorithm [BOADICEA])[ 89 ][ 104 ]、およびMyriad prevalence tablesなどの経験的観察[ 54 ][ 57 ][ 60 ][ 105 ][ 106 ][ 107 ]が含まれる。
BOADICEAに加えて、BRCAPROは臨床状況での遺伝カウンセリングに広く用いられている。BRCAPROおよびBOADICEAは、キャリアである確率を予測し、乳がんリスクの推定値を算出する(表4を参照)。これらのモデルの識別能と精度(予測モデルの性能評価に用いられる因子)は、モデルで一定期間または残りの生涯リスクを予測する場合よりも、保因状態を報告する場合の方がはるかに高い。
BOADICEAは、複合分離解析を用いて、乳がんリスクとBRCA1またはBRCA2病原性多様体を有する確率の両方を調べるポリジーンモデルである。[ 104 ]経験を積んだ医療提供者でさえ、予測モデルを用いると、BRCA1/BRCA2病原性多様体キャリアである確率が最も高い患者を識別する検出力が高まることが示されている。[ 108 ][ 109 ]ほとんどのモデルには、膵がんや前立腺がんなどの、BRCA1およびBRCA2でみられる他の種類のがんは含まれていない。個人ががんを発症する可能性を低下させる介入(卵巣摘出術や乳房切除術など)は、BRCA1およびBRCA2病原性多様体の状態を予測する能力に影響しうる。[ 110 ]1件の研究により、遺伝的リスクの予測モデルは利用可能な家族歴のデータ量による影響を受けやすく、家族の情報が限られている場合はあまりよく機能しないことが示されている。[ 111 ]BOADICEAは、病原性多様体状態をより良く予測し、乳がんおよび卵巣がんリスクの推定値の精度を改善するために拡張され、追加のリスク多様体(ゲノムワイド関連解析[GWAS]一塩基多型[SNP])が組み込まれている。[ 112 ]
モデルの成績は特定の民族集団において変動しうる。BRCAPROモデルはフランス系カナダ人家族のシリーズに最適なようであった。[ 113 ]ヒスパニック系におけるBRCAPROモデルの性能についての結果はさまざまであり[ 114 ][ 115 ]、BRCAPROモデルおよびMyriad tablesの両方が、アジア系米国人集団における病原性多様体キャリアの割合を過小評価した。[ 116 ]BOADICEAは英国女性集団を対象に開発、検証された。したがって、全リスク(表1)と遺伝リスク(表4)の両方に用いられる主要なモデルは、多様な人種または民族の女性を含む大規模集団での開発または検証を経ていない。遺伝的リスクを評価する一般的な臨床モデルの中では、Tyrer-Cuzickモデルだけが非遺伝的な危険因子を取り入れている。
本モデルのいくつかの検出力がさまざまな研究で比較されている。[ 117 ][ 118 ][ 119 ][ 120 ]BOADICEA、BRCAPRO、IBIS、およびeCLAUSの4つの乳がん遺伝子リスクモデルでは、ドイツ人の7,352家系のコホートで、BRCA1/BRCA2病原性多様体を予測するそれぞれの診断精度が評価された。[ 121 ]各家系から病原性多様体を有する可能性が最も高い家系員がBRCA1/BRCA2病原性多様体についてスクリーニングを受けた。各モデルからキャリアの可能性が算出され、実際に検出された多様体と比較された。BRCAPROおよびBOADICEAは、診断精度がIBISまたはeCLAUSより有意に高かった。BOADICEAモデルの精度は、ER、プロゲステロン受容体(PR)、およびヒト上皮成長因子受容体2(HER2/neu)の腫瘍マーカーに関する状態をモデルに含めると、さらに改善された。これらのバイオマーカーの算入により、BRCAPROの性能が改善することが示されている。[ 122 ][ 123 ]
表4.BRCA1/BRCA2病原性多様体の確率を推定する一般的なモデルの特徴 BRCAPRO BOADICEA Tyrer-Cuzick AJ = アシュケナージユダヤ人;BOADICEA = Breast and Ovarian Analysis of Disease Incidence and Carrier Estimation Algorithm(乳がんおよび卵巣がん発生およびキャリア推定に関する解析アルゴリズム);FDR = 第一度近親者;SDR = 第二度近親者。 方法 申請書に報告される個人歴および家族歴に基づくMyriad Geneticsの経験的データ 統計的モデル、常染色体優性遺伝を想定 統計的モデル、多遺伝子リスクを想定 統計的モデル、常染色体優性遺伝を想定 モデルの特徴 発端者が乳がんまたは卵巣がんに罹患している場合もあれば、罹患していない場合もある 発端者が乳がんまたは卵巣がんに罹患している場合もあれば、罹患していない場合もある 発端者が乳がんまたは卵巣がんに罹患している場合もあれば、罹患していない場合もある 発端者は非罹患者である必要がある 乳がん診断年齢を50歳未満、50歳を超えるとして考慮する 乳がんおよび卵巣がん診断時の正確な年齢を考慮する 乳がんおよび卵巣がん診断時の正確な年齢を考慮する 乳がんリスクを推定するため、生殖因子および肥満指数も含める 1人以上の罹患近親者における乳がんは、50歳未満で診断された場合にのみ考慮する 事前の家系(すなわち、BRCA1/BRCA2病原性多様体陰性の近親者)における遺伝子検査を考慮する がんを認めるまたは認めないすべてのFDRおよびSDRを含める 卵巣がんは年齢に関係なく1人以上の近親者で考慮する 卵巣摘出術の状態を考慮する AJ先祖を含める AJ先祖を含める がんを認めるまたは認めないすべてのFDRおよびSDRを含める 非常に使用しやすい AJ先祖を含める 限界 家族構成の考慮が簡素化/限定されている コンピュータソフトウェアおよび時間を要するデータ入力が必要 コンピュータソフトウェアおよび時間を要するデータ入力が必要 乳がんに罹患していない個人向けにデザインされている FDRおよびSDRのみを組み入れる;リスクを最も良く把握するためおよび父方家系の疾患を説明するために発端者を変更する必要がありうる 両側乳がんにおいてリスクを過大評価しうる[ ] 乳がんの早期発症年齢 少数派集団よりも白人において性能が優れている可能性がある[ ][ ] FDRおよびSDRのみを組み入れる;リスクを最も良く把握するために発端者を変更する必要がありうる 高悪性度の漿液性卵巣がんでは、BRCA病原性多様体のリスクが過小評価される可能性があるが、他の組織型のリスクが過大評価される可能性もある[ ] BRCA1およびBRCA2病原性多様体に対する遺伝子検査は1996年から一般の人々が利用可能である。検査を受ける個人が増えるにつれ、リスク評価モデルが改善されている。そしてこれにより、検査提供者は個々の患者の病原性多様体保有リスクを推定するためのより良質なデータを手に入れるが、リスク評価には引き続き熟練を要する。個々の患者の個別の状況(病歴またはリスク低減のための手術など)を含めて、正確なリスク評価を提供する能力を制限しうる因子(すなわち、小規模家族、女性数の不足、または民族性)がある。
BRCA病原性多様体の浸透度
病原性多様体を有する人にその疾患が発症する割合を浸透度と呼ぶ。(詳しい情報については、本要約の遺伝性乳がんおよび/または婦人科がんに対する遺伝的感受性の浸透度のセクションを参照のこと。)
多数の研究で、BRCA1およびBRCA2病原性多様体キャリアにおける乳がんおよび卵巣がんの浸透度が推定されている。乳がんと卵巣がんの両方で、リスクはBRCA2病原性多様体キャリアよりもBRCA1病原性多様体キャリアの方が高いと一貫して推定されている。2件の大規模メタアナリシスの結果を表5に示す。[ 128 ][ 129 ]1件の研究[ 128 ]では、BRCA1病原性多様体陽性の289人およびBRCA2病原性多様体陽性の221人を含む22件の研究からの家系データを併合して解析した。これらの研究の発端者には、女性の乳がん、男性の乳がん、または卵巣がんが含まれたが、家族歴に基づく選択は行われなかった。その後の研究[ 129 ]では、以前の研究に加え、さらにBRCA1病原性多様体陽性の734家系およびBRCA2病原性多様体陽性の400家系を含む9件の研究から得られた浸透度の推定値が併合された。これら2件のメタアナリシスにおける70歳までの乳がん累積リスクの推定値は、BRCA1病原性多様体キャリアで55~65%、BRCA2病原性多様体キャリアで45~47%であった。卵巣がんリスクはBRCA1病原性多様体キャリアで39%、BRCA2病原性多様体キャリアで11~17%であった。
表5.BRCA1およびBRCA2病原性多様体キャリアにおける乳がんおよび卵巣がん累積リスクの推定値 研究 乳がんのリスク(%)(95%CI) 卵巣がんのリスク(%)(95%CI) CI = 信頼区間。 a年齢70歳までのリスク推定値。 b年齢80歳までのリスク推定値。 BRCA1 BRCA2 BRCA1 BRCA2 Antoniou et al.(2003) [ 128 ] 65 (44–78)a 45 (31–56)a 39 (18–54)a 11 (2.4–19)a Chen et al.(2007) [ 129 ] 55 (50–59)a 47 (42–51)a 39 (34–45)a 17 (13–21)a Kuchenbaecker et al.(2017) [ 130 ] 72 (65–79)b 69 (61–77)b 44 (36–53)b 17 (11–25)b 70歳までにがんを発症する累積リスクは、BRCA1病原性多様体キャリアの方がBRCA2病原性多様体キャリアよりも高いが、BRCA1病原性多様体キャリアでは、乳がんの相対リスク(RR)が年齢とともに低下する。[ 128 ]個々の特異的な多様体キャリアに対する浸透度の研究は、通常は安定性のある推定値を提供できるほど十分に規模が大きくはないが、アシュケナージ創始者病原性多様体については多数の研究が実施されている。1つの研究者グループにより、比較的大規模のメタアナリシスからアシュケナージ創始者病原性多様体の1つを有する家系のサブセットが解析され、個々の病原性多様体に対して推定される浸透度は、すべてのキャリアで対応する推定値と非常に類似していることが明らかにされた。[ 131 ]BRCA病原性多様体を有する女性4,649人を対象としたその後の研究によると、BRCA2 6174delT多様体を有する女性では、他のBRCA2多様体を有する女性と比べて乳がんのRRが有意に低いことが報告された(ハザード比[HR]、0.35;信頼区間[CI]、0.18-0.69)。[ 132 ]
1件の研究では、さまざまな年齢の無症状のキャリアにおけるがん発症のプロスペクティブな10年リスクが提供された。[ 129 ]それでも、個々のキャリアにおける正確な浸透度を推定するのは困難である。卵巣がんの生涯リスクはRAD51C病原性多様体キャリアでは5.2%、BRIP1病原性多様体キャリアでは5.8%、およびRAD51D病原性多様体キャリアでは12%である。これらの患者に対し、出産終了時にリスク低減のための卵管-卵巣摘出術(RRSO)を検討してもよい。[ 133 ][ 134 ]
BRCA1病原性多様体キャリア19,581人とBRCA2病原性多様体キャリア11,900人で構成されるConsortium of Investigators of Modifiers of BRCA1/BRCA2(CIMBA)のデータが分析され、病原性多様体型、機能、ヌクレオチド位置に基づいて乳がんおよび卵巣がんのHRが推定された。[ 135 ]両方の遺伝子に乳がん集合領域と卵巣がん集合領域が認められた。乳がんおよび卵巣がんの発生リスクと診断時年齢は多様体の分類によって異なっていた。これらの発見は、実地臨床への適用前にさらなる評価を受ける必要がある。
CIMBAグループによる別の研究では、BRCA1およびBRCA2の両方に遺伝性病原性多様体を有する乳がん女性の表現型が調査された。[ 136 ]大多数の女性が一般的なユダヤ性病原性多様体を保有した。同じ病原性多様体についてヘテロ接合体であった女性(ヘテロ接合体対照)と比較したところ、BRCA1およびBRCA2の両方でヘテロ接合体であった女性は、ヘテロ接合体対照の女性よりも乳がんを診断される可能性が高く、BRCA2のヘテロ接合体対照の女性よりも卵巣がんを診断される可能性が高かったが、この関連はBRCA1病原性多様体を有するヘテロ接合体対照の女性との比較では認められなかった。同様に、乳がんの発症時年齢はBRCA2のヘテロ接合体対照の女性と比較して両方の多様体のキャリアでは若かったが、BRCA1病原性多様体を有する女性とは比較されなかった。両方の多様体を有し、エストロゲン受容体陽性およびプロゲステロン受容体陽性乳がんである女性の割合は、BRCA1病原性多様体を有するヘテロ接合体対照およびBRCA2病原性多様体を有するヘテロ接合体対照間で中程度であった。著者らは、BRCA1およびBRCA2の両方の病原性多様体を受け継いでいる女性はBRCA1多様体のみのキャリアと同様に管理できると結論付けた。
数件の研究により、BRCA病原性多様体が遺伝的表現促進と関係している可能性が示唆されている。ある研究では、BRCA1またはBRCA2の病原性多様体を有し、2代以上の連続世代に同じがんがみられる176の家系を対象に評価された。発端者の世代が乳がんと診断されたのは、親世代より6.8歳若く、祖父母世代より9.8歳若いと推定された。[ 137 ]同様に、他の研究でも、病原性多様体キャリアの母と娘の80ペア間で乳がん診断時年齢の差が示されたが、母が50歳より後に乳がんと診断された場合のみであった。[ 138 ]家系内にBRCA病原性多様体が確認された2代連続世代からの女性106ペアを対象とした別のコホート研究では、後の世代で発症年齢が6~8歳若いことが推定された。[ 139 ]
RRSOおよび/または経口避妊薬の使用は、乳がんリスクと関連するとされている。[ 66 ][ 128 ][ 140 ][ 141 ][ 142 ][ 143 ][ 144 ][ 145 ](詳しい情報については、本要約のRRSOのセクションおよび経口避妊薬のセクションを参照のこと。)このほか、潜在的に修正可能な生殖因子およびホルモン因子もリスクに影響しうる。[ 146 ][ 147 ][ 148 ][ 149 ][ 150 ]乳がんおよび卵巣がんの浸透度の遺伝的修飾因子が次第に研究されるようになってきたが、現時点で臨床的に有用なものは認められていない。[ 151 ][ 152 ][ 153 ](詳しい情報については、BRCA1およびBRCA2病原性多様体キャリアにおけるリスクの修飾因子のセクションを参照のこと。)乳がんおよび卵巣がんの平均浸透度は、当初推定された値ほどは高くないものの、それらは相対的にみても絶対的にみても特に1940年以降に生まれた女性でかなり高い。さらに後に生まれたコホートでは、一貫して50歳前に比較的高いリスクが観察されており[ 64 ][ 66 ][ 139 ]、より正確な個人のリスク予測を得るために、さらに可能性のある修飾因子を特徴付けるべく追加研究が必要とされる。膵がんなど、まれながんの正確な浸透度の推定値は、得られていない。
BRCA病原性多様体キャリアにおける対側乳がん(CBC)
数件の大規模研究で、BRCA1およびBRCA2の病原性多様体キャリアにおけるCBCリスクの増加が確認されており、表6に要約しているように結果はほぼ一定している。
表6.BRCA1/BRCA2病原性多様体キャリアで推定した対側乳がんの10年累積リスク 研究 キャリア(%) キャリア(%) Graeser et al.(2009) [ ] 18.5 13.2 Malone et al.(2010) [ ] 20.5 15.9 van der Kolk et al.(2010) [ ] 34.2 29.2 Metcalfe et al.(2011) [ ] 23.8 18.7 Molina-Montes et al.(2014) [ ] 27 19 Basu et al.(2015) [ ] 25.7 19.5 van den Broek et al.(2016) [ ] 21.1 10.8 公表されている結果には、German Consortium for Hereditary Breast and Ovarian Cancerによる大規模研究が含まれており、そこでBRCA1およびBRCA2病原性多様体が確認された家族の家系員におけるCBCリスクが推定された。最初の乳がん後25年経過時のCBCリスクは、BRCA1およびBRCA2の両方の家系で50%に近かった。この研究において、このリスクは年齢とも逆相関し、最初の乳がんが40歳前に発生した女性で最もリスクが高かった。[ 154 ]
その後、CBCを対象とした大規模な集団ベースのネスティド・ケースコントロール研究であるWomen's Environmental Cancer and Radiation Epidemiology(WECARE)研究の結果から、10年時点でのCBCリスクは、BRCA1/BRCA2病原性多様体キャリアで15.9%、非キャリアで4.9%であったことが報告された。この研究でもリスクは、最初の診断時年齢と逆相関し、乳がんの第一度近親者(FDR)を1人有する個人では1.8倍高かった。[ 155 ]
オランダにおけるBRCA1/BRCA2家系員を対象にしたさらに大規模な研究の報告によると、BRCA1およびBRCA2の家系の女性では10年時点でのCBCリスクが同程度(それぞれ、34.2%と29.2%)であった。[ 156 ]
BRCA1/BRCA2病原性多様体を有し、乳房温存療法または乳房切除術のいずれかを受けた女性655人の比較では、いずれの治療群ともCBCの割合が高く、追跡期間20年までに50%を超えることが注目された。CBCの割合は、BRCA2病原性多様体を有する女性よりもBRCA1病原性多様体を有する女性で、また最初の乳がんが35歳以前に発生した女性で有意に高かった。[ 161 ]
家系内でBRCA1またはBRCA2病原性多様体が同定されたI期またはII期乳がんの女性810人を対象にした研究では、149人(18.4%)がCBCを発症した;生命表法による15年リスクはBRCA1病原性多様体キャリアで36.1%およびBRCA2病原性多様体キャリアで28.5%であった。[ 157 ]50歳未満で診断された女性の方が50歳以上で診断された女性よりもリスクが高かった(37.6% vs 16.8%;P = 0.003)。さらに、最初の乳がんが50歳未満で診断された女性では、CBCのリスクは家族歴によって異なっていた。これらの女性について、50歳未満で乳がんが診断されたFDRが0人、1人、または2人以上の女性におけるCBCのリスクはそれぞれ、33.4%、39.1%、および49.7%であった。
BRCA1およびBRCA2キャリアで、最初に乳がんと診断されてからの対側乳がんのリスクは、レトロスペクティブおよびプロスペクティブ観察疫学研究の両方で調査されている。これらの疫学研究(レトロスペクティブ・コホート研究が18件、プロスペクティブ・コホート研究が2件)の系統的レビューおよび定量メタアナリシスでは、CBCの5年累積リスクがBRCA1キャリアで15%(95%CI、9.50%-20%)、BRCA2キャリアで9%(95%CI、5%-14%)と報告された。[ 158 ]プロスペクティブ研究を個別に解析した場合の5年累積リスクは、BRCA1キャリアで23.4%(95%CI、9.1%-39.5%)、BRCA2キャリアで17.5%(95%CI、9.1%-39.5%)に増加した。レトロスペクティブ・シリーズではバイアスが生じる可能性があるため、報告された頻度の相違は固有なものであろう。
同様に、オランダで50歳前に浸潤性乳がんと診断された患者6,294人(BRCA1キャリア200人およびBRCA2キャリア71人を含む)のコホートにおいて、追跡期間中央値12.5年で、CBCの10年リスクは、BRCA1キャリアで21.1%(95%CI、15.4%-27.4%)、BRCA2キャリアで10.8%(95%CI、4.7%-19.6%)、非キャリアで5.1%(95%CI、4.5%-5.7%)であった。[ 160 ]最初に乳がんと診断された年齢は、BRCA1/BRCA2キャリアのみで、CBCの10年累積リスクの予測因子であった。具体的には、41歳前に診断されたBRCA1/BRCA2キャリアのCBCリスクは23.9%(BRCA1、25.5%;BRCA2、17.2%)であった;対照的に、41~49歳で診断された場合のCBCリスクは12.6%(BRCA1、15.6%;BRCA2、7.2%)であった。
年齢に関係なく乳がんの診断を受けたBRCA1キャリア506人とBRCA2キャリア505人を対象とした英国の研究では、追跡期間中央値7.8年で、CBCの10年リスクがBRCA1キャリアで25.7%、BRCA2キャリアで19.5%であった。[ 159 ]BRCA1およびBRCA2キャリアでは、初回の乳がん診断が早いことと高いCBCリスクに関連がみられ、具体的には40歳未満で初めて診断された場合の20年発生率は55.4%であったのに対し、50歳以上の場合は36.4%であった。加えて、差異はBRCA2キャリアに比べてBRCA1キャリアでより顕著であった。
1件の国際多施設プロスペクティブ・コホート研究において、乳がんの診断を受けた(他のがんを有しない)BRCA1キャリアの女性1,305人とBRCA2キャリアの女性908人に対する追跡期間中央値4年の追跡調査が実施された(範囲、2~7年)。[ 130 ]追跡開始時の年齢中央値は47年であった(範囲、40~55年)。著者らは、初回乳がん診断から20年後のCBC累積リスクとして、BRCA1キャリアで40%(95%CI、35%-45%)、BRCA2キャリアで26%(95%CI、20%-33%)を報告した。これらの20年推定値は表6の10年累積リスク推定値に適合する。
そのため、要約すると、研究デザイン、研究施設、およびサンプルサイズに差があるにもかかわらず、BRCA1/BRCA2病原性多様体を有する女性におけるCBCに関するデータから、以下のようないくつかの一貫性のある知見が示される:
リスク低減のための戦略
BRCA病原性多様体キャリアにおけるリスク低減のための手術の利用に関する情報については、本要約のリスク低減のための乳房切除術のセクションを参照のこと。BRCA病原性多様体キャリアにおけるCBCのリスク低減戦略としてのタモキシフェン使用に関する情報については、本要約の化学予防のセクションを参照のこと。
BRCA病原性多様体キャリアにおける二次悪性腫瘍としての乳がん
最近、2件の遺伝子登録ベース研究により、BRCA関連卵巣がん後の原発性乳がんのリスクが調査されている。1件目の研究では、原発性上皮性卵巣がん、卵管がん、または原発性腹膜がんのBRCA1/BRCA2キャリア164人を対象に、その後のイベントについて追跡した。[ 162 ]卵巣がん診断から5年後の異時性の乳がんリスクは、非罹患BRCA1/BRCA2キャリアで過去に報告されたリスクより低かった。このシリーズでは、全生存が卵巣がん関連死亡によって大きな影響を受けていた。これより小規模な研究で、BRCA関連卵巣がん患者と非罹患キャリアにおける原発性乳がんのリスクが比較された。[ 163 ]卵巣がん患者では、2年、5年、および10年での原発性乳がんリスクがすべて統計的に有意な低下を示した。卵巣がんと診断される前に片側乳がんであった女性も、対側乳がんのリスクは卵巣がんではない女性より低かったが、その差は統計的有意差に達しなかった。これらの研究から、卵巣がんの治療、つまり卵巣摘出およびプラチナ製剤をベースとした化学療法は、その後の乳がん予防に役立っている可能性が示唆される。上皮性卵巣がんでBRCA病原性多様体検査を受けた患者364人を対象にした1件の単一施設のコホート研究では、135人(37.1%)がBRCA1またはBRCA2の生殖細胞病原性多様体を保有することが明らかにされた。BRCA1/BRCA2キャリア135人のうち、12人(8.9%)が乳がんを発症した。乳がんはいずれも0期からII期で次のように診断された:マンモグラム(7)、触知可能な腫瘤(3)、およびリスク低減のための乳房切除術中の偶然の発見(2)。追跡期間中央値6.3年経過時に、卵巣がんの後に乳がんを発症した患者12人中、3人が卵巣がんの再発により死亡し、1人が転移性乳がんにより死亡した。[ 164 ]これらのがんの大多数がマンモグラムまたは診察で発見されたことから、他の方法による追加の乳房のサーベイランスまたはリスク低減のための手術に価値があるかどうかは疑わしいことが示唆されている。数理モデル化により、BRCA関連卵巣がんの女性に対する乳がんスクリーニングはマンモグラフィと乳房視触診で構成すべきであると示唆されている。早期卵巣がんの女性または卵巣がんの長期生存者には、乳房磁気共鳴画像法(MRI)および/またはリスク低減のための乳房切除術の検討が有益な場合がある。[ 165 ]
女性の乳がん/卵巣がん以外のがん
女性の乳がんおよび卵巣がんは、明らかに優性ながんで、BRCA1およびBRCA2に関連している。BRCA病原性多様体ではまた、卵管がんおよび原発性腹膜がんのリスクも増加する。BRCA1病原性多様体キャリアの家系登録に関する大規模研究が1件あり、BRCA1病原性多様体キャリアでは、卵管がんのRRが一般集団と比較して120倍高いことが明らかにされている。[ 6 ]卵巣が損なわれていないBRCA病原性多様体キャリアでは原発性腹膜がんのリスクが高いが、RRSOから20年後でも3~4%のリスクが残存するにもかかわらず、依然として定量化が不十分である。[ 166 ][ 167 ](詳しい情報については、本要約の卵巣がんのセクションのRRSOのセクションを参照のこと。)
膵がん、男性の乳がん、および前立腺がんも一貫してBRCA病原性多様体と関連付けられており、特にBRCA2と関連している。一部の研究では、他のがんが関連付けられている。これらのがんのBRCA病原性多様体との関連性の強さは、病原性多様体キャリアにこれらのがんが観察される数が少ないため、推定がさらに困難となっている。
BRCA2病原性多様体を有する男性、および程度は低いがBRCA1病原性多様体を有する男性は、乳がんのリスクが高く、生涯リスクは、それぞれ5~10%および1~2%と推定されている。[ 6 ][ 8 ][ 9 ][ 168 ]BRCA2病原性多様体を有する男性、および程度は低いがBRCA1病原性多様体を有する男性は、前立腺がんのリスクが約3~7倍高い。[ 7 ][ 8 ][ 12 ][ 107 ][ 169 ][ 170 ][ 171 ][ 172 ]BRCA2に関連した前立腺がんも、より侵攻性であると考えられる。[ 173 ][ 174 ][ 175 ][ 176 ][ 177 ][ 178 ](詳しい情報については、前立腺がんの遺伝学に関するPDQ要約のBRCA1とBRCA2のセクションを参照のこと。)
家族性膵がん(FPC)の研究[ 179 ][ 180 ][ 181 ][ 182 ][ 183 ]、および膵がんの非選択シリーズ[ 184 ][ 185 ][ 186 ]でも、BRCA2、および程度は低いがBRCA1との関連性が裏付けられている。[ 7 ]全体的に、FPCを認める家系の3~15%が生殖細胞系BRCA2病原性多様体を有している可能性があり、罹患した血縁者が多いほどリスクが高くなると考えられる。[ 179 ][ 180 ][ 181 ]同様に、非選択膵がんの研究では、BRCA2病原性多様体の頻度が3~7%で、AJの子孫ではこれらの数値が10%に近いことが報告されている。[ 184 ][ 185 ][ 187 ]BRCA2キャリアにおける膵がんの生涯リスクは、3~5%と推定されるが[ 8 ][ 12 ]、これと比べ一般集団における70歳までの推定生涯リスクは0.5%である。[ 188 ]1,000人以上の病原性多様体キャリアを対象にした単一施設の大規模研究により、一般集団における発生率と比較してBRCA2キャリアにおける膵がんリスクが21倍であること、BRCA1病原性多様体キャリアにおけるリスクが4.7倍であることが明らかにされた。[ 172 ]すべてではなく一部の研究では、BRCA2病原性多様体に関連した他のがんとして、黒色腫、胆道がん、頭頸部がんなどが挙げられているが、これらのリスクは、軽度(生涯リスクが5%未満)であると考えられ、研究が不十分である。[ 12 ]
表7.BRCA1およびBRCA2病原性多様体キャリアにおけるがんの範囲 がんの部位 a前立腺がんとBRCA1およびBRCA2との関連性に関する詳しい情報については、前立腺がんの遺伝学に関するPDQ要約を参照のこと。 +++ 複数の研究で関連が実証されており、比較的一貫している。 ++ 複数の研究および証拠の優位性は、肯定的である。 + おそらく関連している、主に単一の研究;より小規模で限られた研究および/または一貫していないが、関連している傾向が認められる。 証拠の強さ 絶対リスクの大きさ 証拠の強さ 絶対リスクの大きさ 乳房(女性) +++ 高い +++ 高い 卵巣、卵管、腹膜 +++ 高い +++ 中程度 乳房(男性) + 未決定 +++ 低い 膵がん ++ 非常に低い +++ 低い 前立腺a + 未決定 +++ 高い がんのリスクを調査した最初のBreast Cancer Linkage Consortium研究では、BRCA1キャリアにおいて大腸がんが過剰に多いことが報告された(RR、4.1;95%CI、2.4-7.2)。[ 189 ]この知見は、家族ベース研究の一部では裏付けられたが[ 6 ][ 7 ][ 190 ]、すべての研究で裏付けられたわけではなかった。[ 8 ][ 63 ][ 71 ][ 107 ][ 191 ][ 192 ][ 193 ]しかしながら、AJ集団に限定して実施された大腸がんの非選択シリーズでは、BRCA1またはBRCA2病原性多様体の頻度は高くないことが示された。[ 194 ][ 195 ][ 196 ]以上のことを考え合わせると、本データは、大腸がんのリスクの上昇はほとんどなく、たとえあったとしても、おそらく特定の集団にしかみられないことを示唆している。そのため、現時点でBRCA1病原性多様体キャリアは、大腸がんについて集団単位のスクリーニングの推奨に従うべきである。
子宮内膜がんのユダヤ人女性200人または子宮の乳頭状漿液性がんの非選択女性56人では、遺伝性BRCA病原性多様体の保有率に増加は認められなかった。[ 197 ][ 198 ](詳しい情報については、本要約の卵巣がんのセクションにあるリスク低減のための卵管卵巣摘出術のセクションを参照のこと。)
既知の家族性BRCA1/BRCA2病原性多様体に関する検査が陰性の人におけるがんリスク(真陰性)
家系内で分離しているBRCA1/BRCA2病原性多様体の検査が陰性の女性において残存する家系的リスクに関する証拠は矛盾している。その家系で分離しているBRCA1病原性多様体の検査が陰性であった女性353人のプロスペクティブ評価に基づいた初期の研究では、6,000人年を超える観察期間で乳がんが5例発生し、生涯リスクは6.8%で一般集団と同様な発生率であったことが明らかになった。[ 143 ]家系におけるBRCA1またはBRCA2病原性多様体の検査が陰性であった女性のリスクは5倍になりうるという報告[ 199 ]にはその後、観察されたこの過剰リスクの多くが確認バイアスにより説明されることを示唆する多くの書簡が編集者に送られた。[ 200 ][ 201 ][ 202 ][ 203 ][ 204 ][ 205 ] 4件の別の解析により、約1.5倍~2倍の過剰リスクが示唆されている。[ 204 ][ 206 ][ 207 ][ 208 ] 1件の研究では、2例の卵巣がんが報告された。[ 208 ]レトロスペクティブな分析を行っている研究が数件ある;それらの研究はすべて少数の症例の観察に基づいており、統計的有意性および臨床的意義は不明である。
他の数多くのプロスペクティブな研究による結果から、リスクが増加しないことが明らかになっている。BRCA1またはBRCA2における既知の家族性病原性多様体の検査が陰性であった女性375人を対象とした研究では、平均追跡期間4.9年で浸潤性乳がんが2例、非浸潤性(in situ)乳がんが2例報告されたが、卵巣がんの診断はみられなかった。4例の浸潤性乳がんが予想されたが、観察されたのは2例だった。[ 209 ]患者数は同程度だが追跡期間が長い別の研究(女性395人および追跡期間7,008人年)でも、病原性多様体陰性の女性における乳がんリスク(観察/予想[O/E]、0.82;95%CI、0.39-1.51)に統計的に有意な全般的増加は認められなかったが、乳がんのFDRが少なくとも1人いる女性では、統計的に有意でないリスクの増加がみられた(O/E、1.33;95%CI、0.41-2.91)。[ 210 ]Breast Cancer Family Registryから得られたBRCA1病原性多様体陽性の160家系およびBRCA2病原性多様体陽性の132家系を対象とした研究では、これらの家系で非キャリアにおけるリスクが増加する証拠は認められなかった。[ 211 ]多様体陰性のオーストラリアの女性722人を対象とした大規模研究では、中央値6.3年の追跡期間後に6例の浸潤性乳がんが観察され、標準化発生比(SIR)が有意に高いとは認められなかった(SIR、1.14;95%CI、0.51-2.53)。[ 212 ]利用可能なデータに基づくと、既知の家族性BRCA1/BRCA2病原性多様体に関する検査が陰性の女性は、乳房の異型過形成の個人歴、または家族性病原性多様体を保有していない近親者における乳がんの家族歴といった十分な危険因子が他にない限り、一般集団のスクリーニングガイドラインに従えばよいと考えられる。
BRCA1/BRCA2病原性多様体が検出されない乳がん家系における乳がんおよび卵巣がんのリスク(「非決定的」)
部位特異的乳がんが認められる家系の大多数はBRCA1/BRCA2検査が陰性であり、コーデン症候群またはリー-フラウメニ症候群と一致する特徴は認められない。[ 32 ]集団ベースおよびクリニックベースのアプローチを用いた5件の研究では、こうした家系における卵巣がんリスクの増加は実証されていない。卵巣がんリスクは増加していなかったが、乳がんリスクは高いままであった。[ 211 ][ 213 ][ 213 ][ 214 ][ 214 ][ 215 ][ 215 ][ 216 ][ 217 ]
BRCA1およびBRCA2病原性多様体キャリアにおけるリスクの修飾因子
BRCA1およびBRCA2に病原性多様体が存在すると、乳がんと卵巣がんのリスクが高くなる。しかしながら、リスクはすべての病原性多様体キャリアで同一ではなく、がんの種類や発症時年齢、多様体の位置など、さまざまな因子によって異なることが明らかにされている。[ 218 ]このように観察されている浸透度にばらつきがあることから、他の遺伝的および/または環境的因子により病原性多様体キャリアのがんリスクが修飾されるという仮説が立てられている。BRCA1/BRCA2病原性多様体を有する家系にみられるがんの割合にばらつきが観察されているが、このばらつきの一因となっている遺伝的および非遺伝的因子を確認している文献が増えつつある。
乳がんおよび卵巣がんリスクの遺伝的修飾因子
現在までに乳がんおよび卵巣がんリスクの遺伝的修飾因子を調査する最大規模の研究は、BRCA1キャリア15,000人およびBRCA2キャリア10,000人以上を対象にした遺伝子型および表現型のデータに関する大規模な国際事業、CIMBAからのものである。[ 219 ]CIMBAでは、候補遺伝子解析およびGWASを用いて、乳がんおよび卵巣がんリスクの増加と低下の両方に関連するいくつかの遺伝子座が同定されている。SNPの一部は、ホルモン受容体およびHER2/neuの状態など、乳がんのサブタイプに関係している。付加されるリスクはいずれもわずかではあるが、倍数的に作用した場合、BRCA1/BRCA2病原性多様体キャリアにおけるがんリスクに重大な影響を及ぼしうる。現在、これらのSNPは臨床的意思決定のための検証はなされておらず、使用されてもいない。
遺伝子型-表現型の相関
BRCA1およびBRCA2の病原性多様体を有する両方の家系において、いくつかの遺伝子型-表現型の相関が確認されている。これらの研究のどれもが、確実な結論を出すための十分な数の病原性多様体陽性の個人を調べておらず、これらの知見はおそらく個人のリスク評価およびリスク管理に使用できるほど確立されていない。BRCA2の病原性多様体が認められる25家系では、ヌクレオチド3,035と6,629に囲まれたエクソン11に卵巣がん集合領域が同定された。[ 11 ][ 220 ]Breast Cancer Linkage Consortiumによって集められたBRCA2の病原性多様体が認められる164家系を対象にした研究では、この初期の知見を確認した。卵巣がん集合領域内に病原性多様体があると、この領域のいずれかの側に多様体が認められる家系と比較して、卵巣がんリスクが高くなり、乳がんリスクが低下することが報告されている。[ 221 ]また、蛋白切断性のBRCA1病原性多様体を有する356家系がBreast Cancer Linkage Consortiumによって集められた研究は、中央領域(ヌクレオチド2,401-4,190)における多様体は周辺領域に比べ乳がんのリスクが低いことを報告した。卵巣がんのリスクは、3'からヌクレオチド4,191への多様体ではかなり低下した。[ 222 ]これらの観察は一般に、その後の研究で確認されている。[ 128 ][ 223 ][ 224 ]同じ病原性多様体を有する家系をかなりの数で研究できるアシュケナージにおける複数の研究でもまた、BRCA1の5'末端におけるBRCA1:185delAG多様体キャリアでは、この遺伝子の3'末端におけるBRCA1:5382insC多様体キャリアと比べて、卵巣がんの割合がより高いことが明らかにされている。[ 225 ][ 226 ]しかしながら、乳がん(特に両側乳がん)、および同一個人における乳がんと卵巣がんの両方の発生に対するリスクは、BRCA1:185delAGおよびBRCA2:6174delT多様体キャリアと比べて、BRCA1:5382insC病原性多様体キャリアにおいての方が高いようである。卵巣がんのリスクはBRCA1病原性多様体キャリアではかなり高く、BRCA2:6174delT病原性多様体キャリアの45歳未満ではまれである。[ 225 ][ 226 ]
BRCA1に病原性多様体が認められる122家系を対象にしたオーストラリアの1件の研究では、広範なゲノム再編成多様体は、より低い乳がん診断時年齢や両側性乳がんのより高い発生率など、乳がんおよび卵巣がんにおける高リスクの特徴に関連していた。[ 227 ]
乳がんの病理学
BRCA1の病理学
BRCA1関連乳がんにおいてみられる病理学的パターンを評価した数件の研究により、有害な病理学的および生物学的特性との関連が示唆されている。これらの所見には、予想より高い頻度の髄様組織型、高い組織学的悪性度、壊死領域、索状増殖パターン、異数性、高いS期分画、高い分裂指数、および高頻度のTP53多様体が含まれる。[ 228 ][ 229 ][ 230 ][ 231 ][ 232 ][ 233 ][ 234 ][ 235 ]3,797人のBRCA1病原性多様体キャリアを対象とした大規模な国際的シリーズで、乳がん診断時年齢の中央値は40歳であった。[ 235 ]乳房腫瘍が発生したBRCA1キャリアのうち、78%がER陰性;79%がPR陰性;90%がHER2陰性;69%がトリプルネガティブであった。これらの知見は複数のより小規模なシリーズで得られた結果と一貫している。[ 92 ][ 231 ][ 236 ][ 237 ][ 238 ]さらに、乳がん診断時の年齢が高くなるとER陰性腫瘍の割合は有意に低下した。[ 235 ]
トリプルネガティブ乳がんと基底細胞様サブタイプの間には、完全ではないが、かなり多くの重複があり、両者ともBRCA1関連乳がんによくみられ[ 239 ][ 240 ]、特に50歳未満で診断された女性に多い。[ 92 ][ 93 ][ 94 ]BRCA1関連乳がんでER陽性の集団は少数であり、発症年齢が遅いことに関係している。[ 241 ][ 242 ]これらのER陽性の乳がんでは、ER陰性のBRCA1乳がんとER陽性の散発性乳がんとの中間の臨床的挙動特性が認められ、その発症には特異な機序が存在しうるという可能性を高めている。
トリプルネガティブ乳がんの女性では、臨床的な遺伝子検査を受けた女性(および、そのために大半が家族歴で選択された女性)と非選択のトリプルネガティブ患者のいずれでも、BRCA1の生殖細胞病原性多様体の保有率は有意に高く、9~35%に病原性多様体が報告されている。[ 94 ][ 95 ][ 236 ][ 243 ][ 244 ][ 245 ][ 246 ]注目すべきこととして、非選択のトリプルネガティブ乳がんの女性、特に50歳前に診断を受けた女性にBRCA1病原性多様体の割合が高いことが諸研究により実証されている。12件の研究を通じて集められた、家族歴で選択されていないトリプルネガティブ乳がん患者1,824人についての大規模レポートでは、患者の14.6%に遺伝性のがん感受性遺伝子における病原性多様体が同定された。[ 246 ]BRCA1病原性多様体が最も大きな割合を占め(8.5%)、BRCA2(2.7%);PALB2(1.2%)のほか;BARD1、RAD51D、RAD51C、BRIP1(それぞれの遺伝子について0.3~0.5%)がこれに続く。この研究において、BRCA1/BRCA2に病原性多様体または他の遺伝性がん遺伝子が認められる患者は若年齢で診断され、病原性多様体が認められない患者よりも高悪性度の腫瘍を有した。特に、BRCA1病原性多様体キャリアにおける診断時平均年齢は44歳で、94%が高悪性度腫瘍を有した。トリプルネガティブ乳がんの女性308人について調査した研究が1件ある;BRCA1病原性多様体が45人に確認された。家族歴について非選択の女性(58人中11人;19%)および家族歴を有する女性(111人中26人;23%)のいずれにも病原性多様体が確認された。[ 247 ]12件の研究から集めた患者2,533人をベースにした1件のメタアナリシスが実施され、トリプルネガティブ乳がんの高リスク女性におけるBRCA1病原性多様体のリスクが評価された。[ 248 ]結果から、トリプルネガティブ乳がんではない女性と比較したトリプルネガティブ乳がんの女性におけるBRCA1病原性多様体のRRは5.65(95%CI、4.15-7.69)であり、トリプルネガティブ乳がんの女性9人のうち約2人がBRCA1病原性多様体を有することが示された。興味深いことに、非選択のトリプルネガティブ乳がん患者77人で、そのうち15人(19.5%)に生殖細胞病原性多様体または体細胞BRCA1/BRCA2変異がみられた1件の研究において、BRCA1病原性多様体を有するトリプルネガティブ乳がんの患者の方がBRCA1病原性多様体を有しないトリプルネガティブ乳がんの患者よりも再燃リスクが低いことが実証された;この研究には症例数による限界がある。[ 244 ]BRCA1関連 vs 非BRCA1関連のトリプルネガティブ乳がんにおける臨床転帰を調べた別の研究で、差は確認されなかったが、BRCA1関連乳がんの患者で脳転移がみられる傾向が高かった。これらのいずれの研究でも、1人のBRCA1病原性多様体キャリアを除く全例が化学療法を受けた。[ 249 ]対照的に、HER2陽性かつ若年のみで、家族歴または二次原発がんがない場合は、BRCA1、BRCA2、またはTP53の病原性多様体を伴う可能性は増大しない。[ 250 ]
BRCA1腫瘍の多くが正常な乳腺細胞の基底上皮層に由来し、それらは非選択的浸潤性乳管がんの3%から15%を占めるという仮説が立てられている。もし乳房の基底上皮細胞が乳房の幹細胞であるならば、野生型のBRCA1に対して提唱されている制御の役割が、BRCA1の機能が損傷された場合のBRCA1関連乳がんの侵攻的な表現型を部分的に説明しうる。[ 251 ]遺伝性症候群において乳がんのこの亜型の意義を十分に評価するためには、さらなる研究が必要である。
基底細胞様乳がんを同定するための最も正確な方法は遺伝子発現検査を用いるものであり、この方法は乳がんを生物学的および臨床的に意味のあるグループに分類するために用いられている。[ 237 ][ 252 ][ 253 ]この技術はまた、高い割合の症例においてBRCA1およびBRCA2関連腫瘍と散発性腫瘍とを正確に区別することが示されている。[ 254 ][ 255 ][ 256 ]注目すべきこととして、分子表現型を調べるために遺伝子発現アレイ法を用いて研究された乳房腫瘍症例の集団では、BRCA1が変異した腫瘍はすべて基底細胞腫瘍のサブタイプに分類された[ 237 ];しかしながら、この技術はコストが高いためルーチンには用いられていない。代わりに、基底細胞様乳がん(典型的にER、PR、およびHER2について陰性で、サイトケラチン5/6、または上皮成長因子受容体について染色陽性である)を同定するため、基底上皮の免疫組織化学マーカーが提案されている。[ 257 ][ 258 ][ 259 ][ 260 ]蛋白発現を測定するためのこれらの方法に基づいて、多くの研究で大多数のBRCA1関連乳がんが基底上皮マーカーについて陽性であることが明らかにされている。[ 92 ][ 231 ][ 259 ]
前浸潤病変はBRCA表現型の一構成要素であるという証拠が増大している。BRCA1関連乳がんでは、非浸潤性に分類されるがんが相対的に欠けていることが、Breast Cancer Linkage Consortiumにより最初に報告され[ 229 ]、さらにその後のBRCA1/BRCA2キャリアを対象にした2件の研究[ 261 ][ 262 ]でも確認されている。しかしながら、非浸潤性乳管がん(DCIS)の369症例を対象にした研究では、BRCA1およびBRCA2病原性多様体が、それぞれ0.8%および2.4%に検出され、浸潤性乳がん患者を対象にした研究で過去に報告された保有率よりわずかに低いだけであった。[ 263 ]高リスクがんを専門とするクリニックにおける乳がん症例を対象にした1件のレトロスペクティブ研究では、BRCA関連乳がんの73例および病原性多様体陰性の146例において、前浸潤病変、特にDCISの類似した割合が明らかにされた。[ 264 ][ 265 ]AJの女性を対象にした高リスクがんを専門とするクリニックに紹介されたグループおよび非選択のグループの層別研究では、紹介された患者におけるDCISと浸潤性乳がんの有病率がほぼ同じであったのに対し、非選択の被験者ではDCIS症例が浸潤性症例の1/3であった。[ 266 ]同様に、過形成病変の有病率に関するデータは一貫しておらず、有病率が高い報告[ 267 ][ 268 ]も低い報告[ 262 ]もある。浸潤性乳がんと同様に、若い年齢で診断されたDCIS、または乳がんおよび/または卵巣がんの家族歴を伴うDCIS、あるいはその両者とも、BRCA1/BRCA2病原性多様体に関係している可能性が高い。[ 269 ]
総体的に証拠は、DCISがBRCA1/BRCA2多様体のスペクトラム、特にBRCA2に含まれると示唆している;しかしながら、DCIS患者(家族歴で選択を行っていない)における病原性多様体の保有率は5%未満である。[ 263 ][ 266 ]
BRCA2の病理学
BRCA2関連腫瘍の表現型は、BRCA1の表現型よりもさらに不均質であり、まだ十分に特徴付けられていないが、一般的にERおよびPR陽性である。[ 229 ][ 270 ][ 271 ]BRCA2病原性多様体キャリア2,392人を対象とした大規模な国際的シリーズでは、BRCA2病原性多様体キャリアに発生した腫瘍の23%のみがER陰性;36%がPR陰性;87%がHER2陰性;16%がトリプルネガティブであった。[ 235 ]12件の研究を通じて集められた、家族歴で選択されていないトリプルネガティブ乳がん患者1,824人についての大規模レポートでは、患者の2.7%にBRCA2病原性多様体が同定された。[ 246 ](この研究に関する詳しい情報については、本要約のBRCA1の病理学のセクションを参照のこと。)アイスランドの報告によれば、散発性腫瘍の対照群と比較して、BRCA2関連腫瘍では、管状形成が少なく、核多形性が多く認められたほか、細胞分裂能が高かった;しかしながら、単一のBRCA2創始者病原性多様体(999del5)がこの集団のほぼすべての遺伝性乳がんにみられるため、この観察の一般化可能性には限界がある。[ 272 ]北米とヨーロッパの1件の大規模ケースシリーズでは、BRCA2関連腫瘍に、連続する突出境界(pushing margins;浸潤パターンの病理組織学的記述の1つ)の割合が高く、管状形成および細胞分裂数が少ないと報告された。[ 273 ]BRCA2関連腫瘍では、小葉型および管状小葉型の組織型が過剰に発現するという報告もある。[ 230 ][ 270 ]要約すれば、BRCA2病原性多様体と関連する組織学的特徴は一貫していない。
散発性乳がんにおけるBRCA1とBRCA2の役割
BRCA1またはBRCA2の生殖細胞病原性多様体が存在すると乳がんに罹患する可能性がきわめて高くなるということを考慮に入れると、これらの遺伝子が、疾患のより一般的な非遺伝性形態の発生にも関与する可能性があると仮定するのは自然なことであった。BRCA1およびBRCA2の体細胞変異は、散発性乳がんの腫瘍においてまれであるが[ 274 ][ 275 ][ 276 ][ 277 ]、遺伝子プロモーターの高メチル化(BRCA1)およびヘテロ接合性の消失(LOH)(BRCA2)は頻度の高いイベントであるという証拠が増えている。実際、多くの乳がんではBRCA1 mRNAのレベルが低く、これは遺伝子プロモーターの高メチル化の結果であろう。[ 278 ][ 279 ][ 280 ]散発性乳がんの約10~15%はBRCA1プロモーターの高メチル化を有するようであり、他の機序によるBRCA1の発現減少はさらに多くが有する。基底細胞型乳がん(ER陰性、PR陰性、HER2陰性、およびサイトケラチン5/6陽性)では、BRCA1発現減少が他の腫瘍タイプよりも多くみられる。[ 281 ][ 282 ][ 283 ]BRCA1関連腫瘍の特徴もまた、BRCA1プロモーターの構造的高メチル化(constitutional methylation)に関連している。BRCA1生殖細胞病原性多様体がみられない女性のうち、40歳前に乳がんと診断された255人の女性の研究において、末梢血中におけるBRCA1のメチル化は、BRCA1に関連した病理学的特徴(例、高い分裂指数および多核細胞を含む増殖パターン)が腫瘍に複数みられた女性では31%に観察されたのに対し、対照群で観察されたメチル化は4%未満であった。[ 284 ](詳しい情報については、BRCA1の病理学のセクションを参照のこと。)BRCA2病原性多様体については高メチル化が報告されていないが、染色体13q上のBRCA2座は、乳がんにおける高頻度なLOHのターゲットである。[ 285 ][ 286 ]BRCA1またはBRCA2蛋白発現の消失を認める腫瘍に対して、ターゲット療法が開発されている。[ 287 ]
卵巣がんの病理学
BRCA1およびBRCA2病原性多様体を有する女性にみられる卵巣がんは、高悪性度の漿液性腺がんである可能性が高く、粘液性腫瘍または境界型腫瘍である可能性は低い。[ 288 ][ 289 ][ 290 ][ 291 ][ 292 ]卵管がんおよび腹膜がんも、BRCA関連疾患スペクトラムの一部である。[ 72 ][ 293 ]
卵巣がんの遺伝的素因を有する女性から切除した卵管の病理組織学的検査では、前がん性の表現型を示唆する異形成および過形成病変がみられる。[ 294 ][ 295 ]リスク低減のための手術時にBRCA病原性多様体キャリアから切除された付属器では、2~11%に潜伏がんが報告されている。[ 296 ][ 297 ][ 298 ]これらの潜伏病変のほとんどは卵管内にみられることから、BRCA関連卵巣がんの多くは、実質的に卵管に起源があるのではないかという仮説が導き出されている。特に、卵管采が卵巣表面にごく近いこと、卵管采が腹腔に露出していること、および卵管采の表面領域が広範なことに基づいて、卵管遠位部(卵管采を含む)は、BRCA病原性多様体キャリアにみられる高悪性度漿液性がんの一般的な起源とみなされている。[ 299 ]ミュラー管由来組織から発生する高悪性度漿液性がんは多中心性起源であるため、現在、International Federation of Gynecology and Obstetricsでは、卵巣がん、卵管がん、および腹膜がんの病期をまとめて判定している。用語の一貫性を保つために、高悪性度漿液性卵巣がんという用語を用いて、高悪性度骨盤漿液性がんを表すことがある。[ 300 ]
高悪性度漿液性卵巣がんでは、体細胞TP53突然変異の発生率が高い。[ 288 ][ 301 ]DNAマイクロアレイ技術によると、BRCA1関連、BRCA2関連、および散発性の卵巣がんでは、分子的な発がん経路が異なることが示唆される。[ 302 ]さらに、BRCA関連の卵巣がんは、内臓に転移する頻度が高いが、散発性卵巣がんは、腹膜の範囲にとどまることを示唆するデータがある。[ 303 ]
高悪性度漿液性がんとは異なり、低悪性度漿液性卵巣がんがBRCA1/BRCA2関連の疾患スペクトラムに含まれる可能性は低い。[ 304 ][ 305 ]
散発性卵巣がんにおけるBRCA1とBRCA2の役割
BRCA1またはBRCA2の生殖細胞多様体が存在すると卵巣がんに罹患する可能性がきわめて高くなるということを考慮に入れると、これらの遺伝子が、疾患のより一般的な非遺伝性形態の発生にも関与する可能性があると仮定するのは自然なことであった。BRCA1およびBRCA2の体細胞変異は、散発性卵巣がんの腫瘍においてまれであるが[ 274 ][ 275 ][ 276 ][ 277 ]、遺伝子プロモーターの高メチル化(BRCA1)およびLOH(BRCA2)は頻度の高いイベントであるという証拠が増えている。BRCA1またはBRCA2蛋白発現の消失は乳がんよりも卵巣がんにおいてよくみられ[ 306 ]、BRCA1の発現減少はシスプラチンに対する感受性増強およびこの疾患の生存率増加と関連している。[ 307 ][ 308 ]BRCA1またはBRCA2蛋白発現の消失を認める腫瘍に対して、ターゲット療法が開発されている。[ 287 ]
乳がんおよび/または婦人科がんに関連する他の高浸透度の症候群
リンチ症候群
リンチ症候群の特徴は、主に右側結腸がん、子宮内膜がん、卵巣がん、および他の結腸外のがん(腎盂、尿管、小腸、および膵臓のがんを含む)に対して感受性を示す常染色体優性遺伝、多重原発がん、ならびにがん発症年齢が若いことである。[ 309 ]この疾患は、ミスマッチ修復(MMR)遺伝子における生殖細胞多様体によるもので、この遺伝子はDNAミスマッチ多様体の修復に関与している。[ 310 ]MLH1およびMSH2遺伝子は、リンチ症候群で最もよくみられる感受性遺伝子で、観察される病原性多様体の80~90%を占めており[ 311 ][ 312 ]、これらに次いで多くみられる感受性遺伝子にはMSH6およびPMS2がある。[ 313 ][ 314 ][ 315 ][ 316 ][ 317 ][ 318 ](この症候群に関する詳しい情報については、大腸がんの遺伝学に関するPDQ要約のリンチ症候群のセクションを参照のこと。)
リンチ症候群の家系で大腸がんに続いて2番目に特徴的ながんは、子宮内膜がんである。Aldred Scott Warthin博士により記述された最初のFamily Gにおいてでさえ、多くの家系員で子宮内膜がんを含む結腸外のがんが見られることが示された。1999年の初版のアムステルダム基準には子宮内膜がんは含められなかった[ 319 ]が、アムステルダム基準はリスクのある家系を同定するために、リンチ症候群に関連する結腸外の腫瘍として子宮内膜がんを含めるように改訂された。[ 320 ]また、1997年のBethesdaガイドライン(2004年に改訂)には、リンチ症候群が疑われる場合の腫瘍検査を促すリンチ症候群関連がんとして子宮内膜がんおよび卵巣がんが含められた。[ 321 ][ 322 ]
リンチ症候群の女性における卵巣がんの生涯リスクは12%と高いことが推定され、報告されている卵巣がんのRRは、リンチ症候群が既知または疑われることが高リスク専門クリニックにより判明した家系に基づくと、3.6~13の範囲となっている。[ 323 ][ 324 ][ 325 ][ 326 ][ 327 ][ 328 ]リンチ症候群関連の病原性多様体に応じて、卵巣がんのリスクが異なる可能性がある。PMS2関連のリンチ症候群において、284家系を対象としたある研究では、卵巣がんのリスク増加が確認できなかった。[ 329 ]リンチ症候群病原性多様体キャリア3,119人を対象とした他のプロスペクティブ登録研究では、MLH1、MSH2、およびMSH6キャリアにおける卵巣がんの累積リスクが10%から17%の範囲であることが報告された。対照的に、PMS2に病原性多様体を有する女性67人において、追跡年数が303例・年で卵巣がんを発症した女性は0人であった。[ 330 ]全体として、卵巣がん管理に対して確定的な推奨を行うには、PMS2に病原性多様体を有する症例が少なすぎる。リンチ症候群関連卵巣がんの特徴として考えられるものには、診断時にInternational Federation of Gynecology and Obstetrics病期でI期およびII期が過度に多くみられること(報告では81.5%)、漿液サブタイプが少ないこと(報告では22.9%)、集団ベースシリーズおよびBRCA病原性多様体キャリアの両報告より10年生存率が良好なこと(報告では80.6%)などがある。[ 331 ][ 332 ]
リンチ症候群における乳がんのリスクについては、見解の相違がみられる。複数のレトロスペクティブ研究の結果は一致していないが、いくつかの研究ではリンチ症候群の個人が患う乳がんの一部にマイクロサテライト不安定性がみられた[ 333 ][ 334 ][ 335 ][ 336 ];これらの研究の1件は、リンチ症候群の個人における乳がんリスクを評価し、リスクは増大しないことを示した。[ 336 ]しかし、これまでで最大規模のプロスペクティブ研究では、Colon Cancer Family Registryで集められた罹患していない病原性多様体キャリア446人を対象に、[ 337 ]最長で10年間の追跡が実施され、乳がんのSIRは3.95と高値であった(95%CI、1.59-8.13;P = 0.001)。[ 337 ]その後、同じグループが以前に大腸がんと診断されたMMR遺伝子病原性多様体キャリア764人のデータを分析した。その結果、大腸がん後の乳がんの10年リスクは2%(95%CI、1%-4%)、SIRは1.76(95%CI、1.07-2.59)であった。[ 338 ]臨床的に参照されたリンチ症候群家系からなる英国のシリーズでは、確認を補正しようとして、MLH1キャリア157人で乳がんリスクが2倍高いが、他のMMR多様体のキャリアではそうではなかったことが示された。[ 339 ]分子的な腫瘍検査の結果が得られている15件の研究で、リンチ症候群における乳がんリスクのメタアナリシスの結果から、MMR病原性多様体キャリアにおける乳がん122人中62人(51%;95%CI、42%-60%)がMMR欠損であったことが明らかにされた。さらに、計21件の研究の乳がんリスクの推定から、MMR多様体のキャリアと非キャリアを比較した8件の研究では2~18倍のリスク増加が示された一方、13件の研究ではリンチ症候群と乳がんリスクとの関連を示す統計的な証拠は観察されなかった。[ 340 ]
その後の一部の研究で、以前に発表されたものよりも高い乳がんリスクの存在が示唆されている[ 341 ][ 342 ][ 343 ][ 344 ]が、これは一貫して観察されているわけではない。[ 345 ]主にMLH1およびMSH2キャリアを含むリンチ症候群の325のカナダ人家系を対象にした研究では、MSH2キャリアにおける乳がんの生涯累積リスクは22%と報告された。[ 341 ]同様に、リンチ症候群の423人の女性を対象にした研究でも乳がんリスクが高く、MLH1およびMSH2病原性多様体と比較してMSH6およびPMS2病原性多様体キャリアでは実質的にリスクが高かった。[ 342 ]実際、60歳までの乳がんリスクは、PMS2で37.7%、MSH6で31.1%、MSH2で16.1%、およびMLH1で15.5%であった。これらの知見は、リンチ症候群関連病原性多様体(MLH1、MSH2、MSH6、PMS2、EPCAMなど)を有する528人の患者を対象にした別の研究(この研究において、PMS2およびMSH6多様体は、大腸がんのみを有する患者と比較して、乳がんのみを有する患者においての方がはるかに頻度が高かった;P = 2.3 x 10-5)と一致していた。[ 343 ]乳がんとMSH6の関連を裏付ける追加のデータが、遺伝子検査を受けた米国の1万人を超えるがん患者の研究を介して提供された。[ 344 ]この研究の知見から、MSH6は乳がんと関連し、オッズ比(OR)は2.59(95%CI、1.35-5.44)であることが示された。以上を合わせると、これらの研究から、多重遺伝子パネル検査を受ける個人が多くなるにつれてリンチ症候群患者におけるリスクプロファイルが進化し続けている過程が強調されており、以前の研究と比較してPMS2およびMSH6病原性多様体を有する多くの個人が代表となっている。決定的なリスク推定がないため、リンチ症候群の個人は、家族歴に基づいて乳がんのスクリーニングを受ける。[ 97 ]
リンチ症候群の臨床管理に関する情報については、本要約の他の遺伝性乳がんおよび/または婦人科がん症候群の臨床管理のセクションのリンチ症候群のセクションを参照のこと。
リー-フラウメニ症候群(LFS)
乳がんもまた、まれにみられるLFSの1つの構成要素であり、LFSでは、染色体17p上でTP53遺伝子の生殖細胞多様体が実証されている。TP53は、染色体17p上に位置し、DNA塩基配列と結びつき、DNA損傷が起こると細胞成長および細胞増殖の負の調節因子として機能する53kdの核内リン蛋白をコードする。それはまた、プログラム細胞死の1つの活性要素である。[ 346 ]TP53遺伝子の不活性化または蛋白産物の破壊により、DNA損傷が持続し、悪性細胞の発生の可能性が生じる。[ 347 ][ 348 ]LFSについて広く使用されている臨床診断基準は2001年に最初にChompret et al.により策定され(Chompret Criteriaと呼ばれる)[ 349 ]、2009年に追加的に得られたデータに基づいて改訂された。[ 350 ]
LFSは、小児期における肉腫、脳腫瘍、白血病および副腎皮質がんのほか、閉経前乳がんを特徴とする。[ 347 ][ 351 ][ 352 ]
TP53における生殖細胞多様体は、乳がん症例の1%未満しか占めないと考えられている。[ 353 ]TP53関連乳がんは、多くの場合、HER2/neu陽性であることに加え、ER陽性、PR陽性、またはその両方でもある。[ 354 ][ 355 ][ 356 ]化学療法または放射線療法によるTP53関連腫瘍の治療を受けた患者では治療関連の二次悪性腫瘍のリスクが生じてくるとした証拠も存在する。
LFSを定義するための歴史的基準
リー-フラウメニ症候群という用語は1982年に初めて使用され[ 357 ]、その後、この症候群の古典的定義となった以下の基準は1988年にリーおよびフラウメニにより提案された[ 358 ]:
- 45歳以前の肉腫;
- FDRが45歳以前でがんを来した;および
- 別の近親者(FDRまたは第二度近親者[SDR])が、45歳以前でがんを来した、または年齢を問わず肉腫を来した。
その後、2001年に、Chompret et al.が[ 349 ]、肉腫、脳腫瘍、乳がん、および副腎皮質がんとして定義される狭い範囲のLFS腫瘍で、TP53遺伝子検査を推奨する臨床基準を系統的に策定した。この基準は以下の通りであった:
- 発端者が36歳以前に狭い範囲の腫瘍に罹患しており、かつ1人以上のFDRまたはSDRが46歳以前に狭い範囲の腫瘍(発端者が乳がんに罹患している場合は乳がん以外)に罹患しているか、多発性原発腫瘍に罹患している;もしくは
- 発端者に、家族歴に関係なく、多発性原発腫瘍があり、そのうち2つが狭い範囲の腫瘍に該当し、かつ最初の腫瘍が36歳以前に生じた;もしくは
- 発端者が、発症時の年齢および家族歴に関係なく、副腎皮質がんを来した。
これらの基準は、付加的に得られたデータ[ 348 ][ 359 ]に基づいて、2009年に以下のように改訂された[ 350 ]:
- 発端者が46歳以前にLFS腫瘍の範囲*に該当する腫瘍を来し、かつ1人以上のFDRまたはSDRが56歳以前にLFS腫瘍(発端者が乳がんに罹患している場合は乳がん以外)を来したか、多発性腫瘍を来した;もしくは
- 発端者が多発性腫瘍(多発性乳房腫瘍を除く)を来し、そのうち2つがLFS腫瘍の範囲に該当し、かつ最初のものが46歳以前に生じた;もしくは
- 家族歴に関係なく、患者が副腎皮質がんまたは脈絡叢がんを来した。
*2009年版Chompret基準はLFS腫瘍の範囲を以下のがんを含むものと定義している:軟部肉腫、骨肉腫、脳腫瘍、閉経前乳がん、副腎皮質がん、白血病、および気管支肺胞がん。
2015年に、Bougeard et al.が[ 352 ]、415人の病原性多様体キャリアのデータに基づいて基準を改定し、脈絡叢がんおよび副腎皮質がんに対して推奨されるものと同様に、検査の適応として、小児退形成性横紋筋肉腫および31歳以前の乳がんの存在を含めた。この基準は以下のように改訂された:
- 発端者が46歳以前にLFS腫瘍の範囲**に該当する腫瘍を来し、かつ1人以上のFDRまたはSDRが56歳以前にLFS腫瘍(発端者が乳がんに罹患している場合は乳がん以外)を来したか、多発性腫瘍を来した;もしくは
- 発端者が多発性腫瘍(多発性乳房腫瘍を除く)を来し、そのうち2つがLFS腫瘍の範囲に該当し、かつ最初のものが46歳以前に生じた;もしくは
- 家族歴に関係なく、副腎皮質がん、脈絡叢腫瘍、または胎児性退形成性横紋筋肉腫を来した患者;もしくは
- 31歳以前の乳がん。
**2015年版Chompret基準はLFS腫瘍の範囲を以下のがんを含むものと定義している:閉経前乳がん、軟部肉腫、骨肉腫、中枢神経系(CNS)腫瘍、および副腎皮質がん。
LFSの臨床的特徴
TP53の臨床検査のためにCity of Hope研究所に提出された525の標本の17%(n = 91)にTP53生殖細胞病原性多様体が同定された。[ 348 ]TP53病原性多様体を有する家系ではすべて、少なくとも1人の家系員に肉腫、乳がん、脳腫瘍、または副腎皮質がん(基本的ながん)が認められた。さらに、脈絡叢腫瘍を有する8人の患者では全員がTP53病原性多様体を有し、小児副腎皮質がんの患者では21人中14人が有していた。乳がんであるが他の基本的ながんの家族歴がない30~49歳の女性にはTP53多様体はみられなかった。
その後、主に2009年版のChompret基準[ 350 ]に基づいて検査されたフランス人の患者を対象にした1件の大規模臨床シリーズには 、214家系の病原性多様体キャリア415人が含められた。[ 352 ]この研究では、キャリアの43%に複数の悪性疾患が認められ、最初の腫瘍発症の平均年齢は24.9歳であった。小児における腫瘍の範囲は、骨肉腫、副腎皮質がん、CNS腫瘍、および軟部肉腫(集合的に23~30%に認められた)が特徴であったのに対し、成人における腫瘍の範囲には、主として乳がん(女性の79%)および軟部肉腫(キャリアの27%)が含まれていた。乳がんを有するが、LFSを示唆する追加の特徴を有さない31歳未満の女性におけるTP53病原性多様体の検出率は6%であった。遺伝子型-表現型の相関について評価したところ、臨床的重症度の傾斜が示され、発症時平均年齢はドミナントネガティブなミスセンス多様体を有する個人(21.3歳)の方が、すべての機能喪失型多様体(28.5歳)またはゲノム再編成(35.8歳)を有する個人よりも有意に低かった。副腎皮質がんを除いて、罹患小児のほとんどにドミナントネガティブなミスセンス病原性多様体が認められた。乳がんを有する127人の女性の病原性多様体キャリアのうち、31%が対側乳がんを発症した。40の腫瘍について受容体の状態に関する情報が得られ、55%がHER2陽性で、37%がトリプルポジティブ(すなわち、ER、PR、HER2が陽性)であったことが示された。病原性多様体キャリアでは複数の悪性腫瘍の割合が異常に高く(43%)、そのうち83%が異時性であった。最初の腫瘍の治療に放射線療法を受けたキャリア64人について治療記録が利用できた;このうち、19人(30%)が放射線照射野内に26の二次性腫瘍を発症し、その潜伏期間は2~26年(平均、10.7年)であった。
同様に、米国国立がん研究所のLFS StudyにおいてTP53病原性多様体が陽性の個人286人の結果から、累積がん発生率は男女とも70歳までにほぼ100%であることが示された。[ 360 ]性別、年齢、およびがんの種類によってかなりの変動が報告された。特に、累積がん発生率は女性では31歳および男性では46歳までに50%に達したが、男性のリスクは小児期および成人後期においてより高かった。上位4つのがんに対する男女別の累積がん発生率が以下の表8に示されている。1つのがんを有する個人のうち、49%が中央値で10年後に追加で少なくとも1つのがんを発症した。最初のがんまたは2番目のがんを発症する年齢別のリスクはほぼ同じであった。
表8.リー-フラウメニ症候群(LFS)に関連した最も一般的ながんに対する累積がんリスクa,b 70歳までの累積がんリスク a出典:Mai et al.[ ] b副腎皮質がん、白血病、気管支肺胞がんなど、他のがんも一連のLFSがん群の一部であると考えられている。[ ][ ] がんの種類 女性(%) 男性(%) 乳がん 54 – 軟部肉腫 15 22 脳腫瘍 6 19 骨肉腫 5 11 多重遺伝子(パネル)検査の使用が増加するにつれ、TP53の病原性多様体がLFSに特徴的な家族歴を有さない個人において予想外に同定されていることを認識することが重要である。[ 361 ]Chompret基準を満たさない個人または家系における単独のTP53病原性多様体の所見の臨床的意義は不明である。このため、予想外に生殖細胞TP53病原性多様体を有することが認められた個人については、その個人歴および家族歴を考慮に入れながら、がんリスクを解釈し、至適管理戦略を判断することがなおも重要である。
1件のコホート研究では、TP53生殖細胞病原性多様体を有した個人116人がNational Institutes of Health Clinical Centerでガドリニウムを併用したおよび併用しない複合的なスクリーニングを用いて年1回評価された。ベースラインのスクリーニングで8人の患者にがんが確認され(6.9%)、MRIに対する偽陽性率は34.5%(n = 40)であった。[ 362 ]乳房のMRIによる年1回の乳がんスクリーニングが推奨される[ 97 ];また、他のがんに対する追加的なスクリーニングも研究されるようになり、進展がみられている。[ 363 ][ 364 ]
PTEN過誤腫腫瘍症候群(コーデン症候群を含む)
コーデン症候群およびBannayan-Riley-Ruvalcaba症候群(BRRS)は、集合的にはPTEN過誤腫腫瘍症候群として知られる一連の疾患群の1つである。コーデン症候群と診断された患者の約85%とBRRS患者の約60%には、同定可能なPTEN病原性多様体が存在する。[ 365 ]さらに、臨床的に大きく異なった表現型を有する患者でPTEN病原性多様体が確認されている。[ 366 ]PTEN過誤腫腫瘍症候群という用語は、臨床症状にかかわらず、PTEN病原性多様体を有する患者であれば使用される。
PTENは、チロシン、セリン、およびスレオニンからリン酸基を除去する両特異性ホスファターゼとして機能する。PTENの病原性多様体はさまざまで、ナンセンス、ミスセンス、フレームシフト、およびスプライス部位の多様体がある。多様体の約40%はホスファターゼのコアモチーフをコードしているエクソン5に見られ、反復性の病原性多様体がいくつか観察されている。[ 367 ]PTEN遺伝子の5'末端またはホスファターゼコア内に多様体を有する人は、複数の器官系が罹患する傾向がある。[ 368 ]
コーデン症候群の診断に関する実用的な基準は既に公開されており、その後の更新も行われている。[ 369 ][ 370 ]これらには、大基準、小基準、ならびに特定の皮膚粘膜症状および成人発症型小脳異形成性神経節細胞腫(Lhermitte-Duclos病)からなる疾病特徴的基準がある。系統的文献レビューに基づく一連の基準の更新版が提示されており、[ 371 ]現在はNational Comprehensive Cancer Network(NCCN)のガイドラインで使用されている。[ 97 ]以前の基準とは対照的に、著者らは、どの特徴についても疾病特徴的なものとして分類するには証拠が不十分であると結論付けた。遺伝子検査、特に多重遺伝子パネルの使用の増加に伴い、コーデン症候群の臨床基準は、確認されている生殖細胞系PTEN病原性多様体を有していながら、これらの基準に適合しない個人の表現型に合わせて調整する必要がある。その調整が行われるまでは、臨床的所見と遺伝子検査結果のどちらに基づいて、コーデン症候群およびその他のPTEN過誤腫腫瘍症候群を定義するかについて、あいまいさが残る。American College of Medical Genetics and Genomics(ACMG)は、1)成人発症型Lhermitte-Duclos病、または2)コーデン症候群の診断について確立されている大基準または小基準のいずれか3つを満たす個人歴を有する、または第一度近親者のいる個人について、遺伝相談への紹介を考慮すべきであることを示唆している。[ 99 ]コーデン症候群の診断基準を含む詳細な推奨はNCCNおよびACMGのガイドラインに記載されている。[ 97 ][ 99 ]その上、PTEN病原性多様体の可能性を推定する臨床基準を用いる予想モデルが利用可能である;費用対効果解析によると、生殖細胞系PTEN検査は、多様体の可能性が10%より高ければ、費用対効果が高いことが示唆される。[ 372 ]
International Cowden Consortium(ICC)は、米国、ヨーロッパ、アジアにおいて、緩和されたPTEN検査のICC基準に適合する成人および小児患者の連続シリーズを10年にわたりプロスペクティブに募集した。[ 373 ]ほとんどの個人はコーデン症候群またはBRRSの診断に対する臨床基準を満たさなかった。募集に応じて検査を受けた3,399人のうち、発端者295人(8.8%)と73人の家系員が生殖細胞系PTEN病原性多様体を有することが明らかにされた。乳がん、甲状腺がん、子宮内膜がんに加えて、著者らはがんリスクに基づいて、黒色腫、腎がん、大腸がんを生殖細胞系PTEN病原性多様体に起因するがんスペクトルの一部と捉えるべきであると結論した。2つ目の研究では、生殖細胞系PTEN病原性多様体を有する患者約100人について、これらの知見が確認され、70歳までの累積がんリスクが85%であることが示された。[ 374 ]
PTEN病原性多様体は20万人に1人の頻度で発生すると推定されており[ 369 ]、ごく一部の遺伝性乳がんの原因であるに過ぎないが、PTENの機能の特徴が分かれば、その信号経路および正常な細胞生理の維持に貴重な洞察が得られる。[ 369 ][ 375 ]コーデン症候群の女性では、生涯乳がんリスクが25~50%であると推定される。[ 376 ]他の研究では、85%と高いリスクが報告されている[ 373 ][ 374 ][ 377 ][ 378 ];しかしながら、これらの研究では選択バイアスに関して懸念がある。他の遺伝性乳がんの形態と同様に、若年齢でしばしば発症し、両側性である。[ 379 ]子宮内膜がんの生涯リスクは研究されるコホートによって19~28%であると推定され、閉経前での発症リスクが高い。[ 373 ][ 374 ][ 380 ]この集団におけるPTEN病原性多様体の保有率は低いため、コーデン症候群による子宮内膜がんの割合は小さい。PTEN病原性多様体と卵巣がんのリスク増加の関連を示すデータはない。皮膚症状には、多発性外毛根鞘腫、口腔線維腫および乳頭腫、先端角化症、手掌足底角化症がある。既往歴または特徴的な皮膚所見が認められれば、コーデン症候群が疑われる。CNS症状には巨頭症、発達遅滞、および小脳異形成性神経節細胞腫が挙げられる。[ 381 ][ 382 ](PTEN過誤腫腫瘍症候群[コーデン症候群を含む]に関する詳しい情報については、大腸がんの遺伝学および皮膚がんの遺伝学に関するPDQ要約を参照のこと。)
びまん性胃がんおよび小葉がん症候群
1998年、びまん性胃がん(DGC)が複数例みられたマオリ人の3家系についてE-カドヘリン遺伝子CDH1が初めて報告され、後にこうした疾患は遺伝性びまん性胃がん(HDGC)と命名されるに至った。その後、HDGC家系における小葉がんの過剰発現が複数報告されている。[ 383 ]CDH1は染色体16q22.1上に存在し、カルシウム依存性の同種親和性接着分子であるE-カドヘリン蛋白(細胞接着、細胞極性、細胞内信号伝達、細胞分化と組織形態の維持に主要な役割を果たす)をコードする。[ 384 ]E-カドヘリンはさまざまなカテニンと結合して細胞質側の細胞接着複合体を安定させ、E-カドヘリンとアクチンフィラメントの相互作用を維持する。[ 385 ]CDH1の消失は、体細胞変異、LOH、または高メチル化の結果として発生し、ヒトのがんにおける脱分化と浸潤を引き起こす場合がある。[ 386 ][ 387 ]胃切除術検体に関する古典的な病理組織所見には、上皮内の印環細胞および/または印環細胞のパジェット様の拡がりなどがある。すべての胃がんの1~3%は、遺伝性胃がん症候群に起因する。[ 388 ]
HDGCは、胃の低分化型の浸潤性腺がんに関連する常染色体優性症候群であり、形成性胃組織炎として発現する。浸透度が高く、高度に致死的な症候群であり、臨床的なDGCのリスクは40~83%である。[ 383 ]HDGCでは、一列に並んだ(single file)均一な小型細胞を特徴とする小葉がんのリスクも増大する。浸潤性小葉がんはすべての乳がんの10~15%を占めるに過ぎないが、CDH1病原性多様体キャリアにおける小葉がんの生涯リスクは30~50%である。[ 385 ][ 386 ]CDH1に対するスクリーニングのガイドラインはさまざまであるが、家系内での複数のDGC症例、低年齢でのDGC、DGCの家系における小葉がんなどの基準が含まれる。これらの基準に適合する家系の約25%は、CDH1に病原性多様体を有することが明らかにされている。[ 388 ]CDH1病原性多様体はいくつかの小葉がんの家系で認められているが、胃がん家系では見つかっていない。[ 389 ]CDH1病原性多様体を有し、胃がんの家族歴がない個人の管理方法は不明である。[ 389 ]
ポイツ・ジェガース症候群(PJS)
ポイツ・ジェガース症候群は、早期発症型の常染色体優性疾患であり、口唇および口周辺と頬領域のメラニン細胞性斑、ならびに過誤腫性かつ腺腫性の多発性消化管ポリープが特徴である。[ 390 ][ 391 ][ 392 ]染色体19p13.3に存在するSTK11遺伝子の生殖細胞病原性多様体が、ほとんどのPJS家系で同定されている。[ 393 ][ 394 ][ 395 ][ 396 ][ 397 ]ポイツ・ジェガース症候群において最も一般的にみられるがんは消化管のがんである。しかしながら、他の臓器も悪性腫瘍を発症するリスクが高い。例えば、累積リスクは乳がんで32~54%[ 398 ][ 399 ][ 400 ]、卵巣がん(主に卵巣性索腫瘍)で21%と推定されている。[ 398 ]膵がんのリスクは、一般集団の100倍を超えると推定されている。[ 398 ]PJS患者において、系統的レビューでは、生涯の累積がんリスクが全部位を合わせて最大93%であることが明らかになった。[ 398 ][ 401 ]表9に、これらの腫瘍の累積リスクを示している。
PJSの女性は、非常に侵攻性が高いまれな子宮頸部の腺がんである頸部悪性腺腫の素因も有している。[ 402 ]加えて、PJSの女性では良性の卵巣性索腫瘍と輪状細管が発生することがよくあり、一方でPJSの男性はセルトリ細胞腫瘍の素因を有している;[ 403 ]これら2種類の腫瘍はいずれも悪性ではないが、エストロゲン産生の増加に関連する症状を引き起こす場合がある。
公表されている文献によると、PJS患者では悪性腫瘍のリスクがきわめて高いとみられるが、選択バイアスおよび紹介バイアスが、これらのリスクの過大評価につながっている可能性を考慮すべきである。
表9.規定年齢までのポイツ・ジェガース症候群における累積がんリスクa 部位 年齢(歳) 累積リスク(%) 参考文献 GI = 消化管。 a Macmillan Publishers社から許諾を得て転載:Gastroenterology[ ], copyright 2010. b 一般集団と比較した全累積リスクは、頸部がんおよび精巣腫瘍を除いて増加した(P < 0.05)。 c 消化管がんには、大腸がん、小腸がん、胃がん、食道がん、および膵がんを含む。 d Westerman et al.: 消化管がんに膵がんは含まない。[ ] e 頸部悪性腺腫または精巣セルトリ細胞腫瘍を含まない。 すべてのがん 60–70 37–93 [ ][ ][ ][ ][ ][ ] 消化管がんc, d 60–70 38–66 [ ][ ][ ][ ] 婦人科がん 60–70 13–18 [ ][ ] 原発腫瘍別 胃がん 65 29 [ ] 小腸がん 65 13 [ ] 大腸がん 65 39 [ ][ ] 膵がん 65–70 11–36 [ ][ ] 肺がん 65–70 7–17 [ ][ ][ ] 乳がん 60–70 32–54 [ ][ ][ ] 子宮がん 65 9 [ ] 卵巣がん 65 21 [ ] 頸部がんe 65 10 [ ] 精巣腫瘍e 65 9 [ ] ポイツ・ジェガース遺伝子
ポイツ・ジェガース症候群は、染色体19p13上に位置するSTK11(LKB1とも呼ばれる)腫瘍抑制遺伝子の病原性多様体により引き起こされる。[ 394 ][ 395 ]家族性大腸腺腫症にみられる腺腫とは異なり、ポイツ・ジェガース症候群で生じるポリープは過誤腫である。ポイツ・ジェガース症候群患者の過誤腫性ポリープとがんに関する諸研究から、2ヒット仮説に一致するアレルの不均衡(LOH)が示されており、よってSTK11は腫瘍抑制遺伝子であることが実証されている。[ 406 ][ 407 ]しかしながら、ヘテロ接合性のSTK11ノックアウトマウスでは、残存する野生型アレルの不活化がなくても過誤腫が発生することから、ポイツ・ジェガース症候群における最初の腫瘍発生には、ハプロ不全のみで十分な可能性が示唆される。[ 408 ]STK11+/-マウスに起こるがんはその後LOHを示す[ 409 ];実際、STK11+/-における病原性多様体がヘテロ接合性で、TP53-/-における病原性多様体がホモ接合性の複合型ミュータントマウスでは、過誤腫とがんのいずれについても発症が早まっている。[ 410 ]
STK11遺伝子の生殖細胞多様体は、ナンセンス、フレームシフト、ミスセンスなどの一連の多様体のほか、スプライス部位多様体および広範な欠失を示す。[ 393 ][ 399 ]
多様体の約85%は、発現タンパク質のキナーゼドメイン領域に局在している。遺伝子型-表現型の強い相関は特定されていない。[ 399 ]多様体の最大30%は、STK11のエクソンを1つまたは複数含む大規模欠失であり、ポイツ・ジェガース症候群が疑われる症例における欠失解析の重要性が強調される。[ 393 ]
STK11がポイツ・ジェガース症候群を引き起こすことが明白に実証されている。DNAの直接塩基配列決定法を用いた初期の推定では、STK11における病原性多様体の検出率が50%であることが示されたが、広範な欠失を検出する技術を加えた研究では、ポイツ・ジェガース症候群の臨床基準を満たす患者のうち、94%までに病原性多様体が認められている。[ 393 ][ 401 ][ 411 ]これらの研究結果を考えると、他の主要な遺伝子がポイツ・ジェガース症候群を引き起こす可能性は低い。
臨床管理
ポイツ・ジェガース症候群ではがんの累積リスクが高いため、さまざまなスクリーニングが推奨されており、大腸がんの遺伝学に関するPDQ要約のポイツ・ジェガース症候群(PJS)におけるがん診断とサーベイランスのために公表されている推奨事項の表に要約されている。
PALB2
PALB2(BRCA2のパートナーおよびローカライザー)はBRCA2蛋白と相互作用し、相同的組換えおよび二本鎖DNA修復に関与している。BRIP1およびBRCA2と同様に、PALB2における両アレル性病原性多様体もまたファンコニー貧血を引き起こすことが示されている。[ 412 ]
PALB2病原性多様体は、さまざまな集団を対象に家族性乳がんおよび早期発症型乳がんを検討した多くの小規模研究でスクリーニングが実施されている。[ 14 ][ 413 ][ 414 ][ 415 ][ 416 ][ 417 ][ 418 ][ 419 ][ 420 ][ 421 ][ 422 ][ 423 ][ 424 ][ 425 ][ 426 ][ 427 ][ 428 ][ 429 ][ 430 ]病原性多様体の保有率は0.4~3.9%の範囲に及んでいる。BRIP1およびCHEK2と同様に、遺伝性乳がんを認める家系ではPALB2病原性多様体の分離が不完全であった。[ 413 ]対側乳がん症例559人および片側乳がんの対応対照565人において、病因性(切断型)PALB2病原性多様体が症例の0.9%に特定され、対照では認められなかった(RR、5.3;95%CI、1.8-13.2)。[ 424 ]
PALB2の機能喪失多様体を有する154家系に基づくデータは、この遺伝子が、リスクがBRCA2と重複する遺伝性乳がんの重要な原因である可能性を示唆している。[ 431 ]この研究では、PALB2病原性多様体を有する154家系からの家系員362人を対象とした分析から、70歳までの女性の乳がんの絶対リスクは、乳がんの家族歴がない女性における33%(95%CI、24%-44%)から、早期発症型乳がんのFDRが2人以上いる女性における58%(95%CI、50%-66%)までの範囲であることが示された。さらに、HER2の状態が判明している乳がん症例63例のうち、30%がトリプルネガティブ乳がんであった。これより初期のフィンランドの研究は、PALB2創始者病原性多様体(c.1592delT)が70歳までに40%の乳がんリスクをもたらし[ 414 ]、トリプルネガティブがんの高い発生率(54%)や、より低い生存率に関連することを報告した。[ 415 ]多くの集団で、早期発症型乳がんおよび家族性乳がんに病原性多様体が認められている。[ 416 ][ 417 ]12件の研究を通じて集められた、家族歴で選択されていないトリプルネガティブ乳がん患者1,824人についての大規模レポートでは、患者の1.2%にPALB2病原性多様体が同定された。[ 246 ](この研究に関する詳しい情報については、本要約のBRCA1の病理学のセクションを参照のこと。)
後に乳がんの非選択女性12,529人以上と対照4,702人を対象として実施されたポーランドの研究では、PALB2病原性多様体が116例(0.93%;95%CI、0.76%-1.09%)および対照10例(0.21%;95%CI、0.08%-0.34%)で検出され、乳がんのORは4.39(95%CI、2.30-8.37)であった。[ 432 ]この研究の知見は、PALB2病原性多様体を有する75歳までの女性において乳がんリスクがかなり高いこと(24~40%)を裏付けている。対側乳がんの5年累積発生率は、PALB2病原性多様体を有する女性において10%であったのに対し、BRCA1病原性多様体を有する女性では17%であり、いずれの遺伝子にも多様体を有さない女性では3%であった。さらに、PALB2病原性多様体を有する乳がん女性の10年生存率は48%(95%CI、36.5%-63.2%)であったのに対し、BRCA1病原性多様体を有する女性では72.0%、いずれの遺伝子にも多様体がみられない女性では74.7%であった。PALB2キャリアが2cm未満の腫瘍を有する場合の転帰(10年生存率82.4%)と比較して、2cm以上の乳房腫瘍を有する場合の転帰ははるかに不良(10年生存率32.4%)であった。PALB2病原性多様体を有する女性の約3分の1はトリプルネガティブ乳がんを患っており、乳がん診断時の平均年齢は53.3歳であった。
これまでで最大規模の研究によると、PALB2に病原性多様体を有する524家系が国際的な取り組みを介して募集され、女性における乳がんのRRは7.18(95%CI、5.82-8.85)で、80歳までの乳がんリスクが53%(95%CI、44%-63%)であることが報告された。[ 433 ]その他に報告されたリスク上昇は、卵巣がん(RR、2.91;95%CI、1.40-6.04)で生涯リスクが5%(95%CI、2%-10%)、膵がん(RR、2.37;95%CI、1.24-4.50)で生涯リスクが2~3%(女性で95%CI、1%-4%;男性で95%CI、2%-5%)、および男性乳がん(RR、7.34;95%CI、1.28-42.18)で生涯リスクが1%(95%CI、0.2%-5%)などであった。これらの知見から、女性における遺伝性乳がん遺伝子としてのPALB2の役割が確認されると同時に、卵巣がん、膵がん、および男性乳がんとの関連性が確固たるものになる。
男性の乳がんがPALB2病原性多様体陽性乳がんの家系に観察されている。[ 14 ][ 418 ][ 431 ]男性の乳がん症例115人を対象とした研究では、18人の男性がBRCA2病原性多様体で、別の2人の男性が病原性または病原性と予測されるPALB2多様体であった(この研究における生殖細胞多様体の約10%を占め、全サンプルでは1~2%を占める)。[ 14 ]154家系の研究では、PALB2病原性多様体キャリアの男性における乳がんのRRは、一般集団に対して8.30と推定された(95%CI、0.77-88.56;P = 0.08)。[ 431 ]
膵腫瘍にPALB2病原性多様体が特定され、家族性膵臓患者96人中3%に生殖細胞病原性多様体が検出された後に[ 434 ]、数多くの研究が膵がんにおけるPALB2の役割を指摘している。PALB2病原性多様体が検出されたのは、家族性膵がんの81家系で3.7%[ 435 ]、膵がんの個人歴または家族歴があるBRCA1/BRCA2病原性多様体陰性の乳がん患者94人で2.1%であった。[ 436 ]比較的小規模な2件の研究-1件は膵がんの個人歴または家族歴があるBRCA1/BRCA2病原性多様体陰性の発端者77人を対象とした研究で、その中の半数がAJの子孫であり、もう1件は乳がんまたは卵巣がんの個人歴または家族歴があるイタリア人の膵がん患者29人を対象とした-では、どのようなPALB2病原性多様体も検出できなかった。[ 437 ][ 438 ]BRCA1/BRCA2陰性で、PALB2病原性多様体陽性の乳がん発端者33人の近親者では、膵がんが6倍多いことが認められた。[ 418 ]
全体的に、家族性乳がんにおいて観察されたPALB2病原性多様体の保有率は、膵がんおよび卵巣がんの個人歴および家族歴に関連する確認に応じて変化するが、すべての研究で観察された病原性多様体の割合は4%未満であった。データは、特に強い家族歴を有する人において、乳がんのRRがBRCA2の場合と重複している可能性を示唆している;したがって、より大規模な研究でがんリスクの推定を改良することが依然として重要である。さらに、他のがん(例、膵がん)のリスクはほとんど確定されていない。この集団でのPALB2病原性多様体の保有率が低いことから、最適な検査対象者と適切な管理法を明らかにするために、さらなるデータが必要とされる。
de novo病原性多様体の発生率
1990年代までは、遺伝的に受け継いだ乳がんおよび卵巣がん症候群の診断は、臨床症状と家族歴に基づいて下されていた。現在では、こうした症候群に関与する遺伝子の一部が同定されているため、これらの集団における自然病原性多様体の発生率(de novo病原性多様体の発生率)を推定しようとしている研究は2~3件しかない。興味深いことに、ポイツ・ジェガース症候群、PTEN過誤腫症候群、およびLFSはいずれも自然病原性多様体の発生率が高く、10~30%であると考えられている一方[ 439 ][ 440 ][ 441 ][ 442 ]、主として発表されている少数の症例報告によればBRCA遺伝子のde novo病原性多様体の推定値は低いと考えられている。[ 443 ][ 444 ][ 445 ][ 446 ][ 447 ][ 448 ][ 449 ][ 450 ][ 451 ]また、乳がん患者がBRCA病原性多様体の検査を受け、de novo多様体が同定されたケースシリーズは1件のみである。具体的には、散発性乳がん患者193人を対象にしたこの研究で、17の病原性多様体が検出され、そのうち1つがde novo病原性多様体であると確認された。[ 443 ]したがって、de novo病原性多様体の発生率は低いと考えられ、実施された少数の研究に基づけば5%以下になると考えられる。[ 443 ][ 444 ][ 445 ][ 446 ][ 447 ][ 448 ][ 449 ][ 450 ][ 451 ]同様に、リンチ症候群に関連したMMR遺伝子のde novo病原性多様体の推定値は低く、0.9~5%であると考えられている。[ 452 ][ 453 ][ 454 ]しかしながら、BRCA遺伝子およびリンチ症候群遺伝子における自然病原性多様体率のこうした推定値は、さまざまな集団の非実父の割合の推定値(0.6~3.3%)と重複していると考えられるため[ 455 ][ 456 ][ 457 ]、これらの遺伝子に対するde novo病原性多様体率はかなり低くなる。
参考文献- Phipps RF, Perry PM: Familial breast cancer. Postgrad Med J 64 (757): 847-9, 1988.[PUBMED Abstract]
- Sellers TA, Potter JD, Rich SS, et al.: Familial clustering of breast and prostate cancers and risk of postmenopausal breast cancer. J Natl Cancer Inst 86 (24): 1860-5, 1994.[PUBMED Abstract]
- Newman B, Austin MA, Lee M, et al.: Inheritance of human breast cancer: evidence for autosomal dominant transmission in high-risk families. Proceedings of the National Academy of Sciences 85 (9): 3044-48, 1988.[PUBMED Abstract]
- Hall JM, Lee MK, Newman B, et al.: Linkage of early-onset familial breast cancer to chromosome 17q21. Science 250 (4988): 1684-9, 1990.[PUBMED Abstract]
- Narod SA, Feunteun J, Lynch HT, et al.: Familial breast-ovarian cancer locus on chromosome 17q12-q23. Lancet 338 (8759): 82-3, 1991.[PUBMED Abstract]
- Brose MS, Rebbeck TR, Calzone KA, et al.: Cancer risk estimates for BRCA1 mutation carriers identified in a risk evaluation program. J Natl Cancer Inst 94 (18): 1365-72, 2002.[PUBMED Abstract]
- Thompson D, Easton DF; Breast Cancer Linkage Consortium: Cancer Incidence in BRCA1 mutation carriers. J Natl Cancer Inst 94 (18): 1358-65, 2002.[PUBMED Abstract]
- Risch HA, McLaughlin JR, Cole DE, et al.: Population BRCA1 and BRCA2 mutation frequencies and cancer penetrances: a kin-cohort study in Ontario, Canada. J Natl Cancer Inst 98 (23): 1694-706, 2006.[PUBMED Abstract]
- Tai YC, Domchek S, Parmigiani G, et al.: Breast cancer risk among male BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 99 (23): 1811-4, 2007.[PUBMED Abstract]
- Wooster R, Neuhausen SL, Mangion J, et al.: Localization of a breast cancer susceptibility gene, BRCA2, to chromosome 13q12-13. Science 265 (5181): 2088-90, 1994.[PUBMED Abstract]
- Gayther SA, Mangion J, Russell P, et al.: Variation of risks of breast and ovarian cancer associated with different germline mutations of the BRCA2 gene. Nat Genet 15 (1): 103-5, 1997.[PUBMED Abstract]
- Cancer risks in BRCA2 mutation carriers. The Breast Cancer Linkage Consortium. J Natl Cancer Inst 91 (15): 1310-6, 1999.[PUBMED Abstract]
- Liede A, Karlan BY, Narod SA: Cancer risks for male carriers of germline mutations in BRCA1 or BRCA2: a review of the literature. J Clin Oncol 22 (4): 735-42, 2004.[PUBMED Abstract]
- Ding YC, Steele L, Kuan CJ, et al.: Mutations in BRCA2 and PALB2 in male breast cancer cases from the United States. Breast Cancer Res Treat 126 (3): 771-8, 2011.[PUBMED Abstract]
- Tonin P, Weber B, Offit K, et al.: Frequency of recurrent BRCA1 and BRCA2 mutations in Ashkenazi Jewish breast cancer families. Nat Med 2 (11): 1179-83, 1996.[PUBMED Abstract]
- Easton DF, Bishop DT, Ford D, et al.: Genetic linkage analysis in familial breast and ovarian cancer: results from 214 families. The Breast Cancer Linkage Consortium. Am J Hum Genet 52 (4): 678-701, 1993.[PUBMED Abstract]
- Venkitaraman AR: Cancer susceptibility and the functions of BRCA1 and BRCA2. Cell 108 (2): 171-82, 2002.[PUBMED Abstract]
- Narod SA, Foulkes WD: BRCA1 and BRCA2: 1994 and beyond. Nat Rev Cancer 4 (9): 665-76, 2004.[PUBMED Abstract]
- An Open Access On-Line Breast Cancer Mutation Data Base [Database]. Bethesda, Md: National Human Genome Research Institute, 2002. Available online. Last accessed January 22, 2020.[PUBMED Abstract]
- Ford D, Easton DF, Peto J: Estimates of the gene frequency of BRCA1 and its contribution to breast and ovarian cancer incidence. Am J Hum Genet 57 (6): 1457-62, 1995.[PUBMED Abstract]
- Whittemore AS, Gong G, John EM, et al.: Prevalence of BRCA1 mutation carriers among U.S. non-Hispanic Whites. Cancer Epidemiol Biomarkers Prev 13 (12): 2078-83, 2004.[PUBMED Abstract]
- Eng C, Brody LC, Wagner TM, et al.: Interpreting epidemiological research: blinded comparison of methods used to estimate the prevalence of inherited mutations in BRCA1. J Med Genet 38 (12): 824-33, 2001.[PUBMED Abstract]
- Unger MA, Nathanson KL, Calzone K, et al.: Screening for genomic rearrangements in families with breast and ovarian cancer identifies BRCA1 mutations previously missed by conformation-sensitive gel electrophoresis or sequencing. Am J Hum Genet 67 (4): 841-50, 2000.[PUBMED Abstract]
- Walsh T, Casadei S, Coats KH, et al.: Spectrum of mutations in BRCA1, BRCA2, CHEK2, and TP53 in families at high risk of breast cancer. JAMA 295 (12): 1379-88, 2006.[PUBMED Abstract]
- Palma MD, Domchek SM, Stopfer J, et al.: The relative contribution of point mutations and genomic rearrangements in BRCA1 and BRCA2 in high-risk breast cancer families. Cancer Res 68 (17): 7006-14, 2008.[PUBMED Abstract]
- Stadler ZK, Saloustros E, Hansen NA, et al.: Absence of genomic BRCA1 and BRCA2 rearrangements in Ashkenazi breast and ovarian cancer families. Breast Cancer Res Treat 123 (2): 581-5, 2010.[PUBMED Abstract]
- Judkins T, Rosenthal E, Arnell C, et al.: Clinical significance of large rearrangements in BRCA1 and BRCA2. Cancer 118 (21): 5210-6, 2012.[PUBMED Abstract]
- Shannon KM, Rodgers LH, Chan-Smutko G, et al.: Which individuals undergoing BRACAnalysis need BART testing? Cancer Genet 204 (8): 416-22, 2011.[PUBMED Abstract]
- Jackson SA, Davis AA, Li J, et al.: Characteristics of individuals with breast cancer rearrangements in BRCA1 and BRCA2. Cancer 120 (10): 1557-64, 2014.[PUBMED Abstract]
- Weitzel JN, Lagos VI, Herzog JS, et al.: Evidence for common ancestral origin of a recurring BRCA1 genomic rearrangement identified in high-risk Hispanic families. Cancer Epidemiol Biomarkers Prev 16 (8): 1615-20, 2007.[PUBMED Abstract]
- Plon SE, Eccles DM, Easton D, et al.: Sequence variant classification and reporting: recommendations for improving the interpretation of cancer susceptibility genetic test results. Hum Mutat 29 (11): 1282-91, 2008.[PUBMED Abstract]
- Frank TS, Deffenbaugh AM, Reid JE, et al.: Clinical characteristics of individuals with germline mutations in BRCA1 and BRCA2: analysis of 10,000 individuals. J Clin Oncol 20 (6): 1480-90, 2002.[PUBMED Abstract]
- Nanda R, Schumm LP, Cummings S, et al.: Genetic testing in an ethnically diverse cohort of high-risk women: a comparative analysis of BRCA1 and BRCA2 mutations in American families of European and African ancestry. JAMA 294 (15): 1925-33, 2005.[PUBMED Abstract]
- Hall MJ, Reid JE, Burbidge LA, et al.: BRCA1 and BRCA2 mutations in women of different ethnicities undergoing testing for hereditary breast-ovarian cancer. Cancer 115 (10): 2222-33, 2009.[PUBMED Abstract]
- Szabo C, Masiello A, Ryan JF, et al.: The breast cancer information core: database design, structure, and scope. Hum Mutat 16 (2): 123-31, 2000.[PUBMED Abstract]
- Spurdle AB, Healey S, Devereau A, et al.: ENIGMA--evidence-based network for the interpretation of germline mutant alleles: an international initiative to evaluate risk and clinical significance associated with sequence variation in BRCA1 and BRCA2 genes. Hum Mutat 33 (1): 2-7, 2012.[PUBMED Abstract]
- Goldgar DE, Easton DF, Deffenbaugh AM, et al.: Integrated evaluation of DNA sequence variants of unknown clinical significance: application to BRCA1 and BRCA2. Am J Hum Genet 75 (4): 535-44, 2004.[PUBMED Abstract]
- Thompson D, Easton DF, Goldgar DE: A full-likelihood method for the evaluation of causality of sequence variants from family data. Am J Hum Genet 73 (3): 652-5, 2003.[PUBMED Abstract]
- Spearman AD, Sweet K, Zhou XP, et al.: Clinically applicable models to characterize BRCA1 and BRCA2 variants of uncertain significance. J Clin Oncol 26 (33): 5393-400, 2008.[PUBMED Abstract]
- Gómez García EB, Oosterwijk JC, Timmermans M, et al.: A method to assess the clinical significance of unclassified variants in the BRCA1 and BRCA2 genes based on cancer family history. Breast Cancer Res 11 (1): R8, 2009.[PUBMED Abstract]
- Goldgar DE, Easton DF, Byrnes GB, et al.: Genetic evidence and integration of various data sources for classifying uncertain variants into a single model. Hum Mutat 29 (11): 1265-72, 2008.[PUBMED Abstract]
- Fleming MA, Potter JD, Ramirez CJ, et al.: Understanding missense mutations in the BRCA1 gene: an evolutionary approach. Proc Natl Acad Sci U S A 100 (3): 1151-6, 2003.[PUBMED Abstract]
- Tavtigian SV, Deffenbaugh AM, Yin L, et al.: Comprehensive statistical study of 452 BRCA1 missense substitutions with classification of eight recurrent substitutions as neutral. J Med Genet 43 (4): 295-305, 2006.[PUBMED Abstract]
- Mirkovic N, Marti-Renom MA, Weber BL, et al.: Structure-based assessment of missense mutations in human BRCA1: implications for breast and ovarian cancer predisposition. Cancer Res 64 (11): 3790-7, 2004.[PUBMED Abstract]
- Abkevich V, Zharkikh A, Deffenbaugh AM, et al.: Analysis of missense variation in human BRCA1 in the context of interspecific sequence variation. J Med Genet 41 (7): 492-507, 2004.[PUBMED Abstract]
- Couch FJ, Rasmussen LJ, Hofstra R, et al.: Assessment of functional effects of unclassified genetic variants. Hum Mutat 29 (11): 1314-26, 2008.[PUBMED Abstract]
- Chenevix-Trench G, Healey S, Lakhani S, et al.: Genetic and histopathologic evaluation of BRCA1 and BRCA2 DNA sequence variants of unknown clinical significance. Cancer Res 66 (4): 2019-27, 2006.[PUBMED Abstract]
- Ostrow KL, McGuire V, Whittemore AS, et al.: The effects of BRCA1 missense variants V1804D and M1628T on transcriptional activity. Cancer Genet Cytogenet 153 (2): 177-80, 2004.[PUBMED Abstract]
- Wu K, Hinson SR, Ohashi A, et al.: Functional evaluation and cancer risk assessment of BRCA2 unclassified variants. Cancer Res 65 (2): 417-26, 2005.[PUBMED Abstract]
- Weitzel JN, Lagos V, Blazer KR, et al.: Prevalence of BRCA mutations and founder effect in high-risk Hispanic families. Cancer Epidemiol Biomarkers Prev 14 (7): 1666-71, 2005.[PUBMED Abstract]
- Mefford HC, Baumbach L, Panguluri RC, et al.: Evidence for a BRCA1 founder mutation in families of West African ancestry. Am J Hum Genet 65 (2): 575-8, 1999.[PUBMED Abstract]
- Rosenthal E, Moyes K, Arnell C, et al.: Incidence of BRCA1 and BRCA2 non-founder mutations in patients of Ashkenazi Jewish ancestry. Breast Cancer Res Treat 149 (1): 223-7, 2015.[PUBMED Abstract]
- Frey MK, Kopparam RV, Ni Zhou Z, et al.: Prevalence of nonfounder BRCA1/2 mutations in Ashkenazi Jewish patients presenting for genetic testing at a hereditary breast and ovarian cancer center. Cancer 125 (5): 690-697, 2019.[PUBMED Abstract]
- Prevalence and penetrance of BRCA1 and BRCA2 mutations in a population-based series of breast cancer cases. Anglian Breast Cancer Study Group. Br J Cancer 83 (10): 1301-8, 2000.[PUBMED Abstract]
- Papelard H, de Bock GH, van Eijk R, et al.: Prevalence of BRCA1 in a hospital-based population of Dutch breast cancer patients. Br J Cancer 83 (6): 719-24, 2000.[PUBMED Abstract]
- Loman N, Johannsson O, Kristoffersson U, et al.: Family history of breast and ovarian cancers and BRCA1 and BRCA2 mutations in a population-based series of early-onset breast cancer. J Natl Cancer Inst 93 (16): 1215-23, 2001.[PUBMED Abstract]
- Malone KE, Daling JR, Doody DR, et al.: Prevalence and predictors of BRCA1 and BRCA2 mutations in a population-based study of breast cancer in white and black American women ages 35 to 64 years. Cancer Res 66 (16): 8297-308, 2006.[PUBMED Abstract]
- Newman B, Mu H, Butler LM, et al.: Frequency of breast cancer attributable to BRCA1 in a population-based series of American women. JAMA 279 (12): 915-21, 1998.[PUBMED Abstract]
- Basham VM, Lipscombe JM, Ward JM, et al.: BRCA1 and BRCA2 mutations in a population-based study of male breast cancer. Breast Cancer Res 4 (1): R2, 2002.[PUBMED Abstract]
- Risch HA, McLaughlin JR, Cole DE, et al.: Prevalence and penetrance of germline BRCA1 and BRCA2 mutations in a population series of 649 women with ovarian cancer. Am J Hum Genet 68 (3): 700-10, 2001.[PUBMED Abstract]
- Rubin SC, Blackwood MA, Bandera C, et al.: BRCA1, BRCA2, and hereditary nonpolyposis colorectal cancer gene mutations in an unselected ovarian cancer population: relationship to family history and implications for genetic testing. Am J Obstet Gynecol 178 (4): 670-7, 1998.[PUBMED Abstract]
- Pal T, Permuth-Wey J, Betts JA, et al.: BRCA1 and BRCA2 mutations account for a large proportion of ovarian carcinoma cases. Cancer 104 (12): 2807-16, 2005.[PUBMED Abstract]
- Struewing JP, Hartge P, Wacholder S, et al.: The risk of cancer associated with specific mutations of BRCA1 and BRCA2 among Ashkenazi Jews. N Engl J Med 336 (20): 1401-8, 1997.[PUBMED Abstract]
- Gabai-Kapara E, Lahad A, Kaufman B, et al.: Population-based screening for breast and ovarian cancer risk due to BRCA1 and BRCA2. Proc Natl Acad Sci U S A 111 (39): 14205-10, 2014.[PUBMED Abstract]
- Metcalfe KA, Poll A, Royer R, et al.: Screening for founder mutations in BRCA1 and BRCA2 in unselected Jewish women. J Clin Oncol 28 (3): 387-91, 2010.[PUBMED Abstract]
- King MC, Marks JH, Mandell JB, et al.: Breast and ovarian cancer risks due to inherited mutations in BRCA1 and BRCA2. Science 302 (5645): 643-6, 2003.[PUBMED Abstract]
- Gershoni-Baruch R, Dagan E, Fried G, et al.: Significantly lower rates of BRCA1/BRCA2 founder mutations in Ashkenazi women with sporadic compared with familial early onset breast cancer. Eur J Cancer 36 (8): 983-6, 2000.[PUBMED Abstract]
- Hodgson SV, Heap E, Cameron J, et al.: Risk factors for detecting germline BRCA1 and BRCA2 founder mutations in Ashkenazi Jewish women with breast or ovarian cancer. J Med Genet 36 (5): 369-73, 1999.[PUBMED Abstract]
- Struewing JP, Coriaty ZM, Ron E, et al.: Founder BRCA1/2 mutations among male patients with breast cancer in Israel. Am J Hum Genet 65 (6): 1800-2, 1999.[PUBMED Abstract]
- Hirsh-Yechezkel G, Chetrit A, Lubin F, et al.: Population attributes affecting the prevalence of BRCA mutation carriers in epithelial ovarian cancer cases in Israel. Gynecol Oncol 89 (3): 494-8, 2003.[PUBMED Abstract]
- Moslehi R, Chu W, Karlan B, et al.: BRCA1 and BRCA2 mutation analysis of 208 Ashkenazi Jewish women with ovarian cancer. Am J Hum Genet 66 (4): 1259-72, 2000.[PUBMED Abstract]
- Levine DA, Argenta PA, Yee CJ, et al.: Fallopian tube and primary peritoneal carcinomas associated with BRCA mutations. J Clin Oncol 21 (22): 4222-7, 2003.[PUBMED Abstract]
- John EM, Miron A, Gong G, et al.: Prevalence of pathogenic BRCA1 mutation carriers in 5 US racial/ethnic groups. JAMA 298 (24): 2869-76, 2007.[PUBMED Abstract]
- Weitzel JN, Clague J, Martir-Negron A, et al.: Prevalence and type of BRCA mutations in Hispanics undergoing genetic cancer risk assessment in the southwestern United States: a report from the Clinical Cancer Genetics Community Research Network. J Clin Oncol 31 (2): 210-6, 2013.[PUBMED Abstract]
- Torres-Mejía G, Royer R, Llacuachaqui M, et al.: Recurrent BRCA1 and BRCA2 mutations in Mexican women with breast cancer. Cancer Epidemiol Biomarkers Prev 24 (3): 498-505, 2015.[PUBMED Abstract]
- Vicus D, Finch A, Cass I, et al.: Prevalence of BRCA1 and BRCA2 germ line mutations among women with carcinoma of the fallopian tube. Gynecol Oncol 118 (3): 299-302, 2010.[PUBMED Abstract]
- Aziz S, Kuperstein G, Rosen B, et al.: A genetic epidemiological study of carcinoma of the fallopian tube. Gynecol Oncol 80 (3): 341-5, 2001.[PUBMED Abstract]
- Manchanda R, Loggenberg K, Sanderson S, et al.: Population testing for cancer predisposing BRCA1/BRCA2 mutations in the Ashkenazi-Jewish community: a randomized controlled trial. J Natl Cancer Inst 107 (1): 379, 2015.[PUBMED Abstract]
- Manchanda R, Legood R, Burnell M, et al.: Cost-effectiveness of population screening for BRCA mutations in Ashkenazi jewish women compared with family history-based testing. J Natl Cancer Inst 107 (1): 380, 2015.[PUBMED Abstract]
- Metcalfe KA, Poll A, Royer R, et al.: A comparison of the detection of BRCA mutation carriers through the provision of Jewish population-based genetic testing compared with clinic-based genetic testing. Br J Cancer 109 (3): 777-9, 2013.[PUBMED Abstract]
- Manchanda R, Patel S, Antoniou AC, et al.: Cost-effectiveness of population based BRCA testing with varying Ashkenazi Jewish ancestry. Am J Obstet Gynecol 217 (5): 578.e1-578.e12, 2017.[PUBMED Abstract]
- Manchanda R, Patel S, Gordeev VS, et al.: Cost-effectiveness of Population-Based BRCA1, BRCA2, RAD51C, RAD51D, BRIP1, PALB2 Mutation Testing in Unselected General Population Women. J Natl Cancer Inst 110 (7): 714-725, 2018.[PUBMED Abstract]
- Couch FJ, DeShano ML, Blackwood MA, et al.: BRCA1 mutations in women attending clinics that evaluate the risk of breast cancer. N Engl J Med 336 (20): 1409-15, 1997.[PUBMED Abstract]
- Shattuck-Eidens D, Oliphant A, McClure M, et al.: BRCA1 sequence analysis in women at high risk for susceptibility mutations. Risk factor analysis and implications for genetic testing. JAMA 278 (15): 1242-50, 1997.[PUBMED Abstract]
- Spiegelman D, Colditz GA, Hunter D, et al.: Validation of the Gail et al. model for predicting individual breast cancer risk. J Natl Cancer Inst 86 (8): 600-7, 1994.[PUBMED Abstract]
- Frank TS, Manley SA, Olopade OI, et al.: Sequence analysis of BRCA1 and BRCA2: correlation of mutations with family history and ovarian cancer risk. J Clin Oncol 16 (7): 2417-25, 1998.[PUBMED Abstract]
- Chang-Claude J, Dong J, Schmidt S, et al.: Using gene carrier probability to select high risk families for identifying germline mutations in breast cancer susceptibility genes. J Med Genet 35 (2): 116-21, 1998.[PUBMED Abstract]
- Couch FJ, Hartmann LC: BRCA1 testing--advances and retreats. JAMA 279 (12): 955-7, 1998.[PUBMED Abstract]
- Parmigiani G, Berry D, Aguilar O: Determining carrier probabilities for breast cancer-susceptibility genes BRCA1 and BRCA2. Am J Hum Genet 62 (1): 145-58, 1998.[PUBMED Abstract]
- Ready K, Litton JK, Arun BK: Clinical application of breast cancer risk assessment models. Future Oncol 6 (3): 355-65, 2010.[PUBMED Abstract]
- Amir E, Freedman OC, Seruga B, et al.: Assessing women at high risk of breast cancer: a review of risk assessment models. J Natl Cancer Inst 102 (10): 680-91, 2010.[PUBMED Abstract]
- Lakhani SR, Reis-Filho JS, Fulford L, et al.: Prediction of BRCA1 status in patients with breast cancer using estrogen receptor and basal phenotype. Clin Cancer Res 11 (14): 5175-80, 2005.[PUBMED Abstract]
- Kwon JS, Gutierrez-Barrera AM, Young D, et al.: Expanding the criteria for BRCA mutation testing in breast cancer survivors. J Clin Oncol 28 (27): 4214-20, 2010.[PUBMED Abstract]
- Young SR, Pilarski RT, Donenberg T, et al.: The prevalence of BRCA1 mutations among young women with triple-negative breast cancer. BMC Cancer 9: 86, 2009.[PUBMED Abstract]
- Greenup R, Buchanan A, Lorizio W, et al.: Prevalence of BRCA mutations among women with triple-negative breast cancer (TNBC) in a genetic counseling cohort. Ann Surg Oncol 20 (10): 3254-8, 2013.[PUBMED Abstract]
- Robson ME, Storm CD, Weitzel J, et al.: American Society of Clinical Oncology policy statement update: genetic and genomic testing for cancer susceptibility. J Clin Oncol 28 (5): 893-901, 2010.[PUBMED Abstract]
- National Comprehensive Cancer Network: NCCN Clinical Practice Guidelines in Oncology: Genetic/Familial High-Risk Assessment: Breast, Ovarian, and Pancreatic. Version 1.2020. Plymouth Meeting, Pa: National Comprehensive Cancer Network, 2019. Available online with free registration. Last accessed December 23, 2019.[PUBMED Abstract]
- Statement of the American Society of Human Genetics on genetic testing for breast and ovarian cancer predisposition. Am J Hum Genet 55 (5): i-iv, 1994.[PUBMED Abstract]
- Hampel H, Bennett RL, Buchanan A, et al.: A practice guideline from the American College of Medical Genetics and Genomics and the National Society of Genetic Counselors: referral indications for cancer predisposition assessment. Genet Med 17 (1): 70-87, 2015.[PUBMED Abstract]
- Owens DK, Davidson KW, Krist AH, et al.: Risk Assessment, Genetic Counseling, and Genetic Testing for BRCA-Related Cancer: US Preventive Services Task Force Recommendation Statement. JAMA 322 (7): 652-665, 2019.[PUBMED Abstract]
- Lancaster JM, Powell CB, Kauff ND, et al.: Society of Gynecologic Oncologists Education Committee statement on risk assessment for inherited gynecologic cancer predispositions. Gynecol Oncol 107 (2): 159-62, 2007.[PUBMED Abstract]
- Evans DG, Eccles DM, Rahman N, et al.: A new scoring system for the chances of identifying a BRCA1/2 mutation outperforms existing models including BRCAPRO. J Med Genet 41 (6): 474-80, 2004.[PUBMED Abstract]
- Apicella C, Dowty JG, Dite GS, et al.: Validation study of the LAMBDA model for predicting the BRCA1 or BRCA2 mutation carrier status of North American Ashkenazi Jewish women. Clin Genet 72 (2): 87-97, 2007.[PUBMED Abstract]
- Antoniou AC, Pharoah PP, Smith P, et al.: The BOADICEA model of genetic susceptibility to breast and ovarian cancer. Br J Cancer 91 (8): 1580-90, 2004.[PUBMED Abstract]
- Struewing JP, Abeliovich D, Peretz T, et al.: The carrier frequency of the BRCA1 185delAG mutation is approximately 1 percent in Ashkenazi Jewish individuals. Nat Genet 11 (2): 198-200, 1995.[PUBMED Abstract]
- Oddoux C, Struewing JP, Clayton CM, et al.: The carrier frequency of the BRCA2 6174delT mutation among Ashkenazi Jewish individuals is approximately 1%. Nat Genet 14 (2): 188-90, 1996.[PUBMED Abstract]
- Warner E, Foulkes W, Goodwin P, et al.: Prevalence and penetrance of BRCA1 and BRCA2 gene mutations in unselected Ashkenazi Jewish women with breast cancer. J Natl Cancer Inst 91 (14): 1241-7, 1999.[PUBMED Abstract]
- Euhus DM, Smith KC, Robinson L, et al.: Pretest prediction of BRCA1 or BRCA2 mutation by risk counselors and the computer model BRCAPRO. J Natl Cancer Inst 94 (11): 844-51, 2002.[PUBMED Abstract]
- de la Hoya M, Díez O, Pérez-Segura P, et al.: Pre-test prediction models of BRCA1 or BRCA2 mutation in breast/ovarian families attending familial cancer clinics. J Med Genet 40 (7): 503-10, 2003.[PUBMED Abstract]
- Katki HA: Incorporating medical interventions into carrier probability estimation for genetic counseling. BMC Med Genet 8: 13, 2007.[PUBMED Abstract]
- Weitzel JN, Lagos VI, Cullinane CA, et al.: Limited family structure and BRCA gene mutation status in single cases of breast cancer. JAMA 297 (23): 2587-95, 2007.[PUBMED Abstract]
- Jervis S, Song H, Lee A, et al.: A risk prediction algorithm for ovarian cancer incorporating BRCA1, BRCA2, common alleles and other familial effects. J Med Genet 52 (7): 465-75, 2015.[PUBMED Abstract]
- Oros KK, Ghadirian P, Maugard CM, et al.: Application of BRCA1 and BRCA2 mutation carrier prediction models in breast and/or ovarian cancer families of French Canadian descent. Clin Genet 70 (4): 320-9, 2006.[PUBMED Abstract]
- Vogel KJ, Atchley DP, Erlichman J, et al.: BRCA1 and BRCA2 genetic testing in Hispanic patients: mutation prevalence and evaluation of the BRCAPRO risk assessment model. J Clin Oncol 25 (29): 4635-41, 2007.[PUBMED Abstract]
- Kurian AW, Gong GD, John EM, et al.: Performance of prediction models for BRCA mutation carriage in three racial/ethnic groups: findings from the Northern California Breast Cancer Family Registry. Cancer Epidemiol Biomarkers Prev 18 (4): 1084-91, 2009.[PUBMED Abstract]
- Kurian AW, Gong GD, Chun NM, et al.: Performance of BRCA1/2 mutation prediction models in Asian Americans. J Clin Oncol 26 (29): 4752-8, 2008.[PUBMED Abstract]
- Berry DA, Parmigiani G, Sanchez J, et al.: Probability of carrying a mutation of breast-ovarian cancer gene BRCA1 based on family history. J Natl Cancer Inst 89 (3): 227-38, 1997.[PUBMED Abstract]
- Barcenas CH, Hosain GM, Arun B, et al.: Assessing BRCA carrier probabilities in extended families. J Clin Oncol 24 (3): 354-60, 2006.[PUBMED Abstract]
- Kang HH, Williams R, Leary J, et al.: Evaluation of models to predict BRCA germline mutations. Br J Cancer 95 (7): 914-20, 2006.[PUBMED Abstract]
- Antoniou AC, Hardy R, Walker L, et al.: Predicting the likelihood of carrying a BRCA1 or BRCA2 mutation: validation of BOADICEA, BRCAPRO, IBIS, Myriad and the Manchester scoring system using data from UK genetics clinics. J Med Genet 45 (7): 425-31, 2008.[PUBMED Abstract]
- Fischer C, Kuchenbäcker K, Engel C, et al.: Evaluating the performance of the breast cancer genetic risk models BOADICEA, IBIS, BRCAPRO and Claus for predicting BRCA1/2 mutation carrier probabilities: a study based on 7352 families from the German Hereditary Breast and Ovarian Cancer Consortium. J Med Genet 50 (6): 360-7, 2013.[PUBMED Abstract]
- Biswas S, Tankhiwale N, Blackford A, et al.: Assessing the added value of breast tumor markers in genetic risk prediction model BRCAPRO. Breast Cancer Res Treat 133 (1): 347-55, 2012.[PUBMED Abstract]
- Tai YC, Chen S, Parmigiani G, et al.: Incorporating tumor immunohistochemical markers in BRCA1 and BRCA2 carrier prediction. Breast Cancer Res 10 (2): 401, 2008.[PUBMED Abstract]
- Tyrer J, Duffy SW, Cuzick J: A breast cancer prediction model incorporating familial and personal risk factors. Stat Med 23 (7): 1111-30, 2004.[PUBMED Abstract]
- Ready KJ, Vogel KJ, Atchley DP, et al.: Accuracy of the BRCAPRO model among women with bilateral breast cancer. Cancer 115 (4): 725-30, 2009.[PUBMED Abstract]
- Huo D, Senie RT, Daly M, et al.: Prediction of BRCA Mutations Using the BRCAPRO Model in Clinic-Based African American, Hispanic, and Other Minority Families in the United States. J Clin Oncol 27 (8): 1184-90, 2009.[PUBMED Abstract]
- Daniels MS, Babb SA, King RH, et al.: Underestimation of risk of a BRCA1 or BRCA2 mutation in women with high-grade serous ovarian cancer by BRCAPRO: a multi-institution study. J Clin Oncol 32 (12): 1249-55, 2014.[PUBMED Abstract]
- Antoniou A, Pharoah PD, Narod S, et al.: Average risks of breast and ovarian cancer associated with BRCA1 or BRCA2 mutations detected in case Series unselected for family history: a combined analysis of 22 studies. Am J Hum Genet 72 (5): 1117-30, 2003.[PUBMED Abstract]
- Chen S, Parmigiani G: Meta-analysis of BRCA1 and BRCA2 penetrance. J Clin Oncol 25 (11): 1329-33, 2007.[PUBMED Abstract]
- Kuchenbaecker KB, Hopper JL, Barnes DR, et al.: Risks of Breast, Ovarian, and Contralateral Breast Cancer for BRCA1 and BRCA2 Mutation Carriers. JAMA 317 (23): 2402-2416, 2017.[PUBMED Abstract]
- Antoniou AC, Pharoah PD, Narod S, et al.: Breast and ovarian cancer risks to carriers of the BRCA1 5382insC and 185delAG and BRCA2 6174delT mutations: a combined analysis of 22 population based studies. J Med Genet 42 (7): 602-3, 2005.[PUBMED Abstract]
- Finkelman BS, Rubinstein WS, Friedman S, et al.: Breast and ovarian cancer risk and risk reduction in Jewish BRCA1/2 mutation carriers. J Clin Oncol 30 (12): 1321-8, 2012.[PUBMED Abstract]
- Ramus SJ, Song H, Dicks E, et al.: Germline Mutations in the BRIP1, BARD1, PALB2, and NBN Genes in Women With Ovarian Cancer. J Natl Cancer Inst 107 (11): , 2015.[PUBMED Abstract]
- Song H, Dicks E, Ramus SJ, et al.: Contribution of Germline Mutations in the RAD51B, RAD51C, and RAD51D Genes to Ovarian Cancer in the Population. J Clin Oncol 33 (26): 2901-7, 2015.[PUBMED Abstract]
- Rebbeck TR, Mitra N, Wan F, et al.: Association of type and location of BRCA1 and BRCA2 mutations with risk of breast and ovarian cancer. JAMA 313 (13): 1347-61, 2015.[PUBMED Abstract]
- Rebbeck TR, Friebel TM, Mitra N, et al.: Inheritance of deleterious mutations at both BRCA1 and BRCA2 in an international sample of 32,295 women. Breast Cancer Res 18 (1): 112, 2016.[PUBMED Abstract]
- Guindalini RS, Song A, Fackenthal JD, et al.: Genetic anticipation in BRCA1/BRCA2 families after controlling for ascertainment bias and cohort effect. Cancer 122 (12): 1913-20, 2016.[PUBMED Abstract]
- Agranat S, Baris H, Kedar I, et al.: Earlier Age of Breast Cancer Onset in Israeli BRCA Carriers-Is it a Real Phenomenon? Breast J 22 (6): 662-666, 2016.[PUBMED Abstract]
- Litton JK, Ready K, Chen H, et al.: Earlier age of onset of BRCA mutation-related cancers in subsequent generations. Cancer 118 (2): 321-5, 2012.[PUBMED Abstract]
- Wang WW, Spurdle AB, Kolachana P, et al.: A single nucleotide polymorphism in the 5' untranslated region of RAD51 and risk of cancer among BRCA1/2 mutation carriers. Cancer Epidemiol Biomarkers Prev 10 (9): 955-60, 2001.[PUBMED Abstract]
- Levy-Lahad E, Lahad A, Eisenberg S, et al.: A single nucleotide polymorphism in the RAD51 gene modifies cancer risk in BRCA2 but not BRCA1 carriers. Proc Natl Acad Sci U S A 98 (6): 3232-6, 2001.[PUBMED Abstract]
- Narod SA: Modifiers of risk of hereditary breast and ovarian cancer. Nat Rev Cancer 2 (2): 113-23, 2002.[PUBMED Abstract]
- Kramer JL, Velazquez IA, Chen BE, et al.: Prophylactic oophorectomy reduces breast cancer penetrance during prospective, long-term follow-up of BRCA1 mutation carriers. J Clin Oncol 23 (34): 8629-35, 2005.[PUBMED Abstract]
- Antoniou AC, Spurdle AB, Sinilnikova OM, et al.: Common breast cancer-predisposition alleles are associated with breast cancer risk in BRCA1 and BRCA2 mutation carriers. Am J Hum Genet 82 (4): 937-48, 2008.[PUBMED Abstract]
- Iodice S, Barile M, Rotmensz N, et al.: Oral contraceptive use and breast or ovarian cancer risk in BRCA1/2 carriers: a meta-analysis. Eur J Cancer 46 (12): 2275-84, 2010.[PUBMED Abstract]
- Antoniou AC, Rookus M, Andrieu N, et al.: Reproductive and hormonal factors, and ovarian cancer risk for BRCA1 and BRCA2 mutation carriers: results from the International BRCA1/2 Carrier Cohort Study. Cancer Epidemiol Biomarkers Prev 18 (2): 601-10, 2009.[PUBMED Abstract]
- Milne RL, Osorio A, Ramón y Cajal T, et al.: Parity and the risk of breast and ovarian cancer in BRCA1 and BRCA2 mutation carriers. Breast Cancer Res Treat 119 (1): 221-32, 2010.[PUBMED Abstract]
- Friedman E, Kotsopoulos J, Lubinski J, et al.: Spontaneous and therapeutic abortions and the risk of breast cancer among BRCA mutation carriers. Breast Cancer Res 8 (2): R15, 2006.[PUBMED Abstract]
- Jernström H, Lubinski J, Lynch HT, et al.: Breast-feeding and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 96 (14): 1094-8, 2004.[PUBMED Abstract]
- Breast Cancer Family Registry, Kathleen Cuningham Consortium for Research into Familial Breast Cancer (Australasia), Ontario Cancer Genetics Network (Canada): Smoking and risk of breast cancer in carriers of mutations in BRCA1 or BRCA2 aged less than 50 years. Breast Cancer Res Treat 109 (1): 67-75, 2008.[PUBMED Abstract]
- Antoniou AC, Beesley J, McGuffog L, et al.: Common breast cancer susceptibility alleles and the risk of breast cancer for BRCA1 and BRCA2 mutation carriers: implications for risk prediction. Cancer Res 70 (23): 9742-54, 2010.[PUBMED Abstract]
- Ramus SJ, Kartsonaki C, Gayther SA, et al.: Genetic variation at 9p22.2 and ovarian cancer risk for BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 103 (2): 105-16, 2011.[PUBMED Abstract]
- Milne RL, Antoniou AC: Genetic modifiers of cancer risk for BRCA1 and BRCA2 mutation carriers. Ann Oncol 22 (Suppl 1): i11-7, 2011.[PUBMED Abstract]
- Graeser MK, Engel C, Rhiem K, et al.: Contralateral breast cancer risk in BRCA1 and BRCA2 mutation carriers. J Clin Oncol 27 (35): 5887-92, 2009.[PUBMED Abstract]
- Malone KE, Begg CB, Haile RW, et al.: Population-based study of the risk of second primary contralateral breast cancer associated with carrying a mutation in BRCA1 or BRCA2. J Clin Oncol 28 (14): 2404-10, 2010.[PUBMED Abstract]
- van der Kolk DM, de Bock GH, Leegte BK, et al.: Penetrance of breast cancer, ovarian cancer and contralateral breast cancer in BRCA1 and BRCA2 families: high cancer incidence at older age. Breast Cancer Res Treat 124 (3): 643-51, 2010.[PUBMED Abstract]
- Metcalfe K, Gershman S, Lynch HT, et al.: Predictors of contralateral breast cancer in BRCA1 and BRCA2 mutation carriers. Br J Cancer 104 (9): 1384-92, 2011.[PUBMED Abstract]
- Molina-Montes E, Pérez-Nevot B, Pollán M, et al.: Cumulative risk of second primary contralateral breast cancer in BRCA1/BRCA2 mutation carriers with a first breast cancer: A systematic review and meta-analysis. Breast 23 (6): 721-42, 2014.[PUBMED Abstract]
- Basu NN, Ingham S, Hodson J, et al.: Risk of contralateral breast cancer in BRCA1 and BRCA2 mutation carriers: a 30-year semi-prospective analysis. Fam Cancer 14 (4): 531-8, 2015.[PUBMED Abstract]
- van den Broek AJ, van 't Veer LJ, Hooning MJ, et al.: Impact of Age at Primary Breast Cancer on Contralateral Breast Cancer Risk in BRCA1/2 Mutation Carriers. J Clin Oncol 34 (5): 409-18, 2016.[PUBMED Abstract]
- Pierce LJ, Phillips KA, Griffith KA, et al.: Local therapy in BRCA1 and BRCA2 mutation carriers with operable breast cancer: comparison of breast conservation and mastectomy. Breast Cancer Res Treat 121 (2): 389-98, 2010.[PUBMED Abstract]
- Domchek SM, Jhaveri K, Patil S, et al.: Risk of metachronous breast cancer after BRCA mutation-associated ovarian cancer. Cancer 119 (7): 1344-8, 2013.[PUBMED Abstract]
- Vencken PM, Kriege M, Hooning M, et al.: The risk of primary and contralateral breast cancer after ovarian cancer in BRCA1/BRCA2 mutation carriers: Implications for counseling. Cancer 119 (5): 955-62, 2013.[PUBMED Abstract]
- Gangi A, Cass I, Paik D, et al.: Breast cancer following ovarian cancer in BRCA mutation carriers. JAMA Surg 149 (12): 1306-13, 2014.[PUBMED Abstract]
- McGee J, Giannakeas V, Karlan B, et al.: Risk of breast cancer after a diagnosis of ovarian cancer in BRCA mutation carriers: Is preventive mastectomy warranted? Gynecol Oncol 145 (2): 346-351, 2017.[PUBMED Abstract]
- Casey MJ, Synder C, Bewtra C, et al.: Intra-abdominal carcinomatosis after prophylactic oophorectomy in women of hereditary breast ovarian cancer syndrome kindreds associated with BRCA1 and BRCA2 mutations. Gynecol Oncol 97 (2): 457-67, 2005.[PUBMED Abstract]
- Finch A, Beiner M, Lubinski J, et al.: Salpingo-oophorectomy and the risk of ovarian, fallopian tube, and peritoneal cancers in women with a BRCA1 or BRCA2 Mutation. JAMA 296 (2): 185-92, 2006.[PUBMED Abstract]
- Evans DG, Susnerwala I, Dawson J, et al.: Risk of breast cancer in male BRCA2 carriers. J Med Genet 47 (10): 710-1, 2010.[PUBMED Abstract]
- Edwards SM, Kote-Jarai Z, Meitz J, et al.: Two percent of men with early-onset prostate cancer harbor germline mutations in the BRCA2 gene. Am J Hum Genet 72 (1): 1-12, 2003.[PUBMED Abstract]
- Giusti RM, Rutter JL, Duray PH, et al.: A twofold increase in BRCA mutation related prostate cancer among Ashkenazi Israelis is not associated with distinctive histopathology. J Med Genet 40 (10): 787-92, 2003.[PUBMED Abstract]
- van Asperen CJ, Brohet RM, Meijers-Heijboer EJ, et al.: Cancer risks in BRCA2 families: estimates for sites other than breast and ovary. J Med Genet 42 (9): 711-9, 2005.[PUBMED Abstract]
- Mersch J, Jackson MA, Park M, et al.: Cancers associated with BRCA1 and BRCA2 mutations other than breast and ovarian. Cancer 121 (2): 269-75, 2015.[PUBMED Abstract]
- Mitra A, Fisher C, Foster CS, et al.: Prostate cancer in male BRCA1 and BRCA2 mutation carriers has a more aggressive phenotype. Br J Cancer 98 (2): 502-7, 2008.[PUBMED Abstract]
- Tryggvadóttir L, Vidarsdóttir L, Thorgeirsson T, et al.: Prostate cancer progression and survival in BRCA2 mutation carriers. J Natl Cancer Inst 99 (12): 929-35, 2007.[PUBMED Abstract]
- Agalliu I, Gern R, Leanza S, et al.: Associations of high-grade prostate cancer with BRCA1 and BRCA2 founder mutations. Clin Cancer Res 15 (3): 1112-20, 2009.[PUBMED Abstract]
- Narod SA, Neuhausen S, Vichodez G, et al.: Rapid progression of prostate cancer in men with a BRCA2 mutation. Br J Cancer 99 (2): 371-4, 2008.[PUBMED Abstract]
- Edwards SM, Evans DG, Hope Q, et al.: Prostate cancer in BRCA2 germline mutation carriers is associated with poorer prognosis. Br J Cancer 103 (6): 918-24, 2010.[PUBMED Abstract]
- Gallagher DJ, Gaudet MM, Pal P, et al.: Germline BRCA mutations denote a clinicopathologic subset of prostate cancer. Clin Cancer Res 16 (7): 2115-21, 2010.[PUBMED Abstract]
- Couch FJ, Johnson MR, Rabe KG, et al.: The prevalence of BRCA2 mutations in familial pancreatic cancer. Cancer Epidemiol Biomarkers Prev 16 (2): 342-6, 2007.[PUBMED Abstract]
- Hahn SA, Greenhalf B, Ellis I, et al.: BRCA2 germline mutations in familial pancreatic carcinoma. J Natl Cancer Inst 95 (3): 214-21, 2003.[PUBMED Abstract]
- Murphy KM, Brune KA, Griffin C, et al.: Evaluation of candidate genes MAP2K4, MADH4, ACVR1B, and BRCA2 in familial pancreatic cancer: deleterious BRCA2 mutations in 17%. Cancer Res 62 (13): 3789-93, 2002.[PUBMED Abstract]
- Real FX, Malats N, Lesca G, et al.: Family history of cancer and germline BRCA2 mutations in sporadic exocrine pancreatic cancer. Gut 50 (5): 653-7, 2002.[PUBMED Abstract]
- Dagan E: Predominant Ashkenazi BRCA1/2 mutations in families with pancreatic cancer. Genet Test 12 (2): 267-71, 2008.[PUBMED Abstract]
- Goggins M, Schutte M, Lu J, et al.: Germline BRCA2 gene mutations in patients with apparently sporadic pancreatic carcinomas. Cancer Res 56 (23): 5360-4, 1996.[PUBMED Abstract]
- Lal G, Liu G, Schmocker B, et al.: Inherited predisposition to pancreatic adenocarcinoma: role of family history and germ-line p16, BRCA1, and BRCA2 mutations. Cancer Res 60 (2): 409-16, 2000.[PUBMED Abstract]
- Ozçelik H, Schmocker B, Di Nicola N, et al.: Germline BRCA2 6174delT mutations in Ashkenazi Jewish pancreatic cancer patients. Nat Genet 16 (1): 17-8, 1997.[PUBMED Abstract]
- Ferrone CR, Levine DA, Tang LH, et al.: BRCA germline mutations in Jewish patients with pancreatic adenocarcinoma. J Clin Oncol 27 (3): 433-8, 2009.[PUBMED Abstract]
- National Cancer Institute: DevCan: Probability of Developing or Dying of Cancer Software. Version 6.7.7. Bethesda, Md: Division of Cancer Control & Population Sciences, National Cancer Institute, 2017. Available online with free registration. Last accessed January 22, 2020.[PUBMED Abstract]
- Ford D, Easton DF, Bishop DT, et al.: Risks of cancer in BRCA1-mutation carriers. Breast Cancer Linkage Consortium. Lancet 343 (8899): 692-5, 1994.[PUBMED Abstract]
- Anton-Culver H, Cohen PF, Gildea ME, et al.: Characteristics of BRCA1 mutations in a population-based case series of breast and ovarian cancer. Eur J Cancer 36 (10): 1200-8, 2000.[PUBMED Abstract]
- Peelen T, de Leeuw W, van Lent K, et al.: Genetic analysis of a breast-ovarian cancer family, with 7 cases of colorectal cancer linked to BRCA1, fails to support a role for BRCA1 in colorectal tumorigenesis. Int J Cancer 88 (5): 778-82, 2000.[PUBMED Abstract]
- Berman DB, Costalas J, Schultz DC, et al.: A common mutation in BRCA2 that predisposes to a variety of cancers is found in both Jewish Ashkenazi and non-Jewish individuals. Cancer Res 56 (15): 3409-14, 1996.[PUBMED Abstract]
- Aretini P, D'Andrea E, Pasini B, et al.: Different expressivity of BRCA1 and BRCA2: analysis of 179 Italian pedigrees with identified mutation. Breast Cancer Res Treat 81 (1): 71-9, 2003.[PUBMED Abstract]
- Kirchhoff T, Satagopan JM, Kauff ND, et al.: Frequency of BRCA1 and BRCA2 mutations in unselected Ashkenazi Jewish patients with colorectal cancer. J Natl Cancer Inst 96 (1): 68-70, 2004.[PUBMED Abstract]
- Niell BL, Rennert G, Bonner JD, et al.: BRCA1 and BRCA2 founder mutations and the risk of colorectal cancer. J Natl Cancer Inst 96 (1): 15-21, 2004.[PUBMED Abstract]
- Chen-Shtoyerman R, Figer A, Fidder HH, et al.: The frequency of the predominant Jewish mutations in BRCA1 and BRCA2 in unselected Ashkenazi colorectal cancer patients. Br J Cancer 84 (4): 475-7, 2001.[PUBMED Abstract]
- Levine DA, Lin O, Barakat RR, et al.: Risk of endometrial carcinoma associated with BRCA mutation. Gynecol Oncol 80 (3): 395-8, 2001.[PUBMED Abstract]
- Goshen R, Chu W, Elit L, et al.: Is uterine papillary serous adenocarcinoma a manifestation of the hereditary breast-ovarian cancer syndrome? Gynecol Oncol 79 (3): 477-81, 2000.[PUBMED Abstract]
- Smith A, Moran A, Boyd MC, et al.: Phenocopies in BRCA1 and BRCA2 families: evidence for modifier genes and implications for screening. J Med Genet 44 (1): 10-15, 2007.[PUBMED Abstract]
- Goldgar D, Venne V, Conner T, et al.: BRCA phenocopies or ascertainment bias? J Med Genet 44 (8): e86; author reply e88, 2007.[PUBMED Abstract]
- Eisinger F: Phenocopies: actual risk or self-fulfilling prophecy? J Med Genet 44 (8): e87; author reply e88, 2007.[PUBMED Abstract]
- Sasieni P: Phenocopies in families seen by cancer geneticists. J Med Genet 44 (6): e82, 2007.[PUBMED Abstract]
- Tilanus-Linthorst MM: No screening yet after a negative test for the family mutation. J Med Genet 44 (5): e79, 2007.[PUBMED Abstract]
- Katki HA, Gail MH, Greene MH: Breast-cancer risk in BRCA-mutation-negative women from BRCA-mutation-positive families. Lancet Oncol 8 (12): 1042-3, 2007.[PUBMED Abstract]
- Raskin L, Lejbkowicz F, Barnett-Griness O, et al.: BRCA1 breast cancer risk is modified by CYP19 polymorphisms in Ashkenazi Jews. Cancer Epidemiol Biomarkers Prev 18 (5): 1617-23, 2009.[PUBMED Abstract]
- Gronwald J, Cybulski C, Lubinski J, et al.: Phenocopies in breast cancer 1 (BRCA1) families: implications for genetic counselling. J Med Genet 44 (4): e76, 2007.[PUBMED Abstract]
- Rowan E, Poll A, Narod SA: A prospective study of breast cancer risk in relatives of BRCA1/BRCA2 mutation carriers. J Med Genet 44 (8): e89; author reply e88, 2007.[PUBMED Abstract]
- Vos JR, de Bock GH, Teixeira N, et al.: Proven non-carriers in BRCA families have an earlier age of onset of breast cancer. Eur J Cancer 49 (9): 2101-6, 2013.[PUBMED Abstract]
- Domchek SM, Gaudet MM, Stopfer JE, et al.: Breast cancer risks in individuals testing negative for a known family mutation in BRCA1 or BRCA2. Breast Cancer Res Treat 119 (2): 409-14, 2010.[PUBMED Abstract]
- Korde LA, Mueller CM, Loud JT, et al.: No evidence of excess breast cancer risk among mutation-negative women from BRCA mutation-positive families. Breast Cancer Res Treat 125 (1): 169-73, 2011.[PUBMED Abstract]
- Kurian AW, Gong GD, John EM, et al.: Breast cancer risk for noncarriers of family-specific BRCA1 and BRCA2 mutations: findings from the Breast Cancer Family Registry. J Clin Oncol 29 (34): 4505-9, 2011.[PUBMED Abstract]
- Harvey SL, Milne RL, McLachlan SA, et al.: Prospective study of breast cancer risk for mutation negative women from BRCA1 or BRCA2 mutation positive families. Breast Cancer Res Treat 130 (3): 1057-61, 2011.[PUBMED Abstract]
- Kauff ND, Mitra N, Robson ME, et al.: Risk of ovarian cancer in BRCA1 and BRCA2 mutation-negative hereditary breast cancer families. J Natl Cancer Inst 97 (18): 1382-4, 2005.[PUBMED Abstract]
- Lee JS, John EM, McGuire V, et al.: Breast and ovarian cancer in relatives of cancer patients, with and without BRCA mutations. Cancer Epidemiol Biomarkers Prev 15 (2): 359-63, 2006.[PUBMED Abstract]
- Metcalfe KA, Finch A, Poll A, et al.: Breast cancer risks in women with a family history of breast or ovarian cancer who have tested negative for a BRCA1 or BRCA2 mutation. Br J Cancer 100 (2): 421-5, 2009.[PUBMED Abstract]
- Liede A, Karlan BY, Baldwin RL, et al.: Cancer incidence in a population of Jewish women at risk of ovarian cancer. J Clin Oncol 20 (6): 1570-7, 2002.[PUBMED Abstract]
- Ingham SL, Warwick J, Buchan I, et al.: Ovarian cancer among 8,005 women from a breast cancer family history clinic: no increased risk of invasive ovarian cancer in families testing negative for BRCA1 and BRCA2. J Med Genet 50 (6): 368-72, 2013.[PUBMED Abstract]
- Barnes DR, Antoniou AC: Unravelling modifiers of breast and ovarian cancer risk for BRCA1 and BRCA2 mutation carriers: update on genetic modifiers. J Intern Med 271 (4): 331-43, 2012.[PUBMED Abstract]
- Chenevix-Trench G, Milne RL, Antoniou AC, et al.: An international initiative to identify genetic modifiers of cancer risk in BRCA1 and BRCA2 mutation carriers: the Consortium of Investigators of Modifiers of BRCA1 and BRCA2 (CIMBA). Breast Cancer Res 9 (2): 104, 2007.[PUBMED Abstract]
- Ford D, Easton DF, Stratton M, et al.: Genetic heterogeneity and penetrance analysis of the BRCA1 and BRCA2 genes in breast cancer families. The Breast Cancer Linkage Consortium. Am J Hum Genet 62 (3): 676-89, 1998.[PUBMED Abstract]
- Thompson D, Easton D; Breast Cancer Linkage Consortium: Variation in cancer risks, by mutation position, in BRCA2 mutation carriers. Am J Hum Genet 68 (2): 410-9, 2001.[PUBMED Abstract]
- Thompson D, Easton D; Breast Cancer Linkage Consortium: Variation in BRCA1 cancer risks by mutation position. Cancer Epidemiol Biomarkers Prev 11 (4): 329-36, 2002.[PUBMED Abstract]
- Scott CL, Jenkins MA, Southey MC, et al.: Average age-specific cumulative risk of breast cancer according to type and site of germline mutations in BRCA1 and BRCA2 estimated from multiple-case breast cancer families attending Australian family cancer clinics. Hum Genet 112 (5-6): 542-51, 2003.[PUBMED Abstract]
- Lubinski J, Phelan CM, Ghadirian P, et al.: Cancer variation associated with the position of the mutation in the BRCA2 gene. Fam Cancer 3 (1): 1-10, 2004.[PUBMED Abstract]
- Satagopan JM, Boyd J, Kauff ND, et al.: Ovarian cancer risk in Ashkenazi Jewish carriers of BRCA1 and BRCA2 mutations. Clin Cancer Res 8 (12): 3776-81, 2002.[PUBMED Abstract]
- Rennert G, Dishon S, Rennert HS, et al.: Differences in the characteristics of families with BRCA1 and BRCA2 mutations in Israel. Eur J Cancer Prev 14 (4): 357-61, 2005.[PUBMED Abstract]
- James PA, Sawyer S, Boyle S, et al.: Large genomic rearrangements in the familial breast and ovarian cancer gene BRCA1 are associated with an increased frequency of high risk features. Fam Cancer 14 (2): 287-95, 2015.[PUBMED Abstract]
- Eisinger F, Jacquemier J, Charpin C, et al.: Mutations at BRCA1: the medullary breast carcinoma revisited. Cancer Res 58 (8): 1588-92, 1998.[PUBMED Abstract]
- Pathology of familial breast cancer: differences between breast cancers in carriers of BRCA1 or BRCA2 mutations and sporadic cases. Breast Cancer Linkage Consortium. Lancet 349 (9064): 1505-10, 1997.[PUBMED Abstract]
- Armes JE, Egan AJ, Southey MC, et al.: The histologic phenotypes of breast carcinoma occurring before age 40 years in women with and without BRCA1 or BRCA2 germline mutations: a population-based study. Cancer 83 (11): 2335-45, 1998.[PUBMED Abstract]
- Foulkes WD, Stefansson IM, Chappuis PO, et al.: Germline BRCA1 mutations and a basal epithelial phenotype in breast cancer. J Natl Cancer Inst 95 (19): 1482-5, 2003.[PUBMED Abstract]
- Verhoog LC, Brekelmans CT, Seynaeve C, et al.: Survival and tumour characteristics of breast-cancer patients with germline mutations of BRCA1. Lancet 351 (9099): 316-21, 1998.[PUBMED Abstract]
- Manié E, Vincent-Salomon A, Lehmann-Che J, et al.: High frequency of TP53 mutation in BRCA1 and sporadic basal-like carcinomas but not in BRCA1 luminal breast tumors. Cancer Res 69 (2): 663-71, 2009.[PUBMED Abstract]
- Southey MC, Ramus SJ, Dowty JG, et al.: Morphological predictors of BRCA1 germline mutations in young women with breast cancer. Br J Cancer 104 (6): 903-9, 2011.[PUBMED Abstract]
- Mavaddat N, Barrowdale D, Andrulis IL, et al.: Pathology of breast and ovarian cancers among BRCA1 and BRCA2 mutation carriers: results from the Consortium of Investigators of Modifiers of BRCA1/2 (CIMBA). Cancer Epidemiol Biomarkers Prev 21 (1): 134-47, 2012.[PUBMED Abstract]
- Lakhani SR, Van De Vijver MJ, Jacquemier J, et al.: The pathology of familial breast cancer: predictive value of immunohistochemical markers estrogen receptor, progesterone receptor, HER-2, and p53 in patients with mutations in BRCA1 and BRCA2. J Clin Oncol 20 (9): 2310-8, 2002.[PUBMED Abstract]
- Sorlie T, Tibshirani R, Parker J, et al.: Repeated observation of breast tumor subtypes in independent gene expression data sets. Proc Natl Acad Sci U S A 100 (14): 8418-23, 2003.[PUBMED Abstract]
- Lee E, McKean-Cowdin R, Ma H, et al.: Characteristics of triple-negative breast cancer in patients with a BRCA1 mutation: results from a population-based study of young women. J Clin Oncol 29 (33): 4373-80, 2011.[PUBMED Abstract]
- Anders C, Carey LA: Understanding and treating triple-negative breast cancer. Oncology (Williston Park) 22 (11): 1233-9; discussion 1239-40, 1243, 2008.[PUBMED Abstract]
- Atchley DP, Albarracin CT, Lopez A, et al.: Clinical and pathologic characteristics of patients with BRCA-positive and BRCA-negative breast cancer. J Clin Oncol 26 (26): 4282-8, 2008.[PUBMED Abstract]
- Tung N, Wang Y, Collins LC, et al.: Estrogen receptor positive breast cancers in BRCA1 mutation carriers: clinical risk factors and pathologic features. Breast Cancer Res 12 (1): R12, 2010.[PUBMED Abstract]
- Lakhani SR, Khanna KK, Chenevix-Trench G: Are estrogen receptor-positive breast cancers in BRCA1 mutation carriers sporadic? Breast Cancer Res 12 (2): 104, 2010.[PUBMED Abstract]
- Foulkes WD, Metcalfe K, Sun P, et al.: Estrogen receptor status in BRCA1- and BRCA2-related breast cancer: the influence of age, grade, and histological type. Clin Cancer Res 10 (6): 2029-34, 2004.[PUBMED Abstract]
- Gonzalez-Angulo AM, Timms KM, Liu S, et al.: Incidence and outcome of BRCA mutations in unselected patients with triple receptor-negative breast cancer. Clin Cancer Res 17 (5): 1082-9, 2011.[PUBMED Abstract]
- Rummel S, Varner E, Shriver CD, et al.: Evaluation of BRCA1 mutations in an unselected patient population with triple-negative breast cancer. Breast Cancer Res Treat 137 (1): 119-25, 2013.[PUBMED Abstract]
- Couch FJ, Hart SN, Sharma P, et al.: Inherited mutations in 17 breast cancer susceptibility genes among a large triple-negative breast cancer cohort unselected for family history of breast cancer. J Clin Oncol 33 (4): 304-11, 2015.[PUBMED Abstract]
- Robertson L, Hanson H, Seal S, et al.: BRCA1 testing should be offered to individuals with triple-negative breast cancer diagnosed below 50 years. Br J Cancer 106 (6): 1234-8, 2012.[PUBMED Abstract]
- Tun NM, Villani G, Ong K, et al.: Risk of having BRCA1 mutation in high-risk women with triple-negative breast cancer: a meta-analysis. Clin Genet 85 (1): 43-8, 2014.[PUBMED Abstract]
- Lee LJ, Alexander B, Schnitt SJ, et al.: Clinical outcome of triple negative breast cancer in BRCA1 mutation carriers and noncarriers. Cancer 117 (14): 3093-100, 2011.[PUBMED Abstract]
- Eccles DM, Li N, Handwerker R, et al.: Genetic testing in a cohort of young patients with HER2-amplified breast cancer. Ann Oncol 27 (3): 467-73, 2016.[PUBMED Abstract]
- Foulkes WD: BRCA1 functions as a breast stem cell regulator. J Med Genet 41 (1): 1-5, 2004.[PUBMED Abstract]
- Perou CM, Sørlie T, Eisen MB, et al.: Molecular portraits of human breast tumours. Nature 406 (6797): 747-52, 2000.[PUBMED Abstract]
- Sørlie T, Perou CM, Tibshirani R, et al.: Gene expression patterns of breast carcinomas distinguish tumor subclasses with clinical implications. Proc Natl Acad Sci U S A 98 (19): 10869-74, 2001.[PUBMED Abstract]
- Hedenfalk I, Duggan D, Chen Y, et al.: Gene-expression profiles in hereditary breast cancer. N Engl J Med 344 (8): 539-48, 2001.[PUBMED Abstract]
- Wessels LF, van Welsem T, Hart AA, et al.: Molecular classification of breast carcinomas by comparative genomic hybridization: a specific somatic genetic profile for BRCA1 tumors. Cancer Res 62 (23): 7110-7, 2002.[PUBMED Abstract]
- Palacios J, Honrado E, Osorio A, et al.: Immunohistochemical characteristics defined by tissue microarray of hereditary breast cancer not attributable to BRCA1 or BRCA2 mutations: differences from breast carcinomas arising in BRCA1 and BRCA2 mutation carriers. Clin Cancer Res 9 (10 Pt 1): 3606-14, 2003.[PUBMED Abstract]
- Nielsen TO, Hsu FD, Jensen K, et al.: Immunohistochemical and clinical characterization of the basal-like subtype of invasive breast carcinoma. Clin Cancer Res 10 (16): 5367-74, 2004.[PUBMED Abstract]
- Palacios J, Honrado E, Osorio A, et al.: Phenotypic characterization of BRCA1 and BRCA2 tumors based in a tissue microarray study with 37 immunohistochemical markers. Breast Cancer Res Treat 90 (1): 5-14, 2005.[PUBMED Abstract]
- Laakso M, Loman N, Borg A, et al.: Cytokeratin 5/14-positive breast cancer: true basal phenotype confined to BRCA1 tumors. Mod Pathol 18 (10): 1321-8, 2005.[PUBMED Abstract]
- Cheang MC, Voduc D, Bajdik C, et al.: Basal-like breast cancer defined by five biomarkers has superior prognostic value than triple-negative phenotype. Clin Cancer Res 14 (5): 1368-76, 2008.[PUBMED Abstract]
- Hwang ES, McLennan JL, Moore DH, et al.: Ductal carcinoma in situ in BRCA mutation carriers. J Clin Oncol 25 (6): 642-7, 2007.[PUBMED Abstract]
- Adem C, Reynolds C, Soderberg CL, et al.: Pathologic characteristics of breast parenchyma in patients with hereditary breast carcinoma, including BRCA1 and BRCA2 mutation carriers. Cancer 97 (1): 1-11, 2003.[PUBMED Abstract]
- Claus EB, Petruzella S, Matloff E, et al.: Prevalence of BRCA1 and BRCA2 mutations in women diagnosed with ductal carcinoma in situ. JAMA 293 (8): 964-9, 2005.[PUBMED Abstract]
- Arun B, Vogel KJ, Lopez A, et al.: High prevalence of preinvasive lesions adjacent to BRCA1/2-associated breast cancers. Cancer Prev Res (Phila Pa) 2 (2): 122-7, 2009.[PUBMED Abstract]
- Garber JE: BRCA1/2-associated and sporadic breast cancers: fellow travelers or not? Cancer Prev Res (Phila Pa) 2 (2): 100-3, 2009.[PUBMED Abstract]
- Smith KL, Adank M, Kauff N, et al.: BRCA mutations in women with ductal carcinoma in situ. Clin Cancer Res 13 (14): 4306-10, 2007.[PUBMED Abstract]
- Hoogerbrugge N, Bult P, Bonenkamp JJ, et al.: Numerous high-risk epithelial lesions in familial breast cancer. Eur J Cancer 42 (15): 2492-8, 2006.[PUBMED Abstract]
- Kauff ND, Brogi E, Scheuer L, et al.: Epithelial lesions in prophylactic mastectomy specimens from women with BRCA mutations. Cancer 97 (7): 1601-8, 2003.[PUBMED Abstract]
- Hall MJ, Reid JE, Wenstrup RJ: Prevalence of BRCA1 and BRCA2 mutations in women with breast carcinoma In Situ and referred for genetic testing. Cancer Prev Res (Phila) 3 (12): 1579-85, 2010.[PUBMED Abstract]
- Marcus JN, Watson P, Page DL, et al.: Hereditary breast cancer: pathobiology, prognosis, and BRCA1 and BRCA2 gene linkage. Cancer 77 (4): 697-709, 1996.[PUBMED Abstract]
- Marcus JN, Watson P, Page DL, et al.: BRCA2 hereditary breast cancer pathophenotype. Breast Cancer Res Treat 44 (3): 275-7, 1997.[PUBMED Abstract]
- Agnarsson BA, Jonasson JG, Björnsdottir IB, et al.: Inherited BRCA2 mutation associated with high grade breast cancer. Breast Cancer Res Treat 47 (2): 121-7, 1998.[PUBMED Abstract]
- Lakhani SR, Jacquemier J, Sloane JP, et al.: Multifactorial analysis of differences between sporadic breast cancers and cancers involving BRCA1 and BRCA2 mutations. J Natl Cancer Inst 90 (15): 1138-45, 1998.[PUBMED Abstract]
- Futreal PA, Liu Q, Shattuck-Eidens D, et al.: BRCA1 mutations in primary breast and ovarian carcinomas. Science 266 (5182): 120-2, 1994.[PUBMED Abstract]
- Lancaster JM, Wooster R, Mangion J, et al.: BRCA2 mutations in primary breast and ovarian cancers. Nat Genet 13 (2): 238-40, 1996.[PUBMED Abstract]
- Miki Y, Katagiri T, Kasumi F, et al.: Mutation analysis in the BRCA2 gene in primary breast cancers. Nat Genet 13 (2): 245-7, 1996.[PUBMED Abstract]
- Teng DH, Bogden R, Mitchell J, et al.: Low incidence of BRCA2 mutations in breast carcinoma and other cancers. Nat Genet 13 (2): 241-4, 1996.[PUBMED Abstract]
- Berchuck A, Heron KA, Carney ME, et al.: Frequency of germline and somatic BRCA1 mutations in ovarian cancer. Clin Cancer Res 4 (10): 2433-7, 1998.[PUBMED Abstract]
- Thompson ME, Jensen RA, Obermiller PS, et al.: Decreased expression of BRCA1 accelerates growth and is often present during sporadic breast cancer progression. Nat Genet 9 (4): 444-50, 1995.[PUBMED Abstract]
- Dobrovic A, Simpfendorfer D: Methylation of the BRCA1 gene in sporadic breast cancer. Cancer Res 57 (16): 3347-50, 1997.[PUBMED Abstract]
- Birgisdottir V, Stefansson OA, Bodvarsdottir SK, et al.: Epigenetic silencing and deletion of the BRCA1 gene in sporadic breast cancer. Breast Cancer Res 8 (4): R38, 2006.[PUBMED Abstract]
- Turner NC, Reis-Filho JS, Russell AM, et al.: BRCA1 dysfunction in sporadic basal-like breast cancer. Oncogene 26 (14): 2126-32, 2007.[PUBMED Abstract]
- Rakha EA, El-Sheikh SE, Kandil MA, et al.: Expression of BRCA1 protein in breast cancer and its prognostic significance. Hum Pathol 39 (6): 857-65, 2008.[PUBMED Abstract]
- Wong EM, Southey MC, Fox SB, et al.: Constitutional methylation of the BRCA1 promoter is specifically associated with BRCA1 mutation-associated pathology in early-onset breast cancer. Cancer Prev Res (Phila) 4 (1): 23-33, 2011.[PUBMED Abstract]
- Cleton-Jansen AM, Collins N, Lakhani SR, et al.: Loss of heterozygosity in sporadic breast tumours at the BRCA2 locus on chromosome 13q12-q13. Br J Cancer 72 (5): 1241-4, 1995.[PUBMED Abstract]
- Hamann U, Herbold C, Costa S, et al.: Allelic imbalance on chromosome 13q: evidence for the involvement of BRCA2 and RB1 in sporadic breast cancer. Cancer Res 56 (9): 1988-90, 1996.[PUBMED Abstract]
- Farmer H, McCabe N, Lord CJ, et al.: Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy. Nature 434 (7035): 917-21, 2005.[PUBMED Abstract]
- Lakhani SR, Manek S, Penault-Llorca F, et al.: Pathology of ovarian cancers in BRCA1 and BRCA2 carriers. Clin Cancer Res 10 (7): 2473-81, 2004.[PUBMED Abstract]
- Evans DG, Young K, Bulman M, et al.: Probability of BRCA1/2 mutation varies with ovarian histology: results from screening 442 ovarian cancer families. Clin Genet 73 (4): 338-45, 2008.[PUBMED Abstract]
- Tonin PN, Maugard CM, Perret C, et al.: A review of histopathological subtypes of ovarian cancer in BRCA-related French Canadian cancer families. Fam Cancer 6 (4): 491-7, 2007.[PUBMED Abstract]
- Bolton KL, Chenevix-Trench G, Goh C, et al.: Association between BRCA1 and BRCA2 mutations and survival in women with invasive epithelial ovarian cancer. JAMA 307 (4): 382-90, 2012.[PUBMED Abstract]
- Liu J, Cristea MC, Frankel P, et al.: Clinical characteristics and outcomes of BRCA-associated ovarian cancer: genotype and survival. Cancer Genet 205 (1-2): 34-41, 2012 Jan-Feb.[PUBMED Abstract]
- Crum CP, Drapkin R, Kindelberger D, et al.: Lessons from BRCA: the tubal fimbria emerges as an origin for pelvic serous cancer. Clin Med Res 5 (1): 35-44, 2007.[PUBMED Abstract]
- Piek JM, van Diest PJ, Zweemer RP, et al.: Dysplastic changes in prophylactically removed Fallopian tubes of women predisposed to developing ovarian cancer. J Pathol 195 (4): 451-6, 2001.[PUBMED Abstract]
- Carcangiu ML, Radice P, Manoukian S, et al.: Atypical epithelial proliferation in fallopian tubes in prophylactic salpingo-oophorectomy specimens from BRCA1 and BRCA2 germline mutation carriers. Int J Gynecol Pathol 23 (1): 35-40, 2004.[PUBMED Abstract]
- Mehra K, Mehrad M, Ning G, et al.: STICS, SCOUTs and p53 signatures; a new language for pelvic serous carcinogenesis. Front Biosci (Elite Ed) 3: 625-34, 2011.[PUBMED Abstract]
- Powell CB, Chen LM, McLennan J, et al.: Risk-reducing salpingo-oophorectomy (RRSO) in BRCA mutation carriers: experience with a consecutive series of 111 patients using a standardized surgical-pathological protocol. Int J Gynecol Cancer 21 (5): 846-51, 2011.[PUBMED Abstract]
- Finch A, Shaw P, Rosen B, et al.: Clinical and pathologic findings of prophylactic salpingo-oophorectomies in 159 BRCA1 and BRCA2 carriers. Gynecol Oncol 100 (1): 58-64, 2006.[PUBMED Abstract]
- Medeiros F, Muto MG, Lee Y, et al.: The tubal fimbria is a preferred site for early adenocarcinoma in women with familial ovarian cancer syndrome. Am J Surg Pathol 30 (2): 230-6, 2006.[PUBMED Abstract]
- Prat J; FIGO Committee on Gynecologic Oncology: Staging classification for cancer of the ovary, fallopian tube, and peritoneum. Int J Gynaecol Obstet 124 (1): 1-5, 2014.[PUBMED Abstract]
- Schorge JO, Muto MG, Lee SJ, et al.: BRCA1-related papillary serous carcinoma of the peritoneum has a unique molecular pathogenesis. Cancer Res 60 (5): 1361-4, 2000.[PUBMED Abstract]
- Jazaeri AA, Yee CJ, Sotiriou C, et al.: Gene expression profiles of BRCA1-linked, BRCA2-linked, and sporadic ovarian cancers. J Natl Cancer Inst 94 (13): 990-1000, 2002.[PUBMED Abstract]
- Gourley C, Michie CO, Roxburgh P, et al.: Increased incidence of visceral metastases in scottish patients with BRCA1/2-defective ovarian cancer: an extension of the ovarian BRCAness phenotype. J Clin Oncol 28 (15): 2505-11, 2010.[PUBMED Abstract]
- Vineyard MA, Daniels MS, Urbauer DL, et al.: Is low-grade serous ovarian cancer part of the tumor spectrum of hereditary breast and ovarian cancer? Gynecol Oncol 120 (2): 229-32, 2011.[PUBMED Abstract]
- Norquist BM, Harrell MI, Brady MF, et al.: Inherited Mutations in Women With Ovarian Carcinoma. JAMA Oncol 2 (4): 482-90, 2016.[PUBMED Abstract]
- Hilton JL, Geisler JP, Rathe JA, et al.: Inactivation of BRCA1 and BRCA2 in ovarian cancer. J Natl Cancer Inst 94 (18): 1396-406, 2002.[PUBMED Abstract]
- Quinn JE, James CR, Stewart GE, et al.: BRCA1 mRNA expression levels predict for overall survival in ovarian cancer after chemotherapy. Clin Cancer Res 13 (24): 7413-20, 2007.[PUBMED Abstract]
- Geisler JP, Hatterman-Zogg MA, Rathe JA, et al.: Frequency of BRCA1 dysfunction in ovarian cancer. J Natl Cancer Inst 94 (1): 61-7, 2002.[PUBMED Abstract]
- Vasen HF: Clinical description of the Lynch syndrome [hereditary nonpolyposis colorectal cancer (HNPCC)]. Fam Cancer 4 (3): 219-25, 2005.[PUBMED Abstract]
- Jascur T, Boland CR: Structure and function of the components of the human DNA mismatch repair system. Int J Cancer 119 (9): 2030-5, 2006.[PUBMED Abstract]
- Papadopoulos N, Nicolaides NC, Wei YF, et al.: Mutation of a mutL homolog in hereditary colon cancer. Science 263 (5153): 1625-9, 1994.[PUBMED Abstract]
- Peltomäki P, Vasen HF: Mutations predisposing to hereditary nonpolyposis colorectal cancer: database and results of a collaborative study. The International Collaborative Group on Hereditary Nonpolyposis Colorectal Cancer. Gastroenterology 113 (4): 1146-58, 1997.[PUBMED Abstract]
- Akiyama Y, Sato H, Yamada T, et al.: Germ-line mutation of the hMSH6/GTBP gene in an atypical hereditary nonpolyposis colorectal cancer kindred. Cancer Res 57 (18): 3920-3, 1997.[PUBMED Abstract]
- Miyaki M, Konishi M, Tanaka K, et al.: Germline mutation of MSH6 as the cause of hereditary nonpolyposis colorectal cancer. Nat Genet 17 (3): 271-2, 1997.[PUBMED Abstract]
- Huang J, Kuismanen SA, Liu T, et al.: MSH6 and MSH3 are rarely involved in genetic predisposition to nonpolypotic colon cancer. Cancer Res 61 (4): 1619-23, 2001.[PUBMED Abstract]
- Nicolaides NC, Papadopoulos N, Liu B, et al.: Mutations of two PMS homologues in hereditary nonpolyposis colon cancer. Nature 371 (6492): 75-80, 1994.[PUBMED Abstract]
- Hendriks YM, Jagmohan-Changur S, van der Klift HM, et al.: Heterozygous mutations in PMS2 cause hereditary nonpolyposis colorectal carcinoma (Lynch syndrome). Gastroenterology 130 (2): 312-22, 2006.[PUBMED Abstract]
- Worthley DL, Walsh MD, Barker M, et al.: Familial mutations in PMS2 can cause autosomal dominant hereditary nonpolyposis colorectal cancer. Gastroenterology 128 (5): 1431-6, 2005.[PUBMED Abstract]
- Vasen HF, Mecklin JP, Khan PM, et al.: The International Collaborative Group on Hereditary Non-Polyposis Colorectal Cancer (ICG-HNPCC). Dis Colon Rectum 34 (5): 424-5, 1991.[PUBMED Abstract]
- Vasen HF, Watson P, Mecklin JP, et al.: New clinical criteria for hereditary nonpolyposis colorectal cancer (HNPCC, Lynch syndrome) proposed by the International Collaborative group on HNPCC. Gastroenterology 116 (6): 1453-6, 1999.[PUBMED Abstract]
- Rodriguez-Bigas MA, Boland CR, Hamilton SR, et al.: A National Cancer Institute Workshop on Hereditary Nonpolyposis Colorectal Cancer Syndrome: meeting highlights and Bethesda guidelines. J Natl Cancer Inst 89 (23): 1758-62, 1997.[PUBMED Abstract]
- Umar A, Boland CR, Terdiman JP, et al.: Revised Bethesda Guidelines for hereditary nonpolyposis colorectal cancer (Lynch syndrome) and microsatellite instability. J Natl Cancer Inst 96 (4): 261-8, 2004.[PUBMED Abstract]
- Watson P, Lynch HT: Cancer risk in mismatch repair gene mutation carriers. Fam Cancer 1 (1): 57-60, 2001.[PUBMED Abstract]
- Vasen HF, Wijnen JT, Menko FH, et al.: Cancer risk in families with hereditary nonpolyposis colorectal cancer diagnosed by mutation analysis. Gastroenterology 110 (4): 1020-7, 1996.[PUBMED Abstract]
- Aarnio M, Mecklin JP, Aaltonen LA, et al.: Life-time risk of different cancers in hereditary non-polyposis colorectal cancer (HNPCC) syndrome. Int J Cancer 64 (6): 430-3, 1995.[PUBMED Abstract]
- Watson P, Lynch HT: Extracolonic cancer in hereditary nonpolyposis colorectal cancer. Cancer 71 (3): 677-85, 1993.[PUBMED Abstract]
- Brown GJ, St John DJ, Macrae FA, et al.: Cancer risk in young women at risk of hereditary nonpolyposis colorectal cancer: implications for gynecologic surveillance. Gynecol Oncol 80 (3): 346-9, 2001.[PUBMED Abstract]
- Aarnio M, Sankila R, Pukkala E, et al.: Cancer risk in mutation carriers of DNA-mismatch-repair genes. Int J Cancer 81 (2): 214-8, 1999.[PUBMED Abstract]
- Ten Broeke SW, van der Klift HM, Tops CMJ, et al.: Cancer Risks for PMS2-Associated Lynch Syndrome. J Clin Oncol 36 (29): 2961-2968, 2018.[PUBMED Abstract]
- Møller P, Seppälä TT, Bernstein I, et al.: Cancer risk and survival in path_MMR carriers by gene and gender up to 75 years of age: a report from the Prospective Lynch Syndrome Database. Gut 67 (7): 1306-1316, 2018.[PUBMED Abstract]
- Grindedal EM, Renkonen-Sinisalo L, Vasen H, et al.: Survival in women with MMR mutations and ovarian cancer: a multicentre study in Lynch syndrome kindreds. J Med Genet 47 (2): 99-102, 2010.[PUBMED Abstract]
- Pal T, Permuth-Wey J, Sellers TA: A review of the clinical relevance of mismatch-repair deficiency in ovarian cancer. Cancer 113 (4): 733-42, 2008.[PUBMED Abstract]
- Jensen UB, Sunde L, Timshel S, et al.: Mismatch repair defective breast cancer in the hereditary nonpolyposis colorectal cancer syndrome. Breast Cancer Res Treat 120 (3): 777-82, 2010.[PUBMED Abstract]
- Shanley S, Fung C, Milliken J, et al.: Breast cancer immunohistochemistry can be useful in triage of some HNPCC families. Fam Cancer 8 (3): 251-5, 2009.[PUBMED Abstract]
- Walsh MD, Buchanan DD, Cummings MC, et al.: Lynch syndrome-associated breast cancers: clinicopathologic characteristics of a case series from the colon cancer family registry. Clin Cancer Res 16 (7): 2214-24, 2010.[PUBMED Abstract]
- Buerki N, Gautier L, Kovac M, et al.: Evidence for breast cancer as an integral part of Lynch syndrome. Genes Chromosomes Cancer 51 (1): 83-91, 2012.[PUBMED Abstract]
- Win AK, Young JP, Lindor NM, et al.: Colorectal and other cancer risks for carriers and noncarriers from families with a DNA mismatch repair gene mutation: a prospective cohort study. J Clin Oncol 30 (9): 958-64, 2012.[PUBMED Abstract]
- Win AK, Lindor NM, Young JP, et al.: Risks of primary extracolonic cancers following colorectal cancer in lynch syndrome. J Natl Cancer Inst 104 (18): 1363-72, 2012.[PUBMED Abstract]
- Harkness EF, Barrow E, Newton K, et al.: Lynch syndrome caused by MLH1 mutations is associated with an increased risk of breast cancer: a cohort study. J Med Genet 52 (8): 553-6, 2015.[PUBMED Abstract]
- Win AK, Lindor NM, Jenkins MA: Risk of breast cancer in Lynch syndrome: a systematic review. Breast Cancer Res 15 (2): R27, 2013.[PUBMED Abstract]
- Goldberg M, Bell K, Aronson M, et al.: Association between the Lynch syndrome gene MSH2 and breast cancer susceptibility in a Canadian familial cancer registry. J Med Genet 54 (11): 742-746, 2017.[PUBMED Abstract]
- Roberts ME, Jackson SA, Susswein LR, et al.: MSH6 and PMS2 germ-line pathogenic variants implicated in Lynch syndrome are associated with breast cancer. Genet Med 20 (10): 1167-1174, 2018.[PUBMED Abstract]
- Espenschied CR, LaDuca H, Li S, et al.: Multigene Panel Testing Provides a New Perspective on Lynch Syndrome. J Clin Oncol 35 (22): 2568-2575, 2017.[PUBMED Abstract]
- Lu HM, Li S, Black MH, et al.: Association of Breast and Ovarian Cancers With Predisposition Genes Identified by Large-Scale Sequencing. JAMA Oncol 5 (1): 51-57, 2019.[PUBMED Abstract]
- Latham A, Srinivasan P, Kemel Y, et al.: Microsatellite Instability Is Associated With the Presence of Lynch Syndrome Pan-Cancer. J Clin Oncol 37 (4): 286-295, 2019.[PUBMED Abstract]
- Harris CC, Hollstein M: Clinical implications of the p53 tumor-suppressor gene. N Engl J Med 329 (18): 1318-27, 1993.[PUBMED Abstract]
- Malkin D: The Li-Fraumeni syndrome. Cancer: Principles and Practice of Oncology Updates 7(7): 1-14, 1993.[PUBMED Abstract]
- Gonzalez KD, Noltner KA, Buzin CH, et al.: Beyond Li Fraumeni Syndrome: clinical characteristics of families with p53 germline mutations. J Clin Oncol 27 (8): 1250-6, 2009.[PUBMED Abstract]
- Chompret A, Abel A, Stoppa-Lyonnet D, et al.: Sensitivity and predictive value of criteria for p53 germline mutation screening. J Med Genet 38 (1): 43-7, 2001.[PUBMED Abstract]
- Tinat J, Bougeard G, Baert-Desurmont S, et al.: 2009 version of the Chompret criteria for Li Fraumeni syndrome. J Clin Oncol 27 (26): e108-9; author reply e110, 2009.[PUBMED Abstract]
- Bottomley RH, Condit PT: Cancer families. Cancer Bull 20: 22-24, 1968.[PUBMED Abstract]
- Bougeard G, Renaux-Petel M, Flaman JM, et al.: Revisiting Li-Fraumeni Syndrome From TP53 Mutation Carriers. J Clin Oncol 33 (21): 2345-52, 2015.[PUBMED Abstract]
- Sidransky D, Tokino T, Helzlsouer K, et al.: Inherited p53 gene mutations in breast cancer. Cancer Res 52 (10): 2984-6, 1992.[PUBMED Abstract]
- Wilson JR, Bateman AC, Hanson H, et al.: A novel HER2-positive breast cancer phenotype arising from germline TP53 mutations. J Med Genet 47 (11): 771-4, 2010.[PUBMED Abstract]
- Melhem-Bertrandt A, Bojadzieva J, Ready KJ, et al.: Early onset HER2-positive breast cancer is associated with germline TP53 mutations. Cancer 118 (4): 908-13, 2012.[PUBMED Abstract]
- Masciari S, Dillon DA, Rath M, et al.: Breast cancer phenotype in women with TP53 germline mutations: a Li-Fraumeni syndrome consortium effort. Breast Cancer Res Treat 133 (3): 1125-30, 2012.[PUBMED Abstract]
- Pearson AD, Craft AW, Ratcliffe JM, et al.: Two families with the Li-Fraumeni cancer family syndrome. J Med Genet 19 (5): 362-5, 1982.[PUBMED Abstract]
- Li FP, Fraumeni JF, Mulvihill JJ, et al.: A cancer family syndrome in twenty-four kindreds. Cancer Res 48 (18): 5358-62, 1988.[PUBMED Abstract]
- Bougeard G, Sesboüé R, Baert-Desurmont S, et al.: Molecular basis of the Li-Fraumeni syndrome: an update from the French LFS families. J Med Genet 45 (8): 535-8, 2008.[PUBMED Abstract]
- Mai PL, Best AF, Peters JA, et al.: Risks of first and subsequent cancers among TP53 mutation carriers in the National Cancer Institute Li-Fraumeni syndrome cohort. Cancer 122 (23): 3673-3681, 2016.[PUBMED Abstract]
- Kamihara J, Rana HQ, Garber JE: Germline TP53 mutations and the changing landscape of Li-Fraumeni syndrome. Hum Mutat 35 (6): 654-62, 2014.[PUBMED Abstract]
- Mai PL, Khincha PP, Loud JT, et al.: Prevalence of Cancer at Baseline Screening in the National Cancer Institute Li-Fraumeni Syndrome Cohort. JAMA Oncol 3 (12): 1640-1645, 2017.[PUBMED Abstract]
- Villani A, Tabori U, Schiffman J, et al.: Biochemical and imaging surveillance in germline TP53 mutation carriers with Li-Fraumeni syndrome: a prospective observational study. Lancet Oncol 12 (6): 559-67, 2011.[PUBMED Abstract]
- Masciari S, Van den Abbeele AD, Diller LR, et al.: F18-fluorodeoxyglucose-positron emission tomography/computed tomography screening in Li-Fraumeni syndrome. JAMA 299 (11): 1315-9, 2008.[PUBMED Abstract]
- Zhou XP, Waite KA, Pilarski R, et al.: Germline PTEN promoter mutations and deletions in Cowden/Bannayan-Riley-Ruvalcaba syndrome result in aberrant PTEN protein and dysregulation of the phosphoinositol-3-kinase/Akt pathway. Am J Hum Genet 73 (2): 404-11, 2003.[PUBMED Abstract]
- Mester J, Eng C: When overgrowth bumps into cancer: the PTEN-opathies. Am J Med Genet C Semin Med Genet 163C (2): 114-21, 2013.[PUBMED Abstract]
- Eng C: PTEN: one gene, many syndromes. Hum Mutat 22 (3): 183-98, 2003.[PUBMED Abstract]
- Marsh DJ, Kum JB, Lunetta KL, et al.: PTEN mutation spectrum and genotype-phenotype correlations in Bannayan-Riley-Ruvalcaba syndrome suggest a single entity with Cowden syndrome. Hum Mol Genet 8 (8): 1461-72, 1999.[PUBMED Abstract]
- Pilarski R, Eng C: Will the real Cowden syndrome please stand up (again)? Expanding mutational and clinical spectra of the PTEN hamartoma tumour syndrome. J Med Genet 41 (5): 323-6, 2004.[PUBMED Abstract]
- Eng C: PTEN Hamartoma Tumor Syndrome (PHTS). In: Pagon RA, Adam MP, Bird TD, et al., eds.: GeneReviews. Seattle, Wash: University of Washington, 1993-2018, pp. Available online. Last accessed December 19, 2019.[PUBMED Abstract]
- Pilarski R, Burt R, Kohlman W, et al.: Cowden syndrome and the PTEN hamartoma tumor syndrome: systematic review and revised diagnostic criteria. J Natl Cancer Inst 105 (21): 1607-16, 2013.[PUBMED Abstract]
- Ngeow J, Liu C, Zhou K, et al.: Detecting Germline PTEN Mutations Among At-Risk Patients With Cancer: An Age- and Sex-Specific Cost-Effectiveness Analysis. J Clin Oncol 33 (23): 2537-44, 2015.[PUBMED Abstract]
- Tan MH, Mester JL, Ngeow J, et al.: Lifetime cancer risks in individuals with germline PTEN mutations. Clin Cancer Res 18 (2): 400-7, 2012.[PUBMED Abstract]
- Bubien V, Bonnet F, Brouste V, et al.: High cumulative risks of cancer in patients with PTEN hamartoma tumour syndrome. J Med Genet 50 (4): 255-63, 2013.[PUBMED Abstract]
- Myers MP, Tonks NK: PTEN: sometimes taking it off can be better than putting it on. Am J Hum Genet 61 (6): 1234-8, 1997.[PUBMED Abstract]
- Hobert JA, Eng C: PTEN hamartoma tumor syndrome: an overview. Genet Med 11 (10): 687-94, 2009.[PUBMED Abstract]
- Nieuwenhuis MH, Kets CM, Murphy-Ryan M, et al.: Cancer risk and genotype-phenotype correlations in PTEN hamartoma tumor syndrome. Fam Cancer 13 (1): 57-63, 2014.[PUBMED Abstract]
- Ngeow J, Stanuch K, Mester JL, et al.: Second malignant neoplasms in patients with Cowden syndrome with underlying germline PTEN mutations. J Clin Oncol 32 (17): 1818-24, 2014.[PUBMED Abstract]
- Olopade OI, Weber BL: Breast cancer genetics: toward molecular characterization of individuals at increased risk for breast cancer: part I. Cancer: Principles and Practice of Oncology Updates 12 (10): 1-12, 1998.[PUBMED Abstract]
- Pilarski R, Stephens JA, Noss R, et al.: Predicting PTEN mutations: an evaluation of Cowden syndrome and Bannayan-Riley-Ruvalcaba syndrome clinical features. J Med Genet 48 (8): 505-12, 2011.[PUBMED Abstract]
- Nelen MR, Padberg GW, Peeters EA, et al.: Localization of the gene for Cowden disease to chromosome 10q22-23. Nat Genet 13 (1): 114-6, 1996.[PUBMED Abstract]
- Lachlan KL, Lucassen AM, Bunyan D, et al.: Cowden syndrome and Bannayan Riley Ruvalcaba syndrome represent one condition with variable expression and age-related penetrance: results of a clinical study of PTEN mutation carriers. J Med Genet 44 (9): 579-85, 2007.[PUBMED Abstract]
- Benusiglio PR, Malka D, Rouleau E, et al.: CDH1 germline mutations and the hereditary diffuse gastric and lobular breast cancer syndrome: a multicentre study. J Med Genet 50 (7): 486-9, 2013.[PUBMED Abstract]
- Beeghly-Fadiel A, Lu W, Gao YT, et al.: E-cadherin polymorphisms and breast cancer susceptibility: a report from the Shanghai Breast Cancer Study. Breast Cancer Res Treat 121 (2): 445-52, 2010.[PUBMED Abstract]
- McVeigh TP, Choi JK, Miller NM, et al.: Lobular breast cancer in a CDH1 splice site mutation carrier: case report and review of the literature. Clin Breast Cancer 14 (2): e47-51, 2014.[PUBMED Abstract]
- Petridis C, Shinomiya I, Kohut K, et al.: Germline CDH1 mutations in bilateral lobular carcinoma in situ. Br J Cancer 110 (4): 1053-7, 2014.[PUBMED Abstract]
- Tipirisetti NR, Govatati S, Govatati S, et al.: Association of E-cadherin single-nucleotide polymorphisms with the increased risk of breast cancer: a study in South Indian women. Genet Test Mol Biomarkers 17 (6): 494-500, 2013.[PUBMED Abstract]
- Fitzgerald RC, Hardwick R, Huntsman D, et al.: Hereditary diffuse gastric cancer: updated consensus guidelines for clinical management and directions for future research. J Med Genet 47 (7): 436-44, 2010.[PUBMED Abstract]
- Xie ZM, Li LS, Laquet C, et al.: Germline mutations of the E-cadherin gene in families with inherited invasive lobular breast carcinoma but no diffuse gastric cancer. Cancer 117 (14): 3112-7, 2011.[PUBMED Abstract]
- Peutz JL: Very remarkable case of familial polyposis of mucous membrane of intestinal tract and nasopharynx accompanied by peculiar pigmentations of skin and mucous membrane. Ned Tijdschr Geneeskd 10: 134-146, 1921.[PUBMED Abstract]
- Jeghers H, McKusick VA, Katz KH: Generalized intestinal polyposis and melanin spots of the oral mucosa, lips and digits; a syndrome of diagnostic significance. N Engl J Med 241 (26): 1031-6, 1949.[PUBMED Abstract]
- Spigelman AD, Murday V, Phillips RK: Cancer and the Peutz-Jeghers syndrome. Gut 30 (11): 1588-90, 1989.[PUBMED Abstract]
- Aretz S, Stienen D, Uhlhaas S, et al.: High proportion of large genomic STK11 deletions in Peutz-Jeghers syndrome. Hum Mutat 26 (6): 513-9, 2005.[PUBMED Abstract]
- Hemminki A, Markie D, Tomlinson I, et al.: A serine/threonine kinase gene defective in Peutz-Jeghers syndrome. Nature 391 (6663): 184-7, 1998.[PUBMED Abstract]
- Jenne DE, Reimann H, Nezu J, et al.: Peutz-Jeghers syndrome is caused by mutations in a novel serine threonine kinase. Nat Genet 18 (1): 38-43, 1998.[PUBMED Abstract]
- Boudeau J, Kieloch A, Alessi DR, et al.: Functional analysis of LKB1/STK11 mutants and two aberrant isoforms found in Peutz-Jeghers Syndrome patients. Hum Mutat 21 (2): 172, 2003.[PUBMED Abstract]
- Lim W, Hearle N, Shah B, et al.: Further observations on LKB1/STK11 status and cancer risk in Peutz-Jeghers syndrome. Br J Cancer 89 (2): 308-13, 2003.[PUBMED Abstract]
- Giardiello FM, Brensinger JD, Tersmette AC, et al.: Very high risk of cancer in familial Peutz-Jeghers syndrome. Gastroenterology 119 (6): 1447-53, 2000.[PUBMED Abstract]
- Hearle N, Schumacher V, Menko FH, et al.: Frequency and spectrum of cancers in the Peutz-Jeghers syndrome. Clin Cancer Res 12 (10): 3209-15, 2006.[PUBMED Abstract]
- Lim W, Olschwang S, Keller JJ, et al.: Relative frequency and morphology of cancers in STK11 mutation carriers. Gastroenterology 126 (7): 1788-94, 2004.[PUBMED Abstract]
- van Lier MG, Wagner A, Mathus-Vliegen EM, et al.: High cancer risk in Peutz-Jeghers syndrome: a systematic review and surveillance recommendations. Am J Gastroenterol 105 (6): 1258-64; author reply 1265, 2010.[PUBMED Abstract]
- Srivatsa PJ, Keeney GL, Podratz KC: Disseminated cervical adenoma malignum and bilateral ovarian sex cord tumors with annular tubules associated with Peutz-Jeghers syndrome. Gynecol Oncol 53 (2): 256-64, 1994.[PUBMED Abstract]
- Scully RE: Sex cord tumor with annular tubules a distinctive ovarian tumor of the Peutz-Jeghers syndrome. Cancer 25 (5): 1107-21, 1970.[PUBMED Abstract]
- Westerman AM, Entius MM, de Baar E, et al.: Peutz-Jeghers syndrome: 78-year follow-up of the original family. Lancet 353 (9160): 1211-5, 1999.[PUBMED Abstract]
- Mehenni H, Resta N, Park JG, et al.: Cancer risks in LKB1 germline mutation carriers. Gut 55 (7): 984-90, 2006.[PUBMED Abstract]
- Gruber SB, Entius MM, Petersen GM, et al.: Pathogenesis of adenocarcinoma in Peutz-Jeghers syndrome. Cancer Res 58 (23): 5267-70, 1998.[PUBMED Abstract]
- Wang ZJ, Ellis I, Zauber P, et al.: Allelic imbalance at the LKB1 (STK11) locus in tumours from patients with Peutz-Jeghers' syndrome provides evidence for a hamartoma-(adenoma)-carcinoma sequence. J Pathol 188 (1): 9-13, 1999.[PUBMED Abstract]
- Miyoshi H, Nakau M, Ishikawa TO, et al.: Gastrointestinal hamartomatous polyposis in Lkb1 heterozygous knockout mice. Cancer Res 62 (8): 2261-6, 2002.[PUBMED Abstract]
- Nakau M, Miyoshi H, Seldin MF, et al.: Hepatocellular carcinoma caused by loss of heterozygosity in Lkb1 gene knockout mice. Cancer Res 62 (16): 4549-53, 2002.[PUBMED Abstract]
- Takeda H, Miyoshi H, Kojima Y, et al.: Accelerated onsets of gastric hamartomas and hepatic adenomas/carcinomas in Lkb1+/-p53-/- compound mutant mice. Oncogene 25 (12): 1816-20, 2006.[PUBMED Abstract]
- Amos CI, Keitheri-Cheteri MB, Sabripour M, et al.: Genotype-phenotype correlations in Peutz-Jeghers syndrome. J Med Genet 41 (5): 327-33, 2004.[PUBMED Abstract]
- Reid S, Schindler D, Hanenberg H, et al.: Biallelic mutations in PALB2 cause Fanconi anemia subtype FA-N and predispose to childhood cancer. Nat Genet 39 (2): 162-4, 2007.[PUBMED Abstract]
- Rahman N, Seal S, Thompson D, et al.: PALB2, which encodes a BRCA2-interacting protein, is a breast cancer susceptibility gene. Nat Genet 39 (2): 165-7, 2007.[PUBMED Abstract]
- Erkko H, Dowty JG, Nikkilä J, et al.: Penetrance analysis of the PALB2 c.1592delT founder mutation. Clin Cancer Res 14 (14): 4667-71, 2008.[PUBMED Abstract]
- Heikkinen T, Kärkkäinen H, Aaltonen K, et al.: The breast cancer susceptibility mutation PALB2 1592delT is associated with an aggressive tumor phenotype. Clin Cancer Res 15 (9): 3214-22, 2009.[PUBMED Abstract]
- Ding YC, Steele L, Chu LH, et al.: Germline mutations in PALB2 in African-American breast cancer cases. Breast Cancer Res Treat 126 (1): 227-30, 2011.[PUBMED Abstract]
- Foulkes WD, Ghadirian P, Akbari MR, et al.: Identification of a novel truncating PALB2 mutation and analysis of its contribution to early-onset breast cancer in French-Canadian women. Breast Cancer Res 9 (6): R83, 2007.[PUBMED Abstract]
- Casadei S, Norquist BM, Walsh T, et al.: Contribution of inherited mutations in the BRCA2-interacting protein PALB2 to familial breast cancer. Cancer Res 71 (6): 2222-9, 2011.[PUBMED Abstract]
- Southey MC, Teo ZL, Dowty JG, et al.: A PALB2 mutation associated with high risk of breast cancer. Breast Cancer Res 12 (6): R109, 2010.[PUBMED Abstract]
- Hellebrand H, Sutter C, Honisch E, et al.: Germline mutations in the PALB2 gene are population specific and occur with low frequencies in familial breast cancer. Hum Mutat 32 (6): E2176-88, 2011.[PUBMED Abstract]
- Bogdanova N, Sokolenko AP, Iyevleva AG, et al.: PALB2 mutations in German and Russian patients with bilateral breast cancer. Breast Cancer Res Treat 126 (2): 545-50, 2011.[PUBMED Abstract]
- Wong MW, Nordfors C, Mossman D, et al.: BRIP1, PALB2, and RAD51C mutation analysis reveals their relative importance as genetic susceptibility factors for breast cancer. Breast Cancer Res Treat 127 (3): 853-9, 2011.[PUBMED Abstract]
- Zheng Y, Zhang J, Niu Q, et al.: Novel germline PALB2 truncating mutations in African American breast cancer patients. Cancer 118 (5): 1362-70, 2012.[PUBMED Abstract]
- Tischkowitz M, Capanu M, Sabbaghian N, et al.: Rare germline mutations in PALB2 and breast cancer risk: a population-based study. Hum Mutat 33 (4): 674-80, 2012.[PUBMED Abstract]
- Fernandes PH, Saam J, Peterson J, et al.: Comprehensive sequencing of PALB2 in patients with breast cancer suggests PALB2 mutations explain a subset of hereditary breast cancer. Cancer 120 (7): 963-7, 2014.[PUBMED Abstract]
- Janatova M, Kleibl Z, Stribrna J, et al.: The PALB2 gene is a strong candidate for clinical testing in BRCA1- and BRCA2-negative hereditary breast cancer. Cancer Epidemiol Biomarkers Prev 22 (12): 2323-32, 2013.[PUBMED Abstract]
- Teo ZL, Sawyer SD, James PA, et al.: The incidence of PALB2 c.3113G>A in women with a strong family history of breast and ovarian cancer attending familial cancer centres in Australia. Fam Cancer 12 (4): 587-95, 2013.[PUBMED Abstract]
- Snyder C, Metcalfe K, Sopik V, et al.: Prevalence of PALB2 mutations in the Creighton University Breast Cancer Family Registry. Breast Cancer Res Treat 150 (3): 637-41, 2015.[PUBMED Abstract]
- Nguyen-Dumont T, Hammet F, Mahmoodi M, et al.: Mutation screening of PALB2 in clinically ascertained families from the Breast Cancer Family Registry. Breast Cancer Res Treat 149 (2): 547-54, 2015.[PUBMED Abstract]
- Damiola F, Schultz I, Barjhoux L, et al.: Mutation analysis of PALB2 gene in French breast cancer families. Breast Cancer Res Treat 154 (3): 463-71, 2015.[PUBMED Abstract]
- Antoniou AC, Casadei S, Heikkinen T, et al.: Breast-cancer risk in families with mutations in PALB2. N Engl J Med 371 (6): 497-506, 2014.[PUBMED Abstract]
- Cybulski C, Kluźniak W, Huzarski T, et al.: Clinical outcomes in women with breast cancer and a PALB2 mutation: a prospective cohort analysis. Lancet Oncol 16 (6): 638-44, 2015.[PUBMED Abstract]
- Yang X, Leslie G, Doroszuk A, et al.: Cancer Risks Associated With Germline PALB2 Pathogenic Variants: An International Study of 524 Families. J Clin Oncol 38 (7): 674-685, 2020.[PUBMED Abstract]
- Jones S, Hruban RH, Kamiyama M, et al.: Exomic sequencing identifies PALB2 as a pancreatic cancer susceptibility gene. Science 324 (5924): 217, 2009.[PUBMED Abstract]
- Slater EP, Langer P, Niemczyk E, et al.: PALB2 mutations in European familial pancreatic cancer families. Clin Genet 78 (5): 490-4, 2010.[PUBMED Abstract]
- Hofstatter EW, Domchek SM, Miron A, et al.: PALB2 mutations in familial breast and pancreatic cancer. Fam Cancer 10 (2): 225-31, 2011.[PUBMED Abstract]
- Stadler ZK, Salo-Mullen E, Sabbaghian N, et al.: Germline PALB2 mutation analysis in breast-pancreas cancer families. J Med Genet 48 (8): 523-5, 2011.[PUBMED Abstract]
- Ghiorzo P, Pensotti V, Fornarini G, et al.: Contribution of germline mutations in the BRCA and PALB2 genes to pancreatic cancer in Italy. Fam Cancer 11 (1): 41-7, 2012.[PUBMED Abstract]
- Westerman AM, Entius MM, Boor PP, et al.: Novel mutations in the LKB1/STK11 gene in Dutch Peutz-Jeghers families. Hum Mutat 13 (6): 476-81, 1999.[PUBMED Abstract]
- Schreibman IR, Baker M, Amos C, et al.: The hamartomatous polyposis syndromes: a clinical and molecular review. Am J Gastroenterol 100 (2): 476-90, 2005.[PUBMED Abstract]
- Gonzalez KD, Buzin CH, Noltner KA, et al.: High frequency of de novo mutations in Li-Fraumeni syndrome. J Med Genet 46 (10): 689-93, 2009.[PUBMED Abstract]
- Bendig I, Mohr N, Kramer F, et al.: Identification of novel TP53 mutations in familial and sporadic cancer cases of German and Swiss origin. Cancer Genet Cytogenet 154 (1): 22-6, 2004.[PUBMED Abstract]
- De Leeneer K, Coene I, Crombez B, et al.: Prevalence of BRCA1/2 mutations in sporadic breast/ovarian cancer patients and identification of a novel de novo BRCA1 mutation in a patient diagnosed with late onset breast and ovarian cancer: implications for genetic testing. Breast Cancer Res Treat 132 (1): 87-95, 2012.[PUBMED Abstract]
- Diez O, Gutiérrez-Enríquez S, Mediano C, et al.: A novel de novo BRCA2 mutation of paternal origin identified in a Spanish woman with early onset bilateral breast cancer. Breast Cancer Res Treat 121 (1): 221-5, 2010.[PUBMED Abstract]
- Garcia-Casado Z, Romero I, Fernandez-Serra A, et al.: A de novo complete BRCA1 gene deletion identified in a Spanish woman with early bilateral breast cancer. BMC Med Genet 12: 134, 2011.[PUBMED Abstract]
- Hansen TV, Bisgaard ML, Jønson L, et al.: Novel de novo BRCA2 mutation in a patient with a family history of breast cancer. BMC Med Genet 9: 58, 2008.[PUBMED Abstract]
- Kwong A, Ng EK, Tang EY, et al.: A novel de novo BRCA1 mutation in a Chinese woman with early onset breast cancer. Fam Cancer 10 (2): 233-7, 2011.[PUBMED Abstract]
- Marshall M, Solomon S, Lawrence Wickerham D: Case report: de novo BRCA2 gene mutation in a 35-year-old woman with breast cancer. Clin Genet 76 (5): 427-30, 2009.[PUBMED Abstract]
- Robson M, Scheuer L, Nafa K, et al.: Unique de novo mutation of BRCA2 in a woman with early onset breast cancer. J Med Genet 39 (2): 126-8, 2002.[PUBMED Abstract]
- Tesoriero A, Andersen C, Southey M, et al.: De novo BRCA1 mutation in a patient with breast cancer and an inherited BRCA2 mutation. Am J Hum Genet 65 (2): 567-9, 1999.[PUBMED Abstract]
- van der Luijt RB, van Zon PH, Jansen RP, et al.: De novo recurrent germline mutation of the BRCA2 gene in a patient with early onset breast cancer. J Med Genet 38 (2): 102-5, 2001.[PUBMED Abstract]
- Morak M, Laner A, Scholz M, et al.: Report on de-novo mutation in the MSH2 gene as a rare event in hereditary nonpolyposis colorectal cancer. Eur J Gastroenterol Hepatol 20 (11): 1101-5, 2008.[PUBMED Abstract]
- Plasilova M, Zhang J, Okhowat R, et al.: A de novo MLH1 germ line mutation in a 31-year-old colorectal cancer patient. Genes Chromosomes Cancer 45 (12): 1106-10, 2006.[PUBMED Abstract]
- Win AK, Jenkins MA, Buchanan DD, et al.: Determining the frequency of de novo germline mutations in DNA mismatch repair genes. J Med Genet 48 (8): 530-4, 2011.[PUBMED Abstract]
- Anderson KG: How well does paternity confidence match actual paternity? Evidence from worldwide nonpaternity rates. Curr Anthropol 47 (3): 513-20, 2006. Also available online. Last accessed January 22, 2020.[PUBMED Abstract]
- Sasse G, Müller H, Chakraborty R, et al.: Estimating the frequency of nonpaternity in Switzerland. Hum Hered 44 (6): 337-43, 1994 Nov-Dec.[PUBMED Abstract]
- Voracek M, Haubner T, Fisher ML: Recent decline in nonpaternity rates: a cross-temporal meta-analysis. Psychol Rep 103 (3): 799-811, 2008.[PUBMED Abstract]
- 乳がんおよび/または婦人科がんに関連する中浸透度の遺伝子
-
背景
BRCA1、BRCA2、PALB2、および本要約の高浸透度の乳がんおよび/または婦人科がん感受性遺伝子のセクションで述べた他のまれな症候群に関与する遺伝子における病原性多様体が家族性の乳がんリスクに占める割合は25%未満である。[ 1 ]遺伝的連鎖研究が集中的に行われているにもかかわらず、複数の症例を認める残りの家族集積の相当数を説明する、浸透度が高い他の遺伝子は存在しないようである。[ 2 ]しかしながら、乳がんおよび/または婦人科がんに関連するいくつかの中浸透度の遺伝子が特定されている。CHEK2およびATMなどの遺伝子は乳がんの20%以上の生涯リスクと関連している;[ 3 ][ 4 ]同様に、RAD51C、RAD51D、およびBRIP1などの遺伝子は卵巣がんのリスクの5~10%と関連している。[ 5 ][ 6 ]現在、これらの遺伝子の多くは多重遺伝子パネルに含められているが、これらの所見の臨床的利用可能性はなおも不明であり、研究が行われている。
候補遺伝子アプローチにより同定された乳がんおよび婦人科がん感受性遺伝子
さまざまな遺伝子座と乳がんリスク間の関連について記述した遺伝疫学研究に関する非常に大規模な文献がある。これらの研究の多くは重大なデザイン上の制約を受けている。結果としておそらく、ほとんどの研究では、関連は追跡研究で再現されないと報告された。本セクションは、報告されたすべての関連を包括的にレビューしているわけではない。本セクションでは、関連が数件の研究で記述されているか、頑健なメタアナリシスにより支持されているという点で、編集者らにより臨床的に妥当であると考えられている関連について記述している。しかしながら、これらの変異と関連しているリスクは通常、臨床反応を正当化する閾値を下回っているため、これらの観察の臨床的有用性は依然として不明のままである。
ファンコニー貧血遺伝子
ファンコニー貧血(FA)はまれな遺伝性疾患で、骨髄機能不全、悪性腫瘍のリスク増加、および身体的異常を特徴とする。現在までのところ、BRCA1およびBRCA2を含めて、16個のファンコニー貧血関連遺伝子が同定されている(表10で略述している)。ファンコニー貧血は、X連鎖劣性遺伝であるFANCBにおける病原性多様体を原因とする場合を除いて、主に常染色体劣性疾患である。FANCAは病原性多様体の60~70%を占め、FANCCは約14%、残りの遺伝子がそれぞれ3%未満を占める。[ 7 ]
表10.ファンコニー貧血遺伝子および乳がんリスク aBRCA1およびBRCA2病原性多様体キャリアの乳がんの累積リスクに関する情報は、本要約のBRCA1とBRCA2のセクションを参照のこと。 bPALB2病原性多様体キャリアの乳がんの累積リスクに関する情報は、本要約のPALB2のセクションを参照のこと。 c中等度リスクは統計的に有意な2倍までのリスク推定値として定義される。 高リスク遺伝子 – BRCA1(FANCS)a – BRCA2(FANCD1)a – PALB2(FANCN)b 中等度リスク遺伝子c – BRIP1(FANCJ/BACH1) – FANCD2 – RAD51C(FANCO) リスクを増加させるかどうかが不明または有意な増加をもたらさない遺伝子 – FANCA – FANCB – FANCC – FANCE – FANCF – FANCG(XRCC9) – FANCI(KIAA1794) – FANCL – SLX4(FANCP) – ERCC4(FANCQ/XPF) 進行性の骨髄機能不全は、血小板減少症および白血球減少症をしばしば発症する患者で典型的に最初の10年以内に発症する。骨髄機能不全の発生率は、40~50歳までで90%である。血液学的悪性腫瘍(主に急性骨髄性白血病)の発生率は10~30%で、非血液学的悪性腫瘍(特に頭頸部、皮膚、消化[GI]管、生殖管の固形腫瘍)の発生率は25~30%である。罹患者の60~75%に身体的異常(低身長、皮膚色素沈着の異常、母指変形といった放射線欠損など)、尿路、眼球、耳、心臓、消化器系、中枢神経系の異常、甲状腺機能低下症、および発達遅滞が認められる。[ 7 ]
一部のファンコニー貧血遺伝子の多様体、なかでも最も注目すべきはBRCA1およびBRCA2であるが、さらにPALB2、RAD51C(RAD51遺伝子ファミリーにおいて)、BRIP1の多様体も、ヘテロ接合体において乳がんの素因となりうる。多重遺伝子(パネル)検査が広く利用可能なことを前提として、ファンコニー貧血遺伝子の多くに対する遺伝子検査は、がんリスクが不明であり、これらの遺伝子の多くに対して利用可能な証拠に基づく医学的管理の推奨が不足しているにもかかわらず、頻繁に実施されている。
ファンコニー貧血遺伝子の病原性多様体キャリアであるということは、両親が同じ遺伝子の病原性多様体キャリアであれば、これらの遺伝子の病原性多様体により小児に重篤な疾患が発現する可能性があることから、出産に関する意思決定に影響を及ぼす可能性がある。パートナーの検査が検討されることがある。
BRIP1
BRIP1(BACH1としても知られる)は、BRCA1 C-末端(BRCT)領域と相互作用するヘリカーゼをコードする。この遺伝子はBRCA1依存性のDNA修復および細胞周期チェックポイント機能においても役割を担っている。BRIP1における両アレル性病原性多様体はファンコニー貧血の原因であり[ 8 ][ 9 ][ 10 ]、BRCA2における同様の病原性多様体とよく似ている。BRIP1の不活性化多様体は乳がんリスクの増加と関連している。1件の研究で、BRCA1/BRCA2病原性多様体陰性家系出身の3,000人を超える個人が、BRIP1多様体について調べられた。乳がんを認める1,212人中9人に病原性多様体が同定されたが、2,081人の対照では2人にしか同定されなかった(P = 0.003)。乳がんの相対リスク(RR)は、2.0(95%信頼区間[CI]、1.2-3.2;P = 0.012)と推定された。注目すべきことに、BRIP1病原性多様体を認め、乳がん症例を複数生じた家系では、乳がんを伴う病原性多様体の分離が不完全であり、浸透度の低いアレルと一致し、CHEK2でみられるものと類似していた。[ 11 ]卵巣がん女性3,236人を対象とした1件のケースコントロール研究では、BRIP1病原性多様体は卵巣がんリスクとより高頻度に関連していた(RR、11.2;95%CI、3.2-34.1)。[ 12 ]
CHEK2
CHEK2は、DNA損傷修復反応経路に関与する遺伝子である。多数の研究に基づくと、多型の1100delCは、まれで浸透度が中程度のがん感受性アレルであると考えられる。[ 13 ][ 14 ][ 15 ][ 16 ][ 17 ][ 18 ]この病原性多様体を、欧州人対照の1.2%、欧州人のBRCA1/BRCA2陰性の家族性乳がん症例の4.2%、非選択の女性乳がん症例の1.4%で同定した研究が1件ある。[ 13 ]浸潤性乳がんの50歳未満のオランダ人女性1,479人の集団において、3.7%がCHEK2 1100delC病原性多様体を有することが明らかにされた。[ 19 ]別の欧州および米国(この病原性多様体はわずかに少ないとみられる)の研究では、大規模なプロスペクティブ研究[ 20 ]を含め、家族性の乳がんまたは卵巣がん症例で検出されたCHEK2病原性多様体の頻度は、0[ 21 ]~11%の範囲となっている;全体的に、これらの研究から、女性の乳がんリスクが約1.5倍~3倍高いことが明らかになっている。[ 20 ][ 22 ][ 23 ][ 24 ][ 25 ]しかしながら、10件のケースコントロール研究から得られた20,000人近くの被験者を対象にした多施設併合解析および再解析では、病原性多様体キャリアにおいて2.3倍という乳がんの有意な過剰発現が確認されている。[ 26 ]その後のメタアナリシスによると、25件のケースコントロール研究から29,154人の症例および37,064人の対照を基に、CHEK2 1100delC ヘテロ接合型と乳がんリスクとの間に有意な関連性が認められた(オッズ比[OR]、2.75;95%CI、2.25-3.36)。非選択、家族性、および早期発症型の乳がんサブグループにおけるOR(CI)は、それぞれ2.33(1.79-3.05)、3.72(2.61-5.31)、および2.78(2.28-3.39)であった。しかしながら、研究の限界としては、サブグループ解析を実施しないで集団を併合したこと、集団ベースおよび病院ベースの対照を混合して使用していること、および調整していない推定値で得られた結果を基にしていること(少ない共通因子でのみ症例と対照をマッチさせているため)が挙げられる;そのため、これらの限界を考慮に入れて結果を解釈すべきである。[ 27 ]男性の乳がん患者を対象にしたシリーズにおいて、CHEK2 1100delC多様体が対照よりも有意に高頻度に同定されたことから、この多様体は男性の乳がんリスク増加にも関連していることが示唆された。[ 28 ]
CHEK2の1100delC病原性多様体に伴うリスクは両側性乳がんで確認された発端者の家系においてより強かったことが、2件の研究から示唆されている。[ 29 ][ 30 ]さらに、1100delC病原性多様体キャリアのメタアナリシスから、乳がん家族歴を有する女性における乳がんリスクは70歳までで42%と推定された。[ 31 ]同様に、ポーランドの研究では、CHEK2切断型病原性多様体による乳がんリスクが、乳がんの家族歴に基づいて次のように報告された:家族歴なし:20%;第二度近親者が1人:28%;第一度近親者が1人:34%;および第一度および第二度近親者がいる場合:44%。[ 3 ]さらに、オランダの研究では、CHEK2 1100delC多様体のホモ接合体を有する女性はヘテロ接合体を有する女性と比較して、乳がんのリスクが2倍以上であることが示唆された。[ 32 ]CHEK2病原性多様体に関連した乳がん以外のがんについての報告は矛盾しているものの、多様体の型(すなわち、ミスセンス vs 切断型)や研究される集団によって報告結果は異なっており、現在のところ、臨床的有用性は認められない。[ 18 ][ 23 ][ 33 ][ 34 ][ 35 ][ 36 ][ 37 ][ 38 ]CHEK2多様体の乳がんに対する寄与は研究される集団に依存していると考えられ、ポーランドでは多様体保有率が潜在的に高い。[ 39 ]ポーランドにおけるCHEK2病原性多様体キャリアはエストロゲン受容体(ER)陽性乳がんをより発症しやすいようである。[ 40 ]
現在のところ、CHEK多様体の臨床適用性(clinical applicability)は、多様体の保有率が低く、臨床管理のためのガイドラインが存在しないため、不明のままである。[ 41 ]
86,975人を対象にしたオランダの大規模研究では、CHEK2 1100delC病原性多様体のキャリアについて乳がんおよび結腸がん以外のがんリスク増加が報告された[ 42 ]が、こうしたリスクの精度をさらに改良するために追加の研究が必要である。
(詳しい情報については、大腸がんの遺伝学に関するPDQ要約のCHEK2のセクションを参照のこと。)
ATM
毛細血管拡張性運動失調(AT)は、常染色体劣性疾患であり、神経学的悪化、末梢血管拡張症、免疫不全症および電離放射線過敏症が特徴的である。一般集団の1%が、ATM多様体のヘテロ接合体キャリアと推定される。[ 43 ]この遺伝子には、300以上の多様体が同定されており、そのほとんどは切断型多様体である。[ 44 ]ATM蛋白は、細胞周期制御の役割を果たすことが示されている。[ 45 ][ 46 ][ 47 ]in vitroでは、AT欠損細胞は電離放射線および放射線様作用薬に感受性を示し、放射線に曝露したのち、細胞周期制御特性の欠失が認められる。[ 48 ]単一のATM病原性多様体のキャリア(ヘテロ接合体)において放射線療法を控える推奨の証拠は不十分である。
乳がん患者にATM病原性多様体が異常集積することを調査した初期の研究では相反する結果が得られたが、おそらくこれは研究デザインおよび多様体検査の戦略が原因と考えられる。[ 49 ][ 50 ][ 51 ][ 52 ][ 53 ][ 54 ][ 55 ][ 56 ][ 57 ][ 58 ][ 59 ]しかしながら、2件の大規模な疫学研究により、女性のヘテロ接合体キャリアでは乳がんリスクが統計的に高いことが明らかになっており、推定されるRRは約2.0である。[ 4 ][ 59 ]1件のメタアナリシスでは、乳がんのリスクが50歳までで6.02%、80歳までで32.83%とモデル化された。[ 60 ]これらのリスクを考慮して、家族歴と年齢に基づいてスクリーニングやその他の推奨を増やすことを検討してもよい。
ATMと卵巣がんとの関連を示している研究[ 61 ][ 62 ]がいくつかあるが、現時点でリスク管理または疾患特性に対する影響が示唆される証拠は得られていない。
CASP8およびTGFB1
国際的な研究者グループのBreast Cancer Association Consortium(BCAC)では、症例15,000~20,000人と対照15,000~20,000人を対象として、乳がんの過剰リスクと関連している可能性がある以前の研究で同定された一塩基多型(SNP)が調査された。SNPのCASP80 D302HおよびTGFB1 L10Pの2つは、浸潤性乳がんと関連し、RRは、それぞれ0.88(95%CI、0.84-0.92)および1.08(95%CI、1.04-1.11)であった。[ 63 ]
RAD51
RAD51およびRAD51パラログとしても知られるRAD51関連遺伝子ファミリーは、相同的組換えやBRCA1およびBRCA2を含む多くの他のDNA修復蛋白との相互作用を介したDNA損傷修復に関連する蛋白をコードすると考えられる。RAD51蛋白は、DNA損傷応答における一本鎖アニーリングで中心的役割を果たす。損傷部位へのRAD51の関与と組換えDNA修復はRAD51パラログに依存するが、それらの正確な細胞機能は十分に解明されていない。[ 64 ]これらの遺伝子の多様体により、DNA損傷に反応するRAD51フォーカス形成能が失われると考えられている。[ 65 ]
5種類のRAD51関連遺伝子の1つであるRAD51Cは、ファンコニー貧血様疾患と家族性の乳がんおよび卵巣がんの両方に関連することが報告されている。しかし、その文献では相反する結果が示されている。BRCA1およびBRCA2病原性多様体陰性の乳がんおよび卵巣がんを特徴とするドイツ人の480家系を対象とした1件の研究では、RAD51Cの片アレル性の多様体が6例認められた(発生頻度は1.3%)。[ 66 ]別の研究では、乳がんおよび/または卵巣がんのBRCA1/BRCA2陰性患者286人に対してスクリーニングを実施したところ、RAD51C-G153Dに可能性の高い1種類の病原性多様体が認められた。[ 67 ]RAD51C病原性多様体はオーストラリア人、英国人、フィンランド人、スペイン人のBRCA1/BRCA2に関連しない卵巣がんのみおよび乳がん/卵巣がんの家系において、また選択されていない卵巣がん症例においても報告されており、これらの集団における頻度は0%から3%である。[ 5 ][ 12 ][ 68 ][ 69 ][ 70 ][ 71 ][ 72 ][ 73 ]一般的なユダヤ性病原性多様体について事前に検査を受けた高リスクのユダヤ人女性206人(うちアシュケナージ系79人)のサンプルで、以前に記述された、可能性のある2種類のミスセンス病原性多様体が検出された。[ 74 ]他の4件の研究では、RAD51C遺伝子と遺伝性の乳がんまたは卵巣がんとの関連は確認できなかった。[ 75 ][ 76 ][ 77 ][ 78 ]
RAD51C病原性多様体キャリアに加えて、RAD51B、RAD51D、RAD51L1、XRCC2、XRCC3などのRAD51パラログが他にあり、これらは乳がんおよび/または卵巣がんのリスクに関連する可能性があるが[ 6 ][ 12 ][ 79 ][ 80 ][ 81 ][ 82 ][ 83 ]、これらの知見の臨床的意義は不明である。3,429人の卵巣がん患者を対象とした1件のケースコントロール研究では、RAD51CおよびRAD51Dの病原性多様体が卵巣がん症例(0.82%)で対照群(0.11%、P < 0.001)よりも多く認められた。[ 84 ]
生殖細胞多様体に加え、各種のRAD51多型がDNA欠損に対する修復能を低下させ、家族性乳がんへの感受性を増大させたとの仮説が立てられている。Consortium of Investigators of Modifiers of BRCA1/BRCA2(CIMBA)は、BRCA1およびBRCA2病原性多様体キャリア8,512人から得られたデータを集積し、BRCA2キャリアの女性とRAD51 135G→C SNPがCCのホモ接合体である女性では乳がんのリスクが高くなる証拠を明らかにした(ハザード比;1.17;95%CI、0.91-1.51)。[ 85 ]
数件のメタアナリシスで、RAD51 135G→C多型と乳がんのリスクとの関連についての調査が実施された。これらのメタアナリシスで報告された研究には多くの重複する内容が含まれ、対象とされた集団の特性には大きなばらつきがあり、得られた知見に対する重要な方法的限界がある。[ 86 ][ 87 ][ 88 ][ 89 ]BRCA1/BRCA2の状態が不明な症例13,241人および対照13,203人を含む9件の疫学的研究のメタアナリシスにより、CCの遺伝子型を保有する女性は、GGまたはGCの遺伝子型を保有する女性と比較して、乳がんのリスクが高い(OR、1.35;95%CI、1.04-1.74)ことが明らかにされた。症例12,183例と対照10,183例を対象とした14件のケースコントロール研究についてのメタアナリシスでは、BRCA2キャリアであることが判明していた女性のみリスクが高いことが確認された(OR、4.92;95%CI、1.10-21.83)。[ 90 ]既知のBRCA陰性症例の研究のみを対象とした12件の研究についてのメタアナリシスでは、RAD51 135G→Cと乳がんとの間に関連はみられなかった。[ 91 ]
要約すると、これらの相反するデータの中にはRAD51Cの生殖細胞多様体と乳がんおよび卵巣がんとの間に若干の関連性があることを示す実質的な証拠が存在する。また、CC遺伝子型のホモ接合体を有する女性、特にBRCA2キャリアの女性において、RAD51 135G→C多型と乳がんとの関連性を示す証拠も存在している。これらの関連性は、RAD51の既知の役割であるゲノム安定性の維持を考慮すると妥当に思われる。
Abraxas
BRCA1と相互作用する遺伝子Abraxasの病原性多様体が、フィンランドの3つの乳がん家系に認められ、対照にはみられなかった。[ 92 ]この集団外におけるこの知見の意義は明らかになっていない。
RECQL
高リスクのポーランド人家系とケベックのフランス系カナダ人家系に対する完全なエクソーム配列決定から、両方の集団でRECQL遺伝子に複数のまれな切断型多様体が見出された。[ 93 ](全エクソーム配列決定に関する詳しい情報については、がん遺伝学の概要のPDQ要約の臨床シークエンシングのセクションを参照のこと。)この遺伝子の切断型多様体は、同じ集団でその後に実施された2つの検証段階でも、高リスク家系に属する他の乳がん患者、ならびに多様体の頻度が対照における頻度より高かった別の乳がん症例で同定された。ベラルーシおよびドイツの1件のケースコントロール研究では、最も一般的な病原性多様体、c.1667_1667+3delA GTAが調査され、この多様体がER陽性乳がんと関連していることが明らかにされた。この研究単独のORは1.23(95%CI、0.44-3.47;P = 0.69)であったが、ポーランドの研究とのメタアナリシスでのORは2.51(95%CI、1.13-5.57、P = 0.02)であった。[ 94 ]研究結果からは切断型の生殖細胞RECQL病原性多様体が乳がんリスクの増大に関連していることが示唆されるが、依然として正確なリスクの大きさは不明であり、今後の研究で臨床的有用性を見極める必要がある。これら2つの集団外におけるこの知見の意義は明らかになっていない。
SMARCA4
SMARCA4はBRG1をコードし、クロマチンが遺伝子発現の調節に利用できるようにする上で大きな役割を果たすSWI/SNFクロマチン再構築複合体の触媒サブユニットである。
卵巣小細胞がん、高カルシウム血症型(SCCOHT)は、まれな侵攻性の腫瘍であり、発症年齢が低く(40歳以前)、予後不良である。[ 95 ][ 96 ][ 97 ] ときに家族内集積が認められる。SCCOHT腫瘍は片側性または両側性の場合があり、組織学的には活発な有糸分裂活性を示す小さな過染色性細胞の存在を特徴とする。[ 96 ]SCCOHTの治療については手術、化学療法、および放射線療法を含む集学的アプローチが提案されている。[ 96 ][ 97 ]60%の症例で高カルシウム血症の腫瘍随伴現象がみられることを考慮し、疾患の経過のモニタリングにおいてはカルシウム濃度の追跡が有用である。胚細胞腫瘍、性索間質性腫瘍、未分化がんなどの広範な鑑別診断により、SCCOHTは世界保健機関により「その他の腫瘍」として分類されているが、最近、配列決定により悪性ラブドイド腫瘍であるとされている。[ 98 ]エクソーム配列決定により、SCCOHT症例の大半は機能的SMARCA4/BRG1を欠くことが認められている;実際、SMARCA4の病原性多様体がSCCOHTの原因となる唯一の多様体である可能性がある。
文献には約300症例しかないが、3つの別個の研究グループは、SCCOHTがSMARCA4遺伝子の生殖細胞病原性多様体および体細胞変異と関連することを示した。SCCOHTの若年女性12人を対象とした研究では、腫瘍と正常サンプルの対の配列決定から、各症例において両アレル性SMARCA4病原性多様体の不活性化が明らかとなった。[ 99 ]配列決定された他の278遺伝子のすべてで非反復性体細胞遺伝子は他にわずか4つしか同定されなかった。免疫組織化学検査で、検査された9症例中7例でSMARCA4蛋白発現の消失が示されたが、これは腫瘍抑制遺伝子の機能と一致していた。別の患者12人についての2番目の研究で、次世代の塩基配列決定法でも、唯一の反復性多様体を生じた遺伝子としてSMARCA4が同定され、多様体の大多数は短縮蛋白を生じるものと予測された。[ 100 ]3番目の研究では3家系を対象として、全エクソーム配列決定法とともにSanger塩基配列決定法で確認することにより、26例中24例で少なくとも1つの生殖細胞病原性多様体または体細胞変異が同定された。[ 101 ]全体として、SCCOHT腫瘍では43例中38例(88%)がSMARCA4発現の消失を示したのに対し、他の種類の卵巣腫瘍では139例中1例のみ(0.7%)であった。
この腫瘍が希少であることから、SMARCA4の浸透度は不明である。現在、管理についてコンセンサスは存在しないが、SMARCA4は遺伝子検査用に現在利用できるより大規模な多重遺伝子パネルに組み込まれており、病原性多様体のキャリアに対してはリスク低減のための手術が提供されている。[ 102 ]
参考文献- Easton DF: How many more breast cancer predisposition genes are there? Breast Cancer Res 1 (1): 14-7, 1999.[PUBMED Abstract]
- Smith P, McGuffog L, Easton DF, et al.: A genome wide linkage search for breast cancer susceptibility genes. Genes Chromosomes Cancer 45 (7): 646-55, 2006.[PUBMED Abstract]
- Cybulski C, Wokołorczyk D, Jakubowska A, et al.: Risk of breast cancer in women with a CHEK2 mutation with and without a family history of breast cancer. J Clin Oncol 29 (28): 3747-52, 2011.[PUBMED Abstract]
- Thompson D, Duedal S, Kirner J, et al.: Cancer risks and mortality in heterozygous ATM mutation carriers. J Natl Cancer Inst 97 (11): 813-22, 2005.[PUBMED Abstract]
- Pelttari LM, Heikkinen T, Thompson D, et al.: RAD51C is a susceptibility gene for ovarian cancer. Hum Mol Genet 20 (16): 3278-88, 2011.[PUBMED Abstract]
- Loveday C, Turnbull C, Ramsay E, et al.: Germline mutations in RAD51D confer susceptibility to ovarian cancer. Nat Genet 43 (9): 879-82, 2011.[PUBMED Abstract]
- Mehta PA, Tolar J: Fanconi Anemia. In: Adam MP, Ardinger HH, Pagon RA, et al.: GeneReviews. Seattle, Wash: University of Washington, 1993-2018, pp. Available online. Last accessed January 22, 2020.[PUBMED Abstract]
- Levitus M, Waisfisz Q, Godthelp BC, et al.: The DNA helicase BRIP1 is defective in Fanconi anemia complementation group J. Nat Genet 37 (9): 934-5, 2005.[PUBMED Abstract]
- Levran O, Attwooll C, Henry RT, et al.: The BRCA1-interacting helicase BRIP1 is deficient in Fanconi anemia. Nat Genet 37 (9): 931-3, 2005.[PUBMED Abstract]
- Litman R, Peng M, Jin Z, et al.: BACH1 is critical for homologous recombination and appears to be the Fanconi anemia gene product FANCJ. Cancer Cell 8 (3): 255-65, 2005.[PUBMED Abstract]
- Seal S, Thompson D, Renwick A, et al.: Truncating mutations in the Fanconi anemia J gene BRIP1 are low-penetrance breast cancer susceptibility alleles. Nat Genet 38 (11): 1239-41, 2006.[PUBMED Abstract]
- Ramus SJ, Song H, Dicks E, et al.: Germline Mutations in the BRIP1, BARD1, PALB2, and NBN Genes in Women With Ovarian Cancer. J Natl Cancer Inst 107 (11): , 2015.[PUBMED Abstract]
- Meijers-Heijboer H, van den Ouweland A, Klijn J, et al.: Low-penetrance susceptibility to breast cancer due to CHEK2(*)1100delC in noncarriers of BRCA1 or BRCA2 mutations. Nat Genet 31 (1): 55-9, 2002.[PUBMED Abstract]
- Kuschel B, Auranen A, Gregory CS, et al.: Common polymorphisms in checkpoint kinase 2 are not associated with breast cancer risk. Cancer Epidemiol Biomarkers Prev 12 (8): 809-12, 2003.[PUBMED Abstract]
- Sodha N, Bullock S, Taylor R, et al.: CHEK2 variants in susceptibility to breast cancer and evidence of retention of the wild type allele in tumours. Br J Cancer 87 (12): 1445-8, 2002.[PUBMED Abstract]
- Ingvarsson S, Sigbjornsdottir BI, Huiping C, et al.: Mutation analysis of the CHK2 gene in breast carcinoma and other cancers. Breast Cancer Res 4 (3): R4, 2002.[PUBMED Abstract]
- Vahteristo P, Bartkova J, Eerola H, et al.: A CHEK2 genetic variant contributing to a substantial fraction of familial breast cancer. Am J Hum Genet 71 (2): 432-8, 2002.[PUBMED Abstract]
- Meijers-Heijboer H, Wijnen J, Vasen H, et al.: The CHEK2 1100delC mutation identifies families with a hereditary breast and colorectal cancer phenotype. Am J Hum Genet 72 (5): 1308-14, 2003.[PUBMED Abstract]
- Schmidt MK, Tollenaar RA, de Kemp SR, et al.: Breast cancer survival and tumor characteristics in premenopausal women carrying the CHEK2*1100delC germline mutation. J Clin Oncol 25 (1): 64-9, 2007.[PUBMED Abstract]
- Weischer M, Bojesen SE, Tybjaerg-Hansen A, et al.: Increased risk of breast cancer associated with CHEK2*1100delC. J Clin Oncol 25 (1): 57-63, 2007.[PUBMED Abstract]
- Iniesta MD, Gorin MA, Chien LC, et al.: Absence of CHEK2*1100delC mutation in families with hereditary breast cancer in North America. Cancer Genet Cytogenet 202 (2): 136-40, 2010.[PUBMED Abstract]
- Offit K, Pierce H, Kirchhoff T, et al.: Frequency of CHEK2*1100delC in New York breast cancer cases and controls. BMC Med Genet 4 (1): 1, 2003.[PUBMED Abstract]
- Oldenburg RA, Kroeze-Jansema K, Kraan J, et al.: The CHEK2*1100delC variant acts as a breast cancer risk modifier in non-BRCA1/BRCA2 multiple-case families. Cancer Res 63 (23): 8153-7, 2003.[PUBMED Abstract]
- Neuhausen S, Dunning A, Steele L, et al.: Role of CHEK2*1100delC in unselected series of non-BRCA1/2 male breast cancers. Int J Cancer 108 (3): 477-8, 2004.[PUBMED Abstract]
- Ohayon T, Gal I, Baruch RG, et al.: CHEK2*1100delC and male breast cancer risk in Israel. Int J Cancer 108 (3): 479-80, 2004.[PUBMED Abstract]
- CHEK2 Breast Cancer Case-Control Consortium: CHEK2*1100delC and susceptibility to breast cancer: a collaborative analysis involving 10,860 breast cancer cases and 9,065 controls from 10 studies. Am J Hum Genet 74 (6): 1175-82, 2004.[PUBMED Abstract]
- Yang Y, Zhang F, Wang Y, et al.: CHEK2 1100delC variant and breast cancer risk in Caucasians: a meta-analysis based on 25 studies with 29,154 cases and 37,064 controls. Asian Pac J Cancer Prev 13 (7): 3501-5, 2012.[PUBMED Abstract]
- Hallamies S, Pelttari LM, Poikonen-Saksela P, et al.: CHEK2 c.1100delC mutation is associated with an increased risk for male breast cancer in Finnish patient population. BMC Cancer 17 (1): 620, 2017.[PUBMED Abstract]
- Johnson N, Fletcher O, Naceur-Lombardelli C, et al.: Interaction between CHEK2*1100delC and other low-penetrance breast-cancer susceptibility genes: a familial study. Lancet 366 (9496): 1554-7, 2005 Oct 29-Nov 4.[PUBMED Abstract]
- Fletcher O, Johnson N, Dos Santos Silva I, et al.: Family history, genetic testing, and clinical risk prediction: pooled analysis of CHEK2 1100delC in 1,828 bilateral breast cancers and 7,030 controls. Cancer Epidemiol Biomarkers Prev 18 (1): 230-4, 2009.[PUBMED Abstract]
- Weischer M, Bojesen SE, Ellervik C, et al.: CHEK2*1100delC genotyping for clinical assessment of breast cancer risk: meta-analyses of 26,000 patient cases and 27,000 controls. J Clin Oncol 26 (4): 542-8, 2008.[PUBMED Abstract]
- Adank MA, Jonker MA, Kluijt I, et al.: CHEK2*1100delC homozygosity is associated with a high breast cancer risk in women. J Med Genet 48 (12): 860-3, 2011.[PUBMED Abstract]
- Gronwald J, Cybulski C, Piesiak W, et al.: Cancer risks in first-degree relatives of CHEK2 mutation carriers: effects of mutation type and cancer site in proband. Br J Cancer 100 (9): 1508-12, 2009.[PUBMED Abstract]
- Wasielewski M, den Bakker MA, van den Ouweland A, et al.: CHEK2 1100delC and male breast cancer in the Netherlands. Breast Cancer Res Treat 116 (2): 397-400, 2009.[PUBMED Abstract]
- Osorio A, Rodríguez-López R, Díez O, et al.: The breast cancer low-penetrance allele 1100delC in the CHEK2 gene is not present in Spanish familial breast cancer population. Int J Cancer 108 (1): 54-6, 2004.[PUBMED Abstract]
- Syrjäkoski K, Kuukasjärvi T, Auvinen A, et al.: CHEK2 1100delC is not a risk factor for male breast cancer population. Int J Cancer 108 (3): 475-6, 2004.[PUBMED Abstract]
- Tsou HC, Teng DH, Ping XL, et al.: The role of MMAC1 mutations in early-onset breast cancer: causative in association with Cowden syndrome and excluded in BRCA1-negative cases. Am J Hum Genet 61 (5): 1036-43, 1997.[PUBMED Abstract]
- Olopade OI, Weber BL: Breast cancer genetics: toward molecular characterization of individuals at increased risk for breast cancer: part I. Cancer: Principles and Practice of Oncology Updates 12 (10): 1-12, 1998.[PUBMED Abstract]
- Cybulski C, Górski B, Huzarski T, et al.: CHEK2-positive breast cancers in young Polish women. Clin Cancer Res 12 (16): 4832-5, 2006.[PUBMED Abstract]
- Cybulski C, Huzarski T, Byrski T, et al.: Estrogen receptor status in CHEK2-positive breast cancers: implications for chemoprevention. Clin Genet 75 (1): 72-8, 2009.[PUBMED Abstract]
- Offit K, Garber JE: Time to check CHEK2 in families with breast cancer? J Clin Oncol 26 (4): 519-20, 2008.[PUBMED Abstract]
- Näslund-Koch C, Nordestgaard BG, Bojesen SE: Increased Risk for Other Cancers in Addition to Breast Cancer for CHEK2*1100delC Heterozygotes Estimated From the Copenhagen General Population Study. J Clin Oncol 34 (11): 1208-16, 2016.[PUBMED Abstract]
- Savitsky K, Bar-Shira A, Gilad S, et al.: A single ataxia telangiectasia gene with a product similar to PI-3 kinase. Science 268 (5218): 1749-53, 1995.[PUBMED Abstract]
- Telatar M, Teraoka S, Wang Z, et al.: Ataxia-telangiectasia: identification and detection of founder-effect mutations in the ATM gene in ethnic populations. Am J Hum Genet 62 (1): 86-97, 1998.[PUBMED Abstract]
- Uhrhammer N, Bay JO, Bignon YJ: Seventh International Workshop on Ataxia-Telangiectasia. Cancer Res 58 (15): 3480-5, 1998.[PUBMED Abstract]
- Ahmed M, Rahman N: ATM and breast cancer susceptibility. Oncogene 25 (43): 5906-11, 2006.[PUBMED Abstract]
- Khanna KK, Chenevix-Trench G: ATM and genome maintenance: defining its role in breast cancer susceptibility. J Mammary Gland Biol Neoplasia 9 (3): 247-62, 2004.[PUBMED Abstract]
- Gilad S, Chessa L, Khosravi R, et al.: Genotype-phenotype relationships in ataxia-telangiectasia and variants. Am J Hum Genet 62 (3): 551-61, 1998.[PUBMED Abstract]
- FitzGerald MG, Bean JM, Hegde SR, et al.: Heterozygous ATM mutations do not contribute to early onset of breast cancer. Nat Genet 15 (3): 307-10, 1997.[PUBMED Abstract]
- Chen J, Birkholtz GG, Lindblom P, et al.: The role of ataxia-telangiectasia heterozygotes in familial breast cancer. Cancer Res 58 (7): 1376-9, 1998.[PUBMED Abstract]
- Bay JO, Grancho M, Pernin D, et al.: No evidence for constitutional ATM mutation in breast/gastric cancer families. Int J Oncol 12 (6): 1385-90, 1998.[PUBMED Abstract]
- Laake K, Vu P, Andersen TI, et al.: Screening breast cancer patients for Norwegian ATM mutations. Br J Cancer 83 (12): 1650-3, 2000.[PUBMED Abstract]
- Dörk T, Bendix R, Bremer M, et al.: Spectrum of ATM gene mutations in a hospital-based series of unselected breast cancer patients. Cancer Res 61 (20): 7608-15, 2001.[PUBMED Abstract]
- Teraoka SN, Malone KE, Doody DR, et al.: Increased frequency of ATM mutations in breast carcinoma patients with early onset disease and positive family history. Cancer 92 (3): 479-87, 2001.[PUBMED Abstract]
- Chenevix-Trench G, Spurdle AB, Gatei M, et al.: Dominant negative ATM mutations in breast cancer families. J Natl Cancer Inst 94 (3): 205-15, 2002.[PUBMED Abstract]
- Thorstenson YR, Roxas A, Kroiss R, et al.: Contributions of ATM mutations to familial breast and ovarian cancer. Cancer Res 63 (12): 3325-33, 2003.[PUBMED Abstract]
- Cavaciuti E, Laugé A, Janin N, et al.: Cancer risk according to type and location of ATM mutation in ataxia-telangiectasia families. Genes Chromosomes Cancer 42 (1): 1-9, 2005.[PUBMED Abstract]
- Olsen JH, Hahnemann JM, Børresen-Dale AL, et al.: Breast and other cancers in 1445 blood relatives of 75 Nordic patients with ataxia telangiectasia. Br J Cancer 93 (2): 260-5, 2005.[PUBMED Abstract]
- Renwick A, Thompson D, Seal S, et al.: ATM mutations that cause ataxia-telangiectasia are breast cancer susceptibility alleles. Nat Genet 38 (8): 873-5, 2006.[PUBMED Abstract]
- Marabelli M, Cheng SC, Parmigiani G: Penetrance of ATM Gene Mutations in Breast Cancer: A Meta-Analysis of Different Measures of Risk. Genet Epidemiol 40 (5): 425-31, 2016.[PUBMED Abstract]
- Lu HM, Li S, Black MH, et al.: Association of Breast and Ovarian Cancers With Predisposition Genes Identified by Large-Scale Sequencing. JAMA Oncol 5 (1): 51-57, 2019.[PUBMED Abstract]
- Pennington KP, Walsh T, Harrell MI, et al.: Germline and somatic mutations in homologous recombination genes predict platinum response and survival in ovarian, fallopian tube, and peritoneal carcinomas. Clin Cancer Res 20 (3): 764-75, 2014.[PUBMED Abstract]
- Cox Angela, Dunning Alison, Garcia-Closas Montserrat, et al.: Nature genetics. Nat Genet 39 (5): 352-8, 2007.[PUBMED Abstract]
- Suwaki N, Klare K, Tarsounas M: RAD51 paralogs: roles in DNA damage signalling, recombinational repair and tumorigenesis. Semin Cell Dev Biol 22 (8): 898-905, 2011.[PUBMED Abstract]
- Vaz F, Hanenberg H, Schuster B, et al.: Mutation of the RAD51C gene in a Fanconi anemia-like disorder. Nat Genet 42 (5): 406-9, 2010.[PUBMED Abstract]
- Meindl A, Hellebrand H, Wiek C, et al.: Germline mutations in breast and ovarian cancer pedigrees establish RAD51C as a human cancer susceptibility gene. Nat Genet 42 (5): 410-4, 2010.[PUBMED Abstract]
- Clague J, Wilhoite G, Adamson A, et al.: RAD51C germline mutations in breast and ovarian cancer cases from high-risk families. PLoS One 6 (9): e25632, 2011.[PUBMED Abstract]
- Thompson ER, Boyle SE, Johnson J, et al.: Analysis of RAD51C germline mutations in high-risk breast and ovarian cancer families and ovarian cancer patients. Hum Mutat 33 (1): 95-9, 2012.[PUBMED Abstract]
- Vuorela M, Pylkäs K, Hartikainen JM, et al.: Further evidence for the contribution of the RAD51C gene in hereditary breast and ovarian cancer susceptibility. Breast Cancer Res Treat 130 (3): 1003-10, 2011.[PUBMED Abstract]
- Romero A, Pérez-Segura P, Tosar A, et al.: A HRM-based screening method detects RAD51C germ-line deleterious mutations in Spanish breast and ovarian cancer families. Breast Cancer Res Treat 129 (3): 939-46, 2011.[PUBMED Abstract]
- Osorio A, Endt D, Fernández F, et al.: Predominance of pathogenic missense variants in the RAD51C gene occurring in breast and ovarian cancer families. Hum Mol Genet 21 (13): 2889-98, 2012.[PUBMED Abstract]
- Blanco A, Gutiérrez-Enríquez S, Santamariña M, et al.: RAD51C germline mutations found in Spanish site-specific breast cancer and breast-ovarian cancer families. Breast Cancer Res Treat 147 (1): 133-43, 2014.[PUBMED Abstract]
- Norquist BM, Harrell MI, Brady MF, et al.: Inherited Mutations in Women With Ovarian Carcinoma. JAMA Oncol 2 (4): 482-90, 2016.[PUBMED Abstract]
- Kushnir A, Laitman Y, Shimon SP, et al.: Germline mutations in RAD51C in Jewish high cancer risk families. Breast Cancer Res Treat 136 (3): 869-74, 2012.[PUBMED Abstract]
- Wong MW, Nordfors C, Mossman D, et al.: BRIP1, PALB2, and RAD51C mutation analysis reveals their relative importance as genetic susceptibility factors for breast cancer. Breast Cancer Res Treat 127 (3): 853-9, 2011.[PUBMED Abstract]
- Zheng Y, Zhang J, Hope K, et al.: Screening RAD51C nucleotide alterations in patients with a family history of breast and ovarian cancer. Breast Cancer Res Treat 124 (3): 857-61, 2010.[PUBMED Abstract]
- Akbari MR, Tonin P, Foulkes WD, et al.: RAD51C germline mutations in breast and ovarian cancer patients. Breast Cancer Res 12 (4): 404, 2010.[PUBMED Abstract]
- De Leeneer K, Van Bockstal M, De Brouwer S, et al.: Evaluation of RAD51C as cancer susceptibility gene in a large breast-ovarian cancer patient population referred for genetic testing. Breast Cancer Res Treat 133 (1): 393-8, 2012.[PUBMED Abstract]
- Thomas G, Jacobs KB, Kraft P, et al.: A multistage genome-wide association study in breast cancer identifies two new risk alleles at 1p11.2 and 14q24.1 (RAD51L1). Nat Genet 41 (5): 579-84, 2009.[PUBMED Abstract]
- Figueroa JD, Garcia-Closas M, Humphreys M, et al.: Associations of common variants at 1p11.2 and 14q24.1 (RAD51L1) with breast cancer risk and heterogeneity by tumor subtype: findings from the Breast Cancer Association Consortium. Hum Mol Genet 20 (23): 4693-706, 2011.[PUBMED Abstract]
- Osher DJ, De Leeneer K, Michils G, et al.: Mutation analysis of RAD51D in non-BRCA1/2 ovarian and breast cancer families. Br J Cancer 106 (8): 1460-3, 2012.[PUBMED Abstract]
- Pelttari LM, Kiiski J, Nurminen R, et al.: A Finnish founder mutation in RAD51D: analysis in breast, ovarian, prostate, and colorectal cancer. J Med Genet 49 (7): 429-32, 2012.[PUBMED Abstract]
- Golmard L, Castéra L, Krieger S, et al.: Contribution of germline deleterious variants in the RAD51 paralogs to breast and ovarian cancers. Eur J Hum Genet 25 (12): 1345-1353, 2017.[PUBMED Abstract]
- Song H, Dicks E, Ramus SJ, et al.: Contribution of Germline Mutations in the RAD51B, RAD51C, and RAD51D Genes to Ovarian Cancer in the Population. J Clin Oncol 33 (26): 2901-7, 2015.[PUBMED Abstract]
- Antoniou AC, Sinilnikova OM, Simard J, et al.: RAD51 135G-->C modifies breast cancer risk among BRCA2 mutation carriers: results from a combined analysis of 19 studies. Am J Hum Genet 81 (6): 1186-200, 2007.[PUBMED Abstract]
- He XF, Su J, Zhang Y, et al.: Need for clarification of data in the recent meta-analysis about RAD51 135G>C polymorphism and breast cancer risk. Breast Cancer Res Treat 129 (2): 649-51; author reply 652-3, 2011.[PUBMED Abstract]
- Lu W, Wang X, Lin H, et al.: Mutation screening of RAD51C in high-risk breast and ovarian cancer families. Fam Cancer 11 (3): 381-5, 2012.[PUBMED Abstract]
- Wang WW, Spurdle AB, Kolachana P, et al.: A single nucleotide polymorphism in the 5' untranslated region of RAD51 and risk of cancer among BRCA1/2 mutation carriers. Cancer Epidemiol Biomarkers Prev 10 (9): 955-60, 2001.[PUBMED Abstract]
- Wang Z, Dong H, Fu Y, et al.: RAD51 135G>C polymorphism contributes to breast cancer susceptibility: a meta-analysis involving 26,444 subjects. Breast Cancer Res Treat 124 (3): 765-9, 2010.[PUBMED Abstract]
- Zhou GW, Hu J, Peng XD, et al.: RAD51 135G>C polymorphism and breast cancer risk: a meta-analysis. Breast Cancer Res Treat 125 (2): 529-35, 2011.[PUBMED Abstract]
- Yu KD, Yang C, Fan L, et al.: RAD51 135G>C does not modify breast cancer risk in non-BRCA1/2 mutation carriers: evidence from a meta-analysis of 12 studies. Breast Cancer Res Treat 126 (2): 365-71, 2011.[PUBMED Abstract]
- Solyom S, Aressy B, Pylkäs K, et al.: Breast cancer-associated Abraxas mutation disrupts nuclear localization and DNA damage response functions. Sci Transl Med 4 (122): 122ra23, 2012.[PUBMED Abstract]
- Cybulski C, Carrot-Zhang J, Kluźniak W, et al.: Germline RECQL mutations are associated with breast cancer susceptibility. Nat Genet 47 (6): 643-6, 2015.[PUBMED Abstract]
- Bogdanova N, Pfeifer K, Schürmann P, et al.: Analysis of a RECQL splicing mutation, c.1667_1667+3delAGTA, in breast cancer patients and controls from Central Europe. Fam Cancer 16 (2): 181-186, 2017.[PUBMED Abstract]
- Dickersin GR, Kline IW, Scully RE: Small cell carcinoma of the ovary with hypercalcemia: a report of eleven cases. Cancer 49 (1): 188-97, 1982.[PUBMED Abstract]
- Harrison ML, Hoskins P, du Bois A, et al.: Small cell of the ovary, hypercalcemic type -- analysis of combined experience and recommendation for management. A GCIG study. Gynecol Oncol 100 (2): 233-8, 2006.[PUBMED Abstract]
- Callegaro-Filho D, Gershenson DM, Nick AM, et al.: Small cell carcinoma of the ovary-hypercalcemic type (SCCOHT): A review of 47 cases. Gynecol Oncol 140 (1): 53-7, 2016.[PUBMED Abstract]
- Foulkes WD, Clarke BA, Hasselblatt M, et al.: No small surprise - small cell carcinoma of the ovary, hypercalcaemic type, is a malignant rhabdoid tumour. J Pathol 233 (3): 209-14, 2014.[PUBMED Abstract]
- Jelinic P, Mueller JJ, Olvera N, et al.: Recurrent SMARCA4 mutations in small cell carcinoma of the ovary. Nat Genet 46 (5): 424-6, 2014.[PUBMED Abstract]
- Ramos P, Karnezis AN, Craig DW, et al.: Small cell carcinoma of the ovary, hypercalcemic type, displays frequent inactivating germline and somatic mutations in SMARCA4. Nat Genet 46 (5): 427-9, 2014.[PUBMED Abstract]
- Witkowski L, Carrot-Zhang J, Albrecht S, et al.: Germline and somatic SMARCA4 mutations characterize small cell carcinoma of the ovary, hypercalcemic type. Nat Genet 46 (5): 438-43, 2014.[PUBMED Abstract]
- Berchuck A, Witkowski L, Hasselblatt M, et al.: Prophylactic oophorectomy for hereditary small cell carcinoma of the ovary, hypercalcemic type. Gynecol Oncol Rep 12: 20-2, 2015.[PUBMED Abstract]
- 低浸透度の遺伝子および遺伝子座
-
乳がんおよび婦人科がんに対する多遺伝子性の感受性の根底にある多型は低浸透度と考えられているが、低浸透度という用語は、最小から中等度のリスクに関連する塩基配列多様体に対してしばしば用いられる。これは、典型的にはより重度の表現型と関連する高浸透度の多様体またはアレル(例えば、BRCA1/BRCA2病原性多様体は家系内で常染色体優性遺伝様式を示す)、ならびにBRIP1、CHEK2、RAD51Cなどの中浸透度の多様体とは対照的である。(詳しい情報については、本要約の高浸透度の乳がんおよび/または婦人科がん感受性遺伝子および乳がんおよび/または婦人科がんに関連する中浸透度の遺伝子のセクションを参照のこと。)このような塩基配列変異(低浸透度の遺伝子、アレル、多様体、多型とも呼ばれる)は一般集団中に比較的高頻度でみられ、それらのがんリスクへの全体的寄与は、BRCA1およびBRCA2病原性多様体の集団における寄与リスクよりもはるかに大きいと推定される。例えば、分離解析による推定では、全乳がんの半数が最も感受性が高いとされる集団の12%に発生する。[ 1 ]BRCA1/BRCA2には既知の低浸透度の多様体は存在しない。当初は低浸透度のアレルと考えられていたBRCA2のN372H多様体は、ある大規模な併合解析では確認されなかった。[ 2 ]
乳がんの感受性につながる低浸透度の多型を同定するために以下の2つの戦略が試みられている:候補遺伝子および全ゲノム検索。どちらも疫学的なケースコントロール研究デザインを要する。候補遺伝子アプローチでは、既知のまたは推定される生物学的機能、発がんまたは器官生理学との関連性に基づいて遺伝子を選択し、その後がんリスクとの関連について既知の遺伝子多様体の探索または検査を行う。この戦略は不完全および不完備の生物学的知見に依存しており、いくつかの関連(以下に示す)が確認されているにもかかわらず、相対的に期待に反するものとなっている。[ 2 ][ 3 ]候補遺伝子アプローチは、ゲノムワイド関連解析(GWAS)にほとんど取って代わられており、GWASでは非常に多くの一塩基多型(SNP)(約100万~500万)がゲノム内で選択され、ほとんどが可能性のある生物学的機能に関係なく、代わりにゲノム全体ですべての遺伝的変異をより一律に捕捉するために検査される。
全ゲノム検索
候補遺伝子および/またはアレルの評価とは対照的に、GWASではゲノム全体にわたって存在する遺伝子多様体の非常に大きなセットを比較する。現在のパラダイムでは、HapMap計画および1000 Genomes Projectに基づいてゲノム内に一般的にみられる変異の大部分を捕捉するように選択した500万もの多くのSNPセットが用いられる。[ 4 ][ 5 ]多数の症例と対照(典型的にはそれぞれ1,000例以上)間のアレルの頻度を比較し、被験者の複製セットにおける有望な信号を確認することにより、関連についての非常に頑強な統計的信号が得られている。[ 6 ][ 7 ][ 8 ]染色体上で互いに物理的に密接なSNP間の多くに強い相関(連鎖不平衡)がみられるが、これにより、生物学的に関連のある多様体が検査されたSNPのセットに存在しない場合でも、感受性アレルがないかゲノムを「スキャン」することが可能である。このSNP間の相関により、すべてのSNPを分析する必要もなく大部分のゲノムを調べることができるが、相関が確認された際に、相関している多くの多様体のうち、どの多様体が原因であるかは一般に不明である。
全ゲノム検索は、乳がんを含む多くの複合疾患[ 9 ]に対する一般的な低浸透度の感受性アレルを同定する上で非常に有望であることを示している。[ 10 ][ 11 ][ 12 ][ 13 ]最初の研究では家族性乳がん症例で初期スキャンを行い、その後散発性乳がんの2つの大規模なサンプルセットで反復され、最後の研究では、Breast Cancer Association Consortiumからのそれぞれ2万人を超える症例と対照の集合について行われた。[ 10 ]FGFR2、TNRC9、MAP3K1、およびLSP1遺伝子内または付近、または染色体8q領域で5つの異なるゲノム領域が同定された。8q領域およびその他の領域には、リスクに関連する独立した遺伝子座が複数隠れている可能性がある。その後の全ゲノム検索では、これらの遺伝子座が再確認され、新たな遺伝子座が同定されている。[ 11 ][ 12 ][ 14 ][ 14 ][ 15 ][ 16 ][ 17 ][ 18 ][ 19 ]散発性乳がんの大規模な研究で同定された多数のSNPは、エストロゲン受容体(ER)陽性乳がんと比較的強く関連していると思われる[ 20 ];しかしながら、一部のSNPは主として、またはもっぱらトリプルネガティブ乳がんなど、他のサブタイプと関連している。[ 21 ][ 22 ]形質/疾患関連SNPのゲノムの特徴を研究する際に使用するため、発表されているGWASからのSNP-形質関連のオンライン目録が利用できる。
これらの遺伝子座における遺伝的変異と乳がんおよび卵巣がんリスクとの関連性に関する統計的証拠は圧倒的に多いが、生物学的に関連している多様体とそれらによりリスク増加に至る機序は不明であり、遺伝学的および機能的な特徴について、さらに調査が必要である。その上、これらの遺伝子座に伴うリスクは非常に小さく(典型的には、オッズ比[OR] < 1.5)、これよりリスクの高い変異体が同定される可能性が高い。SNPと疫学的な乳がんの危険因子との相互関係は特定されていない。[ 23 ][ 24 ]さらに複数の理論的モデルで、一般的な中等度リスクのSNPが個別化したリスク評価用のモデルを改善する可能性は限られることが示唆されている。[ 25 ][ 26 ][ 27 ]これらのモデルでは、識別の正確度の1つの指標として受信者動作特性(ROC)曲線分析を用いて曲線下面積(AUC)が算出された。その後の研究では、5,500例を超える乳がん症例と6,000例近くの対照の臨床データセットを対象に、ROC曲線分析を用いてSNPの有用性を調査するために、従来の危険因子を用いたモデルと、標準の危険因子および以前に同定された10個のSNPの両方を用いたモデルが比較された。遺伝情報の追加により、AUCは58%から61.8%にわずかに変化したが、結果は臨床的に有意であるとは考えられなかった。これにもかかわらず、遺伝情報を含めた場合の乳がんリスクでは、32.5%の患者がリスクの高い方の五分位に含まれ、20.4%の患者がリスクの低い方の五分位に含まれた。このような情報に臨床的有用性があるかどうかは不明である。[ 25 ][ 28 ]
卵巣がんリスクに関して利用できるデータはさらに限られている。卵巣がんでは、10,000人を超える症例と13,000人の対照を対象とした段階的な解析を伴う3件のGWASが実施されている。[ 29 ][ 30 ][ 31 ]他のGWASと同様に、各ORはわずかに大きいだけで、一般に約1.2以下であるが、その蛋白が複合してBRCA1を制御している可能性があるBABAM1、およびBRCA1/BRCA2欠損細胞では重要な可能性がある分子であるポリ(ADPリボース)ポリメラーゼをコードしているTIRAPRのように、卵巣がんと生物学的に関連している可能性が高い多くの遺伝子に、このORは関係している。
乳がんおよび卵巣がんに対する多遺伝子リスクスコア
最近になって、多数の遺伝子多様体の集合的な影響が総スコアを用いて評価されている。2015年に、Breast Cancer Association Consortium(BCAC)における33,000人超の乳がん症例および33,000人超の対照を含む41件の研究を用いて、既知の乳がんリスク遺伝子多様体またはSNPをすべて包含する多遺伝子リスクスコア(PRS)がヨーロッパ系の女性で推定された。[ 32 ]乳がんに対するPRSを推定するこの初期の試みでは77個のSNPが含められ、PRSが最も低い1%の女性および最も高い1%の女性が80歳までに乳がんを発症する生涯リスクは、それぞれ3.5%および29%と集合的に付与された。[ 32 ]それ以後、PRSは、追加の遺伝子多様体を組み込み、腫瘍の特徴や病理学的特徴、発見方法、対側乳がん(CBC)など、乳がんに関係した他のアウトカムを調査して推定されている。[ 33 ][ 34 ][ 35 ][ 36 ][ 37 ][ 38 ][ 39 ][ 40 ]2019年に、現在までで最も識別能の高いPRSが開発され、利用可能な最大規模(BCACの79件の研究およびU.K. Biobankの19万人以上の女性)のGWASデータセットにおいてプロスペクティブに妥当性が確認されており、このPRSは313個の遺伝子多様体に関する情報を組み込み、ER陽性およびER陰性乳がんに対して最適化されている。[ 39 ]中間五分位の女性と比較して、PRS313が最も高い1%の女性は、全体での乳がん発症リスク、ER陽性乳がん発症リスク、およびER陰性乳がん発症リスクがそれぞれ、4.04倍、4.37倍、および2.78倍であった。[ 39 ]PRS313が最も低い1%の女性および最も高い1%の女性が80歳までに乳がんを発症する生涯絶対リスクの範囲は、ER陽性乳がんで2~31%であったのに対し、ER陰性乳がんに対する絶対リスクの範囲は0.55~4%であった。[ 39 ]
最初の原発性乳がん発生に関連する一般的なゲノム多様体はまた、対側乳がん(CBC)の発生にも関連している。[ 40 ]PRSが最も高い四分位の女性では、最も低い四分位の女性と比較してCBC発生リスクが1.6倍高かった。[ 40 ]さらに、BRCA1およびBRCA2病原性多様体キャリアの女性における乳がんおよび卵巣がんのPRSを評価したところ、これらの女性でがんリスクが予測されることが明らかにされたことから、一般集団と多様体キャリア間でがんリスクの多遺伝子性の要素が共有されているという仮説が支持されている。[ 36 ]ER陰性乳がんに対するPRSはBRCA1多様体キャリアにおける乳がんリスクと最も強く関連していた一方、BRCA2多様体キャリアでは全般的な乳がんのPRSについて最も強い関連が示された。BRCA1多様体キャリアでは、PRSの10パーセンタイルと90パーセンタイルで乳がんを発症する累積生涯リスクがそれぞれ、56%および75%であった。卵巣がんのPRSは、BRCA1とBRCA2の両方の多様体キャリアに対するリスクに強く関連していた。BRCA2多様体キャリアでは、PRSの10パーセンタイルと90パーセンタイルのキャリアに対する80歳までの卵巣がんリスクはそれぞれ、6%および19%であった。著者らは、リスク予測モデルにPRSを組み込むことにより、この集団に対するがんリスク管理における決定により良い情報を提供しうると指摘した。[ 36 ]
数件の研究で、既知の感受性SNPに関する情報を含め、PRSを含めた後に改善された識別の正確度を報告することで臨床での乳がんリスク予測モデルを改善できる程度が調査されている。[ 41 ][ 42 ][ 43 ][ 44 ][ 45 ][ 46 ]例えば、PRS77と複数の臨床モデルを統合した研究で、50歳前に乳がんを予測するAUCは20%以上改善した。[ 42 ]WISDOMおよびMyPeBsを含む臨床試験では、スクリーニングの意思決定を下し、転帰を理解するためのPRSの潜在的な臨床的有用性の研究が進行中である。[ 47 ]PRSはヨーロッパ系の集団で大規模に開発されており、妥当性が確認されていることから、非ヨーロッパ系の集団でのこうしたPRSの有用性および予測の正確度は不明である。
既知の生殖性および生活様式の危険因子がPRSに作用して、乳がんリスクを高めるかどうかが大規模な研究で検討され、すでに確立された危険因子との相乗作用は確認されなかった。[ 48 ]
全ゲノムおよび全エクソーム配列決定法
一般的な遺伝子多様体を調べるGWASに加え、全ゲノムまたは全エクソーム配列決定に関する塩基配列決定に基づく解析[ 49 ]でも、XRCC2や、まれで浸透度が中程度の乳がん感受性遺伝子などの乳がんに関連する遺伝子が特定されている。[ 50 ](全エクソーム配列決定に関する詳しい情報については、がん遺伝学の概要に関するPDQ要約の臨床シークエンシングのセクションを参照のこと。)
参考文献- Pharoah PD, Antoniou A, Bobrow M, et al.: Polygenic susceptibility to breast cancer and implications for prevention. Nat Genet 31 (1): 33-6, 2002.[PUBMED Abstract]
- Breast Cancer Association Consortium: Commonly studied single-nucleotide polymorphisms and breast cancer: results from the Breast Cancer Association Consortium. J Natl Cancer Inst 98 (19): 1382-96, 2006.[PUBMED Abstract]
- Dunning AM, Healey CS, Pharoah PD, et al.: A systematic review of genetic polymorphisms and breast cancer risk. Cancer Epidemiol Biomarkers Prev 8 (10): 843-54, 1999.[PUBMED Abstract]
- Thorisson GA, Smith AV, Krishnan L, et al.: The International HapMap Project Web site. Genome Res 15 (11): 1592-3, 2005.[PUBMED Abstract]
- Clarke L, Zheng-Bradley X, Smith R, et al.: The 1000 Genomes Project: data management and community access. Nat Methods 9 (5): 459-62, 2012.[PUBMED Abstract]
- Evans DM, Cardon LR: Genome-wide association: a promising start to a long race. Trends Genet 22 (7): 350-4, 2006.[PUBMED Abstract]
- Cardon LR: Genetics. Delivering new disease genes. Science 314 (5804): 1403-5, 2006.[PUBMED Abstract]
- Chanock SJ, Manolio T, Boehnke M, et al.: Replicating genotype-phenotype associations. Nature 447 (7145): 655-60, 2007.[PUBMED Abstract]
- Wellcome Trust Case Control Consortium: Genome-wide association study of 14,000 cases of seven common diseases and 3,000 shared controls. Nature 447 (7145): 661-78, 2007.[PUBMED Abstract]
- Easton DF, Pooley KA, Dunning AM, et al.: Genome-wide association study identifies novel breast cancer susceptibility loci. Nature 447 (7148): 1087-93, 2007.[PUBMED Abstract]
- Stacey SN, Manolescu A, Sulem P, et al.: Common variants on chromosomes 2q35 and 16q12 confer susceptibility to estrogen receptor-positive breast cancer. Nat Genet 39 (7): 865-9, 2007.[PUBMED Abstract]
- Hunter DJ, Kraft P, Jacobs KB, et al.: A genome-wide association study identifies alleles in FGFR2 associated with risk of sporadic postmenopausal breast cancer. Nat Genet 39 (7): 870-4, 2007.[PUBMED Abstract]
- Turnbull C, Ahmed S, Morrison J, et al.: Genome-wide association study identifies five new breast cancer susceptibility loci. Nat Genet 42 (6): 504-7, 2010.[PUBMED Abstract]
- Gold B, Kirchhoff T, Stefanov S, et al.: Genome-wide association study provides evidence for a breast cancer risk locus at 6q22.33. Proc Natl Acad Sci U S A 105 (11): 4340-5, 2008.[PUBMED Abstract]
- Zheng W, Long J, Gao YT, et al.: Genome-wide association study identifies a new breast cancer susceptibility locus at 6q25.1. Nat Genet 41 (3): 324-8, 2009.[PUBMED Abstract]
- Kibriya MG, Jasmine F, Argos M, et al.: A pilot genome-wide association study of early-onset breast cancer. Breast Cancer Res Treat 114 (3): 463-77, 2009.[PUBMED Abstract]
- Murabito JM, Rosenberg CL, Finger D, et al.: A genome-wide association study of breast and prostate cancer in the NHLBI's Framingham Heart Study. BMC Med Genet 8 (Suppl 1): S6, 2007.[PUBMED Abstract]
- Stacey SN, Manolescu A, Sulem P, et al.: Common variants on chromosome 5p12 confer susceptibility to estrogen receptor-positive breast cancer. Nat Genet 40 (6): 703-6, 2008.[PUBMED Abstract]
- Ahmed S, Thomas G, Ghoussaini M, et al.: Newly discovered breast cancer susceptibility loci on 3p24 and 17q23.2. Nat Genet 41 (5): 585-90, 2009.[PUBMED Abstract]
- Reeves GK, Travis RC, Green J, et al.: Incidence of breast cancer and its subtypes in relation to individual and multiple low-penetrance genetic susceptibility loci. JAMA 304 (4): 426-34, 2010.[PUBMED Abstract]
- Haiman CA, Chen GK, Vachon CM, et al.: A common variant at the TERT-CLPTM1L locus is associated with estrogen receptor-negative breast cancer. Nat Genet 43 (12): 1210-4, 2011.[PUBMED Abstract]
- Stevens KN, Fredericksen Z, Vachon CM, et al.: 19p13.1 is a triple-negative-specific breast cancer susceptibility locus. Cancer Res 72 (7): 1795-803, 2012.[PUBMED Abstract]
- Campa D, Kaaks R, Le Marchand L, et al.: Interactions between genetic variants and breast cancer risk factors in the breast and prostate cancer cohort consortium. J Natl Cancer Inst 103 (16): 1252-63, 2011.[PUBMED Abstract]
- Milne RL, Gaudet MM, Spurdle AB, et al.: Assessing interactions between the associations of common genetic susceptibility variants, reproductive history and body mass index with breast cancer risk in the breast cancer association consortium: a combined case-control study. Breast Cancer Res 12 (6): R110, 2010.[PUBMED Abstract]
- Pharoah PD, Antoniou AC, Easton DF, et al.: Polygenes, risk prediction, and targeted prevention of breast cancer. N Engl J Med 358 (26): 2796-803, 2008.[PUBMED Abstract]
- Gail MH: Discriminatory accuracy from single-nucleotide polymorphisms in models to predict breast cancer risk. J Natl Cancer Inst 100 (14): 1037-41, 2008.[PUBMED Abstract]
- Gail MH: Value of adding single-nucleotide polymorphism genotypes to a breast cancer risk model. J Natl Cancer Inst 101 (13): 959-63, 2009.[PUBMED Abstract]
- Wacholder S, Hartge P, Prentice R, et al.: Performance of common genetic variants in breast-cancer risk models. N Engl J Med 362 (11): 986-93, 2010.[PUBMED Abstract]
- Song H, Ramus SJ, Tyrer J, et al.: A genome-wide association study identifies a new ovarian cancer susceptibility locus on 9p22.2. Nat Genet 41 (9): 996-1000, 2009.[PUBMED Abstract]
- Goode EL, Chenevix-Trench G, Song H, et al.: A genome-wide association study identifies susceptibility loci for ovarian cancer at 2q31 and 8q24. Nat Genet 42 (10): 874-9, 2010.[PUBMED Abstract]
- Bolton KL, Tyrer J, Song H, et al.: Common variants at 19p13 are associated with susceptibility to ovarian cancer. Nat Genet 42 (10): 880-4, 2010.[PUBMED Abstract]
- Mavaddat N, Pharoah PD, Michailidou K, et al.: Prediction of breast cancer risk based on profiling with common genetic variants. J Natl Cancer Inst 107 (5): , 2015.[PUBMED Abstract]
- Curtit E, Pivot X, Henriques J, et al.: Assessment of the prognostic role of a 94-single nucleotide polymorphisms risk score in early breast cancer in the SIGNAL/PHARE prospective cohort: no correlation with clinico-pathological characteristics and outcomes. Breast Cancer Res 19 (1): 98, 2017.[PUBMED Abstract]
- Cuzick J, Brentnall AR, Segal C, et al.: Impact of a Panel of 88 Single Nucleotide Polymorphisms on the Risk of Breast Cancer in High-Risk Women: Results From Two Randomized Tamoxifen Prevention Trials. J Clin Oncol 35 (7): 743-750, 2017.[PUBMED Abstract]
- Khera AV, Chaffin M, Aragam KG, et al.: Genome-wide polygenic scores for common diseases identify individuals with risk equivalent to monogenic mutations. Nat Genet 50 (9): 1219-1224, 2018.[PUBMED Abstract]
- Kuchenbaecker KB, McGuffog L, Barrowdale D, et al.: Evaluation of Polygenic Risk Scores for Breast and Ovarian Cancer Risk Prediction in BRCA1 and BRCA2 Mutation Carriers. J Natl Cancer Inst 109 (7): , 2017.[PUBMED Abstract]
- Li H, Feng B, Miron A, et al.: Breast cancer risk prediction using a polygenic risk score in the familial setting: a prospective study from the Breast Cancer Family Registry and kConFab. Genet Med 19 (1): 30-35, 2017.[PUBMED Abstract]
- Li J, Ugalde-Morales E, Wen WX, et al.: Differential Burden of Rare and Common Variants on Tumor Characteristics, Survival, and Mode of Detection in Breast Cancer. Cancer Res 78 (21): 6329-6338, 2018.[PUBMED Abstract]
- Mavaddat N, Michailidou K, Dennis J, et al.: Polygenic Risk Scores for Prediction of Breast Cancer and Breast Cancer Subtypes. Am J Hum Genet 104 (1): 21-34, 2019.[PUBMED Abstract]
- Robson ME, Reiner AS, Brooks JD, et al.: Association of Common Genetic Variants With Contralateral Breast Cancer Risk in the WECARE Study. J Natl Cancer Inst 109 (10): , 2017.[PUBMED Abstract]
- Allman R, Dite GS, Hopper JL, et al.: SNPs and breast cancer risk prediction for African American and Hispanic women. Breast Cancer Res Treat 154 (3): 583-9, 2015.[PUBMED Abstract]
- Dite GS, MacInnis RJ, Bickerstaffe A, et al.: Breast Cancer Risk Prediction Using Clinical Models and 77 Independent Risk-Associated SNPs for Women Aged Under 50 Years: Australian Breast Cancer Family Registry. Cancer Epidemiol Biomarkers Prev 25 (2): 359-65, 2016.[PUBMED Abstract]
- Shieh Y, Hu D, Ma L, et al.: Breast cancer risk prediction using a clinical risk model and polygenic risk score. Breast Cancer Res Treat 159 (3): 513-25, 2016.[PUBMED Abstract]
- Starlard-Davenport A, Allman R, Dite GS, et al.: Validation of a genetic risk score for Arkansas women of color. PLoS One 13 (10): e0204834, 2018.[PUBMED Abstract]
- van Veen EM, Brentnall AR, Byers H, et al.: Use of Single-Nucleotide Polymorphisms and Mammographic Density Plus Classic Risk Factors for Breast Cancer Risk Prediction. JAMA Oncol 4 (4): 476-482, 2018.[PUBMED Abstract]
- Zhang X, Rice M, Tworoger SS, et al.: Addition of a polygenic risk score, mammographic density, and endogenous hormones to existing breast cancer risk prediction models: A nested case-control study. PLoS Med 15 (9): e1002644, 2018.[PUBMED Abstract]
- Esserman LJ; WISDOM Study and Athena Investigators: The WISDOM Study: breaking the deadlock in the breast cancer screening debate. NPJ Breast Cancer 3: 34, 2017.[PUBMED Abstract]
- Rudolph A, Song M, Brook MN, et al.: Joint associations of a polygenic risk score and environmental risk factors for breast cancer in the Breast Cancer Association Consortium. Int J Epidemiol 47 (2): 526-536, 2018.[PUBMED Abstract]
- Shendure J: Next-generation human genetics. Genome Biol 12 (9): 408, 2011.[PUBMED Abstract]
- Park DJ, Lesueur F, Nguyen-Dumont T, et al.: Rare mutations in XRCC2 increase the risk of breast cancer. Am J Hum Genet 90 (4): 734-9, 2012.[PUBMED Abstract]
- BRCA病原性多様体キャリアの臨床管理
-
乳がんおよび卵巣がんに対して遺伝的感受性を有する集団を対象に、リスクを低減する介入の結果に関して利用可能なデータが増加している。[ 1 ][ 2 ][ 3 ][ 4 ][ 5 ][ 6 ][ 7 ]本要約の他のセクションで概説しているように、家族歴または遺伝子検査が陽性の場合にみられるがんリスクのレベルに関しては、不確実性が無視できないことが多い。このような環境では、個人の好みがリスク低減戦略について患者が決定する際の重要因子になる可能性が高い。
スクリーニングおよび予防戦略
乳がん
スクリーニング/サーベイランス
一般集団におけるスクリーニングに関する情報については、乳がんのスクリーニングに関するPDQ要約を参照のこと、さらに、スクリーニングおよび予防に関連する証拠レベルに関する情報については、PDQ要約のがん遺伝学研究に関する証拠レベルを参照のこと。
乳房自己検査
一般集団では、乳房自己検査(BSE)の価値を示す証拠が限られている。中国の上海で実施されたBSEのランダム化研究から、予備成績が報告されている。[ 8 ]5年目の時点で、女性の対照群と比較したところ、BSE群では乳がんによる死亡率の低下はみられなかっただけでなく、乳がん診断時の病期分類に実質的な移行もみられなかった。(詳しい情報については、乳がんのスクリーニングに関するPDQ要約を参照のこと。)
乳がんリスクが高い個人において、BSEに関する直接的かつプロスペクティブな証拠はほとんど存在しない。カナダ国家乳がんスクリーニング研究(CNBCSS)では、乳がんに罹患している第一度近親者(FDR)がいる女性は、家族歴のない女性よりもBSE能力スコアが統計的に有意に高いとの報告がある。ある紹介センターでの高リスク女性251人の研究では、以前の検診後1年未満の間に自己検査により5例の乳がんが検出された(臨床医の診察により検出された1例のがん、およびマンモグラフィの結果により検出された11例のがんと比較)。このコホートの女性は自己検査の指導を受けていたが、この期間のがんが計画された自己検査の結果検出されたのか、偶然の乳房腫瘤の発見なのかは述べられていない。[ 9 ]BRCA1/BRCA2病原性多様体キャリアを対象にした別のシリーズでは、がんを発症した9例中4例が、マンモグラムでは正常と報告された後で触知可能な腫瘤と診断されたことから、自己検査の潜在的価値がさらに強く示唆される。[ 10 ]Cancer Genetics Studies Consortiumにより召集された作業部会は、「規則正しい習慣を身につけ、乳房組織の正常な特徴を知っておくためにも、成人期の初期(例、年齢18~21歳まで)から開始する、月1回の自己検査を行うこと」を推奨している。また「自己検査に関する教育と指導を行うこと」を推奨している。[ 11 ]
証拠レベル:5
乳房視触診
乳房視触診(CBE)に関するプロスペクティブなデータはほとんど存在しない。
Cancer Genetics Studies Consortiumの作業部会は、「早発型乳がんの遺伝リスクを有する女性では、自己検査と同様に、臨床検査の役割が特に重要であろう」と結論を下した。彼らはBRCA1またはBRCA2の高リスク病原性多様体の女性キャリアは、年齢25歳~35歳で1年に1回または半年に1回診察を受けるよう推奨している。[ 11 ]
証拠レベル:5
マンモグラフィ
一般集団では、年齢50歳~59歳の女性が定期的にマンモグラフィスクリーニングを受けたことにより、乳がんによる死亡率が25~30%低下したことを示す強力な証拠がある。(詳しい情報については、乳がんのスクリーニングに関するPDQ要約を参照のこと。)40歳~49歳でマンモグラフィによるスクリーニングを受け始めた女性では、スクリーニング開始から15年後に乳がんによる死亡率が17%低下したことが認められている。[ 12 ]28,000人以上の女性を対象にしたコホート研究から得られた観測データにより、若い女性ではマンモグラフィの感度が低いことが示唆されている。この研究では、乳がんに罹患しているFDRが1人いる比較的若い女性(年齢30歳~49歳)に対する感度が最も低かった。このような女性の場合、最初のマンモグラフィのスクリーニングから13ヵ月以内に診断された乳がんの69%がマンモグラフィにより検出された。これとは対照的に、家族歴のない50歳未満の女性に対する感度は、88%(P=0.08)であった。50歳以上の女性の場合、感度は13ヵ月目で93%であり、家族歴によって変わることはない。[ 13 ]予備データにより、マンモグラフィの感度は、BRCA1およびBRCA2の非キャリアよりもキャリアにおける方が低いことが示唆される。[ 10 ]続いて実施された観察研究は、マンモグラフィの陽性適中率(PPV)が年齢とともに高くなり、高齢女性および乳がん家族歴のある女性で最も高いことを明らかにしている。[ 14 ]陽性適中率が高くなるのは、乳がん発症率が増大し、感度および/または特異度が高くなるためである。[ 15 ]1件の研究により、26人がBRCA1病原性多様体を有し、2人がBRCA2病原性多様体を有した全28人の女性において、突出境界の存在と乳腺X線写真偽陰性との関連が明らかにされた。髄様組織型の特徴である突出境界は、線維性反応の欠如と関連している。[ 16 ]さらに、急速な腫瘍倍加時間により、見掛けは正常な検査後間もなく、腫瘍が現れることがある。ある研究では、BRCA1/BRCA2キャリアにおける平均腫瘍倍加時間は45日であったのに対し、非キャリアでは84日であった。[ 17 ]BRCA病原性多様体を有する女性におけるマンモグラフィでの乳腺密度を評価した別の研究では、病原性多様体の保有状況とマンモグラフィでの乳腺密度との間に関連は認められなかった;しかしながら、キャリアと非キャリアのいずれにおいても、高い乳腺密度は乳がんリスクの増大と関連していた。[ 18 ]
カナダのランダム化乳がんスクリーニング研究-2は、一般集団から抽出した50歳~59歳の女性を対象として年1回のCBEとマンモグラフィの併用とCBEのみとを比較した。両群ともBSEに関する指導は受けていた。[ 19 ]マンモグラフィにより、CBEよりも小さな原発浸潤性腫瘍、多くの浸潤性乳管がん、多くの非浸潤性乳管がん(DCIS)が検出されたが、CBEとマンモグラフィの併用群とCBE単独群の乳がんによる死亡率はほぼ同じであり、他の乳がんスクリーニング試験と比べ、勝るとも劣らなかった。平均追跡期間13年(範囲、11.3~16.0年)後の乳がんによる累積死亡比率は1.02(95%信頼区間[CI]、0.78-1.33)であった。この知見に関する1つの可能な解釈として、CBEを実施する医療専門家に対する行き届いた訓練および監督が挙げられた。
デジタルマンモグラフィとは、X線像を検出し記録するデジタル検出器の使用を意味する。この技術によりコントラスト分解能が向上するため[ 20 ]、マンモグラフィの感度が向上する可能性のある戦略として提案されている。40歳以上の女性の6,736の診察において、デジタルとルーチンのマンモグラフィとを比較したスクリーニング研究は、がん検出率における差を見出さなかった[ 21 ];しかしながら、デジタルマンモグラフィの方が、再検診が少ない結果となった。42,760人の女性においてデジタルマンモグラフィとマンモグラフィ単純撮影とを比較した別の研究(ACRIN-6652)では、2つの技術による診断の全体的な正確度はほぼ同じであった。[ 22 ]受信者動作特性曲線を比較したところ、50歳未満の女性、乳房がX線画像で濃く描出される女性、および閉経前または閉経期前後の女性では、デジタルマンモグラフィの方が正確であった。
BRCA病原性多様体を有し、スクリーニングとリスク低減のための手術に関する一律の推奨を受けた個人251人のプロスペクティブ研究において、年1回のマンモグラフィは、BRCAの結果を受け取った後、平均20.2ヵ月で6人の女性の乳がんを発見した。[ 9 ]Cancer Genetics Studies Consortiumの作業部会は、BRCA1またはBRCA2の高リスク病原性多様体の女性キャリアに対して、「25歳~35歳から年1回のマンモグラフィを開始する」ことを勧めている。「マンモグラムは、以前のフィルムがあれば比較することができるため、可能であれば、同じ位置で行うべきである」と推奨している。[ 11 ]電離放射線ツールを用いるスクリーニング vs CBEまたは非電離放射線ツールによるスクリーニングの相対利益および相対リスクに関するプロスペクティブ研究から得られたデータは、有用な可能性がある。[ 23 ][ 24 ][ 25 ]
ある観察によって、BRCA病原性多様体キャリアは、病原性多様体が認められない女性よりも放射線誘発性乳がんに罹患する傾向がより強い可能性があると懸念されている。BRCA1およびBRCA2蛋白は、放射線誘発性の損傷の修復に関与する機序を含めて、DNA損傷修復の細胞メカニズムにおいて重要な役割を果たしていることが知られている。一部の研究では、BRCA多様体についてヘテロ接合性の細胞では中間の放射線感受性が示唆されているが、これは一貫しておらず、実験の体系およびエンドポイントによって異なる。
BRCA1およびBRCA2病原性多様体キャリアを対象とした3件の研究では、電離放射線曝露と乳がんリスクの間に関係があるという納得できる証拠は得られていない。[ 26 ][ 27 ][ 28 ]対照的に、2件の大規模な国際研究では、胸部X線により[ 29 ]、または診断用放射線への総曝露の推定値により[ 30 ]、乳がんリスクが上昇するという証拠が認められた。病原性多様体キャリア1,601人を対象とした大規模な国際共同ケースコントロール研究によると、胸部X線検査をかつて受けたことのある女性では乳がんリスクが高く(ハザード比[HR]、1.54)、1949年より後に出生し、X線への曝露が20歳より前に限られる40歳以下の女性でリスクが最も高いことが報告された。[ 29 ]この研究における被験者の一部は、欧州の3施設による病原性多様体キャリアを対象としたより大規模でより包括的な解析にも含まれていた。[ 30 ]これは、英国、フランス、およびオランダから1,993人のBRCA1およびBRCA2病原性多様体キャリアを対象とした試験で、年齢層ごとの診断用放射線(例えば、X線、マンモグラフィ、蛍光透視、およびコンピュータ断層撮影)による推定総曝露量は、自己報告式質問票から得られた。30歳前に曝露された女性は、それまでに曝露されていない女性に比べリスクが高かった(HR、1.90;95%CI、1.20-3.00)。このリスクは、20歳未満の女性におけるマンモグラフィ以外の放射線曝露(HR、1.62;95%CI、1.02-2.58)により主に導かれたものであった。その後、研究参加時点で乳がんの診断を受けていないBRCA1キャリア1,844人とBRCA2キャリア502人を対象としたプロスペクティブ研究によると、平均追跡期間が5.3年で、マンモグラフィの受診歴と乳がんリスクとの間に有意な関連性は観察されなかった。[ 28 ]30歳未満の女性を対象とした追加のサブグループ解析で、乳がんリスクと関連しないことが実証された。
BRCA1およびBRCA2病原性多様体キャリアにおける磁気共鳴画像法(MRI)のルーチン使用に関して、特に若い女性では、マンモグラフィによるスクリーニングから得られる可能性のある何らかの有益性を、潜在リスクに対して慎重に比較検討しなければならない。[ 31 ]1件の研究から、BRCA1およびBRCA2病原性多様体キャリアで最も費用効果の高いスクリーニング戦略は、年1回のMRIを25歳で開始し、30歳からはMRIとデジタルマンモグラフィを交互に実施する(各検査を年1回実施するが、スクリーニングは6ヵ月ごとになるようにする)ことではないかと提案されている。[ 32 ]現在National Comprehensive Cancer Network(NCCN)は、25~29歳では年1回の乳房造影MRIによるスクリーニング(またはMRIが利用できない場合にのみ、トモシンセシスを検討するマンモグラフィ)、また30~75歳では年1回のマンモグラフィ(トモシンセシスの検討と乳房造影MRI)によるスクリーニングを推奨している。[ 33 ]
磁気共鳴画像法
乳がんについて遺伝性リスクのある女性では、マンモグラフィの感度が比較的低いため、BRCA病原性多様体キャリアを含めた高リスク女性において多くのスクリーニング方法が提案され研究されている。乳がんリスクのある女性を対象とした乳房のMRIによるスクリーニングに関しては、比較的大規模な多施設試験の報告を含め、多くの研究による経験が報告されている。[ 34 ][ 35 ][ 36 ][ 37 ][ 38 ][ 39 ][ 40 ][ 41 ][ 42 ]
こうした研究には制限があるにもかかわらず、研究は、乳房のMRIが遺伝性乳がんの発見に関してマンモグラフィまたは超音波のいずれよりも感度が高いことを一貫して示している。6件の大規模研究の結果が表11、遺伝性乳がんのリスクがある女性におけるMRIスクリーニング検査の要約に示されている。[ 34 ][ 36 ][ 37 ][ 40 ][ 43 ][ 44 ]これらのプログラムにおけるほとんどのがんがスクリーニングで発見されており、スクリーニングとスクリーニングの合間に発症したがんはわずか6%であった。(研究の方法論によって定義されているように)MRIの感度は71~100%であった。研究を総合すると、MRIにより77%のがんが同定され、マンモグラフィにより42%のがんが同定された。
他のスクリーニング方法と比較してMRIの低い特異度に関する問題が提起されている。1件の研究では、最初のMRIスクリーニング後、精密な評価のために16.5%の患者が呼び戻され、6ヵ月経過時にさらに7.6%の患者が短期間の追跡検査を受けるように勧められた。[ 37 ]これらの割合は、後のスクリーニング期間中にかなり低下し、より詳しいMRIのために呼び戻された被験者は10%未満、短期間の追跡検査を受けるように勧められたのは3%未満であった。2つ目の研究、Magnetic Resonance Imaging for Breast Screening (MARIBS)では、追加の評価のために呼び戻された割合は年間10.7%であった。[ 36 ]最初の研究において生検が良性であった割合は、1巡目で11%、2巡目で6.6%、3巡目で4.7%であった。[ 37 ]MARIBS研究における集合外科的生検率(aggregate surgical biopsy rate)はスクリーニング1,000エピソード当たり9例であったが、MARIBSの計算の分子には、追跡の超音波、コア針生検、および穿刺吸引法が含まれていないため、負担が過小評価されている可能性がある。[ 36 ]MRIのPPVはさまざまなシリーズで計算方法が異なっており、検査におけるすべての異常、または生検を来した検査のみが分母に含められるかによっていくぶん変動する。一般に、組織採取のために推奨されるPPVは(追加の調査とは対照的に)ほとんどのシリーズで50%程度である。
これらの試験により、MRIは遺伝性乳がんの発見においてマンモグラフィより優れていること、および年1回のMRIスクリーニングを含むこれらの試験に参加した女性はスクリーニングで見逃されるがんを有する可能性は低かったことが証明されると考えられる。[ 45 ]しかしながら、マンモグラフィは、MRIでは同定されないある種のがん、特にDCISを同定しうる。[ 46 ]
病期の低下に関して、遺伝性乳がんのリスクがある患者では、2つの非ランダム化対照群の女性よりも、腫瘍が小さくリンパ節転移陰性の乳がんと診断される傾向が高かったことを明らかにしたスクリーニング研究が1件ある。[ 34 ]多施設共同ランダム化試験により、BRCA1/BRCA2病原性多様体の検査が陰性であるが、家族の乳がん生涯リスクが20%以上ある女性を対象に、年1回の乳房MRI、年1回のCBE、および年2回のマンモグラムが年1回のマンモグラムおよびCBEと比較された。MRI群では、マンモグラム単独群よりも浸潤がんが小さく、リンパ節転移陽性が少ないうえに、病期が低かった。[ 47 ]
MRIスクリーニングの明らかな感度にもかかわらず、MRIをベースにしたプログラムの一部の女性は致死的な乳がんを発症する。年1回のマンモグラフィおよびMRIでスクリーニングを受けた51人のBRCA1病原性多様体キャリアおよび41人のBRCA2病原性多様体キャリア(このうち80人がリスク低減のための卵巣摘出術を受けた)を対象にした1件のプロスペクティブ研究では、11人に乳がんが発見された(浸潤性:9例およびDCIS:2例)。6人のがんは最初にMRIで発見された;3人が最初にマンモグラムで発見された;2人は中間期がんであった。乳がんはすべてBRCA1病原性多様体キャリアに発生したことから、短期的には卵巣摘出術後もBRCA1関連乳がんのリスクが依然として高いことが示唆される。これらの結果から、BRCA1およびBRCA2病原性多様体キャリアではサーベイランスおよび予防戦略により転帰が異なることが示唆されている。[ 41 ]
3件の大規模研究(MARIBS、カナダの研究、オランダのMRIスクリーニング研究)からの結果を集約した記事が発表され、MRIをマンモグラフィに追加した場合、BRCA2病原性多様体キャリアで検出されたがんの80%がDCISまたは1cm未満の浸潤がんであったことが実証された。BRCA1病原性多様体キャリアではがんの49%がDCISまたは小さい浸潤がんであった。さらに、著者らはBRCA1およびBRCA2の両方の病原性多様体キャリアに対してMRI追加による死亡率の有益性を予測した。このモデルでは、乳がん死亡率の低下をマンモグラフィで42~47%、MRIで48~61%、併用スクリーニングで50~62%と予測した。[ 48 ]1997年から2006年の間にMRIを受けたBRCA1/BRCA2病原性多様体キャリアを調査した別の研究では、発生がんの97%が0期またはI期であったことが実証されている。[ 49 ]2015年に行われた1件のオランダのケースコントロール研究では、さらに2,308人の高リスク患者の評価が行われ、その中にはマンモグラムによるスクリーニングを受けた既知のBRCA病原性多様体を有する女性706人が含まれており、これらの女性とMRIが追加された女性が比較された。[ 50 ]スクリーニングを受けた患者のうち、93人に97のがんが検出され、33人はBRCA1病原性多様体を、18人はBRCA2病原性多様体を有していた。中央値9年の追跡を施行した結果、MRIスクリーニングを受けたコホートでは、無転移生存率が改善した(90% vs 77%)が、サンプル数が少数であったため、BRCA1とBRCA2の亜集団における統計的有意差には達しなかった。コホート全体に含まれるMRIによるスクリーニングを受けた患者では、リンパ節転移陰性が少なく、化学療法が施行される例も少ない傾向がみられた。米国がん協会とNCCNは、遺伝性乳がんリスクのある女性に対して、年1回のMRIによるスクリーニングの利用を推奨している。[ 33 ][ 51 ]
マンモグラフィとMRIの実施時期に関する別の問題は、それらを同時に実施すべきか、交互(各検査を年1回実施するが、スクリーニングは6ヵ月ごとになるようにする)に実施すべきかというものである。1件の研究から、BRCA1およびBRCA2病原性多様体キャリアで最も費用効果の高いスクリーニング戦略は、年1回のMRIを25歳で開始し、30歳からはMRIとデジタルマンモグラフィを交互に実施することではないかと提案されている。[ 32 ]
要約すると、BRCA1/BRCA2病原性多様体キャリアに対する乳がんサーベイランスでは、乳房MRIの不可欠な役割がエビデンスにより強く支持される。
表11.遺伝性乳がんのリスクがある女性における磁気共鳴画像法(MRI)スクリーニング検査の要約 研究シリーズ Rijnsburger Warner MARIBS Kuhl Weinstein Sardanelli 合計 a最初にスクリーニングを受けた1,909人の女性に基づく。[ ] b浸潤性がんのみを有する患者および浸潤性がんと非浸潤性がんの両方を有する患者を含む。 cマンモグラフィとMRIスクリーニングの両方を受けた女性において発見されたがんは75のみである。 d超音波検査が実施された研究に限定される。 患者数 全体 2,157 236 649 687 609 501 4,839 BRCA1/BRCA2キャリア 594 236 120 65 44 330 1,389 スクリーニング回数 6,253 457 1,881 1,679 1,592 11,862 がんの数 ベースライン 22a 13 20 10 0 0 65 その後 97 9 15 17 18 52 208 浸潤性b 78 16 29 8 11 44 186 非浸潤性 19 9 6 9 7 8 58 年間発生率 10.4/1,000 19/1,000 計画されたスクリーニングでの発見例 78 21 33 27 18 49 226 (83%) 各方法での発見数 マンモグラフィ 31c 8 14 9 7 25 94 (42%) MRI 51c 17 27 25 12 42 174 (77%) 超音波d 7 10 3 26 46 (41%) 追跡期間 中央値4.9年 1年以上 2~7年 中央値29.09ヵ月 2年 3年 証拠レベル:3
超音波
数件の研究が、1件のレビューで考察されたように、マンモグラフィでは見落とされたが超音波により検出された乳がんの例を報告している。[ 52 ]家族歴に基づいた中等度のリスクをもつ149人の女性において、マンモグラフィの補助として行われた超音波のパイロット研究では、超音波所見に基づきがんが1例検出された。他に9例の良性病変の生検が実施された。1件がマンモグラフィと超音波両方の異常に基づき、残りの8件が超音波のみの異常に基づいていた。[ 52 ]乳房組織が濃く映る女性2,809人を対象にした大規模研究(ACRIN-6666)により、超音波は乳がんスクリーニングによる検出率をマンモグラフィ単独での1,000例当たり7.6例から、マンモグラフィと超音波併用で1,000例当たり11.8例に増加させることが実証された。[ 53 ]しかしながら、超音波スクリーニングは偽陽性率を増加させ、MRIと併用した場合の有益性は限定的なようである。女性171人(このうち92%がBRCA1/BRCA2病原性多様体キャリア)を対象にした多施設研究では、マンモグラフィ、MRI、および超音波検査を同時に実施したが、超音波単独ではがんは検出されなかった。[ 38 ]超音波に関し不明確なことは、死亡率におけるスクリーニングの効果、偽陽性結果の割合と転帰、経験豊富な乳房超音波検査士へのアクセスである。
証拠レベル:指定なし
他のスクリーニング方法
多くの他の技術が活発に研究されており、これにはTomosynthesis、造影マンモグラフィ、サーモグラフィ、放射性核種スキャンなどがある。これらの技術を実地臨床に組み入れるには、追加の証拠が必要である。
証拠レベル:指定なし
リスク低減のための手術
リスク低減のための乳房切除術
リスク低減のための乳房切除術(RRM)は、乳がん発生リスクが高いと考えられる患者に対する管理の選択肢の1つである。Society of Surgical Oncologyでは、BRCA1/BRCA2病原性多様体を有する女性、または乳がんの強い家族歴を有する女性に対する選択肢の1つとしてRRMを支持している。[ 54 ]歴史的に、全乳房切除術または単純乳房切除術が実施されており、これには乳頭乳輪領域(NAC)までを含めた乳房組織全体の切除が含まれる。患者が関心をもっている場合は、手技のアブレーションと同時に再建術を実施できる。再建術の選択肢には、組織拡張器とインプラントを用いる再建術または乳房の再建に患者自身の組織を用いる自家再建術が挙げられる。乳房の再建には多数のさまざまな組織を用いることができ、それには広背筋、腹直筋、または殿筋をベースにした皮弁が含まれる。深下腹壁動脈穿通枝皮弁などの筋温存技術も利用できるが、高度な微小血管吻合技術が要求される。審美的結果を向上させるために、皮膚温存技術(NACとともに乳房全体を切除するが、乳房の外皮全体を温存する)が利用されている。さらに改善するため、乳頭温存技術が開発されており、この方法では皮下の腺組織を切除しながら乳房の皮膚と乳頭全体が温存される。
非罹患女性におけるリスク低減のための乳房切除術
RRMと経過観察を比較するプロスペクティブ・ランダム化試験が存在しないため、データはコホート研究およびケースコントロール研究に限定されている。利用できるデータは、RRMにより高リスク患者における乳がん発生率が低下するが[ 55 ][ 56 ][ 57 ]、全生存(OS)が乳がんの発生による全リスクとより密接に相関していることを示している。数件の研究で、乳がんリスクおよび死亡率に対するRRMの影響が分析されている。常染色体優性素因を疑わせる家族歴により遺伝的リスクが考えられる214人の女性に関する1件のレトロスペクティブなコホート研究では、中央値で14年間の追跡の間に、両側RRMの施行後に乳がんと診断された女性は3人であった。[ 57 ]37.4個のがんが予測されていたため、リスクの低下は92.0%(95%CI、76.6%-98.3%)と計算された。追跡亜集団解析では、このコホート研究の214人の高リスク女性のうち176人がBRCA1およびBRCA2の病原性多様体に関する遺伝子検査を受けた。中央値にして13.4年間追跡したところ、18人の女性に病原性多様体が確認されたが、その中で乳がんが発生した者はいなかった。[ 55 ]RRMを受けた後に乳がんと診断された女性3人のうちの2人を検査したところ、どちらも病原性多様体をもっていなかった。病原性多様体キャリアにおけるリスクの低下は89.5~100.0%(95%CI、41.4%-100.0%)と計算されたが、この数値は病原性多様体のキャリアに予測されたがんの数について行われた仮定と、乳房切除術後にがんが発生したが検査を受けてない女性の状態に依存する。このレトロスペクティブなコホート研究の結果は、RRMを受けその後平均2.9年間プロスペクティブにモニタリングされた病原性多様体キャリア76人のプロスペクティブ解析により支持されている。これらの女性では乳がんは認められなかったが、一方で定期的なサーベイランスを受けている女性に8個の乳がんが同定された(RRM後の乳がんのHR、0.00[95%CI、0.00-0.36])。[ 56 ]
Prevention and Observation of Surgical Endpoints研究グループもまた、BRCA1/BRCA2病原性多様体キャリアを対象としてRRM後に乳がんリスクがどの程度低下するかを推定した。両側RRMを受けた105人の病原性多様体キャリアにおける乳がんの割合が、同手術を選択しなかった378人のキャリアのそれと比較された。両側乳房切除術の施行により乳がんのリスクは平均6.4年間の追跡の後、約90%低下した。[ 3 ]
また、BRCA1およびBRCA2の病原性多様体を有する女性におけるRRMの役割を評価するために、理論的モデルも利用されている。あるモデルでは、リスク低下を90%程度と仮定し、BRCA1またはBRCA2病原性多様体を保有する30歳の女性グループにRRMを施行すれば、余命が平均2.9年から5.3年延長する可能性を示唆している。[ 58 ]モンテカルロモデルを用いたコンピュータ・シミュレーション生存解析では、乳房MRI、マンモグラフィ、RRM、およびリスク低減のため卵管卵巣摘出術(RRSO)を含め、各介入がBRCA1およびBRCA2病原性多様体キャリアに与える影響について個々に調査した。[ 5 ]最も有効な戦略は、40歳ではRRSO、25歳ではRRMであり、70歳における生存率は一般集団と近い値であることが明らかになった。しかしながら、乳房切除を40歳まで遅らせた場合、またはRRMに代えて乳房MRIおよびマンモグラフィによるスクリーニングを行った場合も、推定生存率にほとんど影響はみられなかった。例えば、RRSOの女性において40歳でRRMに代えてMRIベースのスクリーニングを受けた場合は、25歳でRRMを受けた場合と比べて、生存率の3~5%減少につながった。[ 59 ]いずれのモデルでも同じように、多数の仮定は不確実さを引き起こす;しかしながら、これらの困難な決定を下した女性および医療関係者にとっては、こうした研究から追加情報が得られる。
リスクを有する女性を対象にした別の研究により、RRMに対して70%の時間得失値が示されたが、これは、参加者がRRMを回避するために平均余命の30%を犠牲にすることをいとわなかったということを意味している。[ 60 ]RRMの費用対効果を分析した研究も実施されている。研究者らにより、リスク低減のための手術(乳房切除術または卵巣摘出術)は、延命年数に関してはサーベイランスと比較すると費用対効果が大きいが、QOLの改善に関してはそうではないと結論された。[ 61 ]これらのデータは興味深く、公の方針決定に有用な可能性があるが、データは十分に検証できない仮定を含むので、臨床のための個別化はできない。
証拠レベル:3ai
罹患女性におけるリスク低減のための対側乳房切除術
非罹患女性における乳がんリスクを低下させる上でRRMが有効である場合、片側乳がんの女性に対するRRMの役割は何か。この問題は、片側乳がんで遺伝性リスクを有する女性に対する手術の選択肢に関する議論においてしばしば発生する。本セクションでは、乳房切除術で治療された女性におけるリスク低減のための対側乳房切除術(CRRM)の役割について扱い、乳房温存療法については論じない。複数の研究で、片側乳がん罹患女性におけるCRRMの割合の増加が示されている。[ 62 ][ 63 ]片側乳がん罹患女性に対するCRRMの妥当性を評価する場合、最初の作業は対側乳がん(CBC)のリスクを明らかにすることである。
一般集団における乳がん治療後のCBCリスクの現在の推定値は、年間約0.3%であり、低下しつつある。[ 64 ]乳がんの診断を受けたBRCA病原性多様体キャリアでは、2番目の無関係の乳がんのリスクは、初回診断時の年齢、生物学、および使用した全身療法に関連しているが、一般集団のリスクよりも明らかに高い。[ 65 ](この集団におけるCBCのリスクに関する詳しい情報については、本要約の高浸透度の乳がんおよび/または婦人科がん感受性遺伝子のセクションにあるBRCA病原性多様体キャリアにおける対側乳がんのセクションを参照のこと。)最初のがんの予後がきわめて良好なBRCA病原性多様体キャリアでは、2番目の無関係な乳がんイベントのリスクを推定することがリスク低減のための手術を受けるキャリアの判断に情報をもたらす上で重要であり、この状況で生存率を改善することが報告されている。[ 66 ]遺伝子検査の時期およびBRCA病原性多様体状態の情報は外科的意思決定に影響し、その後の手術を回避させる可能性があり、フォローアップケアに影響しうる。したがって、BRCA病原性多様体を保有するリスクが高い個人について、可能な場合は、手術に先立って遺伝子検査を検討することが重要である。[ 67 ]
片側乳がんのBRCA1およびBRCA2病原性多様体キャリア148人では、79人がCRRMを受け、CBCのリスクは91%減少し、リスク低減のための卵巣摘出術の効果とは無関係であった。生存率はCRRMを受けた女性の方が優れていたが、この結果はおそらく、手術を受けていないグループにおいて指標となるがん(index cancer)、または異時性の卵巣がんによる高い死亡率に関連していた。[ 68 ]550人の女性(BRCAキャリア202人を含む)に関するヨーロッパの10施設のデータから、女性3,334人年の追跡でRRMが非常に有効であることが示された。生涯リスクが25~80%の女性に対しては両側RRMが実施され、平均推定発生率は年間1%であった。追跡期間中にこのコホートで乳がんは発生しなかったが、34個以上の乳がんが予想されていた。[ 69 ]BRCA1およびBRCA2の病原性多様体キャリア593人を対象としたレトロスペクティブ研究ではCRRMを受けた片側乳がん女性105人が含まれ、10年生存率は89%であったのに対して、リスク低減のための対側乳房切除を受けなかった群では71%であった(P < 0.001)。[ 4 ]この研究には、このサンプルの大部分における乳がんスクリーニング、悪性度、エストロゲン受容体の状態に関する情報が不足しているなど、いくつかの要因による限界があった。
オランダで1980年から2011年の間にBRCA病原性多様体を認め、かつ片側乳がんの診断を受けたことが特定された患者583人のコホートについて、CRRMの効果が評価された。[ 70 ]追跡期間中央値11.4年で、患者のうち242人(42%)が診断後のさまざまな時点でRRMを受けた(193人がBRCA1病原性多様体キャリア、49人がBRCA2病原性多様体キャリア)。RRM群では、サーベイランス群と比較してOSの改善が観察され(HR、0.49;95%CI、0.29-0.82)、40歳より前に診断され、腫瘍悪性度が低く、かつ非トリプルネガティブ亜型の患者で改善が最も著しかった。手術までの時間のバイアスについてコントロールしようと、著者らは原発がん診断から2年後に無病状態であることが確認された女性の個別評価を含めた(HR、0.55;95%CI、0.32-0.95)。その上、RRMを受けた群は、両側卵管卵巣摘出術および全身化学療法を受ける可能性が高く、これらの生存所見の意義に影響を及ぼすことがある。
BRCA1/BRCA2病原性多様体が既知の家系出身である初期の乳がん女性390人を対象としたレトロスペクティブ研究によると、両側乳房切除を受けた女性では、片側乳房切除を選択した女性と比較して生存に有意な改善が認められた。[ 66 ]患者は中央値にして14.3年間(範囲:0.1~20.0年)追跡された。診断時年齢、診断年、治療、および他の予後因子で調整した多変量解析によると、CRRMは、乳がんによる死亡の48%の減少と関連していることが明らかになった。これは、比較的小規模な研究であり、著者らは複数の因子に対する調整を行ったが、残存する交絡因子が結果に影響した可能性がある。
これらの研究すべてに、きわめて限られた集団を対象とする比較的小規模のレトロスペクティブ研究に生じるバイアスによる限界がある。社会経済的状態、併存疾患、ケアへのアクセスなどの潜在的な交絡変数に関するデータはしばしば限定的である。RRMを受けることを選択する女性は、より広範囲な手術に耐えることができるという理由でより健康であることが示唆されている。この説は、I~III期の片側乳がん女性においてCRRMと転帰の関連性を検討するためにSurveillance, Epidemiology, and End Results(SEER) Programのデータを使用した1件の研究により裏付けられている。結果は全原因死亡率および乳がん特異的死亡率、またがん以外のイベントによる死亡率の低下を示しており、これはCRRMと関連していることが予想されなかった所見である。[ 71 ]
証拠レベル:3ai
乳輪乳頭温存乳房切除術
リスク低減のための手技を受けるBRCA病原性多様体キャリアにおける乳輪乳頭温存乳房切除術(NSM)の選択肢は、乳頭および乳輪まで含めた部分(NAC)を生存可能状態に維持するために手術時に残される乳房組織が増えるという懸念のために賛否両論がある。しかしながら、残存組織量を最小化する能力は経験および技術に関連している可能性がある。2007年から2014年に2病院で実施されたBRCA病原性多様体キャリアにおけるNSMについてのレトロスペクティブ・レビューでは、NSMがBRCA病原性多様体キャリア201人の397の乳房で施行された。[ 72 ]この研究には、非罹患女性と罹患女性の両方が含められた。RRM施行患者150人中4人(2.7%)およびがん患者51人中2人(3.9%)で偶発がんが認められた。32.6ヵ月(範囲、1.0~76.0ヵ月)の平均追跡期間で、腋窩の再発患者2人、最初のNSMの11ヵ月後の局所および遠隔再発を来した患者1人、および乳房の下部に新規がんを生じた患者1人を含む、その後のがんイベント4件が認められたが、NACでの再発は認められなかった。2005年から2013年にBRCA病原性多様体キャリア89人に対して実施された177件のNSMを対象とした研究では、同様な優れた局所制御率が報告された。63人の患者がリスク低減を目的としたNSMを受け(追跡期間中央値26ヵ月;範囲、11~42ヵ月)、26人の患者がNSMを受け、乳がんと診断された(追跡期間中央値28ヵ月;範囲、15~43ヵ月)。5人の患者では、追加の乳頭切除が必要であった。局所再発または新たな乳がんの診断はみられなかった。[ 73 ]
証拠レベル:3aii
RRM標本の病理組織学
BRCA1またはBRCA2の病原性多様体を有する女性におけるRRMで得られた標本の病理組織所見を記載した研究が複数あるが、それらの結果はいくぶん整合性に欠けている。2件のシリーズでは、片側または両側のRRMのいずれかを受けた病原性多様体キャリア女性の37~46%において、乳がんのリスク増加と関連する増殖性病変(非浸潤性[in situ]小葉がん、小葉の異型過形成、異型乳管過形成、およびDCIS)が報告された。[ 74 ][ 75 ][ 76 ]これらのシリーズでは患者の13~15%において、予防的に切除した乳房中にそれまで疑っていなかったDCISが見つかった。オーストラリアの既知のBRCA1またはBRCA2の病原性多様体キャリアにおいてリスク低減のための両側または対側乳房切除術が実施された47症例では、手術時に3個(6%)のがんが発見された。[ 77 ]一般に、RRM標本の病理組織所見は管理に影響しない。
利用
非罹患女性のRRMおよび片側乳がん女性におけるCRRMに関する意思決定においては、個人の心理学的要因が重要な役割を担っている。(BRCAキャリアにおけるRRMの受診に関する情報については本要約の遺伝性乳がんおよび卵巣がん症候群における心理社会的問題のセクションの遺伝性乳がんおよび卵巣がんに対するがんリスク管理の心理社会的側面のセクションを、RRMの心理社会的アウトカムに関する情報については心理社会的アウトカム研究のセクションを参照のこと。)
結論
要約すると:
リスク低減のための卵管-卵巣摘出術(RRSO)
一般集団において、両卵巣の切除は、出産歴、体重および人工閉経時の年齢にも依存して、最高75%までの乳がんリスクの低下と関連する。(詳しい情報については、乳がんの予防に関するPDQ要約を参照のこと。)家系的リスクのレベルがさまざまな女性680人を対象にしたMayo Clinicの研究では、両側卵巣摘出術を受けた60歳未満の女性における乳がん発症の可能性はすべてのリスクグループで低下した。[ 78 ]しかしながら、卵巣切除は、のぼせ、睡眠障害、膣の乾燥、性交痛、骨粗鬆症および心疾患のリスク増大などの重要な副作用を伴っている。卵巣切除の有害作用を打ち消すためには、さまざまな戦略が必要となる可能性がある。
乳がんに対するRRSOの効果に関するエビデンスが現れつつある。早期の小規模な研究で予防効果が示唆された。初期のレトロスペクティブ研究によって、BRCA病原性多様体が陽性の女性におけるRRSO後の乳がんおよび卵巣がんのリスク低下が裏付けられた。[ 79 ]初期の小規模な研究[ 80 ][ 81 ]を支持して、疾患関連のBRCA1またはBRCA2の多様体を有する女性551人を対象として実施されたレトロスペクティブ研究では、RRSO後に乳がんリスク(HR、0.47;95%CI、0.29-0.77)および卵巣がんリスク(HR、0.04;95%CI、0.01-0.16)が有意に減少したことが明らかになった。[ 79 ]BRCA1またはBRCA2の病原性多様体を有する女性170人を対象とした単一施設のプロスペクティブ研究でも同様な傾向が示された。RRSOが施行された場合のHRは、卵巣がん、卵管がん、または原発性腹膜がんで0.15(95%CI、0.02-1.31)、乳がんで0.32(95%CI、0.08-1.2)であった;いずれかのがんに関するHRは0.25(95%CI、0.08-0.74)であった。[ 82 ]1,079人の女性を対象とした多施設プロスペクティブ研究によると、追跡期間中央値30~35ヵ月で、RRSOはBRCA1およびBRCA2病原性多様体キャリアのいずれにおいても乳がんリスクの低下と関連していたが、このリスク低下はBRCA2キャリアの方に顕著にみられることが明らかになった(HR、0.28;95%CI、0.08-0.92)。[ 6 ]BRCA1/BRCA2病原性多様体キャリアにおけるRRSOと乳がんおよび卵巣/卵管がんのすべての報告を対象としたメタアナリシスでは、RRSOが乳がんリスクにおける有意な低下と関連することが確認された(全体:HR、0.49;95%CI、0.37-0.65;BRCA1:HR、0.47;95%CI、0.35-0.64;BRCA2:HR、0.47;95%CI、0.26-0.84)。[ 83 ]しかしながら、キャリアのスクリーニングが全国的に行われるオランダで施行されたBRCA1/BRCA2病原性多様体キャリア822人を対象としたコホート研究では、RRSO後の乳がんリスクの低下は認められなかった(HR、1.09;95%CI、0.67-1.77)。[ 84 ]著者らは、以前の所見はがん誘発性の検査バイアスおよび無イベント人時間などの方法論的問題により導かれたと主張し、この点を、独自のコホートを用い、以前の研究からの人時間の計数と同じ前提を適用することで経験的に評価した。[ 84 ]これに対し、米国の諸研究の研究者らがこのオランダの研究の前提を使用して自分たちのデータを分析したが、なおもRRSOと乳がんリスク間に逆の相関を認めている。[ 85 ]女性676人を対象にしたレトロスペクティブ・コホートでは、乳がん診断時にRRSOを受けたキャリアは乳がん特異的死亡のリスクが低下した(BRCA1キャリアについてHR、0.38;95%CI、0.19-0.77およびBRCA2キャリアについてHR、0.57;95%CI、0.23-1.43)。[ 86 ]その後のBRCA1およびBRCA2キャリア3,722人を対象に同様な手法を用いた国際多施設共同研究では、50歳前に卵巣摘出術を受けると乳がん予防に有益なことがBRCA2キャリア(HR、0.18;95%CI、0.05-0.63;P = 0.007)で示されたが、BRCA1キャリアでは確認されなかった。[ 87 ]これらの相反する結果を考慮して、Prospective Family Study Cohortに組み入れられた女性17,917人の追加コホートについて評価したところ、乳がんと診断された女性は1,046人で、追跡期間中央値は10.7年であった;RRSOと乳がんとの間に関連性は認められなかった。[ 88 ]
BRCA1/BRCA2病原性多様体キャリア2,482人を対象としたプロスペクティブ多施設コホート研究では、全原因死亡率(HR、0.40;95%CI、0.26-0.61)、乳がん特異的死亡率(HR、0.44;95%CI、0.26-0.76)、および卵巣がん特異的死亡率(HR、0.21;95%CI、0.06-0.80)の低下とRRSOが関連することも報告されている。[ 2 ]その後のメタアナリシスにより、乳がんの個人歴ありなしを含めて、BRCA1およびBRCA2病原性多様体キャリアで、全原因死亡に対するRRSOの効果が確認された(HR、0.32;95%CI、0.27-0.38)。[ 89 ]
既存の文献におけるRRSOと乳がんリスクに関する所見には不一致があるにも関わらず、集計データは有益性が存在することを示唆しているが、この有益性の程度は十分に理解されていない可能性がある。このような所見を確認するためには、さらなるプロスペクティブ研究が必要である。
証拠レベル:3ai
BRCA病原性多様体キャリアにおけるRRSOの卵巣がんへの効果に関する詳しい情報については、本要約の卵巣がんのセクションにあるRRSOのセクションを参照のこと。
化学予防
タモキシフェン
タモキシフェン(合成抗エストロゲン薬)は、乳房細胞増殖抑制因子を増加させ、同時に乳房細胞刺激因子を減少させる。National Surgical Adjuvant Breast and Bowel Project Breast Cancer Prevention Trial(NSABP-P-1)はプロスペクティブ・ランダム化二重盲検試験であり、高リスクの女性(1.66を上回るゲイルモデルリスクスコア、60歳を上回る年齢、または非浸潤性[in situ]小葉がん)を対象に5年間にわたりタモキシフェン(20mg/日)とプラセボが比較された。タモキシフェンは、浸潤性乳がんのリスクを49%減少させた。予防効果は、ほとんどがER陽性の乳がんに限定され、この場合のリスク減少は69%であった。ER陰性がんの発生率では、統計的に有意な減少はみられなかった。[ 90 ]前浸潤性乳がんリスクでも、同じように低下が認められたとの報告がある。乳がん家族歴のある女性でも家族歴のない女性でも、乳がんリスクの減少が認められた。50歳以上の女性では、子宮内膜がんおよび血栓性病変の発生率増大が認められた。ヨーロッパで実施されたタモキシフェン予防研究2件から得られた中間データは、それぞれ追跡調査の中央値48ヵ月後[ 91 ]または70ヵ月後[ 92 ]に、タモキシフェンによる乳がんリスク低下を示さなかった。しかしながら、1件の試験では、ホルモン補充療法(HRT)も受けていたサブグループに乳がんリスクの低下が認められた。[ 91 ]これらの試験は、研究デザインまたは集団がかなり異なっていた。(詳しい情報については、乳がんの予防に関するPDQ要約を参照のこと。)
その後、International Breast Cancer Intervention Study 1(IBIS-1)乳がん予防試験では、35~70歳の女性7,154人が5年間のタモキシフェン投与を受ける群かプラセボ群のいずれかにランダムに割り付けられた。この試験に対する適格性は、家族歴または異常な良性乳房疾患に基づいていた。追跡期間中央値16年の時点で、タモキシフェン群の乳がんリスクに29%の低下が認められた(HR、0.71;95%CI、0.60-0.83)。浸潤性ER陽性乳がん(HR、0.66;95%CI、0.54-0.81)のリスクが43%低下し、DCISのリスクが35%低下した(HR、0.65;95%CI、0.43-1.00)。浸潤性ER陰性乳がんのリスクには低下がみられなかった。[ 93 ]これらの知見は、Breast Cancer Prevention Trial(P-1)の結果を裏付けている。[ 90 ]
証拠レベル(高リスク集団におけるタモキシフェン):1aii
NSABP-P-1試験のサブスタディでは、35歳を過ぎたBRCA1/BRCA2病原性多様体キャリアを対象に、乳がん予防におけるタモキシフェンの有効性が評価された。BRCA2陽性の女性では、タモキシフェンにより、BRCA1/BRCA2病原性多様体陰性の参加者と同程度の有益性が得られた;しかしながら、BRCA1病原性多様体を有する健康な女性にタモキシフェンを使用しても、乳がん発生率は減少しないようであった。標本とした病原性多様体キャリアが少数(BRCA1キャリア8人、BRCA2キャリア11人)であるため、これらデータの取り扱いには注意を要する。[ 94 ]
証拠レベル:1aii
BRCA1およびBRCA2病原性多様体キャリアにおいてタモキシフェンを用いた一次予防に関するデータは非常に限られているのとは対照的に、対側乳がんリスクに対するタモキシフェンの予防効果はいくつかの研究により明らかにされている。[ 95 ][ 96 ][ 97 ]BRCA1/BRCA2病原性多様体キャリアを約600人含む研究が1件あり、タモキシフェンの使用に関連して、対側乳がんに51%の減少が認められた。[ 95 ]この報告の最新情報では、両側乳がんを有するBRCA1/BRCA2病原性多様体キャリア285人および片側乳がんを有するBRCA1/BRCA2病原性多様体キャリア751人(これらの患者の40%は最初の研究に含まれていた)について調査が行われた。タモキシフェンは、BRCA1病原性多様体キャリアにおける対側乳がんリスクの50%の減少、BRCA2病原性多様体キャリアにおける58%の減少と関連していた。タモキシフェンは卵巣摘出術を受けていた女性には利益をもたらさなかったようであるが、このサブグループの数はかなり少数であった。[ 97 ]BRCA1/BRCA2病原性多様体キャリア160人を含む別の研究により、腫瘤摘出術と放射線療法による乳がん治療の後にタモキシフェンを使用することで、対側乳がんリスクが69%低下することが明らかになった。[ 96 ]別の研究で、3つの家系コホートから、乳がんの個人歴を有するBRCA1/BRCA2病原性多様体キャリア2,464人が特定された。レトロスペクティブ・データおよびプロスペクティブ・データを用いると、診断後にタモキシフェンによる補助療法を受けた女性では、対側乳がんのリスクが有意に低下することを研究者らは見出した。研究者らが診断時年齢および初発がんにおけるER状態について調整した後も、この関係は持続した。この研究の主要な限界は、女性の56%で初発乳がんのER状態に関する情報が欠けていたことである。[ 98 ]これらの研究は、レトロスペクティブなケースコントロールデザインである上に、原発腫瘍のER状態に関する情報が欠けていることから限界がある。
STAR試験(NSABP-P-2)には19,000人以上の女性が参加し、浸潤性乳がんのリスク減少について5年間のラロキシフェンがタモキシフェンと比較された。[ 99 ]平均3.9年間の追跡で、浸潤性乳がんの発生率における差は認められなかった;しかしながら、非浸潤がんはタモキシフェン群の方が少なかった。血栓塞栓性イベントの発生率および子宮摘出術件数はラロキシフェン群の方が有意に低かった。QOLの詳細なデータはこの2群間の差がわずかであることを示している。[ 100 ]BRCA1またはBRCA2病原性多様体キャリアにおける効力に関するデータは提供されていない。(閉経後女性を含む一般集団における選択的ERモジュレータおよびアロマターゼ阻害薬の使用に関する情報については、乳がんの予防に関するPDQ要約を参照のこと。)
両側乳がんを有する女性を確認することで同定された病原性多様体キャリアおよび非キャリアを対象とした別のケースコントロール研究では、病原性多様体キャリアにおいて全身補助化学療法によりCBCリスクが低下したことが明らかになった(RR、0.5;95%CI、0.2-1.0)。タモキシフェンは有意ではないリスク減少と関連していた(RR、0.7;95%CI、0.3-1.8)。非キャリアでも同様なリスク減少がみられた;しかしながら、キャリアの方がCBCの絶対リスクが高いことを考えると、リスク減少における補助療法の効果も大きい可能性がある。[ 101 ]
BRCA1病原性多様体キャリア714人においてタモキシフェンの卵巣がんリスクに対する影響が検討された。すべての被験者に乳がんの既往歴があった;タモキシフェンの使用とその後の卵巣がんのリスク増加との関連は認められなかった(オッズ比[OR]、0.78;95%CI、0.46-1.33)。[ 102 ]
生殖因子
一般集団では、初潮が早いほど、および閉経が遅いほど、乳がんリスクは増大し、第1子を満期出産する年齢が低いと、そのリスクは低下する。(詳しい情報については、乳がんの予防に関するPDQ要約を参照のこと。)Nurses'Health studyにより、こういったことは、乳がんに罹患している母親または姉妹がいない女性では危険因子であった。[ 103 ]乳がんの家族歴のある女性では、何歳で妊娠しても妊娠は乳がんリスクと関連するらしく、リスクは年齢70歳まで持続するようである。
1件の研究は、BRCA1の高リスク病原性多様体の女性キャリア333人のリスク修飾因子について評価した。既知のBRCA1遺伝子の病原性多様体を保有する女性では、第1子出産年齢が低く、3人以上出産している場合の乳がんリスクは低かった。出産回数が増え、5回以上になる場合、1回増えるごとのRRは0.85であると推定された;しかしながら、出産回数が増えると、卵巣がんリスクが増大するようであった。[ 104 ][ 105 ]ニュージーランドで実施されたケースコントロール研究では、出産が乳がんリスクに及ぼす影響に関しては、乳がん家族歴のある女性と乳がん家族歴のない女性との間には差は認められなかった。[ 106 ]
乳がんリスクに対する妊娠の影響に関する研究では複雑な結果が示されており、経産との関係は一貫しておらず、BRCA1およびBRCA2病原性多様体キャリア間で異なることがある。[ 107 ][ 108 ][ 109 ]経産は、BRCA1病原性多様体キャリアにおいて、乳がんリスクの低下とより一貫して関連している。[ 107 ][ 108 ][ 109 ][ 110 ][ 111 ]注目すべきことに、治療的流産も自然流産も乳がんリスクの増加とは関連していないようである。[ 109 ][ 112 ]
証拠レベル:4aii
多数の疫学研究を対象にした1件の大規模共同再解析を含め、少数の研究によると、一般集団において授乳は乳がんリスクのわずかな減少と関連しており[ 113 ]、また、少なくとも1件の研究によると、授乳はBRCA1病原性多様体キャリアにおいて予防効果があることが示唆される。複数症例家族から抽出した、乳がんをもつBRCA1病原性多様体キャリア685人および乳がんをもつBRCA2病原性多様体キャリア280人と、乳がんをもたないキャリア965人の多施設ケースコントロール研究によると、BRCA1病原性多様体キャリアでは、1年以上の授乳が乳がんリスクの約45%の減少と関連していた。[ 114 ]BRCA2病原性多様体のキャリアにおいては、そのようなリスクの低下はみられなかった。第二の研究ではこの関連を確認できなかった。[ 112 ]
経口避妊薬
経口避妊薬(OC)の使用により、一般集団における乳がんリスクが増加するという一貫した証拠はない。[ 115 ](詳しい情報については、乳がんの予防に関するPDQ要約を参照のこと。)
数件の比較的小規模な研究では、BRCA1/BRCA2病原性多様体キャリアの経口避妊薬の使用による乳がんリスクのわずかな増加が報告されている[ 116 ][ 117 ]が、1件のメタアナリシスにより、最近の経口避妊薬製剤については使用に伴うリスクは有意ではないと結論付けられた。[ 118 ]しかしながら、1975年以前に製造された経口避妊薬は、乳がんリスクの増加と関係していた。[ 118 ]このメタアナリシスのベースとなった患者の大部分は、表12に要約した3件の大規模研究から抽出されたものである。[ 119 ][ 120 ][ 121 ]
表12.BRCA1/BRCA2病原性多様体キャリアにおける経口避妊薬(OC)の使用と乳がんリスク Kotsopoulos et al.(2014) Brohet et al.(2007) Haile et al.(2006) Narod et al.(2002) CI = 信頼区間。 aリスクの推定値をオッズ比で示し、95%CIとともに報告している。 bリスクの推定値をハザード比で示し、95%CIとともに報告している。 cリスクの推定値は40歳未満のBRCA病原性多様体キャリアに限定している。 研究集団 乳がんのBRCA1キャリア N = 2,492 N = 597 N = 195;50歳未満での診断 N = 981 乳がんのBRCA2キャリア 該当せず N = 249 N = 128;50歳未満での診断 N = 330 OC使用経験 BRCA1 1.18 [CI、1.03-1.36]P = 0.02 1.47 [CI、1.13-1.91] 0.64 [CI、0.35-1.16] 1.38 [CI、1.11-1.72]P = 0.003 BRCA2 該当せず 1.49 [CI、0.8-2.7] 1.29 [CI、0.61-2.76] 0.94 [CI、0.72-1.24] 20歳未満での使用 BRCA1 1.45 [CI、1.20-1.75]P = 0.0001 1.41 [CI、0.99-2.01] 0.84 [CI、0.45-1.55] 1.36 [Cl、1.11-1.67]P = 0.003 BRCA2 該当せず 1.25 [CI、0.57-2.74] 1.64 [CI、0.77-3.46] 報告されなかった 全使用期間 BRCA1 5年未満:1.14 [CI、0.97-1.35] 9年未満:1.51 [CI、1.1-2.08] 5年未満:0.61 [CI、0.31-1.17] 10年未満:1.36 [Cl、1.11-1.67]P = 0.003 5年超:1.22 [CI、1.04-1.49]P = 0.02 BRCA2 該当せず 9年未満:2.27 [CI、1.1-4.65] 5年未満:0.79 [CI、0.26-2.37] 10年未満:0.82 [CI、0.56-1.91] 満期出産前の使用 BRCA1 該当せず 4年超:1.49 [CI、1.05-2.11] 4年超:0.69 [CI、0.41-1.16] 評価されなかった BRCA2 該当せず 4年超:2.58 [CI、1.21-5.49] 4年超:2.08 [CI、1.02-4.25] 1年間の傾向:1.11;傾向性のP = 0.01 避妊の選択肢および避妊方法について患者にカウンセリングを行う場合、経口避妊薬の使用による乳がんおよび卵巣がんのリスクに対する潜在的影響、ならびに経口避妊薬による他の健康に関連する影響について考慮する必要がある。BRCA1またはBRCA2病原性多様体キャリア間で考えられる相違、曝露年齢と曝露期間の影響、浸透度の高い早発型乳がんの家系に対する経口避妊薬の影響など、多くの重要な問題が依然として未解決である。
証拠レベル:3aii
(経口避妊薬の使用とこの集団における卵巣がんに関する考察については、本要約の化学予防のセクションにある経口避妊薬のセクションを参照のこと。)
ホルモン補充療法(HRT)
観察研究およびランダム化臨床試験のデータはともに、一般集団において、HRTと乳がんリスクの増加との間に関連があることを示唆している。[ 123 ][ 124 ][ 125 ][ 126 ]閉経後の女性約160,000人についてのランダム化比較試験であるWomen's Health Initiative(WHI)は、心疾患、乳がん、大腸がん、骨折の発生を減らすための食事介入とホルモン療法のリスクと便益を調査した。16,000人以上の女性を併用ホルモン療法かプラセボ投与のいずれかにランダムに割り付けたこの研究で、エストロゲン + プロゲスチン群は、健康上のリスクが有益性を上回ったために早期に打ち切られた。[ 125 ][ 126 ]中止を促した有害な転帰の1つは、エストロゲン + プロゲスチン群にランダムに割り付けられた女性で全乳がん(245 vs 185症例)および浸潤性乳がん(199 vs 150)のいずれにも有意な増加が認められたことであった(RR、1.24;95%CI、1.02-1.50;P < 0.001)。[ 126 ]追跡研究の結果から、特に50~69歳の女性における最近の乳がん発生率の低下は主に、エストロゲン + プロゲスチンHRTの併用の減少と関係していることが示唆されている。[ 127 ]HRT関連乳がんは、プラセボ群に発生したがんに比べ、有害な予後を示す特徴(より進行した病期およびより大きな腫瘍)をもち、またHRTはマンモグラムの異常がかなり多いこととも関連した。[ 126 ]
閉経後HRTによる乳がんリスクは、乳がん家族歴によって増大するという報告もあれば[ 128 ][ 129 ][ 130 ]、乳がん家族歴の影響を受けないという報告もある[ 104 ][ 131 ][ 132 ];メタアナリシスでは、リスクは家族歴によって変化しなかった。[ 115 ]WHI研究では、乳がんの家族歴に関して層別化した解析が報告されておらず、被験者はBRCA1/BRCA2病原性多様体について系統的に検査されていなかった。[ 126 ]一般集団では、更年期症状の治療のために短期間ホルモン剤を服用しても、乳がんリスクはほとんど変わらないか、または全く変わらないようである。[ 133 ]
BRCA1/BRCA2病原性多様体キャリアにおけるHRT
BRCA1またはBRCA2の病原性多様体キャリアにおける乳がんリスクに対するHRTの影響について、2件の研究が調べている。BRCA1またはBRCA2の病原性多様体キャリア462人を対象としたプロスペクティブ研究によると、両側RRSO(n = 155)を受けることで、全体的な乳がんリスクが有意に低下した(HR、0.40;95%CI、0.18-0.92)。比較群として両側RRSOまたはHRTを受けていない病原性多様体キャリアを用いると、HRTの使用(n = 93)によって、両側RRSOに関連する乳がんリスクの低下に有意な変化は認められなかった(HR、0.37;95%CI、0.14-0.96)。[ 134 ]BRCA1病原性多様体をもつ472人の閉経後の女性に関する1件のマッチさせたケースコントロール研究では、HRTの使用は乳がんリスクの全体的な低減と関連した(OR、0.58;95%CI、0.35-0.96;P = 0.03)。両側卵巣摘出術を受けた女性および受けていない女性の両方において、有意ではないリスク低減が観察された。エストロゲンのみを使用している女性ではORが0.51(95%CI、0.27-0.98;P = 0.04)であったが、エストロゲンとプロゲステロンとの関連性は統計的に有意ではなかった(OR、0.66;95%CI、0.34-1.27;P = 0.21)。[ 135 ]がんの個人歴がありBRCA1病原性多様体を有する閉経後女性とそれにマッチさせた432ペアを対象としたケースコントロール研究で、非罹患BRCA1キャリアと比較された。HRTの使用は、乳がん発症リスクの増加と関係しなかった(OR、0.80;P = 0.24)。[ 136 ]特に、観察研究とWHIとの間で推定したHRT関連リスクにおいて差があるため、これらの知見はランダム化プロスペクティブ研究で確認されるべきであるが[ 137 ]、BRCA1/BRCA2病原性多様体キャリアにおけるHRTは乳がんリスクも上昇させず、また卵巣摘出術の予防効果も打ち消さないことが示唆されている。
証拠レベル:3aii
卵巣がん
スクリーニング/サーベイランス
一般集団におけるスクリーニングに関する情報については、卵巣がん、卵管がん、原発性腹膜がんのスクリーニングに関するPDQ要約を参照のこと、さらに、スクリーニングおよび予防に関連する証拠レベルに関する情報については、PDQ要約のがん遺伝学研究に関する証拠レベルを参照のこと。後者では、特定の医学的状態に対してルーチンの医療行為の一環としてスクリーニングが適切であると考える前に、5つの要件を満たさねばならないことも概説している。
診察
一般集団における卵巣の診察は、早期卵巣がんを確実に同定するための特異度や感度をもってない。卵巣がんの遺伝性リスクを有する女性において、卵巣の診察(双合診)の有益性に関するデータは得られていない。
証拠レベル:指定なし
経膣超音波検査
一般集団では、付属器腫瘤の術前診断において、腹式超音波検査よりも経膣超音波検査(TVUS)の方が優れているようである。いずれの手法でも、閉経前の卵巣では月経周期の変化(例えば、一過性の黄体嚢胞)により解釈が難しくなる可能性があるため、閉経前女性では閉経後女性より特異度が低くなる。プロスペクティブ・ランダム化試験、Prostate, Lung, Colorectal, and Ovarian Cancer Screening Trial(PLCO-1)では、卵巣がんリスクが一般集団レベルにある無症状の閉経後女性のスクリーニングで、TVUSとがん抗原125(CA-125)が年1回併用されたが、死亡率の低下は認められなかった。[ 138 ]
卵巣がんの遺伝性リスクを有する女性のスクリーニングにおける、TVUSの潜在的有益性に関するデータは限られている。多数のレトロスペクティブ研究により、高リスク女性においてCA-125を併用するまたは併用しないTVUSを使用した卵巣がんスクリーニングの経験が報告されている。[ 9 ][ 139 ][ 140 ][ 141 ][ 142 ][ 143 ][ 144 ][ 145 ][ 146 ][ 147 ][ 148 ][ 149 ]しかしながら、高リスクの基準の定義およびスクリーニングの実施に対するコンプライアンス、および検出されたがんが発生症例か、有病症例かについては統一性がほとんどない。報告された最大規模の研究の1つには、TVUSおよびCA-125による年1回のスクリーニングを受けたBRCA1/BRCA2病原性多様体キャリア888人が含まれていた。10人の女性が卵巣がんを発症し;この10人中5人は、診断前の3~10ヵ月以内に実施したスクリーニングでは結果が正常で、その後中間期がんを発症した。卵巣がんの10人中5人はスクリーニングで検出された発生症例であり、診断前の6~14ヵ月以内にスクリーニング結果が正常であった。これらの5例中、4例はIIIB期またはIV期であった。[ 139 ]
同様の研究で、高リスクの女性312人(152人がBRCA1/BRCA2病原性多様体キャリア)からなるコホートを対象に、年1回のTVUSおよびCA-125の結果が報告された。[ 141 ]TVUSおよびCA-125が異常であるために検出された4つのがんについて、4人の患者すべてに症状が認められ、3人の患者が進行期疾患を有した。オランダの研究で、BRCA1/BRCA2病原性多様体キャリアを対象にした骨盤内超音波、TVUS、およびCA-125による年1回のスクリーニングでは、BRCA1/BRCA2病原性多様体キャリア241人で早期の卵巣がんを検出できなかった。[ 150 ]研究期間中に3例のがんが発見されたが、すべて進行IIIC期疾患であった。[ 150 ]最後に、年1回のTVUSおよびCA-125を受けた中等度のリスクおよび高リスク女性1,100人を対象にした1件の研究の報告では、卵巣腫瘍13例中10例がスクリーニングで検出された。I期またはII期であったのは10例中わずか5例であった。[ 140 ]TVUSおよびCA-125による半年ごとのスクリーニングの有効性に関するデータは限られている。[ 9 ][ 148 ]
United Kingdom Familial Ovarian Cancer Screening Studyでは、卵巣がんの生涯リスクが10%以上と推定された女性3,563人に対して年1回の超音波検査と血清CA-125測定によるスクリーニングを平均3.2年にわたって施行した。スクリーニングで発見されたがん13例中4例が、I期またはII期であった。前年にスクリーニングを受けた女性は、IIIC期より高い病期のがんを有する可能性が低かった;また、最適な腫瘍細胞縮小が得られる率が良好でOSが高い傾向がみられた。さらに、ほとんどのがんは既知の卵巣がん感受性遺伝子を有する女性に発生していたことから、これらの女性はスクリーニングを考慮する上でがんリスクの最も高いコホートと考えられる。[ 151 ]この研究の第II相試験では、スクリーニングの頻度が4ヵ月ごとに増やされたが、これによる影響はまだ報告されていない。
主要アウトカムとして生存率を用いたTVUSおよびCA-125に関する最初のプロスペクティブ研究が2009年に完了した。スクーリングを受けた高リスク女性3,532人中、981人がBRCA病原性多様体キャリアで、そのうち49人が卵巣がんを発症した。5年および10年生存率はそれぞれ58.6%(95%CI、50.9%-66.3%)および36%(95%CI、27-45)で、キャリアと非キャリア間で生存に差はみられなかった。この研究の主な制限は対照群がなかったことである。制限にもかかわらず、この研究では、TVUSおよびCA-125値による年1回のサーベイランスは実質的に生存に影響するほど早期の段階で腫瘍を検出するには有効ではないようであると示唆されている。[ 152 ]
証拠レベル:4
血清CA-125
今までのセクションで述べたように、高リスク女性における卵巣がんに対する血清CA-125スクリーニングが、多くのレトロスペクティブ研究においてTVUSとの併用で評価されている。[ 9 ][ 139 ][ 140 ][ 141 ][ 142 ][ 143 ][ 144 ][ 145 ][ 146 ][ 147 ][ 148 ]
米国国立衛生研究所(NIH)の卵巣がんに関する統一見解では、一般集団を対象にした血清CA-125による卵巣がんの定期スクリーニングに反対することを勧告した。(詳しい情報については、卵巣がん、卵管がん、原発性腹膜がんのスクリーニングに関するPDQ要約のProstate, Lung, Colorectal and Ovarian [PLCO] Cancer Screening Trial:単一閾値のCA-125値およびTVUのセクションを参照のこと。)しかしながら、NIHの統一見解(Consensus Statement)では、卵巣がんの遺伝性リスクを有する女性は35歳で開始する6~12ヵ月ごとのTVUSおよび血清CA-125値によるスクリーニングを受けるよう勧告している。[ 153 ]がん遺伝学研究協会(Cancer Genetic Studies Consortium)の作業部会では、BRCA1病原性多様体の女性キャリアは年齢25歳~35歳でTVUSおよび血清CA-125値による年1回または半年に1回のスクリーニングを受け始めるよう推奨している。[ 11 ]いずれの推奨も、専門家の意見および最良の臨床判断だけに基づいている。
証拠レベル:5
他の候補となる卵巣がんバイオマーカー
効果的な卵巣がんスクリーニングの必要性は、特にBRCA1およびBRCA2の病原性多様体およびミスマッチ修復(MMR)遺伝子(例、MLH1、MSH2、MSH6、PMS2)の多様体を保有する女性、卵巣がんのリスクが高い障害を有する女性では重要である。BRCA1病原性多様体キャリアでは、卵巣がんの累積生涯リスクが40%を超える場合があり、特に切迫感がある。
したがって、多くの新たな卵巣がんバイオマーカー(単独または組み合わせて)が今後5年~10年の間に卵巣がんのスクリーニング戦略として提案されると期待されている。これは活発に研究が行われている領域で、多くの有望な新しいバイオマーカーが開発初期にあるが、一般集団または遺伝的リスクの高い女性のいずれにおいても、現時点では、これらのバイオマーカーの単独使用または併用は、十分な研究がなされておらず、スクリーニング目的でルーチンの臨床で使用することは正当化されない。
明らかになりつつある卵巣がんバイオマーカーに関する情報に取り組む前に、新たなバイオマーカーを開発し、さらに重要なことにそのバイオマーカーの妥当性を確認するために必要ないくつかの段階を考慮することが重要である。有用な枠組みの1つは、米国国立がん研究所(NCI)のEarly Detection Research Networkの研究者により発表されたものである。[ 154 ]がんスクリーニングプログラムの目標は、治療が成功する可能性を高めるため腫瘍を早期に検出することであると彼らは指摘した。こうしたプログラムを判定するゴールドスタンダードは、スクリーニングを実施するがんの死亡率がスクリーニングを実施された集団で低下するかどうかである。加えて、スクリーニング検査はスクリーニングが実施される集団で広く使用できるよう十分に侵襲性が低く、安価でなければならない。低い偽陽性率でも、多くの人が不要で高価な診断検査を受け精神的ストレスを経験する必要があるため、高い検査特異度(すなわち、偽陽性の結果がほとんどないこと)を維持することは、集団のスクリーニング検査に必須である。スクリーニング検査の感度と特異度の両方を高くするには、こうしたがんバイオマーカーのいくつかを組み合わせて使用する必要があると考えられる。
さらに、臨床的に有用な検査はPPV(感度、特異度、およびスクリーニングを受ける集団における疾患有病率から得られるパラメータ)が高くなければならない。実際のところ、PPVが10%のバイオマーカーは、1例の卵巣がんを同定するために10回の外科的手技を実施する必要があること;残り9回の手術は偽陽性の検査所見を示すことを意味している。一般的に、卵巣がん研究のコミュニティでは、PPVが10%未満のバイオマーカーは、両側の卵管-卵巣摘出術に関係する合併症を考慮すると臨床では受け入れられないものと考えられている。最後に、新たなバイオマーカーは進行性卵巣がん女性(バイオマーカー開発の初期段階で分析される症例のほとんどを占める)の血清では存在しうる一方で、早期疾患の女性では検出できる場合もあればできない場合もあるが、スクリーニング検査が臨床的に有用であるためには早期で検出できることが必須であるということを心に留めておくことが重要である。
現在、バイオマーカーの開発および妥当性の確認には、以下に示す5つの一般的な段階があると提案されている:
最後に、妥当性が確認されたバイオマーカーの検査を特定の集団に使用するのに適切であるとみなすためには、既知の陽性および陰性が以前に選択されていない特定集団でバイオマーカーを評価する必要がある。さらに、検査では臨床的有用性、つまり検査の適用に関連した有益性とリスクの正の純バランスを実証しなければならない。これらには、健康上のアウトカムの改善とともに、最終的な心理社会的および経済的な有益性が含まれる場合がある。[ 155 ]
卵巣がんには偽陽性検査結果から考えられる影響に関して特有の問題がある。早期疾患に対する非侵襲性の診断検査で信頼性の高いものはなく、臨床的に意義のある早期がんは試験開腹時に肉眼的に見えないことがある。[ 156 ]結果として、検査異常であるが、がんの存在は示されないことが、卵巣および卵管を外科的に切除し、顕微鏡で調べることでのみ再確認される患者がいると考えられる。偽陽性の女性における不必要な手術および早発閉経への誘導を避けるためには、高い検査特異度(すなわち、非常に低い偽陽性率)が必要となる。
CA-125のバリエーション
CA-125値 + 卵巣がんの症状指数
がんの存在を予測するための卵巣がんの症状指数が、症例75人および高リスクの対照254人(BRCA病原性多様体キャリアまたは乳がんおよび卵巣がんの強い家族歴を有する女性)において評価された。[ 157 ]女性は、予め定義された症状(鼓脹または腹部のサイズの増加、腹部痛または骨盤部疼痛、および食べるのが困難または早期満腹感)のいずれかを12ヵ月以内にのみ月12回を超えて報告した場合に症状指数陽性とされた。30 U/mLを超えるCA-125値は、異常と考えられた。症状指数は、CA-125値で調整された後に独立して卵巣がんの存在を予測した(P < 0.05)。CA-125高値および症状指数陽性を併用することで、症例の89.3%が正確に特定された。CA-125高値を示さなかった罹患女性の50%で、症状指数はがんの存在と相関していたが、がんではない高リスク対照の11.8%でも症状指数が陽性であった。CA-125と症状指数の両方を含めた複合指数は、いずれかの検定を単独で用いた場合よりも検出特性が良好であり、この戦略は多段階のスクリーニングプログラムにおける最初のスクリーニング法として使用できることを著者らは提案した。非選択的スクリーニング集団において追加で検査性能の妥当性の確認および臨床的有用性の決定が必要である。
証拠レベル:5
卵巣がんのリスクアルゴリズム
CA-125によるスクリーニングの新たな修正は、CA-125を任意のカットオフ値によって正常または異常に単純に分類するよりも、CA-125値の経時的な上昇により得られる卵巣がんスクリーニングの性能特性の方が優れているのではないかという仮説が基になっている。これは、スクリーニングを受けた被検者に卵巣がんが存在する可能性の推定値を算出する計算に、連続的なCA-125検査結果および他の共変量を組み込む調査の統計モデルである卵巣がんのリスクアルゴリズム(ROCA)の形で実行されている。この戦略の最初の報告では、ストックホルム卵巣がんスクリーニング試験による平均リスクの女性5,550人を対象にした再分析に基づくと、99.7%の感度、83%の特異度、および16%のPPVで卵巣がん症例と対照を識別できることが示唆された。このPPVは、CA-125のみを測定して報告される2%のPPVよりも8倍の増加を示す。[ 158 ]この報告の後に、英国のプロスペクティブ卵巣がんスクリーニング試験において、ROCAが平均リスクの閉経後女性9,233人から得られた33,621の連続的なCA-125値に適用された。[ 159 ]受信者操作曲線下面積は、CA-125を固定したカットオフ値と比較してROCAでは84%から93%(P = 0.01)に増加した。これらの観察は、卵巣がんの臨床前の検出がこのスクリーニング戦略を使用して改善しうるという最初の証拠であった。英国における50歳以上の正常なボランティア13,000人を対象にした1件のプロスペクティブ研究では、連続的なCA-125値およびROCAを使用して参加者を、低リスク、中リスク、および高リスクのサブグループに層別化した。[ 160 ]各グループがそれぞれ規定の管理戦略を有し、これにはTVUSおよび年1回(低リスク)または3ヵ月ごと(中リスク)のCA-125値の反復測定が含まれた。このプロトコルを用いると、ROCAは99.8%の特異度および19%のPPVが得られることが明らかにされた。
英国における2件のプロスペクティブ試験でROCAが使用された。United Kingdom Collaborative Trial of Ovarian Cancer Screening(UKCTOCS)では、通常リスクの女性を対象に、(1)スクリーニングなし、(2)年1回の超音波検査、または(3)複数の方式によるスクリーニングのいずれかにランダムに割り付け(N = 202,638;登録完了;2014年に追跡終了)、U.K. Familial Ovarian Cancer Screening Study(UKFOCSS)では、高リスク女性を対象に評価した(登録完了)。また、米国ではROCAを実施する2件の高リスクコホート研究が評価段階にある:Cancer Genetics Network ROCA Study(N = 2,500;追跡完了;解析中)、およびGynecologic Oncology Group Protocol 199(GOG-0199;登録完了;2011年に追跡終了)。[ 161 ]したがって、この現在研究中のスクリーニング戦略の有用性に関する追加のデータが利用できるようになる。
証拠レベル:4
その他の新たなマーカー
過去10年間に、多彩な新しい卵巣がんバイオマーカー候補が報告されており、例を挙げれば、HE4;メソテリン;カリクレイン6、10、および11;オステオポンチン;プロスタシン;M-CSF;OVX1;リゾホスファチジン酸;血管内皮増殖因子B7-H4;ならびにインターロイキン6および8がある。[ 162 ][ 163 ][ 164 ]これらは単独で、CA-125と組み合わせて、あるいはさまざまな他の順列で研究されている。研究集団のほとんどは比較的小規模で、バイオマーカー開発初期の第1および第2段階で評価されたタイプの厳選された既知の卵巣がん症例および健康な対照からなる。複数の研究で結果は一貫して再現されていない;現在、いずれも広範な臨床適用の準備ができていないと考えられている。
証拠レベル:5
プロテオミクス
当初、血清蛋白の質量分析は卵巣がん症例と対照を判別できる蛋白パターンを同定するために、複雑な解析アルゴリズムと組み合わされた。[ 165 ]このアプローチでは、パターンの認識だけでそうした判別が十分に可能になること、そして同定されたパターンの原因となっている特定の蛋白を同定する必要はないことが想定されていた。この戦略は、同様の検査ツールを用いて、がん早期発見のためにCA-125測定の代わりに、または組み合わせて使用できる限られた数の既知の特異的血清マーカーを同定するために、修正された。[ 166 ]これらの研究[ 164 ][ 167 ]は一般的に、サンプルサイズおよび含まれる早期がんの症例数により制限がある小規模ケースコントロール研究となっている。この方法で同定された追加のマーカーが、関心のある非選択的臨床集団における卵巣がんの早期発見について臨床的有用性を有するかどうかを決定するためにさらなる評価が必要である。
証拠レベル:5
卵巣がんスクリーニングのためのマルチプレックスバイオマーカーアッセイ
個々のバイオマーカーは効果的なスクリーニング検査の基準を満たしていないため、満足のいくスクリーニング検査の結果を得るためには複数の卵巣がんバイオマーカーを組み合わせる必要があると提案されている。この戦略を利用して6つの血清バイオマーカー(レプチン、プロラクチン、オステオポンチン、インスリン様成長因子II、マクロファージ抑制因子、およびCA-125)を定量的に解析するために、複合的な数珠繋ぎのプラットフォーム(multiplex, bead-based platform)が使用された。[ 168 ]同様のアッセイが製造者により市場から自主回収されるまでOvaSureという商品名で市販されていた。[Response to FDA Warning Letter]
この研究の症例は新たに卵巣がんと診断された患者で、手術直前に採血された:36人がI期およびII期;120人がIII期およびIV期であった。対照は健康な年齢でマッチさせた個人で採血の6ヵ月以内に卵巣がんを発症していなかった。この研究の症例も対照も、家系的および/または遺伝的リスク状態に関する特徴解析が不十分であったが、いずれも高リスク集団を含むことが示唆されている。最初に、対照181人および卵巣がん症例113人を検査して、症例と対照を最も良く区別した最初のバイオマーカーパネル(トレーニングセット)が決定された。結果として得られたパネルが、追加の対照181人および卵巣がん症例43人(検査セット)に適用された。トレーニングセットと検査セットを組み合わせた早期および後期卵巣がんの両方をプールしたところ、高度に選択された研究対象集団でみられるように、卵巣がんの有病率を約50%と仮定した公式を用いた検出能力は感度95.3%、特異度99.4%、PPV99.3%、陰性適中率99.2%と報告された。
検査の性能を実際より良いように思わせるバイアスを避けるために、この種の解析でトレーニング集団および検査集団を組み合わせることは、一般に推奨されない。[ 169 ]使用すべき最も適切な有病率は、スクリーニングを実施する非選択的集団における疾患の有病率である。一般集団における卵巣がんの有病率は2,500人に1人である。この文書に対して行われた訂正で[ 168 ]、著者らはスクリーニングを実施した集団における卵巣がんの有病率を1/2,500(0.04%)と想定し、PPVはわずか6.5%であると再計算された。これに基づいて、研究者は、この検査が集団のスクリーニングに適しているという主張を撤回している。この検査が卵巣がんのリスクが高い患者に用いられた場合、そうしたターゲット集団における実際の有病率は一般集団において観察される有病率よりも高いと考えられるが、発表された解析に使用された50%という数字の想定よりはかなり低い。この改訂された6.5%のPPVは、検査が陽性の女性15人中約1人が実際に卵巣がんを有し、I期またはII期であるのは卵巣がんを有する女性のごく一部であることを示している。検査が陽性であった残り14人は偽陽性となり、これらの女性は不必要な不安および両側の卵管-卵巣摘出術を含めた合併症を引き起こす恐れのある診断手順に曝されるリスクがある。
先に述べた基準の背景から判断すると[ 154 ]、このアッセイは開発の第2段階に分類される。これは卵巣がんスクリーニング研究の有望な手段であると思われるが、関心のある臨床的なスクリーニング集団を代表する非選択的集団では特に、妥当性の確認を追加で行う必要がある。このアッセイに関するSociety of Gynecologic Oncologistsの立場表明では、「施設内審査委員会の指揮下で適切なインフォームド・コンセントを得た上で実施された調査研究の状況以外で女性にこの検査を提供する前に、この検査の有効性を確認するために追加の研究が必要であるというのが我々の見解である」と表明された。
証拠レベル:5
リスク低減のための手術
RRSO
多数の研究により、乳がんおよび卵巣がんの遺伝性リスクを有する女性では、RRSOの施行後に卵巣がんリスクが低下することが明らかにされている。(詳しい情報については、本要約の乳がんのセクションのRRSOのセクションを参照のこと。)BRCA1またはBRCA2病原性多様体を有する女性551人を対象としたレトロスペクティブ研究では、両側卵巣摘出術後の乳がんリスク(HR、0.47;95%CI、0.29-0.77)および卵巣がんリスク(HR、0.04;95%CI、0.01-0.16)に有意な低下が明らかになった。[ 79 ]BRCA1またはBRCA2の病原性多様体を有する女性170人を対象とした単一施設プロスペクティブ研究でも同様な傾向が示された。[ 82 ]卵巣摘出術が施行された場合のHRは、卵巣がん、卵管がん、または原発性腹膜がんで0.15(95%CI、0.02-1.31)、乳がんで0.32(95%CI、0.08-1.2)であった;いずれかのがんに関するHRは0.25(95%CI、0.08-0.74)であった。1,079人の女性を対象に中央値で30~35ヵ月追跡した多施設プロスペクティブ研究によると、BRCA1およびBRCA2の病原性多様体キャリアでは、卵巣がんリスクを低減させる上で、RRSOが非常に有効なことが明らかになった。また、この研究により、BRCA1およびBRCA2病原性多様体キャリアでは、いずれもRRSOが乳がんリスクの低下と関連していたことも明らかになった;しかしながら、乳がんリスクの低下はBRCA2キャリアの方に顕著にみられた(HR、0.28;95%CI、0.08-0.92)。[ 6 ]イスラエルのケースコントロール研究では、両側卵巣摘出術が卵巣/腹膜がんリスクの低下と関連していた(OR、0.12;95%CI、0.06-0.24)。[ 170 ]BRCA1/BRCA2病原性多様体キャリアにおけるRRSOと乳がんおよび卵巣/卵管がんのすべての報告を対象としたメタアナリシスにより、RRSOは卵巣がんまたは卵管がんの有意なリスク低下と関連していたことが確認された(HR、0.21;95%CI、0.12-0.39)。また、この研究により、乳がんの有意なリスク低下も明らかになった(全体:HR、0.49;95%CI、0.37-0.65;BRCA1:HR、0.47;95%CI、0.35-0.64;BRCA2:HR、0.47;95%CI、0.26-0.84)。[ 83 ]その後、BRCA1またはBRCA2の病原性多様体を有し、乳がんに罹患しているまたはしていない女性2,854組を対象としたマッチドケースコントロール研究では、外科手術による閉経を経験した女性(OR、0.52;95%CI、0.40-0.66)は、自然閉経を迎えた女性(OR、0.81;95%CI、0.62-1.07)に比べ、乳がんリスクが大幅に低下することが示された。この研究では、自然閉経後に卵巣摘出術を受けた女性の間で乳がんリスクの高度に有意な減少がみられたことも報告されている(OR、0.13;95%CI、0.02-0.54;P = 0.006)。[ 171 ]BRCA1またはBRCA2の病原性多様体を有する女性5,783人を中央値で5.6年追跡した他の研究では、卵巣がん、卵管がん、または腹膜がんのいずれかを発症した女性186人中68人が死亡したことが報告された。両側卵巣切除術に関連したこれらのがんのHRは、0.20(95%CI、0.13-0.30;P = 0.001)であった。がんの既往がないBRCA病原性多様体キャリアでは、卵巣切除術に関連した70歳までの全原因死亡のHRは、0.23(95%CI、0.13-0.39;P < 0.001)であった。[ 7 ]50人以上の被験者を対象にした研究では、有病率が2.3~11%の範囲に及んでいた。こうした有病率の変動は、手術法、組織の病理学的処置、およびRRSO時の年齢における違いが原因となっている可能性が高い。GOG 199研究の高リスク女性966人では、潜伏がん発生率がBRCA1病原性多様体キャリアで最も高く(4.6%)、次いでBRCA2病原性多様体キャリアで高く(3.5%)、非キャリアでは0.5%に過ぎなかった。潜伏病理所見のオッズは、閉経後女性で4倍に上昇した。[ 172 ]
RRSOによって、卵巣がんおよび乳がんのリスク低下に加えて、OS率および乳がんと卵巣がん特異的生存率も有意に改善している可能性がある。BRCA1およびBRCA2の生殖細胞病原性多様体を有する女性666人を対象としたプロスペクティブ・コホート研究で、RRSOを受けた女性では、同手術を受けなかった女性と比較した場合の全死亡のHRが0.24(95%CI、0.08-0.71)であった。[ 173 ]この研究結果は、RRSOを受けた女性における生存の優位性を示唆する初めての証拠となった。
RRSOによるリスク低下の程度に関する研究により、手術時に発見される潜伏がんのスペクトラムの解明が始まっている。原発性卵管がん、原発性腹膜がん、不顕性卵巣がんのすべてが報告されている。数件のケースシリーズで、リスク低減のための卵巣摘出術を受けた病原性多様体キャリアにおける悪性所見の有病率が報告されている。50人以上の被験者を対象にした研究では、有病率が2.3~11%の範囲に及んでいた。[ 9 ][ 82 ][ 174 ][ 175 ][ 176 ][ 177 ][ 178 ][ 179 ][ 180 ]こうした有病率の変動はおそらく、手術法、組織の病理学的処置、およびRRSO時の年齢における違いによるものであろう。GOG 199研究の高リスク女性966人では、潜伏がん発生率がBRCA1病原性多様体キャリアで最も高く(4.6%)、次いでBRCA2病原性多様体キャリアで高く(3.5%)、非キャリアでは0.5%に過ぎなかった。潜伏病理所見のオッズは、閉経後女性で4倍に上昇した。[ 172 ]
潜伏がんに加えて、予防のために切除された卵管組織において前悪性病変も報告されている。リスク低減のための手術を受けたBRCA1病原性多様体を有する女性12人の1件のシリーズでは、卵管上皮に11個の過形成または異形成病変が同定された。これらの症例のいくつかは、多病変であった。[ 181 ]このような病理所見は、卵管がんおよび原発腹膜がんの両方に罹患した女性におけるBRCA1およびBRCA2生殖細胞病原性多様体の同定と一致している。[ 178 ][ 182 ][ 183 ][ 184 ][ 185 ][ 186 ][ 187 ]1件の研究で、早期卵管がん、または卵管上皮内がんとその後の卵管、卵巣、または腹膜の浸潤性漿液性がん(invasive serous carcinoma)との間の因果関係が示唆されている。[ 188 ](詳しい情報については、本要約の卵巣がんの病理学のセクションを参照のこと。)
これらの知見から、一般集団における全婦人科がんの1%未満である卵管がんを、遺伝性卵巣がん症候群の仲間に加えることが支持され、リスク低減のための手術時に卵管の切除が必要となる。RRSOでは、ルーチンで腹膜洗浄液を採取する必要性、および連続切片法を用いた全付属器の総合的な病理学的評価を慎重に遵守する必要性があることを示す明確な証拠がある。[ 180 ][ 189 ][ 190 ]
しかしながら、卵巣摘出術後でも、腹膜にはミュラー管型腺がんが発生するリスクがわずかに残っていると考えられる。[ 191 ][ 192 ][ 193 ][ 194 ][ 195 ]リスク低減のための卵巣摘出術を受けたGilda Radner Familial Ovarian Cancer Registryに登録されている女性患者324人のうちの6例(1.8%)に、その後原発性のがん性腹膜炎が発生した。追跡調査期間は特定されなかった。[ 196 ]Creighton Registryに登録されている患者で、BRCA1/BRCA2病原性多様体を有し、リスク低減のための卵巣摘出術を受けた女性238人のうち5人(2.1%)が、その後に腹腔内がん腫症を発症した。注目すべきことは、これらの女性の5人全員にBRCA1病原性多様体が認められたことである。[ 197 ]BRCA1またはBRCA2の病原性多様体を有する女性1,828人を対象にした研究では、RRSO施行20年後の原発性腹膜がんのリスクが4.3%であったことが示された。[ 198 ]
RRSO時に潜伏病変を有することが明らかになるBRCA1およびBRCA2病原性多様体キャリアの転帰に関するデータは限られている。浸潤がん(n = 15)または漿液性卵管上皮内がん(STIC)(n = 17)のいずれかを有する女性32人を対象にした1件の多施設研究では、浸潤がんを有する女性の47%が中央値32.5ヵ月の時点で再発し、OS率は73%であった。[ 199 ]上皮内病変を有する女性では、患者の1人(約6%)が43ヵ月時に再発し、2つの疾患実体間で疾患の経過が異なると示唆されている。別の研究でSTIC病変の悪性度が確認された。RRSO時に病理学が良性であった女性243人中3人(1.2%)がその後原発性腹膜がんを発症した一方、STICを有した女性では9人中2人(22%)が追跡期間中央値63ヵ月後に、高悪性度骨盤漿液性がんを発症した。[ 200 ]
卵巣がんに対する現在のスクリーニングには限界があり、BRCA1およびBRCA2病原性多様体キャリアでは卵巣がんのリスクが高いことから、NCCNのガイドラインでは、リスク低減のための有効な選択肢として35~40歳の間に実施する、または出産を終了して間もなく実施するRRSOが推奨されている。RRSOの最適な時期は個別に決定する必要があるが、病原性多様体状態に基づいて、ある女性の卵巣がんリスクを評価することは、意思決定の際に有用な可能性がある。米国のBRCA1およびBRCA2家系を対象にした1件の大規模研究において、40歳での卵巣がんの年齢特異的累積リスクは、BRCA1病原性多様体キャリアで4.7%、BRCA2病原性多様体キャリアで1.9%であった。[ 201 ]BRCA1およびBRCA2病原性多様体キャリアを対象とした22件の研究の併合解析によると、BRCA1病原性多様体キャリアでは、卵巣がんリスクが40歳から50歳にかけて最も急激に増加するのに対し、BRCA2病原性多様体キャリアでは、50歳未満ではリスクが低く、50歳から60歳にかけて急激に上昇する。[ 202 ]卵巣がん患者におけるBRCA病原性多様体の集団ベースの研究において、BRCA2多様体を有する患者は、BRCA1多様体を有する患者よりも発症年齢が有意に遅かった(57.3歳[範囲、40-72] vs 52.6歳[範囲、31-78])。[ 203 ]要約すれば、BRCA1病原性多様体を有する女性は、BRCA2病原性多様体を有する女性よりもいくぶん早い年齢で卵巣がんリスクを低下させるためのRRSOを検討してもよい;しかしながら、BRCA2多様体を有する女性も卵巣がんリスクを低下させるためのRRSOを早期に検討してもよい。
BRCA1/BRCA2病原性多様体キャリアでは、RRSO時点での同時子宮摘出の役割に議論の余地がある。子宮摘出を実施しなかった場合、近位卵管のごく一部が残存し、それにより卵管がんの高いリスクが残存する懸念がある。しかしながら、卵管がんを検討したいくつかの研究によると、これらのがんの大多数が卵管の遠位または中位に発生することが示されており、近位卵管がんの発生はきわめてまれな事象と考えられることが示唆される。病原性多様体キャリアに子宮がんの発生増加を示唆している報告がある一方で[ 204 ]、漿液性子宮がんのリスク増加が確認されなかった報告もある。[ 205 ]女性857人を対象としたプロスペクティブ研究によると、子宮がんの発生増加は、タモキシフェンを使用したBRCA1病原性多様体キャリアにみられることが示唆された[ 206 ];このことは、同じグループにより、BRCA1/BRCA2病原性多様体キャリア4,456人を対象とした後続の研究で確認された。[ 207 ]タモキシフェンを使用した場合でも、子宮内膜がんの過剰リスクは低度で、10年累積リスクは2%であった。[ 207 ]さらに、現在では、ラロキシフェン(子宮がんのリスクを高めるリスクはない)および閉経後女性における乳がん予防のためのアロマターゼ阻害薬の選択肢があることを考えると、タモキシフェンの使用は最小限に抑えることが可能である。したがって、BRCA病原性多様体キャリアにおける子宮がんのリスクに関する現在の理解に基づくと、子宮がんのリスクを低減するために、RRSOの時点で子宮摘出を検討しなければならないというやむを得ない理由は単独では存在しない。ホルモン摂取を選択したBRCA病原性多様体キャリアでは、同時に子宮摘出を実施することで、ホルモン補充レジメンを簡略化する利点が得られることは確かである。子宮摘出後の女性は、エストロゲン(乳がんのリスクを高めることはない)のみを摂取することが可能で、プロゲスチン類は不要なため、閉経後出血のリスクがなくなる。
子宮摘出は、リスクを低減するための手段としては必ずしも必要ないことが諸研究で示されている。子宮内膜がんのユダヤ人女性200人または子宮の乳頭状漿液性がんの非選択女性56人では、BRCA病原性多様体の保有率に増加は認められなかった。[ 205 ][ 208 ]しかしながら、子宮の乳頭状漿液性がんは、BRCA関連疾患群の一部である可能性が、小規模な研究で報告されている。[ 204 ][ 209 ][ 210 ]タモキシフェンによる治療を受けたER陽性乳がんのBRCA病原性多様体キャリアにおける子宮内膜がんの累積リスクは、この集団でリスク低減のための子宮摘出術に関するカウンセリングを実施する際に検討すべきさらなる因子となる可能性がある。[ 206 ][ 211 ]HRTを受けることは望まないが、子宮摘出術ではエストロゲン単独の簡易レジメンが使用されると考えられる若い非罹患のBRCA病原性多様体キャリアでは、子宮摘出術が検討される場合もある。BRCA病原性多様体キャリアを対象にしたリスクを低減するための至適な外科的選択肢に関するカウンセリングでは、RRSO実施後の遺残卵管組織によるリスクは、やむを得ず子宮摘出術を提案する理由としては弱いことが集計データから示唆される。そのため、タモキシフェンを使用していないか、子宮または子宮頸部に他の潜在的問題がない場合、子宮摘出術はBRCAキャリアに対するRRSOのルーチンの構成要素ではない。
手術時に閉経前の女性では、外科手術による閉経の症状(例えば、ほてり、気分変動、体重増加、および尿生殖器の愁訴)は、生活の質がかなり障害される原因となる。これらの症状の影響を低下させるために、医療提供者はしばしば手術後、コースに期限を設けた全身HRTを処方している。(詳しい情報については、本要約のBRCA1/BRCA2病原性多様体キャリアにおけるホルモン補充療法のセクションを参照のこと。)
諸研究では、生活の質(QOL)に対するRRSOの効果が調査されている。1件の研究では、846人の高リスク女性が調査され、このうち44%はRRSOを受け、56%は定期的スクリーニングを受けた。[ 212 ]BRCA1/BRCA2病原性多様体キャリア368人のうち、72%がRRSOを受けた。RRSOまたはスクリーニング群間または一般集団と比較して、QOLスコア(Short Form-36により評価)における有意差は観察されなかった;しかしながら、RRSOの女性では乳がんおよび卵巣がんについての心配がより少なく(P < 0.001)、がんリスクの認知がより良好(P < 0.05)であるが、内分泌の症状が多く(P < 0.001)、性機能はより不良(P < 0.05)であった。注目すべき点として、37%の女性がRRSO後にHRTを使用したが、62%は閉経期前後または閉経後であった。[ 212 ]続いて研究者は、RRSO(36%)またはスクリーニング(64%)を選択した閉経前の高リスク女性450人を調査した。RRSO群の女性のうち、47%がHRTを使用した。HRT使用者(n = 77)は非使用者(n = 87;P < 0.05)よりも血管運動性の症状が少なかったが、スクリーニング群の女性(n = 286)と比べると血管運動性の症状が多かった。同様に、RRSOを受け、HRTを使用した女性では、スクリーニング群の女性よりも膣乾燥および性交疼痛症による性交時の不快感が多くみられた(P < 0.01)。そのため、こうした症状はHRTの使用で改善されるが、HRTは十分に有効であるわけではなく、これらの重要な問題を扱うためにさらなる研究が必要である。
BRCA1/BRCA2病原性多様体キャリアにおけるRRSOの腫瘍効果以外の長期的効果は不明である。一般集団において、RRSOは心血管疾患、認知症、肺がんによる死亡、および全死亡率の増加と関連している。[ 213 ][ 214 ][ 215 ][ 216 ][ 217 ]卵巣摘出術時の年齢を分析したところ、45歳以前にRRSOを受け、エストロゲン補充療法を受けていない女性において最も有害な影響が認められている。[ 213 ]RRSOを受けたBRCA1/BRCA2病原性多様体キャリアは、メタボリックシンドロームのリスクが高い可能性がある。[ 218 ]RRSOはまた、この集団における短期死亡率の改善と関連している。[ 173 ]RRSO後のがんリスク低下に関して有益性は明らかであるが、腫瘍以外の長期リスクに関するデータがさらに必要である。
両側卵管切除術
両側卵管切除術は、BRCA病原性多様体キャリアにおけるリスクを低下させるための暫定的な手技として提案されている。[ 219 ][ 220 ]リスク低減のための手技としての卵管切除術の効力に関するデータは得られていない。この手技では卵巣機能が温存され、閉経前の患者は早発閉経の有害作用を免れる。この手技は侵襲性を最小限に抑えたアプローチで実施でき、患者が閉経を迎えるまで、その後の両側卵巣摘出術を延期できる。BRCA病原性多様体キャリアにおいて骨盤の漿液性がんの一部が卵管から発生していることを示す説得力のあるデータがある一方で、一部のがんは明らかに卵巣内に発生する。さらに、両側卵管切除術は、患者が両側卵管卵巣摘出術を受けた場合と同じくらい完全にがんリスクを排除できたという誤った安心感を患者に植えつける可能性がある。若年のBRCA病原性多様体キャリア14人を対象にした1件の小規模研究では、この手技が実施可能であることが実証された。[ 221 ]しかしながら、この研究では効力および卵巣機能への影響は評価されなかった。リスク低減のための介入法としてのこの手技の妥当性を確立するため、今後はプロスペクティブ試験が必要である。
モンテカルロシミュレーションを使用する統計学的なMarkovモデルによると、リスク低下のための卵管切除術と遅延された卵巣摘出術は、BRCA1/BRCA2に病原性多様体を有する女性の質調整余命を検討した上で費用対効果が高い戦略であった。[ 222 ]また、卵巣がんリスクとRRSOと卵管切除術の効果をモデル化する別の研究では、妊娠可能年齢の女性に卵管切除術を施行し、その5~10年後に卵巣摘出術を施行した場合に、RRSOとの間で卵巣がんの推定リスクが低いことが明らかになった。[ 223 ]
患者の満足度および卵巣がん減量に対して、卵巣摘出術を延期した両側卵管切除術の影響を評価するプロスペクティブ研究が進行中である。[ 224 ]
化学予防
経口避妊薬
経口避妊薬は、一般集団において卵巣がんに対し予防効果をもつことが示されている。[ 225 ]大規模な多施設ケースコントロール研究を含む数件の研究では予防効果が示されたが[ 123 ][ 226 ][ 227 ][ 228 ][ 229 ]、一方でイスラエルの1件の集団ベースの研究では予防効果を実証することができなかった。[ 230 ]
同様の有益性が卵巣がんの遺伝的リスクが高い女性に対して拡張されるかどうか判定することに、大きな関心がもたれている。BRCA1またはBRCA2の病原性多様体を有する卵巣がん患者799人、および卵巣がんではないがBRCA1またはBRCA2の病原性多様体を有する対照患者2,424人を対象とした多施設研究では、経口避妊薬の使用により卵巣がんリスクが有意に低下することが示された(OR、0.56;95%CI、0.45-0.71)。経口避妊薬を使用しなかった場合と比較すると、最大1年間の継続使用に伴い、ORが0.67(95%CI、0.50-0.89)となった。経口避妊薬使用の1年ごとのORは0.95(95%CI、0.92-0.97)で、最大の予防効果は使用開始後3~5年で認められた。[ 229 ]この研究では、同じ著者らによる前の研究での女性が含められており、前の研究の結果が確認された。[ 123 ]卵巣がんの集団ベースのケースコントロール研究によると、BRCA1またはBRCA2の病原性多様体キャリアでは経口避妊薬使用による予防効果が認められなかった(5年以上の使用でOR、1.07)が、非キャリアでは予想されたように予防効果が認められた(5年以上の使用でOR、0.53)。[ 230 ]しかしながら、BRCA1病原性多様体キャリア36人を対象とした小規模な集団ベースのケースコントロール研究では、病原性多様体キャリアおよび非キャリアのいずれにも同様の予防効果が認められた(OR、約0.5)。[ 228 ]BRCA1の病原性多様体を有する女性を対象としたより大規模なケースコントロール研究では、5年間の経口避妊薬使用後に最大の利益が実証された一方、BRCA2に病原性多様体を有する女性は3年間の経口避妊薬使用後に最大の利益に達したようである。[ 231 ]多数の登録から得られた被験者を対象とした多施設研究では、卵巣がんのBRCA1またはBRCA2の病原性多様体キャリア147人において、がんではないマッチさせた病原性多様体キャリア304人と比較して経口避妊薬の予防効果が認められた(6年以上の使用でOR、0.62)。[ 227 ]最後に、BRCA病原性多様体キャリア13,627人で、そのうち2,855人が乳がん、1,503人が卵巣がんのキャリアを含む18件の研究を対象としたメタアナリシスでは、経口避妊薬の使用に関連した卵巣がんの有意なリスク低下(要約RR、0.50;95%CI、0.33-0.75)が報告された。この著者らは、経口避妊薬の使用期間が長いほどリスク低下も有意に大きくなることを報告した(経口避妊薬の使用期間が10年増すごとにリスクが36%低下)。1975年以後に製造された経口避妊薬の使用では、乳がんリスクとの関係は認められなかった。[ 118 ]
証拠レベル:3aii
(この集団における経口避妊薬の使用と乳がんの考察については、本要約の生殖因子のセクションにある経口避妊薬のセクションを参照のこと。)
生殖因子
周期性損傷および卵巣上皮組織の修復を伴った間断のない排卵は、卵巣がんリスクを増大させることが示唆されている。一般集団における疫学研究では、排卵を防止する生理状態は卵巣がんのリスク低下と関連していた。また、黄体形成ホルモンによる卵巣の慢性過剰刺激が卵巣がん発生機序の役割を果たすことが示唆されている。[ 232 ]こういったデータの大半は、一般集団を対象にした研究から得られたものであるが、一部の情報は、遺伝的素因により高リスクな女性にも当てはまるとしている。
妊娠
一般集団では、未産婦と比較して経産婦は、卵巣がんリスクが45%低下するとの報告がある。その後の妊娠により、卵巣がんリスクは15%低下するようである。[ 233 ]BRCA1/BRCA2病原性多様体を有する女性を対象にした初期の諸研究で、出産により卵巣がんリスクが低下することが明らかになった。[ 230 ][ 234 ]大規模なケースコントロール研究では、BRCA1病原性多様体を有する女性において、出産が卵巣がんの有意なリスク低下と関連しており、ORは0.67(CI、0.46-0.96)であった。[ 229 ]各出産では、BRCA1病原性多様体キャリアのORは0.87(CI、0.79-0.95)であった。この同じ研究では、BRCA2病原性多様体キャリアにおいて出産回数と卵巣がんのリスク増加が関連していた;しかしながら、各出産では有意な傾向は認められず、ORは1.08(CI、0.90-1.29)であった。BRCA2病原性多様体キャリアにおける出産と卵巣がんリスクとの関連を明らかにするにはさらなる研究が必要であるが、BRCA1キャリアでは散発性卵巣がんの場合と同様に、生児出生を重ねるとそのたびに卵巣がんのリスクは有意に低下する。
授乳と卵管結紮術
一般集団において、授乳は卵巣がんリスクの低下と関連している。[ 235 ]BRCA病原性多様体キャリアにおけるデータは限られている。1件の研究では授乳による予防効果は示されなかった。[ 234 ]BRCA1またはBRCA2の病原性多様体を有する女性を対象としたケースコントロール研究では、卵管結紮した女性に卵巣がんの有意なリスク低下(OR、0.39)が実証された。この保護効果はBRCA1の病原性多様体を有する女性キャリアに限られており、経口避妊薬の使用、出産歴、乳がん歴、および民族特性を調整した後でも保たれた。[ 226 ]イスラエルの卵巣がんのケースコントロール研究では、婦人科の手術(卵管結紮、子宮摘出、卵巣摘出、片側卵巣摘除、卵巣嚢腫摘除で、両側卵巣摘除は除く)を受けた女性において40%から50%の卵巣がんリスクの減少を認めた。[ 170 ]その防御機序は不明である。作用のメカニズムとして提唱されているものには、卵巣への血流量の減少、そしてそれが排卵および/または卵巣ホルモン生産の阻害につながる;卵管の遮断、そしてそれが発がんの可能性のある経路を遮断する;または卵巣に到達する子宮成長因子の濃度の減少、が挙げられる。[ 236 ](一般集団に関する情報については、卵巣がん、卵管がん、原発性腹膜がんの予防に関するPDQ要約を参照のこと。)
男性BRCA病原性多様体キャリアの管理
BRCA病原性多様体を有する男性は、男性の乳がんおよび前立腺がんなどさまざまながんのリスクが高いことを示唆するデータがある(表7を参照のこと)。[ 203 ][ 237 ][ 238 ][ 239 ][ 240 ][ 241 ]しかしながら、BRCA病原性多様体を有する男性キャリアを管理するための臨床ガイドラインは、情報が限られているため統一見解および専門家の意見に基づいている。[ 242 ][ 243 ][ 33 ]
BRCA2関連前立腺がんは侵攻性疾患の表現型と関連していることが示唆されている。[ 244 ][ 245 ][ 246 ][ 247 ][ 248 ][ 249 ]特に、最近の2件の研究では、前立腺がんを有するBRCA2男性キャリアの生存期間中央値の範囲が4~5年であると報告されている。[ 247 ][ 248 ]さらに、これらの研究の1件では5年後の死亡率が60%であったと報告されたが、最近のヨーロッパ[ 250 ]および北米[ 251 ]の前立腺特異抗原(PSA)スクリーニング試験では同等の追跡期間後の死亡率は2~8%であったと報告された。BRCA1関連前立腺がんにおけるデータはさらに限られているが、最近の多くの研究でも同様に侵攻性疾患の表現型が示唆されている。[ 244 ][ 246 ][ 249 ][ 252 ]
BRCAキャリアにおけるPSAスクリーニングの有益性は不明であるが、キャリアでは前立腺がん診断時のPSA値が非キャリアよりも高い可能性があると示唆されている(非常に小規模な研究に基づく)。[ 253 ][ 254 ]これらの知見から、特に侵攻性表現型を考慮すると、BRCA病原性多様体を有する男性におけるPSAスクリーニングの潜在的有用性が示唆されている。IMPACT PSAスクリーニング研究の予備的結果によれば、PSAの上昇に基づいて生検を受けたBRCA2キャリア21人において47.6%のPPVが報告された。[ 255 ]これらの男性のスクリーニングにより臨床的に重要な前立腺がんが発見されたため、著者らはこれらの知見からこうした男性における継続的なスクリーニングの理論的根拠が得られると提案している;しかしながら、こうしたスクリーニングによる生存利益は示されていない。最終的には、男性におけるBRCA病原性多様体の状態に関する情報から、最適なスクリーニングおよび治療戦略を明らかにできる可能性がある。さらに、BRCA2生殖細胞病原性多様体の存在は前立腺がんの生存率に対する独立した予後因子であるという最近のデータから、これらの著者は、積極的サーベイランスは侵攻性疾患の表現型のために最適な管理戦略ではない可能性があると結論付けた。[ 248 ]
BRCA病原性多様体キャリアにおける男性の乳がんのスクリーニングには、NCCN臨床診療ガイドライン[ 33 ]で提唱されているように、乳房自己検査の訓練と教育、および35歳で開始する12ヵ月ごとの乳房視触診がある。さらに、NCCNは、BRCA2キャリアに対しては前立腺がんのスクリーニングを40歳から開始するように、BRCA1キャリアに対しては前立腺がんのスクリーニングを検討するように推奨している。[ 33 ]
BRCA病原性多様体キャリアにおける生殖の考慮事項
詳しい情報については、本要約の遺伝性乳がんおよび卵巣がん症候群における心理社会的問題のセクションにある出生前診断および着床前遺伝子検査のセクションを参照のこと。
治療戦略
乳がん
BRCA1およびBRCA2関連乳がんの予後
BRCA1関連乳がん
BRCA1関連乳房腫瘍の独特な特徴は、予後において重要である。さらに、BRCA1関連乳がんは増殖が速いようであるが、それは高い増殖指数および腫瘍サイズとリンパ節の状態の間に予想された相関関係がないことから示唆される。[ 256 ]これらの病理学的特徴を有する乳がんはより予後不良となり、初期の研究では乳がんのBRCA1病原性多様体キャリアは散発例と比較してより予後不良であることが示唆された。[ 257 ][ 258 ][ 259 ]これらの研究は特に、BRCA1およびBRCA2病原性多様体キャリアにおける同側および対側の二次原発乳がんの増加を指摘した。[ 260 ][ 261 ][ 262 ][ 263 ][ 264 ](詳しい情報については、本要約のBRCA病原性多様体キャリアにおける対側乳がんのセクションを参照のこと。)2施設から得られたアシュケナージ系ユダヤ人(AJ)乳がん患者496人を対象にしたレトロスペクティブ・コホート研究では、BRCA1/BRCA2病原性多様体キャリア56人の相対生存率が追跡調査期間中央値116ヵ月で比較された。BRCA1病原性多様体は独立して、より不良な疾患特異的生存率と関連していた。化学療法を受けた女性では、より不良な予後は観察されなかった。[ 265 ]イスラエル人女性における乳がんの発症例を対象にした1件の大規模集団ベース研究で、非キャリア(n = 1,189)と比較してBRCA1創始者病原性多様体キャリア(n = 76)に対するOSの差は認められなかった。[ 266 ]同様の知見はヨーロッパのコホートでも確認され、BRCA1関連乳がんにおける無病生存の差は認められなかった。[ 267 ]北米およびオーストラリアの乳がんを発症した女性3,220人を対象として平均7.9年の追跡を行ったプロスペクティブ・コホート研究(うち、BRCA1キャリア93人とBRCA2キャリア71人)で、BRCA1/BRCA2キャリアと散発性疾患が認められる患者の間で同程度の転帰が報告された。[ 268 ]しかし、結果は1990年代後半に使用されていた化学療法レジメンに基づくものであり、さらに外科的アプローチ(腫瘤摘出術 vs 乳房切除術)と卵巣摘出術の影響についての調整が行われていない。 Prospective Outcomes in Sporadic versus Hereditary breast cancer(POSH)研究には2,733人の女性が集められ、このうち12%(n = 338)にBRCA1/BRCA2病原性多様体が認められた。キャリアは非キャリアと比較して転帰に有意差を示さなかった。[ 269 ]ただし、トリプルネガティブ乳がんの患者コホート(n = 558)では、非キャリアよりも2年経過時の全生存が優れていた(HR、0.59;P = 0.47)ものの、5年および10年経過時には統計的有意差は認められなかった。
非選択のトリプルネガティブ乳がん患者77人を対象にしたBRCA1/BRCA2検査の結果を報告した研究グループがある。この中の15人(19.5%)は、BRCA1(n = 11;14%)もしくはBRCA2(n = 3;4%)の生殖細胞病原性多様体またはBRCA1の体細胞変異(n = 1)のいずれかを有していた。がん診断時年齢の中央値は、BRCA1病原性多様体キャリアで45歳、非キャリアで53歳であった(P = 0.005)。興味深いことに、この研究でも、BRCA1病原性多様体に関連したトリプルネガティブ乳がんの患者では、BRCA1と関連しないトリプルネガティブ乳がんの患者より再燃リスクが低いことが明らかになったが、この研究はサンプルサイズに限界があった。[ 270 ]BRCA1関連 vs 非BRCA1関連のトリプルネガティブ乳がんにおける臨床転帰を調べた別の研究では差は確認されなかったが、BRCA1関連乳がんの患者では脳転移がみられる傾向が高かった。これらのいずれの研究でも、1人のBRCA1病原性多様体キャリアを除く全例が化学療法を受けた。[ 271 ]その後、トリプルネガティブ乳がんのBRCA1キャリア89人および非キャリア175人を対象とした研究で、BRCA1病原性多様体状態は、年齢、卵巣摘出術、およびリスク低減のための乳房切除術で調整すると、生存の独立した予測因子ではなかった。[ 272 ]しかしながら、卵巣摘出術を受けたキャリアでは、乳がん関連死の割合が有意に低かった。
ポーランドの50歳未満のI期からIII期の乳がん患者3,345人を対象とした研究で、予後に対するBRCA1病原性多様体の影響が検討された。このコホートでは、233人(7%)の患者が3つのポーランドのBRCA1創始者病原性多様体(5382insC、C61G、または4154delA)の1つを保有していた。BRCA1キャリアは年齢が若く、ER陰性およびHER2/neu-negativeの頻度が高かった。10年生存率は同程度であった(BRCA1キャリアで80.9%、非キャリアで82.2%)。BRCA1キャリアでは、卵巣摘出が生存改善と関連していた(HR、0.30;95%CI、0.12-0.75)。[ 273 ]
要約すると、BRCA1関連腫瘍は臨床的、病理組織学的、および分子的特徴からより侵攻性の高い表現型であることが示されているが、予後は散発性腫瘍とほぼ同じようである。化学療法を受けていないBRCA1病原性多様体キャリアの予後はより不良な可能性がある。しかしながら、BRCA1関連乳がんのほとんどはトリプルネガティブ乳がんであるため、通常は補助化学療法を用いて治療される。BRCA1関連乳がんを散発性腫瘍とは異なる治療法で治療すべきかどうかを判断する研究が進行中である。(詳しい情報については、本要約の全身療法への反応におけるBRCA1とBRCA2の役割のセクションを参照のこと。)
乳がんの治療における全身療法
全身療法への反応におけるBRCA1とBRCA2の役割
化学療法単独とBRCA病原性多様体
複数のレトロスペクティブ研究およびプロスペクティブ研究[ 277 ][ 278 ][ 279 ][ 280 ][ 281 ]で、BRCA1病原性多様体キャリアを対象に、乳がんに対して術前補助化学療法を施行した場合、特にシスプラチンを用いた場合における化学療法に対する奏効率が評価されている。[ 279 ]標準化学療法に対する病理学的完全奏効(pCR)率を詳細に記述したレトロスペクティブ・レビューが公表されている。アントラサイクリン系およびタキサン系薬物をベースとした標準化学療法レジメンによる術前補助療法を受けた患者で、pCR率は40~60%の範囲であった。[ 281 ][ 282 ]BRCA病原性多様体を有する患者では、プラチナ製剤による術前補助療法により印象的なpCR率が示された。BRCA1病原性多様体を有するポーランド人女性107人のコホートで、シスプラチン75mg/m2が3週間ごとに4サイクル投与された;全pCR率は61%であった。[ 283 ][ 284 ]しかしながら、50人の患者を対象としたGeparSixto試験で、既知のBRCA病原性多様体を有する個人のサブセットでは、pCR率が66.7%であったが、アントラサイクリン系およびタキサン系薬物を含む術前補助化学療法レジメンにプラチナ製剤を追加しても有益性は認められなかった。[ 285 ]
TNT試験では、転移性トリプルネガティブ乳がん患者376人を対象にドセタキセルとカルボプラチンが比較された。29人の患者がBRCA1またはBRCA2に病原性多様体を有していた。コホート全体では、2群間に客観的奏効率(ORR)の差が認められなかった;しかしながら、BRCAキャリアでは差が確認された。ドセタキセルが投与された病原性多様体キャリアにおけるORRは33%であった;カルボプラチンが投与された同様な患者におけるORRは68%であった(P = 0.03)。[ 286 ]
化学療法併用または非併用の標的療法
複数の試験で、化学療法併用または非併用でポリ(ADPリボース)ポリメラーゼ(PARP)阻害薬の使用が評価されている。BRCA1とBRCA2には、相同的組換えによりDNA二本鎖切断を修復する働きがある;PARPは、DNA鎖に対するPARPトラッピングによる修復に加えて、塩基除去修復による一本鎖切断の修復に関与している。
2017年に、2件の第III相試験で、BRCA病原性多様体を有する転移性乳がん患者におけるPARP阻害薬が探索された。OlympiAD試験では、302人の患者がオラパリブ、300mgの1日2回経口投与または医師が選択した化学療法(カペシタビン、エリブリン、またはビノレルビン)を受けるようにランダムに割り付けられた。オラパリブで治療された患者における無増悪生存(PFS)は、中央値が4.2ヵ月から7.0ヵ月に改善された(HR、0.58;P < 0.001)。OSは副次エンドポイントであったが、統計的有意差は確認されなかった。[ 287 ]EMBRACA試験では、431人の患者がタラゾパリブ、1mgの毎日経口投与 vs 医師が選択したカペシタビン、エリブリン、ビノレルビン、またはゲムシタビンのいずれかを受けるようにランダムに割り付けられた。[ 288 ]タラゾパリブを投与された患者のPFSは、中央値が8.6ヵ月 vs 5.6ヵ月(HR、0.54;P < 0.001)で改善した。EMBRACA試験でのOSは第1種の過誤に対して保護されたエンドポイントであり、最初の報告時にデータはイベントの51%しか報告されておらず不完全であった(HR、0.76;P = 0.105)。これらの結果に基づいて米国食品医薬品局は、生殖細胞BRCA病原性多様体を有する手術不能または転移性乳がん患者の治療にタラゾパリブとオラパリブの両方の使用を承認している。
進行中の研究では、他の生殖細胞病原性多様体および体細胞変異を標的に含めるために、PARP阻害薬を用いた多数の新たな戦略が評価されている。早期および転移の両設定で計画された試験により、奏効を改善するとともに、恩恵が得られる可能性のある患者集団を拡大するために、PARP阻害薬単独ならびにPARP阻害薬と他のDNA損傷修復薬、免疫療法、および他の標的療法との併用が評価されている。
(BRCA関連卵巣がんに対する治療戦略に関する詳しい情報については、本要約の卵巣がんのセクションにある卵巣がんの治療における全身療法のセクションを参照のこと。)
局所療法
BRCA1/BRCA2病原性多様体キャリアに対する乳房温存療法
腫瘤摘出術 + 放射線療法は早期乳がんの女性に対する標準の局所-領域治療となっているが、乳がんの遺伝的素因を有するが両側乳房切除術をすぐには選択しない女性では、この治療の使用はさらに複雑である。BRCA1/BRCA2病原性多様体キャリアにおける治療用放射線による腫瘍の誘発または過剰な毒性発生の可能性に関する当初の懸念は根拠がなかった。[ 289 ][ 290 ][ 291 ]それにもかかわらず、二次性原発乳がんの高い発生率があり、治療選択に影響を与える可能性がある。
二次性原発乳がんのリスク増加が立証されており、BRCA1病原性多様体を有する若い女性ではリスクが最大で60%に上る可能性があるため[ 262 ]、一部のBRCA1/BRCA2病原性多様体キャリアは最初のがん診断時点で両側乳房切除術を選択する。(詳しい情報については、本要約のBRCA病原性多様体キャリアにおける対側乳がんのセクションを参照のこと。)しかしながら、数件の研究が原発腫瘍を治療する妥当な選択肢として乳房温存療法の使用を支持している。[ 292 ][ 293 ][ 294 ]10年時点での同側再発のリスクは10~15%の間にあると推定されており、非キャリアにみられるリスクと同程度である。[ 101 ][ 262 ][ 292 ][ 293 ][ 294 ]追跡期間がより長期の研究では、15年時点での同側性乳房イベントのリスクが(原発腫瘍の再燃ではなく)主に同側性二次乳がんにより、24%と高いことが実証されている。[ 292 ][ 294 ]研究全体で完全に一致しているわけではないが、放射線療法、化学療法、卵巣摘出術、およびタモキシフェンは、散発性乳がんの場合と同様に両側性イベントのリスク低下と関連している。[ 101 ][ 292 ][ 293 ][ 294 ]対側乳がんのリスクは、片側乳房切除術に対して乳房温存療法を受けた女性で異なっているとは考えられず、放射線の照射によって対側乳がんのリスクは増えないことが示唆される。[ 292 ]この知見は、55歳未満で乳がんと診断された女性の集団ベースケースコントロール研究によって支持されている。[ 295 ]すべての女性についてBRCA1/BRCA2の遺伝子型解析が実施された。キャリアでは、対側乳がんのリスクが非キャリアの4倍と有意に高かったが、原発性乳がんに対して最初に放射線療法を受けたキャリアでは、放射線に曝露していないキャリアと比較して、対側乳がんのリスク増加はみられなかった。(放射線と乳がんリスクに関する詳しい情報については、マンモグラフィのセクションを参照のこと。)最後に、BRCA1/BRCA2病原性多様体キャリアで乳房温存療法を選択した患者と乳房切除術を選択した患者では、15年時点でOSの差は認められていない。[ 292 ]
証拠レベル:3a
卵巣がん
BRCA1およびBRCA2関連卵巣がんの予後
一般的に不良な予後因子が報告されているにもかかわらず、数件の研究ではBRCA病原性多様体をもつ卵巣がん患者の生存が向上している。[ 296 ][ 297 ][ 298 ][ 299 ][ 300 ][ 301 ][ 302 ][ 303 ][ 304 ]イスラエルで実施された全国規模の集団ベースのケースコントロール研究では、BRCA創始者病原性多様体のある卵巣がん患者は、対照群に比べ、3年生存率が有意に優れていることが分かった。[ 297 ]同じコホートを5年間追跡したところ、BRCA1とBRCA2の両方の病原性多様体キャリア(54ヵ月)では非キャリア(38ヵ月)よりも生存の改善が示され、これはIII期およびIV期卵巣がん女性および高悪性度腫瘍を有する女性で最も顕著であった。[ 305 ]卵巣がんに罹患しているAJ女性を対象にした米国の1件の研究において、BRCA病原性多様体を有する女性はBRCA病原性多様体を有さない卵巣がんのAJ女性と比較して、また進行期卵巣がんで臨床試験に参加している患者の2つの大規模集団と比較して再発までの期間中央値が長く、全生存率が良好であった。[ 301 ]米国における病院ベースのレトロスペクティブ研究では、アシュケナージ系のBRCA病原性多様体キャリアは、初回治療に対する反応性、無病生存率、およびOSで評価した場合、プラチナベースの化学療法に対する反応が散発例に比べて優れていた。[ 299 ]同様に、非アシュケナージ系のBRCA病原性多様体を有する女性を対象にしたケースコントロール研究では、有意な生存優位性が認められた。[ 306 ]オランダの研究でも、散発性卵巣がん患者220人よりもBRCA1/BRCA2キャリア112人の方がプラチナベースの初回化学療法に対して良好な反応を示した。[ 307 ]米国における1件の集団ベースの研究では、BRCA2キャリアでOSの改善が示されたが、BRCA1キャリアでは示されなかった。[ 308 ]しかしながら、本研究にはBRCA2病原性多様体キャリアが12例、BRCA1病原性多様体キャリアが20例しか含まれていなかった。Cancer Genome Atlas研究からの高悪性度漿液性卵巣がんで既知のBRCA2多様体を有する29症例(生殖細胞20症例、体細胞9症例)において、BRCA病原性多様体が陰性の症例と比較して有意に良好なOSおよびPFSが認められた。BRCA1病原性多様体では、予後との有意な関連はみられなかった。[ 309 ]さらに、上皮性卵巣がんのBRCA病原性多様体キャリア1,213人と非キャリア2,666人を含む26件の観察研究のプール解析によると、病原性多様体キャリアの生存の方が良好なことが示された(BRCA1:HR、0.73;95%CI、0.64-0.84;P < 0.001;BRCA2:HR、0.49;95%CI、0.39-0.61;P < 0.001)。[ 310 ]このように、上皮性卵巣がんのBRCA1およびBRCA2キャリアにおける5年生存率は、いずれも非キャリアで観察されたものより良好で、BRCA2キャリアが最も予後良好であった。日本人患者を対象にした研究では、BRCA1関連のIII期卵巣がん患者にシスプラチンレジメンによって治療したところ、同じ方法で治療した非遺伝性がん症例よりも生存率が良好なことが明らかになった。[ 300 ]
対照的に、数件の研究ではBRCA病原性多様体をもつ卵巣がん患者のOSの向上は認められていない。[ 258 ][ 311 ][ 312 ][ 313 ]このうち最大規模の研究では、カナダおよび米国でBRCA1およびBRCA2の病原性多様体検査を受けた非選択患者の大規模シリーズが含まれていた。3年の時点で、病原性多様体の存在は良好な予後に関連していたが、10年の時点では、もはや予後に差はみられなかった。[ 314 ]さらに、家族歴を有する卵巣がん患者では、生存率が不良なことを示唆した研究が1件ある。[ 312 ]
BRCA病原性多様体キャリアでは、説得力のあるデータにより短期生存で有利なことが示唆される。しかしながら、長期転帰については、まだ確定していない。BRCA1またはBRCA2創始者病原性多様体を有するAJの卵巣がん患者では、生存に改善がみられることは確かである[ 309 ][ 310 ];しかしながら、この生存の優位性がすべてのBRCA関連がんに対してより広く適用されるかどうかを判断するには、適切な対照群を伴う別の集団を対象とした大規模な研究がさらに必要である。
卵巣がんの治療における全身療法
遺伝性BRCA関連卵巣がんにおける良好な予後を説明する分子的機序は不明であるが、BRCA遺伝子の機能に関係している可能性がある。BRCA遺伝子は、細胞周期チェックポイント活性化および相同的組換えによるDNA修復において重要な役割を果たしている。[ 315 ][ 316 ]BRCAに加えて、ATM、BARD1、PALB2、BRIP1、RAD51、BLM、CHEK2、およびNBNなどの他の遺伝子も相同組換えを維持している。より多数の卵巣がんを対象とした包括的な遺伝子検査では、漿液性卵巣腫瘍の約50%が相同組換え欠陥につながる体細胞変異または生殖細胞多様体を保有する可能性が示されている。[ 317 ]
相同的修復の障害は、シスプラチンなどの特定の化学療法薬に起因するDNAクロスリンクを修復する細胞の能力に影響を与える可能性がある。乳がんおよび卵巣がんの細胞株において、BRCA1は化学療法薬感受性に影響を及ぼすことが前臨床データにより実証されている。BRCA1の蛋白発現量が低いと、シスプラチンによる化学療法に対する感受性が増強されることが示されている。[ 318 ]BRCA関連卵巣がんの患者では、散発性のがん患者と比較して、第一選択治療およびその後の治療でもプラチナ製剤をベースとした化学療法に対する反応が高いことが示されており、これらの患者のより良好な転帰に寄与する可能性がある。[ 299 ][ 302 ]生殖細胞多様体または体細胞変異に起因する相同組換え修復遺伝子欠損(HRD)が腫瘍に認められる卵巣がん患者は、相同組換えが正常な女性と比較して生存期間が長い。相同組換え修復遺伝子多様体の大多数は、BRCA1およびBRCA2における体細胞変異または生殖細胞多様体からなり、その3分の1には他の相同修復遺伝子における多様体が寄与している。[ 319 ][ 320 ]
BRCA1またはBRCA2欠損卵巣がんの治療を目的として、PARP経路阻害薬が研究されている。(PARP阻害薬に関する詳しい情報については、本要約の治療戦略のセクションにある全身療法への反応におけるBRCA1とBRCA2の役割のセクションを参照のこと。)PARPが塩基除去修復による一本鎖切断の修復に関与している一方、BRCA1とBRCA2は相同的組換えによるDNA二本鎖切断の修復に活性をもつ。したがって、BRCA1またはBRCA2欠損腫瘍においてPARPの阻害によって塩基除去修復を阻害すると、2つの別々の修復機構が低下するにつれて細胞死の増加に至る-合成致死性の概念が仮定された。同じ概念がHRDを有する腫瘍に適用される場合があり、その結果として、BRCA遺伝子の病原性多様体を超えて、何らかの相同組換え欠損が腫瘍に認められる女性にもPARP阻害薬の使用が拡大する可能性がある。臨床診療では、HRDの腫瘍を判定するために利用可能な腫瘍分析法が異なり、手法および定義に差がある。HRDの卵巣がんを対象としたPARP阻害薬のさらなる研究が進行中である。
PARP阻害薬
オラパリブ
プラチナ製剤ベースの化学療法後の卵巣がんを対象とした研究でPARP阻害薬が用いられている。経口PARP阻害薬のオラパリブに関する第I相研究では、卵巣がん、乳がん、および前立腺がんのBRCA1およびBRCA2病原性多様体キャリアにおける忍容性および効力が実証された。[ 321 ]2つの異なる用量のオラパリブについて検討した第II相試験では、BRCA1またはBRCA2病原性多様体を有する再発卵巣がん患者における忍容性および効力が実証された。[ 322 ]全奏効率は、400mgの1日2回投与を受けたコホートで33%(患者33人中11人)、100mgの1日2回投与(すなわち1日16カプセル)を受けたコホートで13%(患者24人中3人)であった。特に頻度が高かった副作用は、軽度の吐き気と疲労であった。[ 323 ]PARP阻害薬は、生殖細胞BRCA1またはBRCA2病原性多様体を有する卵巣がん患者に加え、体細胞BRCA1またはBRCA2変異を有するか、これらの遺伝子のエピジェネティックサイレンシングを有する卵巣がん患者でも有用な可能性がある。[ 324 ]
数件の第II相治療研究で、再発卵巣がん患者を対象に、プラチナ製剤感受性およびプラチナ製剤抵抗性の両方のがんにおけるオラパリブの効力が探索された。単一治療群研究では、乳がん、膵がん、前立腺がん、卵巣がんなど、一連のBRCA関連がん298例を治療するために、オラパリブ1日2回400mgが用いられた。オラパリブで治療された卵巣がんの女性193人中、31%で反応がみられ、40.4%で8週間以上持続した病態の安定が得られた。[ 325 ]以前に少なくとも3系列の化学療法で治療された154人の女性では、同様に30%の全奏効率がみられ、奏効期間中央値はプラチナ製剤感受性がんで8.2ヵ月およびプラチナ製剤抵抗性がんで8.0ヵ月と同等であった。[ 326 ]プラチナ製剤感受性がんを有する患者173人を対象にした別の研究では、患者がパクリタキセル/カルボプラチン + オラパリブ vs パクリタキセル/カルボプラチン単独で治療された。PFS期間はオラパリブ投与群の方が対照群よりも有意に長く(12.2ヵ月 vs 9.6ヵ月)(HR、0.51;95%CI、0.34-0.77)、特にBRCA病原性多様体を有する患者のサブグループで顕著であった(HR、0.21;95%CI、0.08-0.55)。オラパリブ投与群と対照群間でOSに差は認められなかった。[ 327 ]
対照的に、オラパリブによる治療を受けたプラチナ製剤感受性の卵巣がんの女性でBRCAの状態によって生存延長が予測されなかったことを明らかにした研究もある。1件のランダム化オープンラベル試験では、プラチナ製剤感受性再発卵巣がんを有する女性90人がオラパリブまたはセジラニブとオラパリブの併用に割り付けられた。PFS期間中央値は、併用群で有意に長かった(17.7ヵ月 vs 9ヵ月)(HR、0.42;95%CI、0.23-0.76)。サブセット解析により、セジラニブとオラパリブの併用では、BRCA野生型/不明の患者43人においてオラパリブ単剤よりも有意に長いPFS期間が得られ(16.5ヵ月 vs 5.7ヵ月)(HR、0.32;P = 0.008)、BRCA病原性多様体を有する女性47人においてはPFS期間の延長傾向が小さかった(19.4ヵ月 vs 16.5ヵ月)(HR、0.55;P = 0.16)ことが示された。[ 328 ]
別の研究で、BRCA1/BRCA2病原性多様体が認められ、以前のプラチナ製剤ベースのレジメンから12ヵ月以内に卵巣がんが再発した女性が、リポソーマルドキソルビシン(Doxil)投与群(n = 33) vs オラパリブ200mgの1日2回投与群(n = 32) vs オラパリブ400mgの1日2回投与群(n = 32)にランダムに割り付けられた。この研究では、主要エンドポイントであったPFSのグループ間の差異が示されなかった。[ 329 ]興味深いことに、リポソーム結合ドキソルビシン投与群は予想よりも奏効率が高く、これはBRCA1/BRCA2に関連する卵巣がんは散発性卵巣がんよりもリポソーム結合ドキソルビシンに対する感受性が高い可能性を示した他の研究とも一致している。[ 330 ][ 331 ]別の研究は、再発卵巣がん患者におけるオラパリブに対する有意な奏効を、BRCA1/BRCA2病原性多様体を有する患者(客観的奏効率[ORR]、41%)とBRCA1/BRCA2病原性多様体を有さない患者(ORR、24%)について示している。[ 332 ]この研究は、特定の散発性卵巣がん、特に高悪性度の漿液性の組織像が認められるがんが、BRCA1/BRCA2病原性多様体に関連した腫瘍に似た特性をもつ可能性があることを強調している。
維持療法としてのオラパリブは、プラチナ製剤感受性再発卵巣がんにおけるPFSを有意に改善することが示されている。265人の患者を対象にした1件のランダム化比較研究(Study 19)で、オラパリブを投与された患者のPFSが8.4ヵ月であったのに対して、プラセボを投与された患者では4.8ヵ月であった(HR、0.35;95%CI、0.25-0.49)。[ 333 ]このコホートにおけるプラセボと比較したオラパリブの有益性は、BRCA病原性多様体を有する患者136人で最大となり、PFSは11.2ヵ月 vs 4.3ヵ月(HR、0.18;95%CI、0.1-0.31)であったことが実証された。[ 334 ]コホート全体、またはBRCA病原性多様体のキャリアにおけるOSの差は観察されなかった。その後の探索的な事後解析では、OSに対する交絡因子の影響を最小限に抑えるため、BRCA病原性多様体を有し、増悪時にPARP阻害薬を投与された患者が除外された。この集団の97人の患者では、プラセボと比較してオラパリブにより、OSが改善した(HR、0.52;95%CI、0.28-0.97)。[ 335 ]追跡期間が5年を超えた後のより充実したStudy 19のデータでは、プラセボと比較してオラパリブによりOSの有益性の改善傾向が全コホート(29.8ヵ月 vs 27.8ヵ月;HR、0.73;95%CI、0.55–0.96)またはオラパリブによる治療を受けたBRCA病原性多様体キャリア(24.5ヵ月 vs 26.6ヵ月;HR、0.62;95%CI、0.41–0.94)にみられたが、先験的な有意性の閾値であるP < 0.0001を満たさなかったことが示された。[ 336 ]プラチナ製剤感受性卵巣がんが再発し、BRCA病原性多様体を有する女性の同様な集団において、オラパリブ錠はプラセボと比較して有効な維持療法であることが示されている(SOLO2試験)。オラパリブではPFS期間中央値が19.1ヵ月であったのに対して、プラセボでは5.5ヵ月であった(HR、0.3;095%CI、0.22–0.41)。オラパリブ錠では、1日16カプセルと比較して、1日当たりの服用数(2錠を1日2回)が少ないという利点が得られる。[ 337 ]
新たに進行期のBRCA関連卵巣がんと診断された女性が一次治療に反応を示した後の維持療法として、オラパリブは著しく有益なことが実証されている。SOLO-1試験では、BRCA病原性多様体を有する女性391人が一次手術とプラチナ製剤ベースの化学療法を受けた後に、オラパリブ300mg1日2回投与群(n = 260)またはプラセボ群(n = 131)にランダムに割り付けられた。追跡期間中央値41ヵ月後、オラパリブが投与された女性では、プラセボが投与された女性と比較して疾患進行または死亡のリスクが70%低く、改善したPFSは約3年と推定された。[ 338 ]3年以内の疾患進行または死亡は、オラパリブ群の女性260人中102人(39%)およびプラセボ群の女性131人中96人(73%)にみられた。副作用によって、患者の28%で用量を減量し、過半数の患者で投与を中断した。疲労と吐き気が一般的な副作用であり、用量減量の原因となった。
rucaparib
rucaparibは、PARP-1、-2、および-3の小分子阻害薬で、米国では進行した生殖細胞BRCA1/BRCA2関連卵巣がんの治療に対して2016年12月に承認された。第II相研究では、病原性BRCA関連乳がんおよび卵巣がんの女性において継続投与することで間欠投与よりも奏効率が良好なことが明らかにされた。[ 339 ]その後の第I/II相用量決定研究では、以前に2~4の治療レジメンを受けて再発した生殖細胞BRCA関連高悪性度漿液性がんの女性42人において、管理可能な毒性および59.5%の奏効率に基づいて600mgの1日2回投与が選択された。一般的なグレード3の毒性には、疲労、吐き気、および貧血があった。[ 340 ]
ARIEL-2第II相研究では、BRCA多様体を有する女性だけでなく、HRDがんのマーカーである可能性が高いゲノムのヘテロ接合性の消失(LOH)の割合が高いBRCA野生型の女性でも、高悪性度プラチナ製剤感受性の卵巣がんの再発に対する治療にrucaparibが有効なことが明らかにされた。この研究には女性206人が登録され、そのうち40人がBRCAに生殖細胞病原性多様体または体細胞変異を有していた。別の82人はBRCA野生型であったが、高LOHであった。PFS期間中央値は、BRCA多様体サブグループ(12.8ヵ月)(HR、0.27;95%CI、0.16–44)および高LOHサブグループ(5.8ヵ月)(HR、0.62;95%CI、0.42–0.90)の方が低LOHサブグループ(5.2ヵ月)と比較して有意に長かった。著者らは、プラチナ製剤感受性の高悪性度卵巣がんが再発した女性において、BRCA多様体の状態およびHRDの代替としてのLOHスコアの両方がrucaparib感受性の分子的予測因子であると結論した。[ 341 ]
二次またはそれ以降のプラチナ製剤化学療法に反応を示した後にプラチナ製剤感受性の高悪性度卵巣がんが再発した女性576人を対象とした第III相試験で、rucaparib vs プラセボが評価された。この研究では、女性196人がBRCA病原性多様体を有していた:130人が生殖細胞多様体、56人が体細胞変異。rucaparib群の女性におけるPFS期間中央値は10.8ヵ月 vs 5.4ヵ月(HR、0.35;95%CI、0.30-0.45)であった。PFS期間中央値は、BRCA関連卵巣がんで最も長かった:rucaparib群が16.6ヵ月 vs プラセボ群が5.4ヵ月(HR、0.23;95%CI、0.16-0.34)。HRDがんの女性におけるPFS期間中央値は13.6ヵ月 vs 5.4ヵ月(HR、0.32;95%CI、0.24-0.42)であった。これらのデータに基づいて、著者らは、高悪性度卵巣がんが進行した女性においてrucaparibによる有益性を予測するマーカーとしてプラチナ製剤感受性のみで十分であり、HRDまたはBRCAの検査を追加する必要がないと結論した。[ 342 ]
ニラパリブ
ニラパリブはPARP-1および-2の選択的阻害薬である。第I相用量決定研究では、BRCA関連固形腫瘍が再発した女性において1日300mgの投与により42%の奏効率が観察された。[ 343 ]プラチナ製剤感受性の卵巣がんが再発した患者500人のコホートにおいて、234人がニラパリブ維持療法を受け、116人がプラセボの投与を受けた(NOVA試験)。[ 344 ]ニラパリブ維持療法によりPFSが改善し、BRCA病原性多様体キャリア(21ヵ月)およびHRD陽性の野生型患者(12ヵ月)の方がHRD陽性の腫瘍がない野生型患者(9ヵ月)より長かった。前データと一致して、生殖細胞BRCA病原性多様体を有する患者は、3群のうちPFSが最も長かった。プラチナ製剤への反応または多様体の状態にかかわらず、前治療歴の多い卵巣がん女性におけるニラパリブ維持療法の広範な有効性に基づいて、QUADRA第II相試験では、卵巣がんが再発し病変が測定可能な女性463人を対象にニラパリブの抗腫瘍活性が検討された。女性は、以前に中央値で4ラインの治療を受けていた。中央値9ヵ月の期間で女性の28%に全奏効がみられ、プラチナ製剤感受性のHRD陽性の女性で奏効率が高かった。[ 345 ]
BRCA病原性多様体を有する女性においてプラチナ製剤感受性のみがPARP阻害薬に対する反応のマーカーであるかどうか、および治療法または維持療法としてのPARP阻害薬の最適な投与時期を判断するには、より成熟したデータが必要である。相同修復経路に関与する複数の遺伝子がより明らかになっていることに基づいて、PARP治療に対する反応を予測するためにHRDの状態も使用されることがある。
証拠レベル:3dii
遺伝性乳がんおよび卵巣がんで利用可能な臨床診療ガイドライン
表13に、遺伝性乳がんおよび卵巣がんに関して、がんリスク評価と遺伝カウンセリング、遺伝子検査、および/または管理に対する推奨を公表しているいくつかの機関を掲載している。
表13.遺伝性乳がんおよび卵巣がん(HBOC)で利用可能な臨床診療ガイドライン 機関 紹介の推奨 リスク評価と遺伝カウンセリングの推奨 遺伝子検査の推奨 管理の推奨 ACMG/NSGC = American College of Medical Genetics and Genomics/米国遺伝カウンセラー学会(National Society of Genetic Counselors);ACOG = American College of Obstetricians and Gynecologists;ASCO = 米国臨床腫瘍学会(American Society of Clinical Oncology);ESMO = European Society for Medical Oncology;NAPBC = National Accreditation Program for Breast Centers;NCCN = National Comprehensive Cancer Network;NSGC = 米国遺伝カウンセラー学会(National Society of Genetic Counselors);SGO = Society of Gynecologic Oncology;USPSTF = U.S. Preventive Services Task Force。 a USPSTFガイドラインは、過去にがんの診断を受けていない人に適用する。 ACMG/NSGC(2015)[ 346 ] 提供 リスク評価:提供 非提供 非提供 遺伝カウンセリング:提供 ACOG(2017)[ 347 ] 提供 リスク評価:提供 提供 提供 遺伝カウンセリング:提供 ASCO(2015)[ 348 ] 非提供 リスク評価:一般的推奨;HBOCに特化したものではない 一般的推奨;HBOCに特化したものではない 非提供 遺伝カウンセリング:提供 ESMO(2016)[ 349 ] 他の公表ガイドラインを参照 リスク評価:他の公表ガイドラインを参照 他の公表ガイドラインを参照 提供 遺伝カウンセリング:提供 NAPBC(2014)[ 350 ] 他の公表ガイドラインを参照 リスク評価:他の公表ガイドラインを参照 検査適応は非提供;検査前および検査後のカウンセリングの要素を提供 非提供 遺伝カウンセリング:提供 NSGC(2013)[ 351 ] 提供 リスク評価:他の公表ガイドラインおよび利用可能なモデルを参照 提供 他の公表ガイドラインを参照 遺伝カウンセリング:提供 NCCN(2020)[ 33 ] 提供 リスク評価:提供 提供 提供 遺伝カウンセリング:提供 SGO(2015、2017)[ 347 ][ 352 ] 提供 リスク評価:提供 提供 提供 遺伝カウンセリング:提供 USPSTFa(2019)[ 353 ] 提供 リスク評価:提供 一般論として提供、および他のガイドラインを参照 一般論として提供、および他のガイドラインを参照 遺伝カウンセリング:提供 参考文献- U.S. Preventive Services Task Force: Genetic risk assessment and BRCA mutation testing for breast and ovarian cancer susceptibility: recommendation statement. Ann Intern Med 143 (5): 355-61, 2005.[PUBMED Abstract]
- Domchek SM, Friebel TM, Singer CF, et al.: Association of risk-reducing surgery in BRCA1 or BRCA2 mutation carriers with cancer risk and mortality. JAMA 304 (9): 967-75, 2010.[PUBMED Abstract]
- Rebbeck TR, Friebel T, Lynch HT, et al.: Bilateral prophylactic mastectomy reduces breast cancer risk in BRCA1 and BRCA2 mutation carriers: the PROSE Study Group. J Clin Oncol 22 (6): 1055-62, 2004.[PUBMED Abstract]
- Evans DG, Ingham SL, Baildam A, et al.: Contralateral mastectomy improves survival in women with BRCA1/2-associated breast cancer. Breast Cancer Res Treat 140 (1): 135-42, 2013.[PUBMED Abstract]
- Kurian AW, Sigal BM, Plevritis SK: Survival analysis of cancer risk reduction strategies for BRCA1/2 mutation carriers. J Clin Oncol 28 (2): 222-31, 2010.[PUBMED Abstract]
- Kauff ND, Domchek SM, Friebel TM, et al.: Risk-reducing salpingo-oophorectomy for the prevention of BRCA1- and BRCA2-associated breast and gynecologic cancer: a multicenter, prospective study. J Clin Oncol 26 (8): 1331-7, 2008.[PUBMED Abstract]
- Finch AP, Lubinski J, Møller P, et al.: Impact of oophorectomy on cancer incidence and mortality in women with a BRCA1 or BRCA2 mutation. J Clin Oncol 32 (15): 1547-53, 2014.[PUBMED Abstract]
- Thomas DB, Gao DL, Self SG, et al.: Randomized trial of breast self-examination in Shanghai: methodology and preliminary results. J Natl Cancer Inst 89 (5): 355-65, 1997.[PUBMED Abstract]
- Scheuer L, Kauff N, Robson M, et al.: Outcome of preventive surgery and screening for breast and ovarian cancer in BRCA mutation carriers. J Clin Oncol 20 (5): 1260-8, 2002.[PUBMED Abstract]
- Brekelmans CT, Seynaeve C, Bartels CC, et al.: Effectiveness of breast cancer surveillance in BRCA1/2 gene mutation carriers and women with high familial risk. J Clin Oncol 19 (4): 924-30, 2001.[PUBMED Abstract]
- Burke W, Daly M, Garber J, et al.: Recommendations for follow-up care of individuals with an inherited predisposition to cancer. II. BRCA1 and BRCA2. Cancer Genetics Studies Consortium. JAMA 277 (12): 997-1003, 1997.[PUBMED Abstract]
- Shapiro S: Periodic screening for breast cancer: the Health Insurance Plan project and its sequelae, 1963-1986. Baltimore, Md: Johns Hopkins University Press, 1988.[PUBMED Abstract]
- Kerlikowske K, Grady D, Barclay J, et al.: Effect of age, breast density, and family history on the sensitivity of first screening mammography. JAMA 276 (1): 33-8, 1996.[PUBMED Abstract]
- Kerlikowske K, Carney PA, Geller B, et al.: Performance of screening mammography among women with and without a first-degree relative with breast cancer. Ann Intern Med 133 (11): 855-63, 2000.[PUBMED Abstract]
- Kerlikowske K, Grady D, Barclay J, et al.: Positive predictive value of screening mammography by age and family history of breast cancer. JAMA 270 (20): 2444-50, 1993.[PUBMED Abstract]
- Tilanus-Linthorst M, Verhoog L, Obdeijn IM, et al.: A BRCA1/2 mutation, high breast density and prominent pushing margins of a tumor independently contribute to a frequent false-negative mammography. Int J Cancer 102 (1): 91-5, 2002.[PUBMED Abstract]
- Tilanus-Linthorst MM, Kriege M, Boetes C, et al.: Hereditary breast cancer growth rates and its impact on screening policy. Eur J Cancer 41 (11): 1610-7, 2005.[PUBMED Abstract]
- Mitchell G, Antoniou AC, Warren R, et al.: Mammographic density and breast cancer risk in BRCA1 and BRCA2 mutation carriers. Cancer Res 66 (3): 1866-72, 2006.[PUBMED Abstract]
- Miller AB, To T, Baines CJ, et al.: Canadian National Breast Screening Study-2: 13-year results of a randomized trial in women aged 50-59 years. J Natl Cancer Inst 92 (18): 1490-9, 2000.[PUBMED Abstract]
- Shtern F: Digital mammography and related technologies: a perspective from the National Cancer Institute. Radiology 183 (3): 629-30, 1992.[PUBMED Abstract]
- Lewin JM, D'Orsi CJ, Hendrick RE, et al.: Clinical comparison of full-field digital mammography and screen-film mammography for detection of breast cancer. AJR Am J Roentgenol 179 (3): 671-7, 2002.[PUBMED Abstract]
- Pisano ED, Gatsonis C, Hendrick E, et al.: Diagnostic performance of digital versus film mammography for breast-cancer screening. N Engl J Med 353 (17): 1773-83, 2005.[PUBMED Abstract]
- Sharan SK, Morimatsu M, Albrecht U, et al.: Embryonic lethality and radiation hypersensitivity mediated by Rad51 in mice lacking Brca2. Nature 386 (6627): 804-10, 1997.[PUBMED Abstract]
- Gowen LC, Avrutskaya AV, Latour AM, et al.: BRCA1 required for transcription-coupled repair of oxidative DNA damage. Science 281 (5379): 1009-12, 1998.[PUBMED Abstract]
- Abbott DW, Freeman ML, Holt JT: Double-strand break repair deficiency and radiation sensitivity in BRCA2 mutant cancer cells. J Natl Cancer Inst 90 (13): 978-85, 1998.[PUBMED Abstract]
- Narod SA, Lubinski J, Ghadirian P, et al.: Screening mammography and risk of breast cancer in BRCA1 and BRCA2 mutation carriers: a case-control study. Lancet Oncol 7 (5): 402-6, 2006.[PUBMED Abstract]
- Goldfrank D, Chuai S, Bernstein JL, et al.: Effect of mammography on breast cancer risk in women with mutations in BRCA1 or BRCA2. Cancer Epidemiol Biomarkers Prev 15 (11): 2311-3, 2006.[PUBMED Abstract]
- Giannakeas V, Lubinski J, Gronwald J, et al.: Mammography screening and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers: a prospective study. Breast Cancer Res Treat 147 (1): 113-8, 2014.[PUBMED Abstract]
- Andrieu N, Easton DF, Chang-Claude J, et al.: Effect of chest X-rays on the risk of breast cancer among BRCA1/2 mutation carriers in the international BRCA1/2 carrier cohort study: a report from the EMBRACE, GENEPSO, GEO-HEBON, and IBCCS Collaborators' Group. J Clin Oncol 24 (21): 3361-6, 2006.[PUBMED Abstract]
- Pijpe A, Andrieu N, Easton DF, et al.: Exposure to diagnostic radiation and risk of breast cancer among carriers of BRCA1/2 mutations: retrospective cohort study (GENE-RAD-RISK). BMJ 345: e5660, 2012.[PUBMED Abstract]
- Berrington de Gonzalez A, Berg CD, Visvanathan K, et al.: Estimated risk of radiation-induced breast cancer from mammographic screening for young BRCA mutation carriers. J Natl Cancer Inst 101 (3): 205-9, 2009.[PUBMED Abstract]
- Lowry KP, Lee JM, Kong CY, et al.: Annual screening strategies in BRCA1 and BRCA2 gene mutation carriers: a comparative effectiveness analysis. Cancer 118 (8): 2021-30, 2012.[PUBMED Abstract]
- National Comprehensive Cancer Network: NCCN Clinical Practice Guidelines in Oncology: Genetic/Familial High-Risk Assessment: Breast, Ovarian, and Pancreatic. Version 1.2020. Plymouth Meeting, Pa: National Comprehensive Cancer Network, 2019. Available online with free registration. Last accessed December 23, 2019.[PUBMED Abstract]
- Kriege M, Brekelmans CT, Boetes C, et al.: Efficacy of MRI and mammography for breast-cancer screening in women with a familial or genetic predisposition. N Engl J Med 351 (5): 427-37, 2004.[PUBMED Abstract]
- Lehman CD, Blume JD, Weatherall P, et al.: Screening women at high risk for breast cancer with mammography and magnetic resonance imaging. Cancer 103 (9): 1898-905, 2005.[PUBMED Abstract]
- Leach MO, Boggis CR, Dixon AK, et al.: Screening with magnetic resonance imaging and mammography of a UK population at high familial risk of breast cancer: a prospective multicentre cohort study (MARIBS). Lancet 365 (9473): 1769-78, 2005 May 21-27.[PUBMED Abstract]
- Warner E, Plewes DB, Hill KA, et al.: Surveillance of BRCA1 and BRCA2 mutation carriers with magnetic resonance imaging, ultrasound, mammography, and clinical breast examination. JAMA 292 (11): 1317-25, 2004.[PUBMED Abstract]
- Lehman CD, Isaacs C, Schnall MD, et al.: Cancer yield of mammography, MR, and US in high-risk women: prospective multi-institution breast cancer screening study. Radiology 244 (2): 381-8, 2007.[PUBMED Abstract]
- Sardanelli F, Podo F, D'Agnolo G, et al.: Multicenter comparative multimodality surveillance of women at genetic-familial high risk for breast cancer (HIBCRIT study): interim results. Radiology 242 (3): 698-715, 2007.[PUBMED Abstract]
- Kuhl C, Weigel S, Schrading S, et al.: Prospective multicenter cohort study to refine management recommendations for women at elevated familial risk of breast cancer: the EVA trial. J Clin Oncol 28 (9): 1450-7, 2010.[PUBMED Abstract]
- Shah P, Rosen M, Stopfer J, et al.: Prospective study of breast MRI in BRCA1 and BRCA2 mutation carriers: effect of mutation status on cancer incidence. Breast Cancer Res Treat 118 (3): 539-46, 2009.[PUBMED Abstract]
- Rijnsburger AJ, Obdeijn IM, Kaas R, et al.: BRCA1-associated breast cancers present differently from BRCA2-associated and familial cases: long-term follow-up of the Dutch MRISC Screening Study. J Clin Oncol 28 (36): 5265-73, 2010.[PUBMED Abstract]
- Weinstein SP, Localio AR, Conant EF, et al.: Multimodality screening of high-risk women: a prospective cohort study. J Clin Oncol 27 (36): 6124-8, 2009.[PUBMED Abstract]
- Sardanelli F, Podo F, Santoro F, et al.: Multicenter surveillance of women at high genetic breast cancer risk using mammography, ultrasonography, and contrast-enhanced magnetic resonance imaging (the high breast cancer risk italian 1 study): final results. Invest Radiol 46 (2): 94-105, 2011.[PUBMED Abstract]
- Lord SJ, Lei W, Craft P, et al.: A systematic review of the effectiveness of magnetic resonance imaging (MRI) as an addition to mammography and ultrasound in screening young women at high risk of breast cancer. Eur J Cancer 43 (13): 1905-17, 2007.[PUBMED Abstract]
- Obdeijn IM, Loo CE, Rijnsburger AJ, et al.: Assessment of false-negative cases of breast MR imaging in women with a familial or genetic predisposition. Breast Cancer Res Treat 119 (2): 399-407, 2010.[PUBMED Abstract]
- Saadatmand S, Geuzinge HA, Rutgers EJT, et al.: MRI versus mammography for breast cancer screening in women with familial risk (FaMRIsc): a multicentre, randomised, controlled trial. Lancet Oncol 20 (8): 1136-1147, 2019.[PUBMED Abstract]
- Heijnsdijk EA, Warner E, Gilbert FJ, et al.: Differences in natural history between breast cancers in BRCA1 and BRCA2 mutation carriers and effects of MRI screening-MRISC, MARIBS, and Canadian studies combined. Cancer Epidemiol Biomarkers Prev 21 (9): 1458-68, 2012.[PUBMED Abstract]
- Passaperuma K, Warner E, Causer PA, et al.: Long-term results of screening with magnetic resonance imaging in women with BRCA mutations. Br J Cancer 107 (1): 24-30, 2012.[PUBMED Abstract]
- Saadatmand S, Obdeijn IM, Rutgers EJ, et al.: Survival benefit in women with BRCA1 mutation or familial risk in the MRI screening study (MRISC). Int J Cancer 137 (7): 1729-38, 2015.[PUBMED Abstract]
- Saslow D, Boetes C, Burke W, et al.: American Cancer Society guidelines for breast screening with MRI as an adjunct to mammography. CA Cancer J Clin 57 (2): 75-89, 2007 Mar-Apr.[PUBMED Abstract]
- O'Driscoll D, Warren R, MacKay J, et al.: Screening with breast ultrasound in a population at moderate risk due to family history. J Med Screen 8 (2): 106-9, 2001.[PUBMED Abstract]
- Berg WA, Blume JD, Cormack JB, et al.: Combined screening with ultrasound and mammography vs mammography alone in women at elevated risk of breast cancer. JAMA 299 (18): 2151-63, 2008.[PUBMED Abstract]
- Giuliano AE, Boolbol S, Degnim A, et al.: Society of Surgical Oncology: position statement on prophylactic mastectomy. Approved by the Society of Surgical Oncology Executive Council, March 2007. Ann Surg Oncol 14 (9): 2425-7, 2007.[PUBMED Abstract]
- Hartmann LC, Sellers TA, Schaid DJ, et al.: Efficacy of bilateral prophylactic mastectomy in BRCA1 and BRCA2 gene mutation carriers. J Natl Cancer Inst 93 (21): 1633-7, 2001.[PUBMED Abstract]
- Meijers-Heijboer H, van Geel B, van Putten WL, et al.: Breast cancer after prophylactic bilateral mastectomy in women with a BRCA1 or BRCA2 mutation. N Engl J Med 345 (3): 159-64, 2001.[PUBMED Abstract]
- Hartmann LC, Schaid DJ, Woods JE, et al.: Efficacy of bilateral prophylactic mastectomy in women with a family history of breast cancer. N Engl J Med 340 (2): 77-84, 1999.[PUBMED Abstract]
- Schrag D, Kuntz KM, Garber JE, et al.: Decision analysis--effects of prophylactic mastectomy and oophorectomy on life expectancy among women with BRCA1 or BRCA2 mutations. N Engl J Med 336 (20): 1465-71, 1997.[PUBMED Abstract]
- Kurian AW, Munoz DF, Rust P, et al.: Online tool to guide decisions for BRCA1/2 mutation carriers. J Clin Oncol 30 (5): 497-506, 2012.[PUBMED Abstract]
- Unic I, Stalmeier PF, Verhoef LC, et al.: Assessment of the time-tradeoff values for prophylactic mastectomy of women with a suspected genetic predisposition to breast cancer. Med Decis Making 18 (3): 268-77, 1998 Jul-Sep.[PUBMED Abstract]
- Grann VR, Panageas KS, Whang W, et al.: Decision analysis of prophylactic mastectomy and oophorectomy in BRCA1-positive or BRCA2-positive patients. J Clin Oncol 16 (3): 979-85, 1998.[PUBMED Abstract]
- Tuttle TM, Habermann EB, Grund EH, et al.: Increasing use of contralateral prophylactic mastectomy for breast cancer patients: a trend toward more aggressive surgical treatment. J Clin Oncol 25 (33): 5203-9, 2007.[PUBMED Abstract]
- Jones NB, Wilson J, Kotur L, et al.: Contralateral prophylactic mastectomy for unilateral breast cancer: an increasing trend at a single institution. Ann Surg Oncol 16 (10): 2691-6, 2009.[PUBMED Abstract]
- Nichols HB, Berrington de González A, Lacey JV, et al.: Declining incidence of contralateral breast cancer in the United States from 1975 to 2006. J Clin Oncol 29 (12): 1564-9, 2011.[PUBMED Abstract]
- Fayanju OM, Stoll CR, Fowler S, et al.: Contralateral prophylactic mastectomy after unilateral breast cancer: a systematic review and meta-analysis. Ann Surg 260 (6): 1000-10, 2014.[PUBMED Abstract]
- Metcalfe K, Gershman S, Ghadirian P, et al.: Contralateral mastectomy and survival after breast cancer in carriers of BRCA1 and BRCA2 mutations: retrospective analysis. BMJ 348: g226, 2014.[PUBMED Abstract]
- Chiba A, Hoskin TL, Hallberg EJ, et al.: Impact that Timing of Genetic Mutation Diagnosis has on Surgical Decision Making and Outcome for BRCA1/BRCA2 Mutation Carriers with Breast Cancer. Ann Surg Oncol 23 (10): 3232-8, 2016.[PUBMED Abstract]
- van Sprundel TC, Schmidt MK, Rookus MA, et al.: Risk reduction of contralateral breast cancer and survival after contralateral prophylactic mastectomy in BRCA1 or BRCA2 mutation carriers. Br J Cancer 93 (3): 287-92, 2005.[PUBMED Abstract]
- Evans DG, Baildam AD, Anderson E, et al.: Risk reducing mastectomy: outcomes in 10 European centres. J Med Genet 46 (4): 254-8, 2009.[PUBMED Abstract]
- Heemskerk-Gerritsen BA, Rookus MA, Aalfs CM, et al.: Improved overall survival after contralateral risk-reducing mastectomy in BRCA1/2 mutation carriers with a history of unilateral breast cancer: a prospective analysis. Int J Cancer 136 (3): 668-77, 2015.[PUBMED Abstract]
- Jatoi I, Parsons HM: Contralateral prophylactic mastectomy and its association with reduced mortality: evidence for selection bias. Breast Cancer Res Treat 148 (2): 389-96, 2014.[PUBMED Abstract]
- Yao K, Liederbach E, Tang R, et al.: Nipple-sparing mastectomy in BRCA1/2 mutation carriers: an interim analysis and review of the literature. Ann Surg Oncol 22 (2): 370-6, 2015.[PUBMED Abstract]
- Manning AT, Wood C, Eaton A, et al.: Nipple-sparing mastectomy in patients with BRCA1/2 mutations and variants of uncertain significance. Br J Surg 102 (11): 1354-9, 2015.[PUBMED Abstract]
- Kauff ND, Brogi E, Scheuer L, et al.: Epithelial lesions in prophylactic mastectomy specimens from women with BRCA mutations. Cancer 97 (7): 1601-8, 2003.[PUBMED Abstract]
- Hoogerbrugge N, Bult P, de Widt-Levert LM, et al.: High prevalence of premalignant lesions in prophylactically removed breasts from women at hereditary risk for breast cancer. J Clin Oncol 21 (1): 41-5, 2003.[PUBMED Abstract]
- Kroiss R, Winkler V, Kalteis K, et al.: Prevalence of pre-malignant and malignant lesions in prophylactic mastectomy specimens of BRCA1 mutation carriers: comparison with a control group. J Cancer Res Clin Oncol 134 (10): 1113-21, 2008.[PUBMED Abstract]
- Scott CI, Iorgulescu DG, Thorne HJ, et al.: Clinical, pathological and genetic features of women at high familial risk of breast cancer undergoing prophylactic mastectomy. Clin Genet 64 (2): 111-21, 2003.[PUBMED Abstract]
- Olson JE, Sellers TA, Iturria SJ, et al.: Bilateral oophorectomy and breast cancer risk reduction among women with a family history. Cancer Detect Prev 28 (5): 357-60, 2004.[PUBMED Abstract]
- Rebbeck TR, Lynch HT, Neuhausen SL, et al.: Prophylactic oophorectomy in carriers of BRCA1 or BRCA2 mutations. N Engl J Med 346 (21): 1616-22, 2002.[PUBMED Abstract]
- Struewing JP, Watson P, Easton DF, et al.: Prophylactic oophorectomy in inherited breast/ovarian cancer families. J Natl Cancer Inst Monogr (17): 33-5, 1995.[PUBMED Abstract]
- Rebbeck TR, Levin AM, Eisen A, et al.: Breast cancer risk after bilateral prophylactic oophorectomy in BRCA1 mutation carriers. J Natl Cancer Inst 91 (17): 1475-9, 1999.[PUBMED Abstract]
- Kauff ND, Satagopan JM, Robson ME, et al.: Risk-reducing salpingo-oophorectomy in women with a BRCA1 or BRCA2 mutation. N Engl J Med 346 (21): 1609-15, 2002.[PUBMED Abstract]
- Rebbeck TR, Kauff ND, Domchek SM: Meta-analysis of risk reduction estimates associated with risk-reducing salpingo-oophorectomy in BRCA1 or BRCA2 mutation carriers. J Natl Cancer Inst 101 (2): 80-7, 2009.[PUBMED Abstract]
- Heemskerk-Gerritsen BA, Seynaeve C, van Asperen CJ, et al.: Breast cancer risk after salpingo-oophorectomy in healthy BRCA1/2 mutation carriers: revisiting the evidence for risk reduction. J Natl Cancer Inst 107 (5): , 2015.[PUBMED Abstract]
- Chai X, Domchek S, Kauff N, et al.: RE: Breast Cancer Risk After Salpingo-Oophorectomy in Healthy BRCA1/2 Mutation Carriers: Revisiting the Evidence for Risk Reduction. J Natl Cancer Inst 107 (9): , 2015.[PUBMED Abstract]
- Metcalfe K, Lynch HT, Foulkes WD, et al.: Effect of Oophorectomy on Survival After Breast Cancer in BRCA1 and BRCA2 Mutation Carriers. JAMA Oncol 1 (3): 306-13, 2015.[PUBMED Abstract]
- Kotsopoulos J, Huzarski T, Gronwald J, et al.: Bilateral Oophorectomy and Breast Cancer Risk in BRCA1 and BRCA2 Mutation Carriers. J Natl Cancer Inst 109 (1): , 2017.[PUBMED Abstract]
- Terry MB, Daly MB, Phillips KA, et al.: Risk-Reducing Oophorectomy and Breast Cancer Risk Across the Spectrum of Familial Risk. J Natl Cancer Inst 111 (3): 331-334, 2019.[PUBMED Abstract]
- Marchetti C, De Felice F, Palaia I, et al.: Risk-reducing salpingo-oophorectomy: a meta-analysis on impact on ovarian cancer risk and all cause mortality in BRCA 1 and BRCA 2 mutation carriers. BMC Womens Health 14: 150, 2014.[PUBMED Abstract]
- Fisher B, Costantino JP, Wickerham DL, et al.: Tamoxifen for prevention of breast cancer: report of the National Surgical Adjuvant Breast and Bowel Project P-1 Study. J Natl Cancer Inst 90 (18): 1371-88, 1998.[PUBMED Abstract]
- Veronesi U, Maisonneuve P, Costa A, et al.: Prevention of breast cancer with tamoxifen: preliminary findings from the Italian randomised trial among hysterectomised women. Italian Tamoxifen Prevention Study. Lancet 352 (9122): 93-7, 1998.[PUBMED Abstract]
- Powles T, Eeles R, Ashley S, et al.: Interim analysis of the incidence of breast cancer in the Royal Marsden Hospital tamoxifen randomised chemoprevention trial. Lancet 352 (9122): 98-101, 1998.[PUBMED Abstract]
- Cuzick J, Sestak I, Cawthorn S, et al.: Tamoxifen for prevention of breast cancer: extended long-term follow-up of the IBIS-I breast cancer prevention trial. Lancet Oncol 16 (1): 67-75, 2015.[PUBMED Abstract]
- King MC, Wieand S, Hale K, et al.: Tamoxifen and breast cancer incidence among women with inherited mutations in BRCA1 and BRCA2: National Surgical Adjuvant Breast and Bowel Project (NSABP-P1) Breast Cancer Prevention Trial. JAMA 286 (18): 2251-6, 2001.[PUBMED Abstract]
- Narod SA, Brunet JS, Ghadirian P, et al.: Tamoxifen and risk of contralateral breast cancer in BRCA1 and BRCA2 mutation carriers: a case-control study. Hereditary Breast Cancer Clinical Study Group. Lancet 356 (9245): 1876-81, 2000.[PUBMED Abstract]
- Pierce LJ, Levin AM, Rebbeck TR, et al.: Ten-year multi-institutional results of breast-conserving surgery and radiotherapy in BRCA1/2-associated stage I/II breast cancer. J Clin Oncol 24 (16): 2437-43, 2006.[PUBMED Abstract]
- Gronwald J, Tung N, Foulkes WD, et al.: Tamoxifen and contralateral breast cancer in BRCA1 and BRCA2 carriers: an update. Int J Cancer 118 (9): 2281-4, 2006.[PUBMED Abstract]
- Phillips KA, Milne RL, Rookus MA, et al.: Tamoxifen and risk of contralateral breast cancer for BRCA1 and BRCA2 mutation carriers. J Clin Oncol 31 (25): 3091-9, 2013.[PUBMED Abstract]
- Vogel VG, Costantino JP, Wickerham DL, et al.: Effects of tamoxifen vs raloxifene on the risk of developing invasive breast cancer and other disease outcomes: the NSABP Study of Tamoxifen and Raloxifene (STAR) P-2 trial. JAMA 295 (23): 2727-41, 2006.[PUBMED Abstract]
- Land SR, Wickerham DL, Costantino JP, et al.: Patient-reported symptoms and quality of life during treatment with tamoxifen or raloxifene for breast cancer prevention: the NSABP Study of Tamoxifen and Raloxifene (STAR) P-2 trial. JAMA 295 (23): 2742-51, 2006.[PUBMED Abstract]
- Reding KW, Bernstein JL, Langholz BM, et al.: Adjuvant systemic therapy for breast cancer in BRCA1/BRCA2 mutation carriers in a population-based study of risk of contralateral breast cancer. Breast Cancer Res Treat 123 (2): 491-8, 2010.[PUBMED Abstract]
- Vicus D, Rosen B, Lubinski J, et al.: Tamoxifen and the risk of ovarian cancer in BRCA1 mutation carriers. Gynecol Oncol 115 (1): 135-7, 2009.[PUBMED Abstract]
- Colditz GA, Rosner BA, Speizer FE: Risk factors for breast cancer according to family history of breast cancer. For the Nurses' Health Study Research Group. J Natl Cancer Inst 88 (6): 365-71, 1996.[PUBMED Abstract]
- Narod S, Lynch H, Conway T, et al.: Increasing incidence of breast cancer in family with BRCA1 mutation. Lancet 341 (8852): 1101-2, 1993.[PUBMED Abstract]
- Narod SA, Goldgar D, Cannon-Albright L, et al.: Risk modifiers in carriers of BRCA1 mutations. Int J Cancer 64 (6): 394-8, 1995.[PUBMED Abstract]
- McCredie M, Paul C, Skegg DC, et al.: Family history and risk of breast cancer in New Zealand. Int J Cancer 73 (4): 503-7, 1997.[PUBMED Abstract]
- Jernström H, Lerman C, Ghadirian P, et al.: Pregnancy and risk of early breast cancer in carriers of BRCA1 and BRCA2. Lancet 354 (9193): 1846-50, 1999.[PUBMED Abstract]
- Cullinane CA, Lubinski J, Neuhausen SL, et al.: Effect of pregnancy as a risk factor for breast cancer in BRCA1/BRCA2 mutation carriers. Int J Cancer 117 (6): 988-91, 2005.[PUBMED Abstract]
- Friedman E, Kotsopoulos J, Lubinski J, et al.: Spontaneous and therapeutic abortions and the risk of breast cancer among BRCA mutation carriers. Breast Cancer Res 8 (2): R15, 2006.[PUBMED Abstract]
- Milne RL, Osorio A, Ramón y Cajal T, et al.: Parity and the risk of breast and ovarian cancer in BRCA1 and BRCA2 mutation carriers. Breast Cancer Res Treat 119 (1): 221-32, 2010.[PUBMED Abstract]
- Antoniou AC, Shenton A, Maher ER, et al.: Parity and breast cancer risk among BRCA1 and BRCA2 mutation carriers. Breast Cancer Res 8 (6): R72, 2006.[PUBMED Abstract]
- Andrieu N, Goldgar DE, Easton DF, et al.: Pregnancies, breast-feeding, and breast cancer risk in the International BRCA1/2 Carrier Cohort Study (IBCCS). J Natl Cancer Inst 98 (8): 535-44, 2006.[PUBMED Abstract]
- Col: Breast cancer and breastfeeding: collaborative reanalysis of individual data from 47 epidemiological studies in 30 countries, including 50302 women with breast cancer and 96973 women without the disease. Lancet 360 (9328): 187-95, 2002.[PUBMED Abstract]
- Jernström H, Lubinski J, Lynch HT, et al.: Breast-feeding and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 96 (14): 1094-8, 2004.[PUBMED Abstract]
- Breast cancer and hormonal contraceptives: collaborative reanalysis of individual data on 53 297 women with breast cancer and 100 239 women without breast cancer from 54 epidemiological studies. Collaborative Group on Hormonal Factors in Breast Cancer. Lancet 347 (9017): 1713-27, 1996.[PUBMED Abstract]
- Ursin G, Henderson BE, Haile RW, et al.: Does oral contraceptive use increase the risk of breast cancer in women with BRCA1/BRCA2 mutations more than in other women? Cancer Res 57 (17): 3678-81, 1997.[PUBMED Abstract]
- Jernström H, Loman N, Johannsson OT, et al.: Impact of teenage oral contraceptive use in a population-based series of early-onset breast cancer cases who have undergone BRCA mutation testing. Eur J Cancer 41 (15): 2312-20, 2005.[PUBMED Abstract]
- Iodice S, Barile M, Rotmensz N, et al.: Oral contraceptive use and breast or ovarian cancer risk in BRCA1/2 carriers: a meta-analysis. Eur J Cancer 46 (12): 2275-84, 2010.[PUBMED Abstract]
- Brohet RM, Goldgar DE, Easton DF, et al.: Oral contraceptives and breast cancer risk in the international BRCA1/2 carrier cohort study: a report from EMBRACE, GENEPSO, GEO-HEBON, and the IBCCS Collaborating Group. J Clin Oncol 25 (25): 3831-6, 2007.[PUBMED Abstract]
- Haile RW, Thomas DC, McGuire V, et al.: BRCA1 and BRCA2 mutation carriers, oral contraceptive use, and breast cancer before age 50. Cancer Epidemiol Biomarkers Prev 15 (10): 1863-70, 2006.[PUBMED Abstract]
- Narod SA, Dubé MP, Klijn J, et al.: Oral contraceptives and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 94 (23): 1773-9, 2002.[PUBMED Abstract]
- Kotsopoulos J, Lubinski J, Moller P, et al.: Timing of oral contraceptive use and the risk of breast cancer in BRCA1 mutation carriers. Breast Cancer Res Treat 143 (3): 579-86, 2014.[PUBMED Abstract]
- Narod SA, Risch H, Moslehi R, et al.: Oral contraceptives and the risk of hereditary ovarian cancer. Hereditary Ovarian Cancer Clinical Study Group. N Engl J Med 339 (7): 424-8, 1998.[PUBMED Abstract]
- Chen CL, Weiss NS, Newcomb P, et al.: Hormone replacement therapy in relation to breast cancer. JAMA 287 (6): 734-41, 2002.[PUBMED Abstract]
- Writing Group for the Women's Health Initiative Investigators: Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women's Health Initiative randomized controlled trial. JAMA 288 (3): 321-33, 2002.[PUBMED Abstract]
- Chlebowski RT, Hendrix SL, Langer RD, et al.: Influence of estrogen plus progestin on breast cancer and mammography in healthy postmenopausal women: the Women's Health Initiative Randomized Trial. JAMA 289 (24): 3243-53, 2003.[PUBMED Abstract]
- Chlebowski RT, Kuller LH, Prentice RL, et al.: Breast cancer after use of estrogen plus progestin in postmenopausal women. N Engl J Med 360 (6): 573-87, 2009.[PUBMED Abstract]
- Schuurman AG, van den Brandt PA, Goldbohm RA: Exogenous hormone use and the risk of postmenopausal breast cancer: results from The Netherlands Cohort Study. Cancer Causes Control 6 (5): 416-24, 1995.[PUBMED Abstract]
- Steinberg KK, Thacker SB, Smith SJ, et al.: A meta-analysis of the effect of estrogen replacement therapy on the risk of breast cancer. JAMA 265 (15): 1985-90, 1991.[PUBMED Abstract]
- Colditz GA, Egan KM, Stampfer MJ: Hormone replacement therapy and risk of breast cancer: results from epidemiologic studies. Am J Obstet Gynecol 168 (5): 1473-80, 1993.[PUBMED Abstract]
- Sellers TA, Mink PJ, Cerhan JR, et al.: The role of hormone replacement therapy in the risk for breast cancer and total mortality in women with a family history of breast cancer. Ann Intern Med 127 (11): 973-80, 1997.[PUBMED Abstract]
- Stanford JL, Weiss NS, Voigt LF, et al.: Combined estrogen and progestin hormone replacement therapy in relation to risk of breast cancer in middle-aged women. JAMA 274 (2): 137-42, 1995.[PUBMED Abstract]
- Gorsky RD, Koplan JP, Peterson HB, et al.: Relative risks and benefits of long-term estrogen replacement therapy: a decision analysis. Obstet Gynecol 83 (2): 161-6, 1994.[PUBMED Abstract]
- Rebbeck TR, Friebel T, Wagner T, et al.: Effect of short-term hormone replacement therapy on breast cancer risk reduction after bilateral prophylactic oophorectomy in BRCA1 and BRCA2 mutation carriers: the PROSE Study Group. J Clin Oncol 23 (31): 7804-10, 2005.[PUBMED Abstract]
- Eisen A, Lubinski J, Gronwald J, et al.: Hormone therapy and the risk of breast cancer in BRCA1 mutation carriers. J Natl Cancer Inst 100 (19): 1361-7, 2008.[PUBMED Abstract]
- Kotsopoulos J, Huzarski T, Gronwald J, et al.: Hormone replacement therapy after menopause and risk of breast cancer in BRCA1 mutation carriers: a case-control study. Breast Cancer Res Treat 155 (2): 365-73, 2016.[PUBMED Abstract]
- Chlebowski RT, Prentice RL: Menopausal hormone therapy in BRCA1 mutation carriers: uncertainty and caution. J Natl Cancer Inst 100 (19): 1341-3, 2008.[PUBMED Abstract]
- Buys SS, Partridge E, Black A, et al.: Effect of screening on ovarian cancer mortality: the Prostate, Lung, Colorectal and Ovarian (PLCO) Cancer Screening Randomized Controlled Trial. JAMA 305 (22): 2295-303, 2011.[PUBMED Abstract]
- Hermsen BB, Olivier RI, Verheijen RH, et al.: No efficacy of annual gynaecological screening in BRCA1/2 mutation carriers; an observational follow-up study. Br J Cancer 96 (9): 1335-42, 2007.[PUBMED Abstract]
- Stirling D, Evans DG, Pichert G, et al.: Screening for familial ovarian cancer: failure of current protocols to detect ovarian cancer at an early stage according to the international Federation of gynecology and obstetrics system. J Clin Oncol 23 (24): 5588-96, 2005.[PUBMED Abstract]
- Olivier RI, Lubsen-Brandsma MA, Verhoef S, et al.: CA125 and transvaginal ultrasound monitoring in high-risk women cannot prevent the diagnosis of advanced ovarian cancer. Gynecol Oncol 100 (1): 20-6, 2006.[PUBMED Abstract]
- Meeuwissen PA, Seynaeve C, Brekelmans CT, et al.: Outcome of surveillance and prophylactic salpingo-oophorectomy in asymptomatic women at high risk for ovarian cancer. Gynecol Oncol 97 (2): 476-82, 2005.[PUBMED Abstract]
- Dørum A, Kristensen GB, Abeler VM, et al.: Early detection of familial ovarian cancer. Eur J Cancer 32A (10): 1645-51, 1996.[PUBMED Abstract]
- Tailor A, Bourne TH, Campbell S, et al.: Results from an ultrasound-based familial ovarian cancer screening clinic: a 10-year observational study. Ultrasound Obstet Gynecol 21 (4): 378-85, 2003.[PUBMED Abstract]
- Karlan BY, Raffel LJ, Crvenkovic G, et al.: A multidisciplinary approach to the early detection of ovarian carcinoma: rationale, protocol design, and early results. Am J Obstet Gynecol 169 (3): 494-501, 1993.[PUBMED Abstract]
- Muto MG, Cramer DW, Brown DL, et al.: Screening for ovarian cancer: the preliminary experience of a familial ovarian cancer center. Gynecol Oncol 51 (1): 12-20, 1993.[PUBMED Abstract]
- Liede A, Karlan BY, Baldwin RL, et al.: Cancer incidence in a population of Jewish women at risk of ovarian cancer. J Clin Oncol 20 (6): 1570-7, 2002.[PUBMED Abstract]
- Laframboise S, Nedelcu R, Murphy J, et al.: Use of CA-125 and ultrasound in high-risk women. Int J Gynecol Cancer 12 (1): 86-91, 2002 Jan-Feb.[PUBMED Abstract]
- Woodward ER, Sleightholme HV, Considine AM, et al.: Annual surveillance by CA125 and transvaginal ultrasound for ovarian cancer in both high-risk and population risk women is ineffective. BJOG 114 (12): 1500-9, 2007.[PUBMED Abstract]
- van der Velde NM, Mourits MJ, Arts HJ, et al.: Time to stop ovarian cancer screening in BRCA1/2 mutation carriers? Int J Cancer 124 (4): 919-23, 2009.[PUBMED Abstract]
- Rosenthal AN, Fraser L, Manchanda R, et al.: Results of annual screening in phase I of the United Kingdom familial ovarian cancer screening study highlight the need for strict adherence to screening schedule. J Clin Oncol 31 (1): 49-57, 2013.[PUBMED Abstract]
- Evans DG, Gaarenstroom KN, Stirling D, et al.: Screening for familial ovarian cancer: poor survival of BRCA1/2 related cancers. J Med Genet 46 (9): 593-7, 2009.[PUBMED Abstract]
- NIH consensus conference. Ovarian cancer. Screening, treatment, and follow-up. NIH Consensus Development Panel on Ovarian Cancer. JAMA 273 (6): 491-7, 1995.[PUBMED Abstract]
- Pepe MS, Etzioni R, Feng Z, et al.: Phases of biomarker development for early detection of cancer. J Natl Cancer Inst 93 (14): 1054-61, 2001.[PUBMED Abstract]
- Grosse SD, Khoury MJ: What is the clinical utility of genetic testing? Genet Med 8 (7): 448-50, 2006.[PUBMED Abstract]
- Finch A, Shaw P, Rosen B, et al.: Clinical and pathologic findings of prophylactic salpingo-oophorectomies in 159 BRCA1 and BRCA2 carriers. Gynecol Oncol 100 (1): 58-64, 2006.[PUBMED Abstract]
- Andersen MR, Goff BA, Lowe KA, et al.: Combining a symptoms index with CA 125 to improve detection of ovarian cancer. Cancer 113 (3): 484-9, 2008.[PUBMED Abstract]
- Skates SJ, Xu FJ, Yu YH, et al.: Toward an optimal algorithm for ovarian cancer screening with longitudinal tumor markers. Cancer 76 (10 Suppl): 2004-10, 1995.[PUBMED Abstract]
- Skates SJ, Menon U, MacDonald N, et al.: Calculation of the risk of ovarian cancer from serial CA-125 values for preclinical detection in postmenopausal women. J Clin Oncol 21 (10 Suppl): 206s-210s, 2003.[PUBMED Abstract]
- Menon U, Skates SJ, Lewis S, et al.: Prospective study using the risk of ovarian cancer algorithm to screen for ovarian cancer. J Clin Oncol 23 (31): 7919-26, 2005.[PUBMED Abstract]
- Greene MH, Piedmonte M, Alberts D, et al.: A prospective study of risk-reducing salpingo-oophorectomy and longitudinal CA-125 screening among women at increased genetic risk of ovarian cancer: design and baseline characteristics: a Gynecologic Oncology Group study. Cancer Epidemiol Biomarkers Prev 17 (3): 594-604, 2008.[PUBMED Abstract]
- Gagnon A, Ye B: Discovery and application of protein biomarkers for ovarian cancer. Curr Opin Obstet Gynecol 20 (1): 9-13, 2008.[PUBMED Abstract]
- Hennessy BT, Murph M, Nanjundan M, et al.: Ovarian cancer: linking genomics to new target discovery and molecular markers--the way ahead. Adv Exp Med Biol 617: 23-40, 2008.[PUBMED Abstract]
- Badgwell D, Bast RC: Early detection of ovarian cancer. Dis Markers 23 (5-6): 397-410, 2007.[PUBMED Abstract]
- Petricoin EF, Ardekani AM, Hitt BA, et al.: Use of proteomic patterns in serum to identify ovarian cancer. Lancet 359 (9306): 572-7, 2002.[PUBMED Abstract]
- Zhang Z, Bast RC, Yu Y, et al.: Three biomarkers identified from serum proteomic analysis for the detection of early stage ovarian cancer. Cancer Res 64 (16): 5882-90, 2004.[PUBMED Abstract]
- Koehn H, Oehler MK: Proteins' promise--progress and challenges in ovarian cancer proteomics. Menopause Int 13 (4): 148-53, 2007.[PUBMED Abstract]
- Visintin I, Feng Z, Longton G, et al.: Diagnostic markers for early detection of ovarian cancer. Clin Cancer Res 14 (4): 1065-72, 2008.[PUBMED Abstract]
- Simon R: Roadmap for developing and validating therapeutically relevant genomic classifiers. J Clin Oncol 23 (29): 7332-41, 2005.[PUBMED Abstract]
- Rutter JL, Wacholder S, Chetrit A, et al.: Gynecologic surgeries and risk of ovarian cancer in women with BRCA1 and BRCA2 Ashkenazi founder mutations: an Israeli population-based case-control study. J Natl Cancer Inst 95 (14): 1072-8, 2003.[PUBMED Abstract]
- Kotsopoulos J, Lubinski J, Lynch HT, et al.: Oophorectomy after menopause and the risk of breast cancer in BRCA1 and BRCA2 mutation carriers. Cancer Epidemiol Biomarkers Prev 21 (7): 1089-96, 2012.[PUBMED Abstract]
- Sherman ME, Piedmonte M, Mai PL, et al.: Pathologic findings at risk-reducing salpingo-oophorectomy: primary results from Gynecologic Oncology Group Trial GOG-0199. J Clin Oncol 32 (29): 3275-83, 2014.[PUBMED Abstract]
- Domchek SM, Friebel TM, Neuhausen SL, et al.: Mortality after bilateral salpingo-oophorectomy in BRCA1 and BRCA2 mutation carriers: a prospective cohort study. Lancet Oncol 7 (3): 223-9, 2006.[PUBMED Abstract]
- Leeper K, Garcia R, Swisher E, et al.: Pathologic findings in prophylactic oophorectomy specimens in high-risk women. Gynecol Oncol 87 (1): 52-6, 2002.[PUBMED Abstract]
- Olivier RI, van Beurden M, Lubsen MA, et al.: Clinical outcome of prophylactic oophorectomy in BRCA1/BRCA2 mutation carriers and events during follow-up. Br J Cancer 90 (8): 1492-7, 2004.[PUBMED Abstract]
- Colgan TJ, Murphy J, Cole DE, et al.: Occult carcinoma in prophylactic oophorectomy specimens: prevalence and association with BRCA germline mutation status. Am J Surg Pathol 25 (10): 1283-9, 2001.[PUBMED Abstract]
- Powell CB, Kenley E, Chen LM, et al.: Risk-reducing salpingo-oophorectomy in BRCA mutation carriers: role of serial sectioning in the detection of occult malignancy. J Clin Oncol 23 (1): 127-32, 2005.[PUBMED Abstract]
- Callahan MJ, Crum CP, Medeiros F, et al.: Primary fallopian tube malignancies in BRCA-positive women undergoing surgery for ovarian cancer risk reduction. J Clin Oncol 25 (25): 3985-90, 2007.[PUBMED Abstract]
- Domchek SM, Friebel TM, Garber JE, et al.: Occult ovarian cancers identified at risk-reducing salpingo-oophorectomy in a prospective cohort of BRCA1/2 mutation carriers. Breast Cancer Res Treat 124 (1): 195-203, 2010.[PUBMED Abstract]
- Powell CB, Chen LM, McLennan J, et al.: Risk-reducing salpingo-oophorectomy (RRSO) in BRCA mutation carriers: experience with a consecutive series of 111 patients using a standardized surgical-pathological protocol. Int J Gynecol Cancer 21 (5): 846-51, 2011.[PUBMED Abstract]
- Piek JM, van Diest PJ, Zweemer RP, et al.: Dysplastic changes in prophylactically removed Fallopian tubes of women predisposed to developing ovarian cancer. J Pathol 195 (4): 451-6, 2001.[PUBMED Abstract]
- Paley PJ, Swisher EM, Garcia RL, et al.: Occult cancer of the fallopian tube in BRCA-1 germline mutation carriers at prophylactic oophorectomy: a case for recommending hysterectomy at surgical prophylaxis. Gynecol Oncol 80 (2): 176-80, 2001.[PUBMED Abstract]
- Rose PG, Shrigley R, Wiesner GL: Germline BRCA2 mutation in a patient with fallopian tube carcinoma: a case report. Gynecol Oncol 77 (2): 319-20, 2000.[PUBMED Abstract]
- Zweemer RP, van Diest PJ, Verheijen RH, et al.: Molecular evidence linking primary cancer of the fallopian tube to BRCA1 germline mutations. Gynecol Oncol 76 (1): 45-50, 2000.[PUBMED Abstract]
- Piek JM, Torrenga B, Hermsen B, et al.: Histopathological characteristics of BRCA1- and BRCA2-associated intraperitoneal cancer: a clinic-based study. Fam Cancer 2 (2): 73-8, 2003.[PUBMED Abstract]
- Levine DA, Argenta PA, Yee CJ, et al.: Fallopian tube and primary peritoneal carcinomas associated with BRCA mutations. J Clin Oncol 21 (22): 4222-7, 2003.[PUBMED Abstract]
- Aziz S, Kuperstein G, Rosen B, et al.: A genetic epidemiological study of carcinoma of the fallopian tube. Gynecol Oncol 80 (3): 341-5, 2001.[PUBMED Abstract]
- Kindelberger DW, Lee Y, Miron A, et al.: Intraepithelial carcinoma of the fimbria and pelvic serous carcinoma: Evidence for a causal relationship. Am J Surg Pathol 31 (2): 161-9, 2007.[PUBMED Abstract]
- Rabban JT, Krasik E, Chen LM, et al.: Multistep level sections to detect occult fallopian tube carcinoma in risk-reducing salpingo-oophorectomies from women with BRCA mutations: implications for defining an optimal specimen dissection protocol. Am J Surg Pathol 33 (12): 1878-85, 2009.[PUBMED Abstract]
- Society of Gynecologic Oncologists Clinical Practice Committee Statement on Prophylactic Salpingo-oophorectomy. Gynecol Oncol 98 (2): 179-81, 2005.[PUBMED Abstract]
- Chen KT, Schooley JL, Flam MS: Peritoneal carcinomatosis after prophylactic oophorectomy in familial ovarian cancer syndrome. Obstet Gynecol 66 (3 Suppl): 93S-94S, 1985.[PUBMED Abstract]
- Lynch HT, Bewtra C, Lynch JF: Familial ovarian carcinoma. Clinical nuances. Am J Med 81 (6): 1073-6, 1986.[PUBMED Abstract]
- Lynch HT, Watson P, Bewtra C, et al.: Hereditary ovarian cancer. Heterogeneity in age at diagnosis. Cancer 67 (5): 1460-6, 1991.[PUBMED Abstract]
- Tobacman JK, Greene MH, Tucker MA, et al.: Intra-abdominal carcinomatosis after prophylactic oophorectomy in ovarian-cancer-prone families. Lancet 2 (8302): 795-7, 1982.[PUBMED Abstract]
- Truong LD, Maccato ML, Awalt H, et al.: Serous surface carcinoma of the peritoneum: a clinicopathologic study of 22 cases. Hum Pathol 21 (1): 99-110, 1990.[PUBMED Abstract]
- Piver MS, Jishi MF, Tsukada Y, et al.: Primary peritoneal carcinoma after prophylactic oophorectomy in women with a family history of ovarian cancer. A report of the Gilda Radner Familial Ovarian Cancer Registry. Cancer 71 (9): 2751-5, 1993.[PUBMED Abstract]
- Casey MJ, Synder C, Bewtra C, et al.: Intra-abdominal carcinomatosis after prophylactic oophorectomy in women of hereditary breast ovarian cancer syndrome kindreds associated with BRCA1 and BRCA2 mutations. Gynecol Oncol 97 (2): 457-67, 2005.[PUBMED Abstract]
- Finch A, Beiner M, Lubinski J, et al.: Salpingo-oophorectomy and the risk of ovarian, fallopian tube, and peritoneal cancers in women with a BRCA1 or BRCA2 Mutation. JAMA 296 (2): 185-92, 2006.[PUBMED Abstract]
- Powell CB, Swisher EM, Cass I, et al.: Long term follow up of BRCA1 and BRCA2 mutation carriers with unsuspected neoplasia identified at risk reducing salpingo-oophorectomy. Gynecol Oncol 129 (2): 364-71, 2013.[PUBMED Abstract]
- Zakhour M, Danovitch Y, Lester J, et al.: Occult and subsequent cancer incidence following risk-reducing surgery in BRCA mutation carriers. Gynecol Oncol 143 (2): 231-235, 2016.[PUBMED Abstract]
- Chen S, Iversen ES, Friebel T, et al.: Characterization of BRCA1 and BRCA2 mutations in a large United States sample. J Clin Oncol 24 (6): 863-71, 2006.[PUBMED Abstract]
- Antoniou A, Pharoah PD, Narod S, et al.: Average risks of breast and ovarian cancer associated with BRCA1 or BRCA2 mutations detected in case Series unselected for family history: a combined analysis of 22 studies. Am J Hum Genet 72 (5): 1117-30, 2003.[PUBMED Abstract]
- Risch HA, McLaughlin JR, Cole DE, et al.: Population BRCA1 and BRCA2 mutation frequencies and cancer penetrances: a kin-cohort study in Ontario, Canada. J Natl Cancer Inst 98 (23): 1694-706, 2006.[PUBMED Abstract]
- Lavie O, Hornreich G, Ben-Arie A, et al.: BRCA germline mutations in Jewish women with uterine serous papillary carcinoma. Gynecol Oncol 92 (2): 521-4, 2004.[PUBMED Abstract]
- Goshen R, Chu W, Elit L, et al.: Is uterine papillary serous adenocarcinoma a manifestation of the hereditary breast-ovarian cancer syndrome? Gynecol Oncol 79 (3): 477-81, 2000.[PUBMED Abstract]
- Beiner ME, Finch A, Rosen B, et al.: The risk of endometrial cancer in women with BRCA1 and BRCA2 mutations. A prospective study. Gynecol Oncol 104 (1): 7-10, 2007.[PUBMED Abstract]
- Segev Y, Iqbal J, Lubinski J, et al.: The incidence of endometrial cancer in women with BRCA1 and BRCA2 mutations: an international prospective cohort study. Gynecol Oncol 130 (1): 127-31, 2013.[PUBMED Abstract]
- Levine DA, Lin O, Barakat RR, et al.: Risk of endometrial carcinoma associated with BRCA mutation. Gynecol Oncol 80 (3): 395-8, 2001.[PUBMED Abstract]
- Karlan BY: Defining cancer risks for BRCA germline mutation carriers: implications for surgical prophylaxis. Gynecol Oncol 92 (2): 519-20, 2004.[PUBMED Abstract]
- Biron-Shental T, Drucker L, Altaras M, et al.: High incidence of BRCA1-2 germline mutations, previous breast cancer and familial cancer history in Jewish patients with uterine serous papillary carcinoma. Eur J Surg Oncol 32 (10): 1097-100, 2006.[PUBMED Abstract]
- Lu KH, Kauff ND: Does a BRCA mutation plus tamoxifen equal hysterectomy? Gynecol Oncol 104 (1): 3-4, 2007.[PUBMED Abstract]
- Madalinska JB, Hollenstein J, Bleiker E, et al.: Quality-of-life effects of prophylactic salpingo-oophorectomy versus gynecologic screening among women at increased risk of hereditary ovarian cancer. J Clin Oncol 23 (28): 6890-8, 2005.[PUBMED Abstract]
- Rocca WA, Grossardt BR, de Andrade M, et al.: Survival patterns after oophorectomy in premenopausal women: a population-based cohort study. Lancet Oncol 7 (10): 821-8, 2006.[PUBMED Abstract]
- Rocca WA, Bower JH, Maraganore DM, et al.: Increased risk of parkinsonism in women who underwent oophorectomy before menopause. Neurology 70 (3): 200-9, 2008.[PUBMED Abstract]
- Shuster LT, Rhodes DJ, Gostout BS, et al.: Premature menopause or early menopause: long-term health consequences. Maturitas 65 (2): 161-6, 2010.[PUBMED Abstract]
- Parker WH, Broder MS, Chang E, et al.: Ovarian conservation at the time of hysterectomy and long-term health outcomes in the nurses' health study. Obstet Gynecol 113 (5): 1027-37, 2009.[PUBMED Abstract]
- Rivera CM, Grossardt BR, Rhodes DJ, et al.: Increased cardiovascular mortality after early bilateral oophorectomy. Menopause 16 (1): 15-23, 2009 Jan-Feb.[PUBMED Abstract]
- Michelsen TM, Pripp AH, Tonstad S, et al.: Metabolic syndrome after risk-reducing salpingo-oophorectomy in women at high risk for hereditary breast ovarian cancer: a controlled observational study. Eur J Cancer 45 (1): 82-9, 2009.[PUBMED Abstract]
- Greene MH, Mai PL, Schwartz PE: Does bilateral salpingectomy with ovarian retention warrant consideration as a temporary bridge to risk-reducing bilateral oophorectomy in BRCA1/2 mutation carriers? Am J Obstet Gynecol 204 (1): 19.e1-6, 2011.[PUBMED Abstract]
- Dietl J, Wischhusen J, Häusler SF: The post-reproductive Fallopian tube: better removed? Hum Reprod 26 (11): 2918-24, 2011.[PUBMED Abstract]
- Leblanc E, Narducci F, Farre I, et al.: Radical fimbriectomy: a reasonable temporary risk-reducing surgery for selected women with a germ line mutation of BRCA 1 or 2 genes? Rationale and preliminary development. Gynecol Oncol 121 (3): 472-6, 2011.[PUBMED Abstract]
- Kwon JS, Tinker A, Pansegrau G, et al.: Prophylactic salpingectomy and delayed oophorectomy as an alternative for BRCA mutation carriers. Obstet Gynecol 121 (1): 14-24, 2013.[PUBMED Abstract]
- Harmsen MG, IntHout J, Arts-de Jong M, et al.: Salpingectomy With Delayed Oophorectomy in BRCA1/2 Mutation Carriers: Estimating Ovarian Cancer Risk. Obstet Gynecol 127 (6): 1054-63, 2016.[PUBMED Abstract]
- Nebgen DR, Hurteau J, Holman LL, et al.: Bilateral salpingectomy with delayed oophorectomy for ovarian cancer risk reduction: A pilot study in women with BRCA1/2 mutations. Gynecol Oncol 150 (1): 79-84, 2018.[PUBMED Abstract]
- Collaborative Group on Epidemiological Studies of Ovarian Cancer, Beral V, Doll R, et al.: Ovarian cancer and oral contraceptives: collaborative reanalysis of data from 45 epidemiological studies including 23,257 women with ovarian cancer and 87,303 controls. Lancet 371 (9609): 303-14, 2008.[PUBMED Abstract]
- Narod SA, Sun P, Ghadirian P, et al.: Tubal ligation and risk of ovarian cancer in carriers of BRCA1 or BRCA2 mutations: a case-control study. Lancet 357 (9267): 1467-70, 2001.[PUBMED Abstract]
- Whittemore AS, Balise RR, Pharoah PD, et al.: Oral contraceptive use and ovarian cancer risk among carriers of BRCA1 or BRCA2 mutations. Br J Cancer 91 (11): 1911-5, 2004.[PUBMED Abstract]
- McGuire V, Felberg A, Mills M, et al.: Relation of contraceptive and reproductive history to ovarian cancer risk in carriers and noncarriers of BRCA1 gene mutations. Am J Epidemiol 160 (7): 613-8, 2004.[PUBMED Abstract]
- McLaughlin JR, Risch HA, Lubinski J, et al.: Reproductive risk factors for ovarian cancer in carriers of BRCA1 or BRCA2 mutations: a case-control study. Lancet Oncol 8 (1): 26-34, 2007.[PUBMED Abstract]
- Modan B, Hartge P, Hirsh-Yechezkel G, et al.: Parity, oral contraceptives, and the risk of ovarian cancer among carriers and noncarriers of a BRCA1 or BRCA2 mutation. N Engl J Med 345 (4): 235-40, 2001.[PUBMED Abstract]
- Kotsopoulos J, Lubinski J, Gronwald J, et al.: Factors influencing ovulation and the risk of ovarian cancer in BRCA1 and BRCA2 mutation carriers. Int J Cancer 137 (5): 1136-46, 2015.[PUBMED Abstract]
- Risch HA: Hormonal etiology of epithelial ovarian cancer, with a hypothesis concerning the role of androgens and progesterone. J Natl Cancer Inst 90 (23): 1774-86, 1998.[PUBMED Abstract]
- Hankinson SE, Colditz GA, Hunter DJ, et al.: A prospective study of reproductive factors and risk of epithelial ovarian cancer. Cancer 76 (2): 284-90, 1995.[PUBMED Abstract]
- Gronwald J, Byrski T, Huzarski T, et al.: Influence of selected lifestyle factors on breast and ovarian cancer risk in BRCA1 mutation carriers from Poland. Breast Cancer Res Treat 95 (2): 105-9, 2006.[PUBMED Abstract]
- Whittemore AS, Harris R, Itnyre J: Characteristics relating to ovarian cancer risk: collaborative analysis of 12 US case-control studies. IV. The pathogenesis of epithelial ovarian cancer. Collaborative Ovarian Cancer Group. Am J Epidemiol 136 (10): 1212-20, 1992.[PUBMED Abstract]
- Miracle-McMahill HL, Calle EE, Kosinski AS, et al.: Tubal ligation and fatal ovarian cancer in a large prospective cohort study. Am J Epidemiol 145 (4): 349-57, 1997.[PUBMED Abstract]
- Cancer risks in BRCA2 mutation carriers. The Breast Cancer Linkage Consortium. J Natl Cancer Inst 91 (15): 1310-6, 1999.[PUBMED Abstract]
- van Asperen CJ, Brohet RM, Meijers-Heijboer EJ, et al.: Cancer risks in BRCA2 families: estimates for sites other than breast and ovary. J Med Genet 42 (9): 711-9, 2005.[PUBMED Abstract]
- Risch HA, McLaughlin JR, Cole DE, et al.: Prevalence and penetrance of germline BRCA1 and BRCA2 mutations in a population series of 649 women with ovarian cancer. Am J Hum Genet 68 (3): 700-10, 2001.[PUBMED Abstract]
- Liede A, Malik IA, Aziz Z, et al.: Contribution of BRCA1 and BRCA2 mutations to breast and ovarian cancer in Pakistan. Am J Hum Genet 71 (3): 595-606, 2002.[PUBMED Abstract]
- Moslehi R, Chu W, Karlan B, et al.: BRCA1 and BRCA2 mutation analysis of 208 Ashkenazi Jewish women with ovarian cancer. Am J Hum Genet 66 (4): 1259-72, 2000.[PUBMED Abstract]
- Mohamad HB, Apffelstaedt JP: Counseling for male BRCA mutation carriers: a review. Breast 17 (5): 441-50, 2008.[PUBMED Abstract]
- Liede A, Karlan BY, Narod SA: Cancer risks for male carriers of germline mutations in BRCA1 or BRCA2: a review of the literature. J Clin Oncol 22 (4): 735-42, 2004.[PUBMED Abstract]
- Mitra A, Fisher C, Foster CS, et al.: Prostate cancer in male BRCA1 and BRCA2 mutation carriers has a more aggressive phenotype. Br J Cancer 98 (2): 502-7, 2008.[PUBMED Abstract]
- Tryggvadóttir L, Vidarsdóttir L, Thorgeirsson T, et al.: Prostate cancer progression and survival in BRCA2 mutation carriers. J Natl Cancer Inst 99 (12): 929-35, 2007.[PUBMED Abstract]
- Agalliu I, Gern R, Leanza S, et al.: Associations of high-grade prostate cancer with BRCA1 and BRCA2 founder mutations. Clin Cancer Res 15 (3): 1112-20, 2009.[PUBMED Abstract]
- Narod SA, Neuhausen S, Vichodez G, et al.: Rapid progression of prostate cancer in men with a BRCA2 mutation. Br J Cancer 99 (2): 371-4, 2008.[PUBMED Abstract]
- Edwards SM, Evans DG, Hope Q, et al.: Prostate cancer in BRCA2 germline mutation carriers is associated with poorer prognosis. Br J Cancer 103 (6): 918-24, 2010.[PUBMED Abstract]
- Gallagher DJ, Gaudet MM, Pal P, et al.: Germline BRCA mutations denote a clinicopathologic subset of prostate cancer. Clin Cancer Res 16 (7): 2115-21, 2010.[PUBMED Abstract]
- Schröder FH, Hugosson J, Roobol MJ, et al.: Screening and prostate-cancer mortality in a randomized European study. N Engl J Med 360 (13): 1320-8, 2009.[PUBMED Abstract]
- Andriole GL, Grubb RL, Buys SS, et al.: Mortality results from a randomized prostate-cancer screening trial. N Engl J Med 360 (13): 1310-9, 2009.[PUBMED Abstract]
- Fiorentino M, Judson G, Penney K, et al.: Immunohistochemical expression of BRCA1 and lethal prostate cancer. Cancer Res 70 (8): 3136-9, 2010.[PUBMED Abstract]
- Horsburgh S, Matthew A, Bristow R, et al.: Male BRCA1 and BRCA2 mutation carriers: a pilot study investigating medical characteristics of patients participating in a prostate cancer prevention clinic. Prostate 65 (2): 124-9, 2005.[PUBMED Abstract]
- Hubert A, Peretz T, Manor O, et al.: The Jewish Ashkenazi founder mutations in the BRCA1/BRCA2 genes are not found at an increased frequency in Ashkenazi patients with prostate cancer. Am J Hum Genet 65 (3): 921-4, 1999.[PUBMED Abstract]
- Mitra AV, Bancroft EK, Barbachano Y, et al.: Targeted prostate cancer screening in men with mutations in BRCA1 and BRCA2 detects aggressive prostate cancer: preliminary analysis of the results of the IMPACT study. BJU Int 107 (1): 28-39, 2011.[PUBMED Abstract]
- Foulkes WD, Metcalfe K, Hanna W, et al.: Disruption of the expected positive correlation between breast tumor size and lymph node status in BRCA1-related breast carcinoma. Cancer 98 (8): 1569-77, 2003.[PUBMED Abstract]
- Verhoog LC, Brekelmans CT, Seynaeve C, et al.: Survival and tumour characteristics of breast-cancer patients with germline mutations of BRCA1. Lancet 351 (9099): 316-21, 1998.[PUBMED Abstract]
- Jóhannsson OT, Ranstam J, Borg A, et al.: Survival of BRCA1 breast and ovarian cancer patients: a population-based study from southern Sweden. J Clin Oncol 16 (2): 397-404, 1998.[PUBMED Abstract]
- Stoppa-Lyonnet D, Ansquer Y, Dreyfus H, et al.: Familial invasive breast cancers: worse outcome related to BRCA1 mutations. J Clin Oncol 18 (24): 4053-9, 2000.[PUBMED Abstract]
- Haffty BG, Harrold E, Khan AJ, et al.: Outcome of conservatively managed early-onset breast cancer by BRCA1/2 status. Lancet 359 (9316): 1471-7, 2002.[PUBMED Abstract]
- Robson M, Levin D, Federici M, et al.: Breast conservation therapy for invasive breast cancer in Ashkenazi women with BRCA gene founder mutations. J Natl Cancer Inst 91 (24): 2112-7, 1999.[PUBMED Abstract]
- Graeser MK, Engel C, Rhiem K, et al.: Contralateral breast cancer risk in BRCA1 and BRCA2 mutation carriers. J Clin Oncol 27 (35): 5887-92, 2009.[PUBMED Abstract]
- van den Broek AJ, van 't Veer LJ, Hooning MJ, et al.: Impact of Age at Primary Breast Cancer on Contralateral Breast Cancer Risk in BRCA1/2 Mutation Carriers. J Clin Oncol 34 (5): 409-18, 2016.[PUBMED Abstract]
- Menes TS, Terry MB, Goldgar D, et al.: Second primary breast cancer in BRCA1 and BRCA2 mutation carriers: 10-year cumulative incidence in the Breast Cancer Family Registry. Breast Cancer Res Treat 151 (3): 653-60, 2015.[PUBMED Abstract]
- Robson ME, Chappuis PO, Satagopan J, et al.: A combined analysis of outcome following breast cancer: differences in survival based on BRCA1/BRCA2 mutation status and administration of adjuvant treatment. Breast Cancer Res 6 (1): R8-R17, 2004.[PUBMED Abstract]
- Rennert G, Bisland-Naggan S, Barnett-Griness O, et al.: Clinical outcomes of breast cancer in carriers of BRCA1 and BRCA2 mutations. N Engl J Med 357 (2): 115-23, 2007.[PUBMED Abstract]
- Kriege M, Seynaeve C, Meijers-Heijboer H, et al.: Sensitivity to first-line chemotherapy for metastatic breast cancer in BRCA1 and BRCA2 mutation carriers. J Clin Oncol 27 (23): 3764-71, 2009.[PUBMED Abstract]
- Goodwin PJ, Phillips KA, West DW, et al.: Breast cancer prognosis in BRCA1 and BRCA2 mutation carriers: an International Prospective Breast Cancer Family Registry population-based cohort study. J Clin Oncol 30 (1): 19-26, 2012.[PUBMED Abstract]
- Copson ER, Maishman TC, Tapper WJ, et al.: Germline BRCA mutation and outcome in young-onset breast cancer (POSH): a prospective cohort study. Lancet Oncol 19 (2): 169-180, 2018.[PUBMED Abstract]
- Gonzalez-Angulo AM, Timms KM, Liu S, et al.: Incidence and outcome of BRCA mutations in unselected patients with triple receptor-negative breast cancer. Clin Cancer Res 17 (5): 1082-9, 2011.[PUBMED Abstract]
- Lee LJ, Alexander B, Schnitt SJ, et al.: Clinical outcome of triple negative breast cancer in BRCA1 mutation carriers and noncarriers. Cancer 117 (14): 3093-100, 2011.[PUBMED Abstract]
- Tung N, Gaughan E, Hacker MR, et al.: Outcome of triple negative breast cancer: comparison of sporadic and BRCA1-associated cancers. Breast Cancer Res Treat 146 (1): 175-82, 2014.[PUBMED Abstract]
- Huzarski T, Byrski T, Gronwald J, et al.: Ten-year survival in patients with BRCA1-negative and BRCA1-positive breast cancer. J Clin Oncol 31 (26): 3191-6, 2013.[PUBMED Abstract]
- Verhoog LC, Berns EM, Brekelmans CT, et al.: Prognostic significance of germline BRCA2 mutations in hereditary breast cancer patients. J Clin Oncol 18 (21 Suppl): 119S-24S, 2000.[PUBMED Abstract]
- Brekelmans CT, Tilanus-Linthorst MM, Seynaeve C, et al.: Tumour characteristics, survival and prognostic factors of hereditary breast cancer from BRCA2-, BRCA1- and non-BRCA1/2 families as compared to sporadic breast cancer cases. Eur J Cancer 43 (5): 867-76, 2007.[PUBMED Abstract]
- Budroni M, Cesaraccio R, Coviello V, et al.: Role of BRCA2 mutation status on overall survival among breast cancer patients from Sardinia. BMC Cancer 9: 62, 2009.[PUBMED Abstract]
- Byrski T, Huzarski T, Dent R, et al.: Response to neoadjuvant therapy with cisplatin in BRCA1-positive breast cancer patients. Breast Cancer Res Treat 115 (2): 359-63, 2009.[PUBMED Abstract]
- Chappuis PO, Goffin J, Wong N, et al.: A significant response to neoadjuvant chemotherapy in BRCA1/2 related breast cancer. J Med Genet 39 (8): 608-10, 2002.[PUBMED Abstract]
- Byrski T, Gronwald J, Huzarski T, et al.: Pathologic complete response rates in young women with BRCA1-positive breast cancers after neoadjuvant chemotherapy. J Clin Oncol 28 (3): 375-9, 2010.[PUBMED Abstract]
- Fourquet A, Stoppa-Lyonnet D, Kirova YM, et al.: Familial breast cancer: clinical response to induction chemotherapy or radiotherapy related to BRCA1/2 mutations status. Am J Clin Oncol 32 (2): 127-31, 2009.[PUBMED Abstract]
- Arun B, Bayraktar S, Liu DD, et al.: Response to neoadjuvant systemic therapy for breast cancer in BRCA mutation carriers and noncarriers: a single-institution experience. J Clin Oncol 29 (28): 3739-46, 2011.[PUBMED Abstract]
- Wunderle M, Gass P, Häberle L, et al.: BRCA mutations and their influence on pathological complete response and prognosis in a clinical cohort of neoadjuvantly treated breast cancer patients. Breast Cancer Res Treat 171 (1): 85-94, 2018.[PUBMED Abstract]
- Silver DP, Richardson AL, Eklund AC, et al.: Efficacy of neoadjuvant Cisplatin in triple-negative breast cancer. J Clin Oncol 28 (7): 1145-53, 2010.[PUBMED Abstract]
- Byrski T, Huzarski T, Dent R, et al.: Pathologic complete response to neoadjuvant cisplatin in BRCA1-positive breast cancer patients. Breast Cancer Res Treat 147 (2): 401-5, 2014.[PUBMED Abstract]
- Hahnen E, Lederer B, Hauke J, et al.: Germline Mutation Status, Pathological Complete Response, and Disease-Free Survival in Triple-Negative Breast Cancer: Secondary Analysis of the GeparSixto Randomized Clinical Trial. JAMA Oncol 3 (10): 1378-1385, 2017.[PUBMED Abstract]
- Tutt A, Tovey H, Cheang MCU, et al.: Carboplatin in BRCA1/2-mutated and triple-negative breast cancer BRCAness subgroups: the TNT Trial. Nat Med 24 (5): 628-637, 2018.[PUBMED Abstract]
- Robson M, Im SA, Senkus E, et al.: Olaparib for Metastatic Breast Cancer in Patients with a Germline BRCA Mutation. N Engl J Med 377 (6): 523-533, 2017.[PUBMED Abstract]
- Litton JK, Rugo HS, Ettl J, et al.: Talazoparib in Patients with Advanced Breast Cancer and a Germline BRCA Mutation. N Engl J Med 379 (8): 753-763, 2018.[PUBMED Abstract]
- Leong T, Whitty J, Keilar M, et al.: Mutation analysis of BRCA1 and BRCA2 cancer predisposition genes in radiation hypersensitive cancer patients. Int J Radiat Oncol Biol Phys 48 (4): 959-65, 2000.[PUBMED Abstract]
- Pierce LJ, Strawderman M, Narod SA, et al.: Effect of radiotherapy after breast-conserving treatment in women with breast cancer and germline BRCA1/2 mutations. J Clin Oncol 18 (19): 3360-9, 2000.[PUBMED Abstract]
- Shanley S, McReynolds K, Ardern-Jones A, et al.: Late toxicity is not increased in BRCA1/BRCA2 mutation carriers undergoing breast radiotherapy in the United Kingdom. Clin Cancer Res 12 (23): 7025-32, 2006.[PUBMED Abstract]
- Pierce LJ, Phillips KA, Griffith KA, et al.: Local therapy in BRCA1 and BRCA2 mutation carriers with operable breast cancer: comparison of breast conservation and mastectomy. Breast Cancer Res Treat 121 (2): 389-98, 2010.[PUBMED Abstract]
- Kirova YM, Savignoni A, Sigal-Zafrani B, et al.: Is the breast-conserving treatment with radiotherapy appropriate in BRCA1/2 mutation carriers? Long-term results and review of the literature. Breast Cancer Res Treat 120 (1): 119-26, 2010.[PUBMED Abstract]
- Metcalfe K, Lynch HT, Ghadirian P, et al.: Risk of ipsilateral breast cancer in BRCA1 and BRCA2 mutation carriers. Breast Cancer Res Treat 127 (1): 287-96, 2011.[PUBMED Abstract]
- Bernstein JL, Thomas DC, Shore RE, et al.: Contralateral breast cancer after radiotherapy among BRCA1 and BRCA2 mutation carriers: a WECARE study report. Eur J Cancer 49 (14): 2979-85, 2013.[PUBMED Abstract]
- Rubin SC, Benjamin I, Behbakht K, et al.: Clinical and pathological features of ovarian cancer in women with germ-line mutations of BRCA1. N Engl J Med 335 (19): 1413-6, 1996.[PUBMED Abstract]
- Ben David Y, Chetrit A, Hirsh-Yechezkel G, et al.: Effect of BRCA mutations on the length of survival in epithelial ovarian tumors. J Clin Oncol 20 (2): 463-6, 2002.[PUBMED Abstract]
- Jazaeri AA, Yee CJ, Sotiriou C, et al.: Gene expression profiles of BRCA1-linked, BRCA2-linked, and sporadic ovarian cancers. J Natl Cancer Inst 94 (13): 990-1000, 2002.[PUBMED Abstract]
- Cass I, Baldwin RL, Varkey T, et al.: Improved survival in women with BRCA-associated ovarian carcinoma. Cancer 97 (9): 2187-95, 2003.[PUBMED Abstract]
- Aida H, Takakuwa K, Nagata H, et al.: Clinical features of ovarian cancer in Japanese women with germ-line mutations of BRCA1. Clin Cancer Res 4 (1): 235-40, 1998.[PUBMED Abstract]
- Boyd J, Sonoda Y, Federici MG, et al.: Clinicopathologic features of BRCA-linked and sporadic ovarian cancer. JAMA 283 (17): 2260-5, 2000.[PUBMED Abstract]
- Tan DS, Rothermundt C, Thomas K, et al.: "BRCAness" syndrome in ovarian cancer: a case-control study describing the clinical features and outcome of patients with epithelial ovarian cancer associated with BRCA1 and BRCA2 mutations. J Clin Oncol 26 (34): 5530-6, 2008.[PUBMED Abstract]
- Hyman DM, Zhou Q, Iasonos A, et al.: Improved survival for BRCA2-associated serous ovarian cancer compared with both BRCA-negative and BRCA1-associated serous ovarian cancer. Cancer 118 (15): 3703-9, 2012.[PUBMED Abstract]
- Liu J, Cristea MC, Frankel P, et al.: Clinical characteristics and outcomes of BRCA-associated ovarian cancer: genotype and survival. Cancer Genet 205 (1-2): 34-41, 2012 Jan-Feb.[PUBMED Abstract]
- Chetrit A, Hirsh-Yechezkel G, Ben-David Y, et al.: Effect of BRCA1/2 mutations on long-term survival of patients with invasive ovarian cancer: the national Israeli study of ovarian cancer. J Clin Oncol 26 (1): 20-5, 2008.[PUBMED Abstract]
- Lacour RA, Westin SN, Meyer LA, et al.: Improved survival in non-Ashkenazi Jewish ovarian cancer patients with BRCA1 and BRCA2 gene mutations. Gynecol Oncol 121 (2): 358-63, 2011.[PUBMED Abstract]
- Vencken PM, Kriege M, Hoogwerf D, et al.: Chemosensitivity and outcome of BRCA1- and BRCA2-associated ovarian cancer patients after first-line chemotherapy compared with sporadic ovarian cancer patients. Ann Oncol 22 (6): 1346-52, 2011.[PUBMED Abstract]
- Pal T, Permuth-Wey J, Kapoor R, et al.: Improved survival in BRCA2 carriers with ovarian cancer. Fam Cancer 6 (1): 113-9, 2007.[PUBMED Abstract]
- Yang D, Khan S, Sun Y, et al.: Association of BRCA1 and BRCA2 mutations with survival, chemotherapy sensitivity, and gene mutator phenotype in patients with ovarian cancer. JAMA 306 (14): 1557-65, 2011.[PUBMED Abstract]
- Bolton KL, Chenevix-Trench G, Goh C, et al.: Association between BRCA1 and BRCA2 mutations and survival in women with invasive epithelial ovarian cancer. JAMA 307 (4): 382-90, 2012.[PUBMED Abstract]
- Zweemer RP, Verheijen RH, Coebergh JW, et al.: Survival analysis in familial ovarian cancer, a case control study. Eur J Obstet Gynecol Reprod Biol 98 (2): 219-23, 2001.[PUBMED Abstract]
- Pharoah PD, Easton DF, Stockton DL, et al.: Survival in familial, BRCA1-associated, and BRCA2-associated epithelial ovarian cancer. United Kingdom Coordinating Committee for Cancer Research (UKCCCR) Familial Ovarian Cancer Study Group. Cancer Res 59 (4): 868-71, 1999.[PUBMED Abstract]
- Buller RE, Shahin MS, Geisler JP, et al.: Failure of BRCA1 dysfunction to alter ovarian cancer survival. Clin Cancer Res 8 (5): 1196-202, 2002.[PUBMED Abstract]
- McLaughlin JR, Rosen B, Moody J, et al.: Long-term ovarian cancer survival associated with mutation in BRCA1 or BRCA2. J Natl Cancer Inst 105 (2): 141-8, 2013.[PUBMED Abstract]
- Yang H, Jeffrey PD, Miller J, et al.: BRCA2 function in DNA binding and recombination from a BRCA2-DSS1-ssDNA structure. Science 297 (5588): 1837-48, 2002.[PUBMED Abstract]
- Xu X, Weaver Z, Linke SP, et al.: Centrosome amplification and a defective G2-M cell cycle checkpoint induce genetic instability in BRCA1 exon 11 isoform-deficient cells. Mol Cell 3 (3): 389-95, 1999.[PUBMED Abstract]
- Cancer Genome Atlas Research Network: Integrated genomic analyses of ovarian carcinoma. Nature 474 (7353): 609-15, 2011.[PUBMED Abstract]
- Husain A, He G, Venkatraman ES, et al.: BRCA1 up-regulation is associated with repair-mediated resistance to cis-diamminedichloroplatinum(II). Cancer Res 58 (6): 1120-3, 1998.[PUBMED Abstract]
- Pennington KP, Walsh T, Harrell MI, et al.: Germline and somatic mutations in homologous recombination genes predict platinum response and survival in ovarian, fallopian tube, and peritoneal carcinomas. Clin Cancer Res 20 (3): 764-75, 2014.[PUBMED Abstract]
- Norquist BM, Brady MF, Harrell MI, et al.: Mutations in Homologous Recombination Genes and Outcomes in Ovarian Carcinoma Patients in GOG 218: An NRG Oncology/Gynecologic Oncology Group Study. Clin Cancer Res 24 (4): 777-783, 2018.[PUBMED Abstract]
- Fong PC, Boss DS, Yap TA, et al.: Inhibition of poly(ADP-ribose) polymerase in tumors from BRCA mutation carriers. N Engl J Med 361 (2): 123-34, 2009.[PUBMED Abstract]
- Audeh MW, Carmichael J, Penson RT, et al.: Oral poly(ADP-ribose) polymerase inhibitor olaparib in patients with BRCA1 or BRCA2 mutations and recurrent ovarian cancer: a proof-of-concept trial. Lancet 376 (9737): 245-51, 2010.[PUBMED Abstract]
- Fong PC, Yap TA, Boss DS, et al.: Poly(ADP)-ribose polymerase inhibition: frequent durable responses in BRCA carrier ovarian cancer correlating with platinum-free interval. J Clin Oncol 28 (15): 2512-9, 2010.[PUBMED Abstract]
- Hennessy BT, Timms KM, Carey MS, et al.: Somatic mutations in BRCA1 and BRCA2 could expand the number of patients that benefit from poly (ADP ribose) polymerase inhibitors in ovarian cancer. J Clin Oncol 28 (22): 3570-6, 2010.[PUBMED Abstract]
- Kaufman B, Shapira-Frommer R, Schmutzler RK, et al.: Olaparib monotherapy in patients with advanced cancer and a germline BRCA1/2 mutation. J Clin Oncol 33 (3): 244-50, 2015.[PUBMED Abstract]
- Domchek SM, Aghajanian C, Shapira-Frommer R, et al.: Efficacy and safety of olaparib monotherapy in germline BRCA1/2 mutation carriers with advanced ovarian cancer and three or more lines of prior therapy. Gynecol Oncol 140 (2): 199-203, 2016.[PUBMED Abstract]
- Oza AM, Cibula D, Benzaquen AO, et al.: Olaparib combined with chemotherapy for recurrent platinum-sensitive ovarian cancer: a randomised phase 2 trial. Lancet Oncol 16 (1): 87-97, 2015.[PUBMED Abstract]
- Liu JF, Barry WT, Birrer M, et al.: Combination cediranib and olaparib versus olaparib alone for women with recurrent platinum-sensitive ovarian cancer: a randomised phase 2 study. Lancet Oncol 15 (11): 1207-14, 2014.[PUBMED Abstract]
- Kaye SB, Lubinski J, Matulonis U, et al.: Phase II, open-label, randomized, multicenter study comparing the efficacy and safety of olaparib, a poly (ADP-ribose) polymerase inhibitor, and pegylated liposomal doxorubicin in patients with BRCA1 or BRCA2 mutations and recurrent ovarian cancer. J Clin Oncol 30 (4): 372-9, 2012.[PUBMED Abstract]
- Adams SF, Marsh EB, Elmasri W, et al.: A high response rate to liposomal doxorubicin is seen among women with BRCA mutations treated for recurrent epithelial ovarian cancer. Gynecol Oncol 123 (3): 486-91, 2011.[PUBMED Abstract]
- Safra T, Borgato L, Nicoletto MO, et al.: BRCA mutation status and determinant of outcome in women with recurrent epithelial ovarian cancer treated with pegylated liposomal doxorubicin. Mol Cancer Ther 10 (10): 2000-7, 2011.[PUBMED Abstract]
- Gelmon KA, Tischkowitz M, Mackay H, et al.: Olaparib in patients with recurrent high-grade serous or poorly differentiated ovarian carcinoma or triple-negative breast cancer: a phase 2, multicentre, open-label, non-randomised study. Lancet Oncol 12 (9): 852-61, 2011.[PUBMED Abstract]
- Ledermann J, Harter P, Gourley C, et al.: Olaparib maintenance therapy in platinum-sensitive relapsed ovarian cancer. N Engl J Med 366 (15): 1382-92, 2012.[PUBMED Abstract]
- Ledermann J, Harter P, Gourley C, et al.: Olaparib maintenance therapy in patients with platinum-sensitive relapsed serous ovarian cancer: a preplanned retrospective analysis of outcomes by BRCA status in a randomised phase 2 trial. Lancet Oncol 15 (8): 852-61, 2014.[PUBMED Abstract]
- Matulonis UA, Harter P, Gourley C, et al.: Olaparib maintenance therapy in patients with platinum-sensitive, relapsed serous ovarian cancer and a BRCA mutation: Overall survival adjusted for postprogression poly(adenosine diphosphate ribose) polymerase inhibitor therapy. Cancer 122 (12): 1844-52, 2016.[PUBMED Abstract]
- Ledermann JA, Harter P, Gourley C, et al.: Overall survival in patients with platinum-sensitive recurrent serous ovarian cancer receiving olaparib maintenance monotherapy: an updated analysis from a randomised, placebo-controlled, double-blind, phase 2 trial. Lancet Oncol 17 (11): 1579-1589, 2016.[PUBMED Abstract]
- Pujade-Lauraine E, Ledermann JA, Selle F, et al.: Olaparib tablets as maintenance therapy in patients with platinum-sensitive, relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 18 (9): 1274-1284, 2017.[PUBMED Abstract]
- Moore K, Colombo N, Scambia G, et al.: Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med 379 (26): 2495-2505, 2018.[PUBMED Abstract]
- Drew Y, Ledermann J, Hall G, et al.: Phase 2 multicentre trial investigating intermittent and continuous dosing schedules of the poly(ADP-ribose) polymerase inhibitor rucaparib in germline BRCA mutation carriers with advanced ovarian and breast cancer. Br J Cancer 114 (7): 723-30, 2016.[PUBMED Abstract]
- Kristeleit R, Shapiro GI, Burris HA, et al.: A Phase I-II Study of the Oral PARP Inhibitor Rucaparib in Patients with Germline BRCA1/2-Mutated Ovarian Carcinoma or Other Solid Tumors. Clin Cancer Res 23 (15): 4095-4106, 2017.[PUBMED Abstract]
- Swisher EM, Lin KK, Oza AM, et al.: Rucaparib in relapsed, platinum-sensitive high-grade ovarian carcinoma (ARIEL2 Part 1): an international, multicentre, open-label, phase 2 trial. Lancet Oncol 18 (1): 75-87, 2017.[PUBMED Abstract]
- Coleman RL, Oza AM, Lorusso D, et al.: Rucaparib maintenance treatment for recurrent ovarian carcinoma after response to platinum therapy (ARIEL3): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 390 (10106): 1949-1961, 2017.[PUBMED Abstract]
- Sandhu SK, Schelman WR, Wilding G, et al.: The poly(ADP-ribose) polymerase inhibitor niraparib (MK4827) in BRCA mutation carriers and patients with sporadic cancer: a phase 1 dose-escalation trial. Lancet Oncol 14 (9): 882-92, 2013.[PUBMED Abstract]
- Mirza MR, Monk BJ, Herrstedt J, et al.: Niraparib Maintenance Therapy in Platinum-Sensitive, Recurrent Ovarian Cancer. N Engl J Med 375 (22): 2154-2164, 2016.[PUBMED Abstract]
- Moore KN, Secord AA, Geller MA, et al.: Niraparib monotherapy for late-line treatment of ovarian cancer (QUADRA): a multicentre, open-label, single-arm, phase 2 trial. Lancet Oncol 20 (5): 636-648, 2019.[PUBMED Abstract]
- Hampel H, Bennett RL, Buchanan A, et al.: A practice guideline from the American College of Medical Genetics and Genomics and the National Society of Genetic Counselors: referral indications for cancer predisposition assessment. Genet Med 17 (1): 70-87, 2015.[PUBMED Abstract]
- Committee on Practice Bulletins–Gynecology, Committee on Genetics, Society of Gynecologic Oncology: Practice Bulletin No 182: Hereditary Breast and Ovarian Cancer Syndrome. Obstet Gynecol 130 (3): e110-e126, 2017.[PUBMED Abstract]
- Robson ME, Bradbury AR, Arun B, et al.: American Society of Clinical Oncology Policy Statement Update: Genetic and Genomic Testing for Cancer Susceptibility. J Clin Oncol 33 (31): 3660-7, 2015.[PUBMED Abstract]
- Paluch-Shimon S, Cardoso F, Sessa C, et al.: Prevention and screening in BRCA mutation carriers and other breast/ovarian hereditary cancer syndromes: ESMO Clinical Practice Guidelines for cancer prevention and screening. Ann Oncol 27 (suppl 5): v103-v110, 2016.[PUBMED Abstract]
- American College of Surgeons: National Accreditation Program for Breast Centers Standards Manual 2014 Edition. Chicago, IL: American College of Surgeons, 2014. Available online. Last accessed January 22, 2020.[PUBMED Abstract]
- Berliner JL, Fay AM, Cummings SA, et al.: NSGC practice guideline: risk assessment and genetic counseling for hereditary breast and ovarian cancer. J Genet Couns 22 (2): 155-63, 2013.[PUBMED Abstract]
- Lancaster JM, Powell CB, Chen LM, et al.: Society of Gynecologic Oncology statement on risk assessment for inherited gynecologic cancer predispositions. Gynecol Oncol 136 (1): 3-7, 2015.[PUBMED Abstract]
- Owens DK, Davidson KW, Krist AH, et al.: Risk Assessment, Genetic Counseling, and Genetic Testing for BRCA-Related Cancer: US Preventive Services Task Force Recommendation Statement. JAMA 322 (7): 652-665, 2019.[PUBMED Abstract]
- 他の遺伝性乳がんおよび/または婦人科がん症候群の臨床管理
-
リンチ症候群
リンチ症候群の遺伝子的根拠としてミスマッチ修復遺伝子が同定されため、ミスマッチ修復遺伝子異常の一般的な分子マーカーとしてマイクロサテライト不安定性が同定された。散発性大腸がんの約15%でマイクロサテライト不安定性が示される一方、散発性子宮内膜がんでは最大28%がこの分子変化を有する。[ 1 ][ 2 ]マイクロサテライト不安定性を示す散発性腫瘍では、最も頻繁にMLH1プロモーターの高メチル化が認められる。マイクロサテライト不安定性を示すリンチ症候群関連腫瘍では、典型的にミスマッチ修復遺伝子に関連する蛋白が1つ以上消失している。
腫瘍浸潤リンパ球、腫瘍周囲リンパ球、未分化がん、子宮下部腫瘍の存在など、特定の病理組織学的特徴もまたマイクロサテライト不安定性の表現型を強く示唆する。臨床基準の使用は、腫瘍検査のための選択基準戦略の1つである。ミスマッチ修復の遺伝的多様体の確率の予測にはコンピュータモデルも使用されており、マイクロサテライト不安定性または免疫組織化学に関する情報がない場合に使用できる。[ 3 ][ 4 ][ 5 ][ 6 ]しかしながら、全体としては腫瘍組織が利用できる場合には大腸および子宮内膜腫瘍の普遍的な検査に向かう動きがある。(詳しい情報については、大腸がんの遺伝学に関するPDQ要約のリンチ症候群のスクリーニングのための普遍的腫瘍検査のセクションを参照のこと。)
参考文献- Vilar E, Gruber SB: Microsatellite instability in colorectal cancer-the stable evidence. Nat Rev Clin Oncol 7 (3): 153-62, 2010.[PUBMED Abstract]
- Nakamura A, Osonoi T, Terauchi Y: Relationship between urinary sodium excretion and pioglitazone-induced edema. J Diabetes Investig 1 (5): 208-11, 2010.[PUBMED Abstract]
- Balmaña J, Stockwell DH, Steyerberg EW, et al.: Prediction of MLH1 and MSH2 mutations in Lynch syndrome. JAMA 296 (12): 1469-78, 2006.[PUBMED Abstract]
- Barnetson RA, Tenesa A, Farrington SM, et al.: Identification and survival of carriers of mutations in DNA mismatch-repair genes in colon cancer. N Engl J Med 354 (26): 2751-63, 2006.[PUBMED Abstract]
- Kastrinos F, Allen JI, Stockwell DH, et al.: Development and validation of a colon cancer risk assessment tool for patients undergoing colonoscopy. Am J Gastroenterol 104 (6): 1508-18, 2009.[PUBMED Abstract]
- Khan O, Blanco A, Conrad P, et al.: Performance of Lynch syndrome predictive models in a multi-center US referral population. Am J Gastroenterol 106 (10): 1822-7; quiz 1828, 2011.[PUBMED Abstract]
- 遺伝性乳がんおよび卵巣がん症候群における心理社会的問題
-
序
がん遺伝子検査を背景にした心理社会的研究は、心理学的結果、個人間および家族内での影響、文化的反応と地域社会の反応を明確にする。この研究タイプにより、スクリーニングおよびその他の健康上の行動を促進または妨害する行動因子も同定される。さらに、リスク低減のための介入に関する意思決定能力の向上、リスクの告知や遺伝子検査に関係する苦悩および/またはその他の負の後遺症を軽減するための心理社会的介入の評価、倫理的問題の解決のためのデータの提供、さまざまな集団を対象にした検査への関心の予測なども可能となる。
本セクションでは、遺伝性乳がんおよび卵巣がん症候群における心理社会的問題について扱う。リンチ症候群関連婦人科がんに関係した心理社会的問題およびスクリーニングの問題は、大腸がんの遺伝学に関するPDQ要約の遺伝性結腸がん症候群における心理社会的問題のセクションで考察されている。
遺伝カウンセリングと遺伝子検査の受診
遺伝カウンセリングと遺伝子検査の受診率
各研究の方法論は、実施されたサンプリング方法、募集状況、高リスクのコホートまたは家系を対象とした研究プロトコルによる検査などの点で異なるため、遺伝カウンセリングと遺伝子検査が提供された研究間で受診率を比較することは困難である。2002年以前に実施された40件の研究を対象として遺伝子検査の利用状況を調べた系統的レビューでは、受診率は25~96%と幅広く、平均受診率は59%だった。[ 1 ]多変量解析の結果、BRCA1/BRCA2遺伝子検査の利用率は、乳がんまたは卵巣がんの既往歴または家族歴があること、ならびにサンプリング方法や募集状況、研究で実際の受診数と検査意図に基づく件数のどちらを規定しているかといった各研究の方法論的特徴に関連していることが示された。
他のいくつかの要因もBRCA1/BRCA2遺伝子検査の受診率と正の相関を示したが、それらはすべての研究で一貫して認められたわけではない。検査の利用と正の相関が認められた心理学的要因には、がんに特異的な苦悩の大きさと、乳がんまたは卵巣がんの発症のリスクに対する認識の強さがあった。がんに罹患した近親者の多さも、検査受診率の増大に相関していた。
表14に、米国の臨床コホートと研究コホートにおける遺伝子検査の受診状況を要約した。
表14.遺伝子検査(GT)の受診率に関連する予測因子 研究の引用番号 研究集団 サンプルサイズ(N) GTの受診率 GTの受診に関連する予測因子 コメント GC = 遺伝カウンセリング;HMO = 健康維持機構。 aデータソースは自己報告。 bデータソースは医療記録。 Schwartz et al.(2005) [ 2 ] BRCA1/BRCA2病原性多様体を有するリスクが10%以上で、新たに診断されたが局所療法を受けていない乳がん患者a 231 177/231人(77%)がGTを受診 根治的局所療法の実施に対する決心。根治的局所療法を受けると決めていない女性には検査を受ける傾向がみられた。 提案された検査は無料であった。 34/231人(15%)はベースラインのインタビューを受けたがGTを辞退 検査に対する医師の推奨。医師からGTを勧められた女性は検査を受ける傾向がみられた。 38/177人は検査結果が出る前に治療段階を進める決定を下した。 20/231人はベースラインのインタビューを辞退 Kieran et al.(2007) [ 3 ] 2002年から2004年にGCを受診した女性a 250 88/250人(35%)がGTを受診 GTにかかる費用の支払い能力(費用全額または保険でカバーされない費用)。 検査費用を負担できない女性の非受診率は5.5倍。 研究期間中に女性450人が乳がんと卵巣がんのリスクに対するGCを受診。適格と判断された女性250人に研究質問票がメール送信された。 36/88人が調査に再び参加 GC後に提示されたリスク推定値を想起できるかどうか。リスク推定値を想起できなかった女性の非受診率は15.5倍。 女性は全員が何らかの保険に加入していた。 162/250人(65%)が適格 65/162人が調査に再び参加 Susswein et al.(2008) [ 4 ] 乳がんのアフリカ系米国人女性と白人女性b 768 529/768人(69%)がGTを受診 人種/民族性。アフリカ系米国人女性は白人女性に比べ検査を受ける割合が低かった。 サンプルは臨床データベースから収集。検査が保険でカバーされていない場合にも、無償で実施されることが示された。診断時期に関する影響は、アフリカ系米国人では有意であったが、白人女性のサブグループでは明確ではなかった。 アフリカ系米国人女性:77/132人(58%)がGTを受診 最近の診断。最近診断が下されたアフリカ系米国人女性は、検査を受ける割合が高かった。 白人女性:452/636人(71%)がGTを受診 Olaya et al.(2009) [ 5 ] 2001年から2008年にGTを受診するために紹介された患者b 213 111/213人(52%)がGTを受診 乳がんの個人歴。個人歴のある被験者は検査の受診のオッズが3倍。 検査の保険適用は、91.1%(175/213人)の患者に該当した。GTが保険の適用範囲であった患者の51.4%が検査を受けたが、48.6%は受けなかった。保険が適用されなかった患者では、41.2%がGTを受診し、58.9%は受けなかった。 102/213人(48%)がGTを辞退 教育水準の高さ。高校教育以下の学歴の患者は、大学かそれ以上の教育を受けている患者に比べ、検査を受けるオッズが1/3。 Levy et al.(2010) [ 6 ] 新しく早発型乳がんと診断された20~40歳の女性b 1,474 446/1,474人(30%)がGTを受診 人種/民族性。ユダヤ人女性が検査を受ける率は、それ以外の女性の3倍。アフリカ系米国人女性およびヒスパニック系女性は、非ユダヤ系白人女性に比べ検査を受ける割合が有意に低かった。 サンプルは民間保険に加入している個人についての国内データベースから収集。 ユダヤ人女性:18/32人(56%)がGTを受診 居住地。南部在住の女性は北東部在住の女性より検査を受ける割合が高かった。 アフリカ系米国人女性:10/82人(12%)がGTを受診 保険の種類。POS(point-of-service)プランに加入している女性は、HMOプランに加入している女性より検査を受ける割合が高かった。 最近の診断。2007年に診断を受けた女性は、2004年に診断を受けた女性に比べ、検査を受ける割合が3.8倍。 米国以外において実施された数件の研究で、遺伝子検査の受診率が調査されている。[ 7 ][ 8 ][ 9 ][ 10 ][ 11 ]BRCA1/BRCA2病原性多様体キャリアの近親者でリスクのある人を対象に検査の受診率を調べた研究では、受診率が平均で50%未満(範囲:36~48%)であり、報告された受診率は男性近親者より女性近親者で高かった。高い検査受診率に関連する他の因子については、複数の研究間で一貫して報告されているものはないが、最も一般的な因子として親であること、ならびに子供のリスクについて情報を求めていることが挙げられる。
遺伝カウンセリングと遺伝子検査の受診率に影響する因子
BRCA1/BRCA2遺伝子検査の受診率に対する予測因子に関して蓄積された証拠を検討する数件のレビューでは、検査の受診の重要な予測因子として、高齢、アシュケナージユダヤ人(AJ)の血筋を引くこと、未婚、乳がんの個人歴、乳がんの家族歴が挙げられた。病院環境で被験者を募集した研究は、地域環境で募集した研究に比べ、動員率が有意に高かった。検査の受診を即座に決定する必要があった研究では、意思決定に時間的猶予が与えられた研究より高い受診率が報告される傾向が認められた。[ 1 ]しかし、乳がんと診断された女性は、乳がんの根治的手術を受ける前後いずれの場合でも、同等に遺伝カウンセリング(提示された情報、および医師によるカウンセリング推奨の強さと時期を含む)に満足していたという証拠がある。[ 12 ]別のレビューでは[ 13 ]、BRCA1/BRCA2病原性多様体に対する遺伝子検査の受診は、心理学的因子(例、乳がんに対する不安や乳がんのリスクの認識)と人口統計学的因子および医学的因子(例、乳がんまたは卵巣がんの既往歴、子供の存在、罹患した第一度近親者[FDR]が多いこと)に関連していることが認められた。BRCA1/BRCA2病原性多様体が既知の家族の家系員は、検査を求める率が高かった;BRCA1/BRCA2検査の知識が豊富な人、リスクをよく認識している人、マンモグラフィが健康上の利益を高めると考えている人、検査を受ける意思が強い人は、検査を受ける率が高かった。[ 14 ]
BRCA1/BRCA2検査の受診率に影響を及ぼす人種/民族性の相違に関するレビューで、アフリカ系米国人女性が遺伝子検査を受診する意思は、乳がんまたは卵巣がんのFDRが1人以上いること、キャリアである場合のリスクを強く認識していること、遺伝子のキャリアである可能性についての予測的な罪悪感が小さいことに関連していた。[ 15 ]1件の系統的なレビューにより、アフリカ系米国人およびヒスパニック系を含む特定の民族的マイノリティ集団は遺伝カウンセリングおよび遺伝子検査に関して、白人と比較してより消極的な考えおよび大きな懸念を抱いていることが明らかにされた。アフリカ系米国人およびヒスパニック系は、自らの民族集団が他の集団よりも劣っていることを示すために遺伝子検査が用いられると考える傾向が強かった。さらに、アフリカ系米国人およびヒスパニック系は、がんにおける遺伝学、BRCAの状態、および遺伝子検査の重要性について認識と知識が低いことが明らかにされた。[ 16 ]
検査を最後までやり遂げる理由としては、子供のリスクについて知りたい、不確かな状況から解放されたい、スクリーニングやリスク低減のための手術の判断のための情報を得たい、結婚や出産など人生の重要な判断のための情報を得たいことなどが挙げられた。[ 14 ][ 17 ]アフリカ系米国人女性が検査を受ける最も重要な理由に、他の近親者が遺伝子検査の受診を決意するのを促したいという動機がある。[ 15 ]
医師の推奨は検査に対する別の動機付け要因になる。遺伝子検査受診を検討している女性335人を対象にした1件のレトロスペクティブ研究において、77%が検査を受けるべきかどうか遺伝子専門医の意見を聞きたいと報告し、49%がプライマリケア提供者の意見を望んでいた。[ 18 ]しかし、乳がんまたは卵巣がんの母系家族歴を有する女性に有利に働く紹介バイアスの存在を示す証拠がある。カナダの患者315人を対象としたレトロスペクティブ・レビューでは、乳がんまたは卵巣がんの母系家族歴を有する患者が医師によるがんの遺伝相談を紹介される頻度は、父系家族歴を有する患者の4.9倍(95%信頼区間、3.6-6.7)高い傾向がみられた(P < 0.001)。[ 19 ]複数の研究で、医師が父系家族歴を適切に評価できていない[ 20 ]、または遺伝リスクに関する父系家族歴の意義を過小評価している可能性があることが明らかにされている。[ 20 ][ 21 ][ 22 ]米国予防サービス作業部会(U.S. Preventive Services Task Force)のガイドラインを満たす患者のBRCA遺伝カウンセリングへの医師による紹介は最適以下であることが、他の研究で示されている。[ 23 ]
外科的治療が提案される場合に外科的治療の決定に対する情報を得るためのBRCA検査の受診は、研究コホートで高いようである[ 2 ][ 24 ];しかしながら、他の研究からの知見では、乳がん治療の決定に対する情報を得るための検査は臨床現場では十分に利用されていないことが示唆されている。[ 6 ][ 25 ][ 26 ]新たに診断された患者の遺伝カウンセリングへの医師の紹介が不十分であること、保険の適用範囲の種類(メディケアまたはメディケイドなど)、検査の時期および調整における困難など、外科的治療の決定に対する情報を得るためのBRCA検査利用の障壁が報告されている。[ 6 ][ 27 ][ 28 ][ 29 ][ 30 ]新たに乳がんと診断された患者を対象に、率先した迅速な遺伝カウンセリングの提供(手術前に遺伝カウンセリングを実施)を通常ケアと比較したランダム化試験の結果から、介入群では遺伝カウンセリングの受診率が高いが、これは遺伝子検査の高い実施率、手術前の結果の受領、または両側乳房切除術の決定に結び付かないことが示唆された。[ 31 ]
保険の補償範囲
保険の補償範囲は、遺伝子検査を受けるかどうかを決定する個人にとって重要な考慮事項である。(詳しい情報については、がんの遺伝学的リスク評価とカウンセリングのPDQ要約の保険の補償範囲のセクションを参照のこと。)
多様な集団における遺伝カウンセリングと遺伝子検査の受診
多様な集団における遺伝カウンセリングと遺伝子検査の受診率
非白人集団での遺伝カウンセリングおよび検査の受診率に関するデータは限られており、これらの集団での受診率に影響を与える要素を定義するためさらなる調査が必要となる可能性がある。[ 32 ]BRCA検査の受診状況は、いくつかの人種/民族集団の間でさまざまである。少数の研究でアフリカ系米国人と白人女性の受診率が比較された。[ 4 ][ 33 ]大学ベースのプライマリケア医システムを受診した女性のケースコントロール研究では、乳がんまたは卵巣がんの家族歴を有するアフリカ系米国人女性は、同様の家族歴を有する白人女性と比較してBRCA1/BRCA2検査を受ける率が低かった。[ 33 ]臨床状況でBRCA1/BRCA2のリスクについてのカウンセリングを受けた乳がん患者を対象とした別の研究では、アフリカ系米国人女性の間で報告された受診率は白人女性よりも低かった。[ 4 ]
注目すべきなのは、これらの研究で観察された人種差が、費用、ケアを受ける機会、BRCA1またはBRCA2病原性多様体を有することに対する危険因子、または検査に対するリスク認識、懸念、態度など心理的因子の相違では説明されないと考えられることである。
多様な集団における遺伝カウンセリングと遺伝子検査の受診率に影響を及ぼす因子
数件の研究で、遺伝子研究プログラムに登録したアフリカ系米国人を対象にBRCA検査の受診または「受容」の状況が調査された。ユタ州のアフリカ系米国人家系からの登録者では、83%がBRCA1検査を受診していた。[ 34 ]年齢、キャリアである場合のリスクの認識、がんの知識を多くもっていることが、検査の受容を予測した。別の研究では、医師の紹介と地域による紹介を通じてアフリカ系米国人女性を募集したところ、BRCA1/BRCA2検査の受容率は22%であったことが報告された。[ 35 ]検査の受容を予測する因子として、病原性多様体の可能性が高いこと、結婚していること、当人のがんのリスクが不確かであることが挙げられた。最後に、都市部のがんスクリーニング実施施設での募集を通じて、リスクを有するがんアフリカ系米国人女性を対象として行われた3つ目の研究では、BRCA検査を受けた人の方が、乳がんの遺伝学について多くの知識をもっていたほか、否定的な情動反応、病気の烙印を押されるとの心配、家族に関係する罪悪感といった検査に対する障壁が低かった。[ 36 ]これらは遺伝子検査受診の独立した予測因子であるが、異なる民族間の検査受診率にみられる差異は説明できない。これらの差異を説明可能な因子は、多様な集団に属する個人が有する、検査に対するいくつかの態度と信念である。
ラテン系およびアフリカ系米国人の集団を対象とした乳がん遺伝子検査に対する態度を調査した研究では、検査についての知識や認識は乏しいものの、説明を受けた後は一般的に受容的であることが示された;白人と比較して、ラテン系およびアフリカ系米国人の集団では検査に対する関心が高い。
例えば、リスク状態で選別されていないラテン系米国人51人の質的研究で、被験者は遺伝学の知識が非常に乏しいにもかかわらず、遺伝性のがん感受性に対する遺伝子検査に高い関心を抱いていたという重要な知見が得られた。重大な障壁の1つは、がんと遺伝について家族で話し合った内容を明かしたくない、あるいはそれに困惑しているということに関係していたが、これらは介入戦略で対処することが可能である。[ 37 ]遺伝性乳がんのリスクがあるラテン系女性54人を対象とした別の定性的研究では、こうした女性はBRCA1/BRCA2カウンセリングについての知識は低いものの、家系員についてのリスク情報を得るためのカウンセリングについてもっと知りたいと関心を抱いていることが示された。カウンセリングに対する障壁には、生活要求、コスト、および言語の問題などがある。[ 38 ]
ペンシルバニア州ピッツバーグ都心部の健康センターネットワークから募集した患者314人(うち50%はアフリカ系米国人)に対する電話調査で、過半数の被験者(57%)(アフリカ系米国人と白人の両方)は、疾患リスクを評価する遺伝子検査はよい考えであるとの意見をもっていることを明らかにした;しかし、白人よりもアフリカ系米国人の方が、遺伝子検査は人種差別につながる(それぞれ37% vs 22%)と考え、遺伝学研究は非倫理的で自然を不当に改変している(それぞれ20% vs 11%)とみていた。[ 39 ]最後に、ジョージア州サバナの女性222人を対象とした研究では、過半数が乳がんの個人歴のない女性(70%)か家族歴のない女性(60%)であったが、アフリカ系米国人女性(サンプルの26%)は乳がん遺伝子と遺伝子検査を認識している率が低かった。認識率は、収入の高さ、教育水準の高さ、乳がんの家族歴があることにも関連していた。しかし、サンプル全体の74%が乳がん感受性を調べる検査を受診する意思を表明していた。[ 40 ]
BRCA1/BRCA2病原性多様体検査の基準を満たしているアフリカ系米国人女性146人のサンプルでは、米国外で生まれた女性は予期的な負の情動反応(例、恐怖、絶望、検査を情動的に受容するための自信の不足)をより高いレベルで報告した。乳がんに特異的な苦悩のレベルが高いことは、予期的な負の情動反応、守秘についての懸念、乳がん遺伝子検査が家族に与える影響に関して予想される罪悪感に関連していた。[ 41 ]将来への志向(例、「今の私の行いが、年をとってからの健康にどう影響するのか、よく考えるんです」)は、この集団における全体的な乳がん遺伝子検査の有益性に対する認識に関連していた(n = 140);しかし、将来への志向は、家族への罪悪感や検査が家族に及ぼす影響についての懸念など、家族に関連した見地からの検査に対する反対との間にも正の関連が認められた。[ 42 ]
BRCA1/BRCA2の多様体に対する遺伝子検査に関する提供者との話し合いと患者の受診には、人種による差がみられる。2007年から2009年に浸潤性乳がんと診断された18~64歳までの女性を対象にした研究では、病原性多様体リスクの調整後でさえ、アフリカ系米国人女性は医師による遺伝子検査の推奨を受け入れたと報告する割合が低かった。BRCA1/BRCA2検査が高価すぎることへの懸念はすべての人種間で差がなく、検査に対する態度や保険に関する懸念には最小限の差しかみられず、いずれの因子も検査の受診に影響を及ぼさなかった。[ 43 ]BRCA1/BRCA2遺伝子検査に適格な乳がんまたは卵巣がん生存者(N = 50)を対象にした1件の研究で、48%が遺伝カウンセリングおよび遺伝子検査に紹介された、および/または遺伝子検査を受けたことが明らかにされた。乳がん遺伝学についての知識が豊富であるか、自己効力のレベルが高い個人は、遺伝カウンセリングおよび遺伝子検査を受ける可能性が高かった。[ 44 ]2009年から2012年に浸潤性乳がんと診断され、Florida Cancer Data Systemの州の登録を介して確認され、既存のガイドラインの基準でBRCA1/BRCA2遺伝子検査に適格とされた50歳未満の女性を対象とした研究では、アフリカ系米国人は担当の医療提供者との話し合いを報告した率と遺伝子検査の利用率の両方が低かった。[ 45 ]同研究では、ヒスパニック系(61%)および非ヒスパニック系(65%)の白人で全体的な検査率が同程度であることが明らかにされた。ただし、検査率は、自宅で主にスペイン語を話すヒスパニック系で低く(スペイン語を話す人で50% vs 英語を話す人で69%;P = 0.0009)、一般にヒスパニック系は遺伝子検査が紹介される傾向が低かった。[ 46 ]しかしながら、この所見はすべての研究で一貫しているわけではない。Georgia and Los Angeles CountyにおけるSurveillance, Epidemiology, and End Results(SEER)登録を介して確認された非浸潤性(in situ)乳管がんまたは浸潤性乳がんの20~79歳の女性を対象にした研究では、既存のガイドラインの基準で全員がBRCA1/BRCA2遺伝子検査に適格とされたが、遺伝カウンセリングの受診または遺伝子検査に関する医師の判断による話し合いについて民族の差はみられなかった。[ 30 ]
遺伝カウンセリングと遺伝子検査の辞退に関連する因子
検査の辞退に関する主要な理由は、子供がいないことに関係していることが示されているが、この理由は家族関連のあらゆる受診動機を低下させる;さらに、保険を維持する上での困難、または個人の健康に関する心配など、検査による負の副産物に対する懸念も辞退の理由になる。
リスクがありながら検査を辞退した、つまり受けなかった個人の特徴についてのデータは限られている。検査辞退者は調査研究に参加したがらない場合もあるため、辞退者たちのサンプルにアクセスするのは困難である。遺伝子検査の受診についての研究は、診断を辞退するタイミングが異なること、また診断前の教育やカウンセリングの度合いが異なることから、比較が難しい。1件の研究では、検査に関するベースラインのインタビューを終えた、遺伝性乳がん/卵巣がん家系の罹患した個人および罹患していない個人の43%が診断を辞退したことが明らかになった。検査を辞退した個人の大半が教育セミナーへの参加を希望しなかった。辞退者は男性で未婚者である可能性がより高く、乳がんに罹患した近親者の数がより少なかった。高いレベルのがん関連ストレスを感じている辞退者は、より高いレベルの抑うつを訴えた。追跡ができない辞退者はがんに罹患する可能性が有意に高かった。[ 47 ]
別の研究では、BRCA病原性多様体を保有する可能性が25~50%の小人数の女性辞退者(13人)が対象とされた;検査を受けないこれらの女性は子供がなく、より高レベルの教育を受けている可能性が高いことが明らかになった。この研究では、ほとんどの女性がリスクと有益性についての真剣な説明を受けた後、受診しないと決めたことが示された。これらの女性の大半において、検査を受けない1つの理由として、頻繁なサーベイランスに対する満足度が挙げられた。[ 48 ]辞退の他の理由として、子供がないこと、および人生の比較的早い時期に家族において乳がん/卵巣がんをよく知るようになることが含まれる。[ 47 ][ 48 ]
第3の研究では、英国の大規模な多施設研究においてBRCA1/BRCA2の検査を拒否した34人の特徴が評価された。断った人は、検査を受けた国内のサンプルと比較して若く、断った女性は、がんに対する心配の測定でより低い平均スコアを示した。検査を断った人/延期した人の78%は自身の健康にリスクがあると考えていたが、BRCA1/BRCA2の病原性多様体状態について知ることは、以下に関する心配を引き起こすと報告した:
検査結果がもたらす影響に関する不安は、遺伝学診療所に行く時間や、仕事、家族、および社会的義務から離れる時間といった具体的な負担よりも、検査の辞退を決定する重要な因子であった。[ 49 ]遺伝学教育およびカウンセリングを受け、家系において証明された病原性多様体に対する検査を断った、遺伝性乳がんおよび卵巣がんの13家系の15%の個人(n = 31)では、検査を希望した個人と比較して、家族関係の前向きな変化、特に表現性と結束の高まりが報告された。[ 50 ]
小児における遺伝カウンセリングと遺伝子検査
BRCA1/BRCA2病原性多様体の検査はほぼ一般的に、18歳を超える成人に限定されている。子供の医学的理解力や、インフォームド・コンセントの同意能力に関する発育上のデータから推測して、成人発症型疾患(乳がんおよび卵巣がんなど)のために子供の遺伝子検査を行うことのリスクが、複数の報告において概説されている。[ 51 ][ 52 ][ 53 ][ 54 ]
複数の研究により、BRCA1/BRCA2遺伝子検査を受けた個人、または検査を受けた個人の子孫である成人は一般的に未成年者の検査を支持しないことが示唆されている。[ 55 ][ 56 ]データは限られているが、研究によると、男性、病原性多様体の非キャリア、母親に乳がんの個人歴がない個人は、一般的に未成年者の遺伝子検査を支持する傾向が強い。[ 55 ]研究実施時に未成年の子供がいた個人のうち、自身の子供に検査を受けさせることが望ましいと述べた人は、わずか17%であった。未成年の検査に関する懸念には、心理的リスクと十分に成熟していないことが挙げられた。潜在的有益性には、健康行動に影響を及ぼしうることが挙げられた。[ 56 ]
一部の研究者は、小児の乳がん/卵巣がんや他の成人発症型疾患に関する遺伝子多様体の検査が一般的に禁止されていることの根底にある仮定について、その妥当性を調べる必要があると考えているが、小児のBRCA1/BRCA2病原性多様体の検査に関するデータは存在しない。[ 57 ][ 58 ][ 59 ]ある研究では、遺伝子検査を受診した母親から選択されたグループ(その80%に乳がんの既往があり、全員がBRCA1/BRCA2検査について子供と話し合ったことがある)の子供20人(11~17歳)が、自身のがんに対する健康上の考え方や態度、がんに関する意識、および行動上の問題について記入した自己報告型の質問票を提出した。[ 60 ]子供たちの90%が自分たちも大人と同じようにがんリスクに関する情報が欲しいと考え、半分が自分自身または家族の誰かががんに罹患するのではと心配していた。感情的な苦悶および行動に関する問題の証拠は見られなかった。
人々が遺伝子検査にもち込むもの:リスクの認識、健康上の信念、および人格の特徴の影響
この分野の新しい文献では、乳がん/卵巣がん遺伝子検査に関する意思決定を行う上では、リスクの認識、健康上の信条、心理的状態、および人格の特徴が重要因子となることが示唆されている。BRCA1/BRCA2検査のために学術センターを受診する女性の多くは、自身が病原性多様体を保有していると強く信じ、遺伝子検査を受けることを決心しているが、リスクまたは検査の限界については、ほとんど情報をもたずに来院する。[ 61 ]遺伝カウンセリングの研究の被験者において、心理学的機能のベースラインの平均スコアのほとんどが、正常範囲内にあった。[ 62 ]それにもかかわらず、多くの遺伝カウンセリング研究の被験者のサブセットでは、不安、抑うつ、がんに対する心配の増加がみられる。[ 63 ][ 64 ]有害な結果を防ぐためには、これらの個人の同定は不可欠である。遺伝カウンセリングを求めた女性205人を対象にした研究では、がんに対する心配、乳がんリスクの認識、および乳がんの遺伝的多様体を有していることの重大性の認識の間に相互作用が認められ、心配しすぎで、乳がんリスクの認識が高く、重大性の認識が低い女性は、BRCA1/BRCA2検査を遂行する傾向がその他の女性より2倍高かった。[ 65 ]
リスク集団[ 66 ][ 67 ][ 68 ][ 69 ]、がん患者[ 67 ][ 70 ][ 71 ]、乳がんおよび卵巣がん患者の配偶者[ 72 ]、および一般集団の女性[ 73 ][ 74 ][ 75 ]において、乳がんおよび卵巣がんの遺伝的リスクを過大評価するという一般的な傾向が指摘されているが、比較的高リスクおよび平均リスクの女性における乳がんリスクの過小評価もまた報告されている。[ 76 ]このような過大評価により、BRCA1/BRCA2遺伝子検査は、現在考えられているより情報価値が高いという考えが助長される可能性がある。カウンセリングを実施しても、低リスクから中リスクの女性がもつBRCA1診断が価値あるものという思い込みを消すことができないという証拠がいくつかある。[ 32 ]医師の勧めたスクリーニングの実践を遵守しないことと、乳がんと卵巣がんの両リスクの過大評価は関連している。[ 77 ][ 78 ]乳がん/卵巣がんの遺伝カウンセリングの結果に関する12件の研究をまとめたメタアナリシスでは、カウンセリングによってリスク認識の正確性が改善されたことが示された。[ 79 ]
女性は、乳がん家族歴に関する家系内の主要な伝達者である。[ 80 ]父系伝達症例よりも母系伝達症例の方が数多く報告されているが[ 81 ]、それはおそらく家庭内のコミュニケーションのパターンにより、また、乳がんリスクは、母親側からのみ伝達されるという誤解、ならびに父方の家族歴を認識する方が、より遠いがん罹患近親者を同定する必要があり、より困難であるという理由が考えられる。Family Healthware Impact Trialに参加した2,505人の女性を対象とした解析では[ 82 ]、特定された父系家族歴が過少報告されている証拠が示されただけでなく、父系の乳がん家族歴を有する女性が知覚し報告した乳がんリスクは、母系の乳がん家族歴を有する女性よりも低いレベルにとどまっていた。[ 83 ]家族歴を調べる医師およびカウンセラーは、乳がん、卵巣がん、またはそれ以外の関連するがんについて、父方および母方の家族歴を聴取することが奨励されている。[ 80 ]
報告された乳がんまたは卵巣がんの家族歴の正確度はさまざまで、90%を上回る正確度が得られている研究もあるが[ 84 ][ 85 ]、第二度近親者またはそれより遠い血縁者のがん[ 86 ]またはがんの発症年齢[ 87 ]に関する報告では多くの誤りが認められる研究もある。乳がん以外のがんの報告では、より正確度が劣ることが明らかにされている。ある研究では、乳がん歴の報告の正確度は83%であるのに対し、卵巣がん歴の報告の正確度は60%であった。[ 88 ]医療提供者は、誤った乳がん家族歴の報告の中に、少数の公表されたミュンヒハウゼン症候群症例が含まれていることを認識する必要がある。[ 89 ]一部のケースでは、がん家族歴に関する母方情報提供者の早期死亡に関連して、意図しない間違いまたは知識不足が生じ、乳がん家族歴に関して間違った報告をすることは非常によくみられる。[ 80 ](詳しい情報については、PDQ要約がんの遺伝学的リスク評価とカウンセリングの家族歴の文書化のセクションを参照のこと。)
目的を絞った解説本[ 90 ][ 91 ]、ビデオ、CD-ROM、双方向型のコンピュータプログラム、ウェブサイト[ 92 ][ 93 ][ 94 ][ 95 ][ 96 ][ 97 ][ 98 ][ 99 ]、および文化的に目的を絞った教材[ 100 ][ 101 ][ 102 ]は、遺伝子検査の賛否について知識を増やす有効かつ効率の良い手段である。このような補助教材により、遺伝学とプライマリケア提供者による検査前教育およびカウンセリングに当てられる時間をより効率的に使え、非適格個人に遺伝子検査を見合わせるよう諭すことができる。[ 90 ]
乳がんの遺伝素因に関する遺伝カウンセリング
乳がんリスクについてのカウンセリングは、一般的に、BRCA1またはBRCA2に起因する可能性がある家族歴もつ個人を対象とする。しかしながら、リー-フラウメニ症候群、毛細血管拡張性運動失調症、コーデン症候群、またはポイツ・ジェガース症候群の家族歴を有する個人を含めることもある。[ 103 ](詳しい情報については、本要約の高浸透度の乳がんおよび/または婦人科がん感受性遺伝子のセクションを参照のこと。)
キャリアに対する管理戦略には、スクリーニングの性質、頻度、およびタイミングについての決定、ならびにサーベイランスの手順、化学予防、リスク減少のための手術、およびホルモン補充療法(HRT)の使用がある。保因者の女性のがん療法としての乳房温存術と放射線の利用は、病原性多様体状態の情報に左右される。(詳しい情報については、本要約のBRCA病原性多様体キャリアの臨床管理のセクションを参照のこと。)
また、カウンセリング項目には、関連する心理社会的懸念に対する配慮、計画的家庭内コミュニケーションの考察、乳がん、卵巣がんをはじめとするがんリスクの増大の可能性に関する他の家系員への警告に対する責任が含まれる。成人の受診に対する個々の反応は、他の家系員の結果に影響されることをデータが示唆している。[ 104 ][ 105 ]不安および苦悩への対処方法は、生活の質の因子として重要であるだけでなく、強い不安は、複雑な遺伝学および医療情報についての理解および統合、ならびにスクリーニングの遵守を妨げる可能性があるという理由からも重要である。[ 106 ][ 107 ][ 108 ]このような結果に対する正式かつ客観的な評価が詳細に報告されている。(詳しい情報については、本要約の感情的結果および行動に関する結果のセクションを参照のこと。)
BRCA1(後にはBRCA2も)検査に対するカウンセリングプログラムの公表された記述には、家族歴の収集と受診資格の評価の戦略、乳がん/卵巣がんの遺伝学および関連する医学的および心理社会的リスクと有益性についての相当量の関連情報を伝達するための戦略、そして、守秘と家庭内コミュニケーションについての専門化された倫理的考慮事項の考察がある。[ 109 ][ 110 ][ 111 ][ 112 ][ 113 ][ 114 ][ 115 ][ 116 ]多くのプロスペクティブ検査の候補者において、参加者の苦悩、がんについての侵入的思考、対処の方法および社会的支援が評価された。このようなプログラムで評価された心理社会的アウトカムには、カウンセリング後の乳がん/卵巣がんの遺伝学に関する知識、リスクに対する理解、心理的適応、家族および社会的機能、生殖および健康行動における変化が挙げられる。[ 117 ]遺伝性がん症候群に対するがんの遺伝カウンセリングを受けたカウンセリーとのコミュニケーション過程およびカウンセリーの満足度について調査したオランダの1件の研究により、(カウンセラーによって)医学的な質問を多く尋ねられること、多くの心理社会的情報が提供されること、およびカウンセラーによる長いアイコンタクトは満足度が低下することが示された。カウンセラーによって医学的情報が提供されることが、満足度および要求が満たされているという認識と最も強く関係した。[ 118 ]
心理社会的アウトカム研究の多くは、特殊化され、特に選択された調査集団を対象としており、この集団の一部は、BRCA1およびBRCA2をマップし、クローン化するために用いられた。このような例の1つは、広範囲に研究されたユタ州の1モルモン家系で800人を超える家系員を有する一族のK2082であり、この家系ではBRCA1病原性多様体が乳がんおよび卵巣がんの割合増大の原因となっている。この家系の家系員の乳がん/卵巣がんの遺伝学に関する理解度を調べた研究では、乳がん研究の対象となった集団においてでさえ、結腸がんおよび前立腺がんの関連リスク、RRMおよびRRSOという選択肢の存在、ならびに存在する心理社会的リスクの複雑さについて、知識が不十分であったことが示された。[ 109 ]21件の研究をまとめたメタアナリシスでは、カウンセリングが知識の向上およびリスク認識の正確性の改善に有効であったことが示された。遺伝カウンセリングは、不安、苦悩、またはがん特異的な心配を含め、がんのサーベイランス活動の情緒的アウトカムと、行動的アウトカムに与える長期影響に統計的有意性を示さなかった。[ 62 ]しかしながら、これらのプロスペクティブ研究は、がん特異的な心配に関する測定値の不均一性、およびベースラインからの効果の推移における矛盾した所見が特徴的にみられた。[ 62 ]
感情的結果
BRCA検査による有害な感情的結果の可能性について初期には懸念されていたが、長年にわたって実施されたほとんどの研究で、キャリアと非キャリアの両者における心理的苦悩のレベルは特に期間が長くなるほど低くなることが示されている。[ 119 ][ 120 ][ 121 ]検査結果を受け取った後、短期間(0~4週間)、中程度の期間(5~24週間)、および長期間(25~52週間)にわたってがん特異的な苦悩について調査した1件のメタアナリシスにおいて、キャリアでは結果を受け取った後、短期では苦悩のレベルが高くなり、中程度から長期間になるまでにベースライン時のレベルに戻ることが明らかにされた。[ 119 ]対照的に、非キャリアおよび結果の結論が出なかった個人は、経時的に苦悩のレベルが低くなることが示された。[ 119 ][ 122 ]心理的苦悩のパターンは、がんの個人歴、研究が実施された国といったいくつかの因子の関数として異なることが明らかにされた。がんの個人歴を有するキャリアでは、苦悩の低下が経時的にわずかに認められた一方、がんの個人歴のないキャリアでは変化は観察されなかった。結果の結論が出なかった個人に関して、がんの個人歴のない個人ではがんの個人歴を有する個人よりも大きな苦悩の低下が観察された。非キャリアに関して、米国の個人はヨーロッパおよびオーストラリアの非キャリアよりも心理的苦悩の低下が有意に大きかった。オーストリアで実施された研究では、カウンセリーの特定のサブグループ(高齢者、最近がんの診断を受けた、またはカウンセリングを受診したがBRCA検査を断られたなど)はより大きな苦悩を経験したことが示された。[ 123 ]
数件の研究により、上述のメタアナリシスで報告された感情的結果よりも長期間にわたる追跡(すなわち、結果の開示から12ヵ月以上)で示された感情的結果が報告されている。[ 119 ]英国の研究では、がんに関連する心配は3年間の追跡時にキャリアと非キャリアで差がなかった。[ 124 ]このメタアナリシスのレビュー[ 119 ]以降に発表された米国の2件の研究では、BRCA検査結果を受けた後、3年以上経過時に調査された女性においてよく似た所見が報告されている。[ 125 ][ 126 ]1件の横断研究[ 125 ]において、BRCA検査の結果を受けた後、4年以上が経過した時点で調査された女性167人は遺伝子検査に特異的な懸念のレベル(Multidimensional Impact of Cancer Risk Assessment Scaleを用いて測定)が低かった。[ 127 ]多変量回帰モデルによると、病原性多様体キャリアは苦悩を経験する可能性が非キャリアよりも有意に高かった。第2の研究[ 126 ]では、464人の女性が検査後中央値にして5年間(範囲、3.4~9.1年間)プロスペクティブに追跡された。罹患した参加者と非罹患の参加者の両者で、BRCAキャリアは、家系内の既知の病原性多様体に対する結果が陰性であった女性よりも、有意に高いレベルの苦悩、不確実性(罹患者のみ)、ストレスの認識(罹患者のみ)、および検査の経験を肯定的に考える割合の低さ(罹患者のみ)を報告した。[ 126 ]どちらの研究[ 125 ][ 126 ]も、非キャリアよりもBRCAキャリアの方が強い苦悩を報告したが、苦悩のレベルは臨床的に顕著な機能不全を表すほどではなかった。
ほとんどの研究では、陽性のBRCA検査結果は心理的苦悩に対して比較的わずかな影響しか及ぼさないことが報告されているが、これらの研究の多くは、乳がんまたは卵巣がんの強力な家族歴を有しており、検査前に広範な遺伝カウンセリングを受けた家系において実施されたものであった。このため、感情的反応は、異なる背景で検査を受ける個人に対し一般化されない可能性がある。例えば、集団BRCAスクリーニングにより検査を受ける個人はがんの家族歴を有さない場合がある。[ 128 ][ 129 ][ 130 ]検査前の遺伝カウンセリングが推奨されるが、遺伝子検査が遺伝学を専門としない医療提供者[ 131 ]に依頼されるか、商業会社を通じて直接依頼される場合はこれは必ずしも行われない。[ 132 ][ 133 ]
例えば、ユダヤ人の血筋を引く家系に一般的な3つのBRCA病原性多様体がないかを検査する集団ベースの遺伝子スクリーニング研究に参加したユダヤ人女性2,080人を対象にしたカナダの研究において、直接面談による遺伝カウンセリングは女性に提供されず、DNAサンプル提供前にBRCA1/BRCA2の遺伝子検査に関するパンフレットが渡された。遺伝子検査から1年後、病原性多様体が陽性であった女性(n = 18)では、がん特異的な苦悩における有意な増加がみられた一方で、病原性多様体が陰性であった女性では苦悩の変化が観察されなかった。[ 129 ]病原性多様体が既知の女性18人の苦悩の平均スコアは、Impact of Event Scaleで25.3(範囲、2~51)であった;18人中10人(56%)のスコアが中等度(26~43)(n = 7)または重度(44+)(n = 3)の範囲に入った。追跡の1年経過時に観察された苦悩の増加が直接面談による遺伝カウンセリングが行われなかったためであるのか、あるいはベースライン時に観察された苦悩のレベルが低かったのはこの研究の女性が低リスクであったが先祖のために検査に適格となったためなのか、この研究からは不明である。このコホートの追跡調査により、苦悩は検査後1~2年の間に低下したこと、およびキャリアが選択したリスク低減のための選択肢によって苦悩の変化は異なったことが明らかにされた。特に、リスク低減のための乳房切除術または卵巣摘出術を受けた女性では、いずれの手術も受けなかった女性と比較して苦悩が有意に低下した。[ 130 ]別のより小規模な定性的研究でも、これらの知見が支持されている。[ 134 ]
同様に、商業会社を介した消費者向け(DTC)BRCA検査の影響についても、さらに評価する必要がある。複数の症例研究により、DTC遺伝子検査でBRCA陽性の結果を受けた後に有害な情動反応が報告されていることから、商業会社を介して遺伝子検査を受けた女性の感情的結果をさらに評価する必要性が示唆されている。[ 132 ][ 133 ]商業会社により実施された唯一の研究で、この状況におけるBRCA検査の影響の評価が試みられている。[ 135 ]アシュケナージユダヤ人に一般的な3つのBRCA創始者病原性多様体の1つについて検査で陽性となった計32人の個人(女性16人、男性16人)が半構造化面接を受けた。極度の不安を報告したキャリアはいなかったが、一部のキャリアは中等度の不安(13%)または初期の失望および経時的に消散していく不安(28%)を経験した。案内されたBRCA病原性多様体キャリアのうち、この研究に参加したのがわずか24%(136人中32人)であったため、これらの所見の解釈には注意が必要であり、選択バイアスに関する懸念が生じている。
遺伝子検査の結果を受けた後、短期的に苦悩が増加するという証拠にもかかわらず、陽性のキャリア状態に対する有害な反応は12ヵ月以内に消散する。[ 119 ]検査前の遺伝カウンセリングの提供を受けない個人の感情的結果を検討するためにはさらなる研究が必要である。[ 131 ]
乳がんを新たに診断された患者における感情的結果
治療法の意思決定の助けとするために、診断時に遺伝カウンセリングと遺伝子検査を希望する乳がんの女性がますます一般的になりつつある。(詳しい情報については、本要約の序のセクションのがん診断時に遺伝子検査を提案する有益性のセクションを参照のこと。)診断と手術の間に迅速に遺伝カウンセリングおよび遺伝子検査を提供することの心理的悪影響に関する懸念が提起されているが[ 136 ][ 137 ]、ランダム化試験[ 141 ]を含む他の研究[ 138 ][ 139 ][ 140 ]では、新たに診断された乳がん患者にさらなる心理的悪影響がないことを示唆する証拠が得られている。1件のランダム化比較試験により、遺伝カウンセリングおよび遺伝子検査を早期に受けた患者は、標準ケアを受けている患者よりも治療法の意思決定に積極的に関わっていると感じていることが明らかにされた。[ 142 ]しかしながら、新たに乳がんと診断された患者20人を対象とした定性的研究では、がんの家族歴のないキャリア、識別できる近親者の中に罹患した人がいない患者、情報価値のないBRCA陰性の結果を知った高リスク女性など、患者のいくつかのサブグループにおいて、BRCA検査結果への対処がより困難になりうることが明らかになった。[ 136 ]
家族の効果
遺伝子検査および遺伝性リスクに関する家庭内コミュニケーション
がん感受性に関する遺伝子検査についての家庭内コミュニケーション、特にBRCA1/BRCA2遺伝子検査の結果についての家庭内コミュニケーションは複雑である。家庭内コミュニケーションおよび心理学的結果では、性別が重要な変数であると考えられる。複数の研究で、女性キャリアは、男性キャリアよりも他の家系員(特に姉妹および年齢14~18歳の子供)[ 143 ]に対して自分の状況を明かす可能性が高いことが実証された。[ 143 ][ 144 ]男性では、非キャリアの方がキャリアよりも姉妹または子供に検査結果を明かすことが多かった。自身の検査結果を姉妹に明かしたBRCA1/BRCA2キャリアでは、心理的苦悩がわずかに軽減したのに対して、検査結果を姉妹に話さないことを選択したキャリアでは心理的苦悩がわずかに増大した。家系員に病原性多様体が既知であることを明かすことが非常に困難であったと報告した男性の割合は女性より高かった(90% vs 70%)ことを明らかにした研究が1件ある。[ 145 ]
近親者に対するBRCA1/BRCA2検査結果の家庭内コミュニケーションは、検査受診に影響する別の因子である。FDRおよび第二度近親者とのコミュニケーションに関する研究はより離れた家系員とのコミュニケーションに関する研究よりも多い。BRCA1/BRCA2検査結果についての姉妹間のコミュニケーションのプロセスおよび内容を調査した研究がある。[ 146 ][ 147 ]研究結果から、病原性多様体キャリア[ 146 ]および情報価値のない結果を受け取った女性[ 146 ][ 147 ]はいずれも遺伝的リスクに関する情報を提供するために姉妹とコミュニケーションをもつことが示唆される。情報価値のない結果を受け取った女性が検査結果を娘に明かすという同様の所見が報告された。[ 147 ]近親者間で遺伝子検査結果について話し合わない場合、最も重要な理由として罹患した女性は彼女たちの近親者と近しくない[ 146 ]か、近親者との関係が乏しい[ 147 ]ことが挙げられた。複数の研究で、BRCA病原性多様体を保有する女性は、彼女らの父親や成人した兄弟、息子よりも、母親や成人した姉妹、娘に検査結果をより頻繁に話すことが判明した。[ 80 ][ 148 ][ 149 ][ 150 ][ 151 ]開示後4ヵ月経過時点で検査結果をFDRに話したかを評価した1件の研究では、40歳以上の女性はそれより若い女性と比べて、検査結果を両親に知らせる可能性が高いことが明らかにされた。参加者は、BRCA病原性多様体が父系遺伝による場合、結果を兄弟に知らせる可能性もより高かった。[ 149 ]別の研究では、開示は主としてFDRに限定されること、およびより遠い近親者に情報を流すのは問題があることが明らかにされた。[ 152 ]年齢は遠い近親者への情報提供という点で重要な因子であり、若年の患者の方が遺伝子検査結果について話すことをいとわなかった。[ 146 ][ 148 ][ 152 ]また、1件の研究で、遺伝的な心配が低い、ゲノム情報への関心が高い、BRCA1またはBRCA2病原性多様体を保有する、あるいは未婚であると、より多くの家系員とコミュニケーションを取ることが明らかにされた。[ 144 ]対照的に、診断からの期間が長くなると、コミュニケーションを取る家系員が少なくなった。[ 144 ]
少数の徹底的な定性的研究で、遺伝子検査についての家族のコミュニケーションと関連する問題が調べられている。これらの研究からの知見は、より大きなリスク集団に一般化することはできないものの、それらは家族の中で遺伝性のがんリスクを伝えることに関係する問題の複雑さを表している。[ 153 ]家族性がんの遺伝子クリニックに来る女性に行った15件のインタビューを基に、女性は近親者と遺伝子検査について議論しなければいけないという義務感を感じ、また、半信半疑、敬愛、孤立の矛盾する感情も抱くと著者は結論した。遺伝性のがんおよび遺伝子検査について、家族の中で誰に知らせるか、どのように伝えるかの決定は、女性の社会的役割を満たす必要性と自分自身や他の者に対する彼女らの責任との間の緊張に影響される可能性がある。[ 153 ]家族性乳がんおよび卵巣がんの遺伝子クリニックを受診した女性21人の別の定性的研究では、がんに関する自身の恐れおよび心配のために、パートナーおよび特定の近親者、特に兄弟に遺伝性がんリスクに関して伝えることは難しいと考える女性がいることが示唆された。[ 151 ]この研究ではまた、家系内で遺伝性リスク情報がどの程度共有されるかは、一般的にがんについてコミュニケーションを取るための既存の基準によって異なることが示唆された。例えば、家系員は一般的にがんに関する情報を互いにオープンに共有する、自身または他の近親者を否定的な情動反応から保護するために特定の家系員とはがんの情報について話し合うことを選択的に回避する、または他の家系員への情報開示の仲介者になってもらうよう、特定の血縁者に頼むことがある。[ 154 ]友人、遺伝性がんリスクの情報について信頼のおける友人、このような情報に対処するための支えの源など、家系以外の人の潜在的な重要性もまたこの研究で指摘された。[ 151 ]
BRCA病原性多様体が明らかになった母親31人の研究では、子供に対する伝達パターンが調査された。[ 155 ]検査結果を子供に開示することを選択した母親では、子供の年齢が最も重要な因子であった。結果を教えられた子供の50%が20歳~29歳で、19歳以下の子供は25%をわずかに上回るに過ぎなかった。結果を知らされた息子と娘の数は同じであった。70%を超える母親が検査結果を知ってから1週間以内に子供に結果を知らせた。子供と結果を共有しないことを選択した母親の93%が、その理由を子供が若すぎるからと指摘した。これらの知見は、13歳未満の子供はより年齢の高い子供と比較して検査結果を知らされる可能性が低いことを示す3件の別の研究とも一致した。[ 149 ][ 156 ][ 157 ]BRCA1/BRCA2検査を受けた母親187人を対象にした別の研究では、BRCA1/BRCA2検査の結果を子供も共有することについて、円滑に話し合いを進めるために用意する資料の必要性が評価された。78%の母親が3つ以上の資源に関心を示し、これには文献(93%)、家族のカウンセリング(86%)、以前の参加者との会話(79%)、およびサポートグループ(54%)が含まれた。[ 156 ]
BRCA1およびBRCA2病原性多様体に対する遺伝子検査を自ら紹介した153人の女性および彼女らの118人のパートナーを対象にした縦断的研究では、遺伝子検査についてのコミュニケーションおよび苦悩が検査前および検査後6ヵ月経過時に評価された。[ 158 ]この研究により、ほとんどのカップルが検査を受ける決定について話し合い(98%)、検査参加者のほとんどはパートナーが支持的で、ほとんどの女性が検査結果をパートナーに開示したことが明らかにされた(97%、n = 148)。検査前の話し合いでパートナーが支持的であると感じた検査参加者は開示後の苦悩がより少なく、検査参加者と検査前に心配を共有することに安らぎを感じたパートナーは開示後の苦悩がより少なかった。6ヵ月の追跡で、参加者の22%が面談前の1週間中に検査の経験についてパートナーと話す必要があると考えたことが明らかにされた。ほとんどの参加者(72%、n = 107)は、パートナーとの心配の共有で安らぎを報告し、5%(n = 7)は遺伝子検査の結果として関係の緊張を報告した。遺伝子検査の結果が陽性であった女性のカップルでは、結果が真陰性または情報価値のないものであった女性のカップルよりも、関係の緊張、パートナーの保護的な緩衝、および関係する心配についての話し合いが多くなったことが報告された。[ 158 ]
BRCA1/BRCA2遺伝子検査を受けた女性のFDR561人を対象にした研究では、遺伝子検査の結果は共有されていると女性が報告しているにもかかわらず、FDRの22%が遺伝子検査の結果について知らされたことを思い出せなかった。[ 159 ]男性は結果を受けたことをさらに思い出せなかった(P > 0.001)。検査結果を受けたことについて覚えているFDRのうち、10.5%は所見について思い出せなかった。結果を覚えているFDRのうち、17.9%は解釈が正しい結果と一致していなかった。検査結果の記憶の正確度は、情報価値のある検査結果(真の陽性または真の陰性のいずれかの結果)については大きかった(P = 0.029)。しかしながら、検査結果にかかわらず、FDRは所見について知る前の方が後よりもがんリスクが高いと認識していた(検査結果を聞く前と後では、それぞれFDRの74%および53%が平均よりもがんリスクが大きいと思うと報告していた)。
乳がんの家族歴を有する男性およびBRCA診断受診を考慮しているかまたは受診した男性における心理的影響に関する、小規模だが増えつつある論文がある。アイルランドの16組の高リスク家族に属する22人の男性の定性的研究では、娘がいる男性の方がいない男性よりも検査を受ける人数が多かった。これらの男性は、親戚とこの病気についてのコミュニケーションはほとんどないと報告し、女性の家系員たちの間で行われるがんに関する話し合いから排除されていると報告する者もいた。この研究の何人かの男性はまた、娘や他の近親者とのオープンな話し合いを意識的に避けたと報告した。[ 160 ]対照的に、BRCA1/BRCA2病原性多様体検査が陽性の男性59人を対象にした研究では、ほとんどの男性が乳がんおよび/または卵巣がんについての家庭内での話し合いに参加していた。しかしながら、リスク低減のための手術についての家庭内での話し合いに参加している男性は全体の半数以下であった。BRCA診断を受診する主な理由として、子供たちに対する配慮、および自分の病原性多様体が子供に遺伝したかどうかについての確信が必要であることが挙げられた。この研究では、参加男性の79%が少なくとも1人の娘をもっていた。ほとんどの男性がBRCA検査結果を受け取った後に彼らの関係がどう強化され、それが家庭におけるコミュニケーションおよび理解を深める助けとなったことを述べている。[ 161 ]両研究の男性はともに、自分自身にがんが発生することに対する恐怖を表した。アイルランド人男性は、特に性的器官におけるがんに対する恐怖を報告した。
家族の機能
1件の研究では、遺伝カウンセリングを受け、家系に病原性多様体が確認されているためにBRCA1/BRCA2検査を勧められた遺伝性乳がんおよび卵巣がんの13家系に属する212人が評価された。検査を受けなかった個人では、6~9ヵ月後の家族の表現力および結束力において、検査を受けた人と比較して有意に大きな増加が認められた。問題解決のための遺伝カウンセリング介入にランダムに割り付けた人に対して、クライアントを中心にした遺伝カウンセリング介入にランダムに割り付けた人では、検査結果に関係なく葛藤が有意に大きく減少した。[ 50 ]
高リスク女性のパートナー
がんを発症するリスクが高い女性を対象に、BRCA1/BRCA2病原性多様体を保有していること、またはがんの強い家族歴を有することを基にして、その心理学的影響を調査している研究が多くある。そうした女性のパートナーに対する影響について調査している研究もある。
カナダの研究では、BRCA1/BRCA2病原性多様体を有することが確認された女性の配偶者59人が評価された。配偶者は全員、遺伝子検査を受ける妻の決定を支持し、17%は遺伝子検査の過程にもっと関わりたかったと願っていた。遺伝子検査は自分たちの関係に影響しなかったと報告した配偶者は長期にわたる関係を有していた(平均期間27年間)。46%の配偶者が、主な心配事はパートナーががんで死亡することだと報告した。配偶者ががんを発症するのではないかと19%が心配し、子供もBRCA1/BRCA2病原性多様体キャリアではないかと14%が心配した。[ 162 ]
米国の研究で、BRCA1およびBRCA2病原性多様体の遺伝子検査を受けた女性のパートナー118人が、検査前および結果開示から6ヵ月後に調査を受けた。6ヵ月時に検査結果を話されていないと報告したパートナーはわずか10人であった。91%が検査は自分たちの関係に緊張を引き起こさなかったと報告した。検査前に心配事を共有することに問題がなかったパートナーでは、検査後の苦悩が低かった。保護的な緩衝(protective buffering)はパートナーの苦悩レベルに影響すると明らかにされなかった。[ 158 ]
乳がんおよび/または卵巣がんを発症するリスクが高い非罹患女性95人(病原性多様体キャリア13人および多様体状態が不明の女性82人)およびそのパートナーを対象にしたオーストラリアの研究によると、男性パートナーの大部分は標準的集団のサンプルと同程度の苦悩のレベルを示したが、10%はさらなる臨床介入を必要とする有意な苦悩レベルを示したことが明らかにされた。よく監視を行う対処スタイルで妻の乳がんリスクを強く認識している男性ほど、高いレベルの苦悩を報告した。過去1年間の妻の家系におけるがんに関係したイベントの発生に関して男性とパートナーとのコミュニケーションがオープンである場合は、苦悩のレベルがより低かった。自身とパートナーに対し、どのような種類の情報や支援を男性が希望するかと質問された場合、57.9%の男性が乳がんおよび卵巣がんに関するより多くの情報を希望し、32.6%の男性がパートナーのリスクに対処する際により多くの支援を希望した。25%の男性により、パートナーを最も良好に支援する方法に関する方策、診察に参加するよう医療専門家からの強い奨励、および他のパートナーとの集会など、高リスク女性のパートナーに対するサービスを改善する方法についての示唆が得られた。[ 163 ]
この文献のレビューから、BRCA検査の過程は、特に配偶者がキャリアとして同定された男性パートナーに苦痛を与える可能性があることが報告された。男性パートナーの苦痛は、女性パートナーの乳がんリスクに関する信念、カップルのコミュニケーション不足、および検査の過程からの疎外感と関連しているようである。[ 164 ]
高リスクの男性
BRCA1およびBRCA2病原性多様体が既知の家系における男性の経験に関する文献レビューによると、データは限定的であるが、多様体陽性家系の男性は、カウンセリングおよび検査過程を含むすべての段階において、女性よりも遺伝に関するコミュニケーションに参加しない傾向があることが報告されている。男性には女性近親者が受け取った遺伝検査結果がほとんど知らされない傾向があり、また、これらの家系の多くの男性は自身の遺伝子検査を進めようとしない。[ 165 ]
BRCA1病原性多様体を継承するリスクが高いオランダ人男性を対象にしたある研究によると、男性たちは、自分のリスク状態から受ける感情的影響を否定するか、または最小限に抑え、ひたすら女性近親者に対する医学的な意味合いに注目する傾向があったと報告している。しかしながら、このような家系の男性は、女性近親者に関連する相当な心理的負担を報告した。[ 166 ]乳がん検査実施中における男性の心理学的機能に関する別の研究では、異なった高リスクの18家系(BRCA1/BRCA2病原性多様体を受け継いでいるリスクが25%または50%)に属する男性28人が参加した。この研究の目的は、BRCA1/BRCA2病原性多様体を保有するリスクがあり、遺伝子検査を申し込んだ男性を対象に苦悩について解析することであった。この研究では、ほとんどの男性の診断前の苦悩は小さく;楽天的な男性または娘がいない男性でスコアは最も低かった。病原性多様体キャリアのほとんどは、正常レベルの不安と抑うつを訴え、罪悪感の報告はなかったが、娘が乳がんまたは卵巣がんを発病したら苦悩および責任感が増大するだろうと述べた者もいた。非キャリアで罪悪感を報告したものはいなかった。[ 167 ]1件の研究[ 161 ]では、検査後の推奨される検診ガイドラインへの遵守度が解析された。この研究では、男性病原性多様体キャリアの半数以上が遺伝子検査結果開示後に推奨された検診ガイドラインを遵守しなかった。これらの知見は、BRCA1/BRCA2病原性多様体の女性キャリアに関する知見と一致する。[ 161 ][ 168 ]
英国の多施設コホート研究で、BRCA1/BRCA2検査のプロスペクティブな結果が193人を対象に調査されたが、このうちの20%が28~86歳の男性であった。男性の苦悩のレベルは低く、キャリアと非キャリアで差は認められず、ベースライン(遺伝子検査前)から3年の追跡で変化しなかった。男性病原性多様体キャリアの22%が大腸がんスクリーニングを受け、44%が前立腺がんスクリーニングを受けた[ 124 ];しかしながら、この研究における男性が年齢に応じたスクリーニングのガイドラインに従っていたかどうかは不明である。
小児
数件の研究において、リスクのある子供に対するBRCA検査結果の伝達が調査されている。すべての研究において、4歳~25歳に及ぶ子供への開示率は約50%である。[ 148 ][ 149 ][ 152 ][ 156 ][ 169 ][ 170 ][ 171 ][ 172 ]一般的に、検査結果を開示するかどうかを決定する際には、子供の年齢が最も重要な因子であった。BRCA検査結果を開示した母親31人を対象とする1件の研究において、結果を教えられた子供の50%が20歳~29歳で、19歳以下の子供は25%をわずかに上回るに過ぎなかった。結果を知らされた息子と娘の数は同じであった。[ 155 ]同様に、BRCA病原性多様体キャリアの女性42人を対象にした別の研究において、18歳を超える子供の83%が結果を教えられたのに対して、13歳以下の子供で結果を教えられたのはわずか21%であった。[ 156 ]
数件の研究ではまた、親が検査結果を受けた後の子供への開示の時期も調べられている。大部分の子供が結果開示後1週間から数ヵ月以内に知らされたが[ 149 ][ 155 ][ 156 ]、開示を遅らせることを選択した親もいる。[ 156 ]開示を遅らせる理由は、子供が成長するのを待っている、親が情報に適応する時間を与えている、および直接会って結果を共有できるまで待っている(成人した子供が家を出て生活している場合)が挙げられた。[ 156 ]
ある研究では、自分がキャリアであることを13歳以下の子供に話した参加者は、心理的苦悩が増大し、子供に話さなかった被験者は、心理的苦悩がわずかに軽減した。若年の子供とのコミュニケーションは、年齢や親/子のコミュニケーションスタイルなどの発達変数によって影響されることが明らかになった。[ 171 ]
1件の研究により、結果開示に対する子供の反応または結果伝達が親子関係に及ぼす影響が調べられた。[ 156 ]子供の情報の理解については、1件の研究における親のほぼ半数が子供は陽性の検査結果の重要性を理解していないようであると報告したが、年齢の高い子供はより良く理解していることが報告された。この同じ研究ではまた、親の48%が子供の少なくとも1つの否定的な反応を報告し、それは不安または心配(22%)から泣くことおよび恐怖(26%)に及んだことが示された。しかしながら、この研究において子供の理解のレベルおよび検査結果への反応は定性的に測定され、親の認識のみに基づいていたことに注意すべきである。また、研究デザインがレトロスペクティブであったため、思い出しバイアスの可能性もあった。子供の年齢または性別による情動反応における有意差は認められなかった。最後に65%の親が子供との関係に変化はないと報告した一方で、5人の親(22%)は関係が強くなったことを報告した。
興味深いことに、母娘ペア869組(娘は6~13歳)を対象とした大規模な多施設共同研究によると、乳がんの家族歴または家族性BRCA1/BRCA2病原性多様体(BCFH+)を有する少女は、このような家族歴がない少女と比較して母親報告による心理社会的対応が良好であることが明らかになった。[ 173 ]しかしながら、母親報告と10~13歳の少女の直接評価を組み合わせた結果に基づくと、BCFH+ の少女は、このような家族歴のない同年齢の少女よりも大きな乳がん特異的苦痛と強い乳がんリスク認識を経験した。さらに、娘の苦痛が大きいほど母親の苦痛も大きかった。11~19歳の年長の女児を対象とした同様なデザインの研究で、娘で乳がん特異的苦悩が高いことは、認識されたリスクおよび母親の苦痛と関係していることが明らかにされた。この年長グループでは、乳がんの家族歴がない同年齢の女児より自尊心が強かった。[ 174 ]
BRCA1/BRCA2検査を受けた母親187人を対象にした別の研究では、BRCA1/BRCA2検査の結果を子供も共有することについて、円滑に話し合いを進めるために用意する資料の必要性が評価された。78%の母親が3つ以上の資源に関心を示し、これには文献(93%)、家族のカウンセリング(86%)、以前の参加者との会話(79%)、およびサポートグループ(54%)が含まれた。[ 175 ]
BRCA1/BRCA2の検査は、ほとんど例外なく18歳を超える成人に限定されている。子供の医学的理解力や、インフォームド・コンセントの同意能力に関する発育上のデータから推測して、成人発症型疾患(乳がんおよび卵巣がんなど)のために子供の遺伝子検査を行うことのリスクが、複数の報告において概説されている。[ 51 ][ 52 ][ 53 ][ 54 ]成人発症型遺伝性がんのために子供を受診させることへの両親の関心に関する調査では、両親は、自分自身が乳がん遺伝子検査を受診するよりも子供が受診することにより熱心であり、医療提供者側に葛藤が生じる可能性がある。[ 176 ][ 177 ]米国の一般集団を対象にした調査では、親の71%が、自分たちが乳がん素因遺伝子の病原性多様体キャリアと仮定した場合に、乳がん遺伝子の状態を調べるために13歳の娘に直ちに検査を受けさせる可能性が中等度に、非常に、またはきわめて高いと回答した。[ 176 ]現在まで、子供に対するBRCA1/BRCA2検査に関するデータは存在しないが、子供に対して乳がん/卵巣がんおよび他の成人発症型疾患の遺伝子検査を一般的に禁止する根底にある仮定の妥当性を、検証する必要があると考えている研究者もいる。[ 57 ][ 58 ][ 59 ]ある研究では、遺伝子検査を受診した母親から選択されたグループ(その80%に乳がんの既往があり、全員がBRCA1/BRCA2検査について子供と話し合ったことがある)の子供20人(11~17歳)が、自身のがんに対する健康上の考え方や態度、がんに関する意識、および行動上の問題について記入した自己報告型の質問票を提出した。[ 60 ]子供たちの90%が自分たちも大人と同じようにがんリスクに関する情報が欲しいと考え、半分が自分自身または家族の誰かががんに罹患するのではと心配していた。感情的な苦悶および行動に関する問題の証拠は見られなかった。同グループによる別の研究では[ 171 ]、BRCA1/BRCA2遺伝子検査結果を開示した1ヵ月後に、登録された8~17歳の子供の母親42人のうち53%が、1人以上の子供と診断結果について話し合ったことが明らかにされた。家族の健康に関するコミュニケーションスタイルと同様に、母親の病原性多様体の状態よりも、むしろ子供の年齢が結果を話すかどうかに影響していた。
出生前診断および着床前遺伝子検査
遺伝性乳がんおよび卵巣がん(HBOC)が影響する家族にとって、子供に病原性多様体を伝達する可能性によって懸念が生じる場合があり[ 178 ]、おそらくキャリアによっては出産を回避する程度の懸念が生じる。[ 179 ][ 180 ]これらの懸念から、伝達のリスクを低下させるのに役立つように出生前検査法の利用を検討する女性もいる。[ 178 ][ 181 ]出生前診断は、胎児における遺伝学的障害の存在を評価するために実施される何らかの医学的手技を表す場合に用いられる包括的な用語である。方法としては、羊水穿刺および絨毛膜絨毛サンプリング(CVS)などがある。[ 182 ][ 183 ]どちらの手技もある程度の流産のリスクがあり、これらの検査を使用した結果、胎児異常が起こりうることを示唆する証拠もある。[ 182 ][ 183 ]さらに、胎児が遺伝学的欠陥のキャリアであると分かると、カップルは妊娠の継続か中絶かに関する難しい意思決定を迫られる場合がある。こうした検査に代わる方法としては、受精した胚を子宮着床前に遺伝学的障害がないか検査するために用いられる手技である着床前遺伝子検査(PGT)があり[ 178 ][ 184 ][ 185 ]、これにより羊水穿刺およびCVSに伴う潜在的な危険性も、妊娠中絶の決定も回避できる。遺伝子検査から得られる情報を利用して、妊娠を希望する両親は着床させるかどうかを決定できる。PGTを用いて、BRCAなど、遺伝性がん素因遺伝子における病原性多様体を検出することができる。[ 178 ][ 181 ]
米国では、HBOCリスクの高い個人に焦点を当てた提唱組織であるFacing Our Risk of Cancer Empowered(FORCE)のメンバーにおけるPGTに関する認識、関心(例、PGTの利用を検討する)、および態度が一連の研究で評価されている。[ 178 ][ 181 ][ 186 ]最初の研究は283人のメンバーを対象にしたインターネットでの調査で[ 178 ]、第2の研究には2007年のFORCEの年次会議に参加した205人が含められ[ 181 ]、第3の研究は962人のメンバーを対象にしたインターネットでの調査であった。[ 186 ][ 187 ]これらの研究により認識の低さが証明され、研究参加前にPGTについて聞いたことがあると報告したのは、研究に回答したメンバーの20~32%であった。[ 181 ][ 186 ]PGTへの関心については、最初の研究[ 178 ]ではPGTを利用する可能性が高い女性はわずか13%であると分かったが、その後のFORCEの研究では33%の回答者がPGTの利用を検討すると報告された。[ 181 ][ 186 ]第3のFORCEによる研究(n = 962)[ 186 ]では、多変量解析によりPGTへの関心は、より多くの子供をもうけたいという願望、以前に出生前遺伝子検査を受けていること、およびPGTの以前からの認識に関連していることが明らかにされた。PGTへの関心の態度予測因子としては、HBOCのリスクを有する他の人にPGTを提供すべきであるという合意;HBOCのリスクを有する人にPGTは容認できるという考え;HBOCのリスクを有する人にPGTの情報を与えるべきであるという考え;および遺伝的多様体がない子供を授かり、遺伝性疾患を排除するPGTの利益に対する支持が挙げられる。逆に、PGTは「あまりにも神のような振る舞い」であると指摘し、宗教的にPGTを考えていることを報告した個人はPGTにあまり関心を示さなかった。
PGTに対するFORCEメンバーの態度がBRCAキャリアの大多数を代表するものであるかどうかは明らかでない。BRCAキャリア1,081人を対象とした横断研究では、その65%がFORCEを通して、また残りがUniversity of Pennsylvaniaにより募集され、キャリアに対するPGTおよび出生前診断が提供されることをキャリアの大多数(PGTで59%および出生前診断で55.5%)が支持したことが明らかになった。[ 188 ]家族が不完全だと表明した人のうち、BRCAキャリアの41%は、将来の生物学的な子供に関する決定にキャリア状態が影響を及ぼしたと報告した。この研究では、パートナーのいないBRCAキャリアの21.5%が結婚したいと考えていることも明らかにされた。
英国のHuman Fertilization and Embryologyの権威により、遺伝性乳がんおよび卵巣がんに対するPGTの使用が承認されている。BRCA病原性多様体を有する女性102人のサンプルにおいて、ほとんどがPGTを支持したが、出産を完了していた女性のうちPGTが利用できていたら個人的にPGTを検討していただろうと返答したのは38%のみで、将来の妊娠を考えていた女性のうちPGTを検討すると返答したのは14%のみであった。[ 189 ]スペインの1件の多施設コホート研究の一環としてBRCA検査を受けた個人77人の研究では、回答者の61%がPGTを検討すると報告した。PGTへの関心と関連した因子は、40歳以上および以前のがん診断経験であった。[ 190 ]
フランスでは、集学的な出生前診断チームにより承認されたカップルは、国の医療制度のサービスとして無料でPGTを利用することができる。しかし、これまでBRCAキャリアにPGTの利用が承認されたことはない。生殖可能年齢(女性18~49歳;男性18~69歳)の非罹患BRCA病原性多様体キャリア490人を対象とした国内研究では、16%がBRCA検査結果により進行中の出産計画を変更していた。[ 191 ]回答者が記述したコメントの定性分析によると、主な影響は妊娠時期を早めることや、病原性多様体が子孫に受け継がれる可能性に対する罪悪感、将来子供をもうけることに関連していた。仮にPGTが広く利用されるようになったらどうするかという設問に対しては、被験者の33%がPGTを受けると回答した。この意思に関連する要因は、調査時点で将来子供をつくる計画がないこと、BRCA病原性多様体が特定された場合に妊娠中絶という選択肢を受容できること、家族に乳がんおよび/または卵巣がんに罹患した人が少ないことであった。PGTまたは出生前診断(PND)情報の提供を期待するかどうかの設問については、回答者の85%がBRCA検査結果とともに提示すべきと考えていた;また45%はキャリアが子供をつくることを決めた時点で提示すべきとした。また回答者は、この情報の提供者として適していると考えられるのは、がん遺伝学者(92%)、産科医/婦人科医(76%)、一般医(48%)であると回答した。
生殖可能年齢で子供をつくる前に遺伝子検査を受けたBRCA病原性多様体陽性の女性(N = 25)を対象とした小規模な定性的研究では、自身のBRCAの状態が生殖遺伝子検査(PGTよびPNDの両方)に関する考え方および子供をつくる決心にどのように影響を与えたかを評価した。[ 192 ]この研究で、BRCA検査を受ける決断は、将来出産を決断するための情報を得たいというよりも、個人的ながんリスクを管理したいことが第一の動機であった。HBOCの重症度の認識は、BRCA病原性多様体が子供に受け継がれることに関する懸念に影響を与えるとともに、PGTまたはPNDを検討する意欲にも影響を与えたが、個人的な経験によってさまざまであった。BRCA病原性多様体が既知であることが妊娠中絶の理由になるとはほとんどの人が考えなかった。先の研究で観察されたように、出産の選択肢に関する理解度はさまざまであった;しかしながら、参加者の間では妊娠中絶に関してPNDよりPGTの方が受け入れやすいとみなす傾向にあった。妊娠中絶でPGT vs PNDの賛否に関する決断は、道徳的判断ではなく、主に個人的な好みおよび経験によって導かれた。例えば、体外(in vitro)受精を受けてがんリスクを高める可能性があるホルモンを摂取する必要性を基に、この治療を受けた他の人の経験を観察することによってPGTを思いとどまった女性たちがいた。
FORCEおよびCraigslist(掲示板ウェブサイト)により募集された高リスクの男性(N = 228)を対象に、これらの問題を検討した研究が1件ある。[ 193 ]女性を対象とした過去の研究と同様に、調査への参加前にPGTについて知っていた男性は、わずか20%であった。多変量解析によると、いくつかの規定選択肢(例えば、遺伝的多様体のない子供をもつことなど)から選択した男性、および(健康上および安全上に対して)信仰上の理由でPGTを検討した男性と比較して、PGTの潜在的有益性のために「その他」の選択肢を選択した男性は、次があればPGTの使用を検討するだろうと回答する傾向が低かった。
文化的/地域社会的影響
乳がん/卵巣がん家系だけでなく、いくつかの民族集団においてBRCA1/BRCA2病原性多様体が広く認められるという認識は[ 194 ]、個人の民族性を疾患素因決定における一因子とすることの倫理的、心理学的、およびその他の意味合いについての多くの議論につながっている。人々がすべてはもっぱら遺伝的要因によって決定されると考えるようになることや、遺伝的な下層階級を作り出すことに対する懸念[ 195 ]が表明されている。乳がんに対する遺伝的脆弱性を有するものとして選び出される集団に対する影響に関する問題が提起されている。また、この集団の遺伝的アイデンティティの研究に関与するために、誰が許可を与え、または与えずにおくのかについて混乱もある。これらの問題は、個人の自主性の1機能としてのインフォームド・コンセントに対する従来の見方に挑むものである。[ 196 ]
さまざまな文化的サブグループに影響を与える固有の要因に関する文献が増えており、それらは文化に合った遺伝カウンセリングおよび教育的アプローチを開発することの重要性を提唱する。[ 100 ][ 197 ][ 198 ][ 199 ][ 200 ][ 201 ]利害が一致した団体内のメンバー(例えば、乳がん生存者、擁護者、団体リーダーなど)を含めることで、個々の文化に応じた遺伝カウンセリング教材の開発が促進される可能性がある。[ 101 ]1件の研究では、何らかの遺伝カウンセリングへの参加(文化的に仲介されたアプローチまたは標準のアプローチ)によって、認識されていた乳がん発症リスクが低下したことが示された。[ 202 ]
倫理的問題
複数の症例研究[ 203 ]、エッセイ[ 204 ][ 205 ]および研究報告の中で、乳がん/卵巣がん感受性に関する遺伝子検査の出現によって提起された倫理問題の人間的意味合いが記述されている。遺伝リスクについての情報の広がりに関する家族の権利および責任の問題は、今後数十年間、主要な倫理的かつ法的なジレンマになると見込まれる。
複数の研究で、調査対象家系員の62%が家族歴について認識しているほか、遺伝性乳がん/卵巣がん家系員の88%がプライバシーまたは守秘についてかなりの懸念を有していることが示されている。第三度近親者またはさらに遠い血縁者のがんについて表明された懸念は、発端者の第一度近親者および第二度近親者に対する懸念と同程度のものであった。[ 206 ]乳がんまたは卵巣がんに罹患している女性のFDRを調査したところ、配偶者または直近の家系員にBRCA1/BRCA2検査結果を開示するには、書面による許可が必ず必要であると考えていたのはわずか半数であった。遺伝子検査に対する態度は、民族性、以前の遺伝情報への曝露、年齢、楽観主義および情報のスタイルよって変化した。ある人々においては、愛他主義も遺伝子検査を動機付ける1つの因子である。[ 207 ]多くの専門家集団が、インフォームド・コンセントに関する勧告をしている。[ 113 ][ 207 ][ 208 ][ 209 ][ 210 ]すべての開業医が、このようなガイドラインを認識し、遵守しているわけではないといういくつかの証拠がある。[ 211 ]BRCA1/BRCA2遺伝子検査の同意書の多くは、取り組むべき11分野に関する専門家集団による勧告[ 212 ]を満たしておらず、情報の非常に重要な点を省略していることが研究[ 211 ]で示されている。乳がんまたは卵巣がんの病歴をもつ女性の研究において、女性たちは、家族に遺伝的情報を知らせるときに、倫理的ジレンマと遭遇することに対する準備不足の印象を報告したとインタビュアーは述べている。[ 213 ]このようなデータは、検査前に家族への開示についての心構えをしっかりしている方が、家族に遺伝的情報を伝えることの感情的重荷は少ないことを表している。患者や医療提供者は、遺伝性のがんリスクについて家族に警告することの倫理的問題を十分検討することで恩恵が得られよう。(がん遺伝学および遺伝子検査の倫理に関する詳しい情報については、がんの遺伝学的リスク評価とカウンセリングおよびがん遺伝学の概要のPDQ要約を参照のこと。)
遺伝性乳がんおよび卵巣がんに対するがんリスク管理の心理社会的側面
遺伝性乳がんおよび卵巣がんに対するリスク管理の選択肢を検討する人向けの意思決定支援
がんリスクの管理に関して説明を受けた上での意思決定において患者を支援するため、標準的な遺伝カウンセリングの補助として意思決定支援を使用することに関する小規模だが深まりをみせている一群の文献がある。[ 214 ][ 215 ][ 216 ][ 217 ][ 218 ]非罹患女性を対象にした6ヵ月の追跡調査で、BRCA1/BRCA2検査による陽性の結果を受け取った後に、個々の価値評価およびがんリスク管理情報から構成される意思決定支援を利用することは、侵入思考がより少なく、抑うつレベルがより低いことと関係していたことを示した研究が1件ある。意思決定支援の使用によってがんリスク管理の意思および行動が変わることはなかった。しかしながら、幸福およびいくつかの意思決定に関係する結果についてわずかに好ましくない影響が罹患女性において確認された。[ 216 ]別の研究では、個々に適合した意思決定支援(価値の明確化のための練習を含む)に対する反応と女性が卵巣がんリスクの管理に関して意思決定を行えるように意図された一般情報を掲載した小冊子に対する反応とが比較された。短期では、個々に適合した意思決定支援を受けた女性は、小冊子を渡された女性と比較して、意思決定に関する葛藤の減少および知識の増加を示したが、2群間で意思決定の結果に差は認められなかった。さらに、デシジョンエイドによって参加者のベースライン時のがんリスク管理の意思決定が変わることはなかったようである。[ 215 ]BRCA1/BRCA2病原性多様体を有する非罹患女性150人を対象とした多施設共同ランダム化試験では、乳がんリスク管理の決定および心理社会的アウトカムに対する意思決定支援の効果が評価された。6ヵ月および12ヵ月の追跡で、意思決定支援群にランダムに割り付けられた女性では、がん関連の苦悩レベルが対照群より低かった(6ヵ月でP = 0.01、12ヵ月でP = 0.05)。[ 218 ]いずれの群でも意思決定に関する葛藤のスコアは、ベースラインで相対的に低く、時間とともに低下した;2群間のスコアに統計的差はみられなかった。
がんリスク管理の選択肢の受診率
BRCA1およびBRCA2病原性多様体に関する遺伝カウンセリングおよび遺伝子検査を受けた個人におけるがんリスク管理の選択肢の受診率および遵守について調査している研究の数が増えている。これらの研究の結果は、表15および表16に報告されている。結果は研究間で異なっており、スクリーニング(マンモグラフィ、磁気共鳴画像法[MRI]、がん抗原[CA]125、経膣超音波検査[TVUS])の受診率または遵守率、RRMおよびRRSOの選択などが含まれている。研究の結果は、一般的に病原性多様体キャリアごとまたは検査状態(例、病原性多様体陽性、病原性多様体陰性、または遺伝子検査の拒絶)別に報告される。遺伝的リスク状態の告知後の追跡期間もまた研究間で異なっており、12ヵ月~数年に及んだ。
これらの研究からの知見により、BRCA1/BRCA2病原性多様体キャリア状態の告知後、乳房のスクリーニングはしばしば改善することが示唆されている;にもかかわらず、スクリーニングは依然として最適以下である。スクリーニング方法としてのMRIの採用について調査している研究はほとんどないが、おそらく効力のデータが最近は利用できるためである。卵巣がんのスクリーニングは研究間で大幅に異なり、またスクリーニング検査の種類(すなわち、血清CA-125検査 vs TVUSスクリーニング)によって異なった。しかしながら、卵巣がんスクリーニングは、BRCA1/BRCA2病原性多様体キャリアで広く採用されていないようである。RRMの受診率は研究間で大幅に異なっていたが、これは個人的要因(より低い年齢や乳がんの家族歴を有するなど)、心理社会的因子(がんに関係した苦悩を低下させたい願望など)、医療提供者の推奨、および文化的または保健医療システムの因子による影響を受けている可能性がある。両側乳房切除術を受けるという個人の選択はまた、遺伝子検査の結果に関係なく治療前の遺伝学教育およびカウンセリングによる影響を受けるようである。[ 219 ]同様に、RRSOの受診率もまた研究間で異なっていたが、より高い年齢、乳がんの個人歴、卵巣がんリスクの認識、文化的因子(すなわち、国)、および医療提供者の推奨など、同様の因子による影響を受けている可能性がある。
表15.BRCA1およびBRCA2病原性多様体キャリアにおけるリスク低減のための乳房切除術(RRM)および/または乳がんスクリーニングの受診率 研究の引用番号 研究集団 RRMの受診率 乳房スクリーニングマンモグラフィおよび/または乳房MRIの受診率 追跡期間 コメント MRI = 磁気共鳴画像法;RRSO = リスク低減のための卵管卵巣摘出術。 aデータソースは自己報告。 bデータソースは医療記録。 Botkin et al.(2003) [ 220 ] キャリア(n = 37)a キャリア0% マンモグラフィ 24ヵ月 - キャリア 57% 非キャリア(n = 92)a 非キャリア0% - 非キャリア 49% - 検査を断った 20% 検査拒否(n = 15)a MRI - 評価されなかった Beattie et al.(2009) [ 221 ] キャリア(n = 237)b キャリア23% 該当せず 平均、3.7年 RRMを選択した女性は60歳未満で、以前に乳がんを診断されており、RRSOも受けていた。 RRMまでの期間中央値:結果を受けてから124日。 O'Neill et al.(2010) [ 222 ] キャリア(n = 146)a キャリア13% 該当せず 12ヵ月 検査結果を開示する意思は、RRM決定を予測させた。 Schwartz et al.(2012) [ 223 ] キャリア(n = 108)a キャリア37% マンモグラフィ 平均、5.3年 RRMの予測因子は、低年齢、カウンセリング前のがん苦悩が大きい、乳がんまたは卵巣がんの診断から間がない、および卵巣が正常といったものであった。 - 罹患したキャリア 92% - 罹患していないキャリア 82% 非キャリア(n = 60)a 非キャリア0% - 非キャリア 66% - 罹患した情報不明者 89% MRI 情報不明者(n = 206)a 情報不明者 6.8% - 罹患したキャリア 51% - 罹患していないキャリア 46% - 非キャリア 11% - 情報不明者 27% Garcia et al.(2013) [ 224 ] キャリア(n = 250)b キャリア44% RRM後の女性を除く: 41ヵ月;範囲、26~66ヵ月 乳房サーベイランス率は追跡の1~5年から有意に減少した:マンモグラフィ 43%から7%;MRI 35%から3%。 マンモグラフィ: - キャリア 43% MRI: - キャリア 35% Singh et al.(2013) [ 225 ] キャリア(n = 136)b キャリア42% 該当せず 範囲、1~11年 RRMの予測因子は、第一度または第二度近親者の乳がんへの罹患、少なくとも1回の出産経験、2005年以降の検査の受診であった。 Phillips et al.(2006) [ 226 ] キャリア(n = 70)a キャリア11% マンモグラフィ 3年 - キャリア 89% MRI - 評価されなかった Metcalfe et al.(2008) [ 227 ] キャリア(N = 2,677)a キャリア18%(非罹患) マンモグラフィ 3.9年;範囲、1.5~10.3年 国別のリスク管理の選択肢の受診率には大きな差が認められた。 - キャリア87% MRI 1,294人の参加者が乳がんの個人歴を有した。 - キャリア31% Julian-Reynier et al.(2011) [ 228 ] キャリア(n = 101)a キャリア6.9% マンモグラフィ 5年 非キャリアは多くがスクリーニングを継続した。 - キャリア59% - 30~39歳の非キャリア 53% 非キャリア(n = 145)a 非キャリア0% MRI - キャリア31% - 非キャリア 4.8% 表16.BRCA1およびBRCA2病原性多様体キャリアにおけるリスク低減のための卵管卵巣摘出術(RRSO)および/または婦人科スクリーニングの受診率 研究の引用番号 研究集団 RRSOの受診率 婦人科スクリーニングの受診率 追跡期間 コメント CA-125 = がん抗原125;RRM = リスク低減のための乳房切除術;TVUS = 経膣超音波検査。 aデータソースは自己報告。 bデータソースは医療記録。 cデータソースは明記されていない。 Scheuer et al.(2002) [ 229 ] キャリア(n = 179)a キャリア50.3% CA-125 平均、24.8ヵ月;範囲、1.6~66.0ヵ月 RRSOを受けた女性は年齢が高く、乳がんの個人歴を有することが多かった。 - キャリア67.6% TVUS - キャリア72.9% Beattie et al.(2009) [ 221 ] キャリア(n = 240)b キャリア51% 該当せず 平均、3.7年 RRSOを選択した女性は60歳未満で、乳がんの診断歴があり、RRMも受けていた。 RRSOまでの期間中央値:結果を受けてから123日。 O'Neill et al.(2010) [ 222 ] キャリア(n = 146)a キャリア32% 該当せず 12ヵ月 Schwartz et al.(2012) [ 223 ] キャリア(n = 100)a キャリア65% CA-125 平均、5.3年 RRSOの予測因子は、40歳以上であること、および乳がんと診断されてから10年を超えることであった。 非キャリア(n = 52)a 非キャリア1.9% - キャリア56% - 非キャリア12% - 情報不明者 33% 情報不明者(n = 203)a 情報不明者 13.3% TVUS - キャリア42% - 非キャリア20% - 情報不明者 26% Garcia et al.(2013) [ 224 ] キャリア(n = 305)b キャリア74% RRSO後の女性を除く: 41ヵ月;範囲、26~66ヵ月 卵巣サーベイランス率は追跡の1~5年から有意に減少した;CA-125:47%から2%;TVUS:45%から2.3% CA-125 - キャリア47% TVUS - キャリア45% Mannis et al.(2013) [ 230 ] キャリア(n = 201)a キャリア69.6% CA-125 中央値、3.7年 RRSOおよびスクリーニングの予測因子には、BRCA病原性多様体キャリアであること、年齢が40~49歳であること、比較的高所得であること、子供が2人以上いること、乳がんの個人歴を有すること、および卵巣がんの第一度近親者がいることが含まれた。 – 26.3% TVUS – 26.3% 非キャリア(n = 103)a 非キャリア2.0% 報告されなかった 情報価値がない(n = 773)a;59/773は意義不明の多様体であった 情報価値がない12.3% CA-125 – 10.4% TVUS – 6.5% Singh et al.(2013) [ 225 ] キャリア(n = 136)b キャリア52% 該当せず 範囲、1~11年 RRSOの予測因子は、乳がんの第一度または第二度近親者、骨盤がんによる母親の死亡、1回以上の出産経験、50歳以上の年齢、および2005年以降の検査受診であった。 Phillips et al.(2006) [ 226 ] キャリア(n = 70)a キャリア29% CA-125 3年 - キャリア0% TVUS - キャリア67% Friebel et al.(2007) [ 231 ] キャリア(N = 537)c キャリア55% 該当せず 最低6ヵ月;中央値36ヵ月 40歳を超える経産女性ではRRSOが最も多かった。 Madalinska et al.(2007) [ 232 ] キャリア(n = 160)a、b キャリア74% キャリア26% 12ヵ月 RRSOを受けた女性は教育レベルがより低く、卵巣がんは治癒不能とみなし、RRSOの有益性を強く信用していた。 婦人科スクリーニングの特異的方法は報告されていない。 Metcalfe et al.(2008) [ 227 ] キャリア(N = 2,677)a キャリア57% 該当せず 3.9年;範囲、1.5~10.3年 国別のリスク管理の選択肢の受診率には大きな差が認められた。 Julian-Reynier et al.(2011) [ 228 ] キャリア(n = 101)a キャリア42.6% TVUS 5年 RRSOの実施率は年齢に伴って増加した。RRSOを受けたことで乳がんリスクの認識は変わらなかった。非キャリアは多くがスクリーニングを継続した。 非キャリア(n = 145)a 非キャリア2% - 非キャリア43.2% Rhiem et al.(2011) [ 233 ] キャリア(N = 306)b キャリア57% 評価されなかった 平均、卵巣摘出後47.8ヵ月 RRSO実施時の年齢中央値 = 47歳。RRSO実施時点で潜伏卵管がんが1例検出された。RRSOから26ヵ月後に腹膜がんが1例診断された。 Sidon et al.(2012) [ 234 ] キャリア(N = 700)a;386/700人には乳がんの個人歴があった BRCA1キャリア: 評価されなかった 乳がんに罹患している場合 60歳以上の女性におけるRRSOの受診率は低かった(5年経過時で22%の受診率)。70歳以上の女性でRRSOを受けた人はいなかった。 – 54.5% BRCA2キャリア: – BRCA1:平均、2.29年;範囲、0.1~11.45年 – 45.5% 乳がんの個人歴がない全キャリア – BRCA2:平均、1.77年;範囲、0.1~11.1年 乳がんに罹患していない場合 – 54.2% 乳がんの個人歴がある全キャリア – BRCA1:平均、1.63年;範囲、0.1~11.28年 – 43.2% – BRCA2:平均、1.75年;範囲、0.1~8.98年 その一方で、病原性多様体のキャリアと判明した多くの女性は、自身の乳がんリスクを可能な限り小さくしたいという希望から、RRMに関心を示す。以前にリスク低減のための手術を受けておらず、がんにも罹患していない多数の女性を対象とした1件の研究では、遺伝カウンセリングの実施後にBRCA1検査の結果を告知された場合、キャリアの17%(12人中2人)が乳房切除術を受ける意向を示し、33%(12人中4人)が卵巣摘出術を受ける意向を示した。[ 235 ]同じ集団を対象にしたその後の研究では、検査結果が陽性であった女性の35%がRRMを重要な選択肢と考えており、76%の女性がリスク低減のための卵巣摘出術を重要な選択肢と考えていた。1件のプロスペクティブ研究により、BRCA病原性多様体が証明されたオランダ人女性80人において、5つの時点(BRCA検査前から結果開示後9ヵ月まで)でリスク管理の選好の安定性が評価された。46人の参加者がベースライン時にスクリーニングへの選好を示した。ベースライン時にRRMを好んだ女性25人のうち、22人が検査結果開示から9ヵ月後も同じ選好を示した;しかしながら、実際にRRMを受けた女性の数は報告されなかった。[ 236 ]
当初の関心が常に手術の決定に移行するとは限らない。2件の異なる研究により、結果開示後の1年間に病原性多様体キャリアにおけるRRMの割合の低さが明らかにされ、1件ではキャリアの3%(29人中1人)、もう1件ではキャリアの9%(34人中3人)がこの手術を受けたことが示された。[ 168 ][ 237 ]大規模なBRCA1家系の家系員において、がんスクリーニングおよび/またはリスク低減のための手術の利用状況の評価が、ベースライン時(結果の開示前)とBRCA1検査結果告知の1年後および2年後に実施された。参加した269人の男性および女性のうち、37人の女性キャリアおよび92人の女性非キャリア(全員25歳以上)に関しては完全なデータが得られた。検査結果告知の2年後の時点において、RRMを受けた女性はなかったが、キャリア37人中の4人(10.8%)はこの手術を検討中であることを表明した。対照的に、ベースライン前に卵巣摘出術を受けていなかった26人の女性のうち、46%(26人中12人)が検査後2年までに卵巣摘出術を受けた。25~39歳のキャリアのうち、29%(17人中5人)が卵巣摘出術を受けた一方で、40歳以上のキャリアの78%(9人中7人)がこの手技を受けた。[ 220 ]BRCA1検査結果の開示から3ヵ月後にリスク低減のための手術の実施状況について評価した研究では、62人中7人の女性がRRMを受け、62人中13人の女性がRRSOを受けていた。検査前のRRSOを受ける意思は、手術の実施と相関した。対照的にRRMを受ける意思は受診と相関しなかった。全体的に、リスク低減のための手術を決断しない理由として得られたものは、病原性多様体がみられない場合でも家族歴が重要であるというような複雑な判定因子、外科的処置への懸念、ならびに早期閉経およびHRTの使用に関する時期と不確実性といったものであった。[ 238 ]英国の研究では、41人の女性に対する遺伝カウンセリングの観察中と遺伝カウンセリング後の半構造化面接の間にデータ収集が行われた。[ 239 ]リスク低減のための手術という選択肢が29件のカウンセリングでもち出され、カウンセリング後のインタビュー35件で議論された。15人の女性は、将来卵巣摘出術を受けることを考慮するだろうと述べ、9人が乳房切除術を受けることを考慮するだろうと述べた。相談後のインタビューでは、卵巣摘出術および乳腺摘出術を受けることの意味合いが検討された。カウンセリーはリスク低減のための手術を、(a)他の家系員に対する義務を果たすための手段、そして(b)リスクを減らしがんに対する不安を抑える手段、と述べた。この形態のリスクマネジメントのコストは、回答者によって以下のように述べられている:
多くの女性が遺伝子検査を受けることなくRRMおよびRRSOを受けることを選択する理由としては、以下のものがある:
サーベイランス外来にかかっている乳がん患者のFDRの中で、RRMへの関心を示した、および/または乳房切除術を受けた女性は、RRMに関心のない女性よりも有意に乳がんの生検回数が多く(P < 0.05)、主観的な10年乳がんリスク推定値が高い(P < 0.05)ことが明らかにされた。サーベイランス外来に登録する際のがんに対する心配は、興味は示したが未だ手術を受けていない女性、および手術を受ける意思がない女性と比べて、その後にRRMを受けた女性が最も高かった(P < 0.001)。[ 242 ]
BRCA検査は、乳がんの診断を新たに受けた女性に提供する場合に、キャリアでは非キャリアに比べて両側乳房切除を選択する可能性が高くなるという点で、手術に関する意思決定に影響を及ぼすことが示されている。[ 219 ][ 243 ][ 244 ]乳がん生存者435人における対側RRMの予測因子を評価した研究では、16%が遺伝カウンセリングおよびBRCA1/BRCA2遺伝子検査を紹介される前に対側RRM(罹患した乳房の乳房切除術を併用)を受けていた。[ 245 ]遺伝カウンセリングおよび遺伝子検査前の対側RRMの予測因子としては、より若年での乳がん診断、診断からの経過期間が長いこと、乳がんに罹患したFDRが少なくとも1人いること、およびパートタイムでの雇用が挙げられた。検査結果開示から1年間で、BRCA1/BRCA2病原性多様体の検査が陽性であった女性の18%、および検査結果が情報価値のないものであった女性の2%が対側RRMを受けた。遺伝子検査後の対側RRMの予測因子は、乳がん診断時年齢が若いこと、遺伝カウンセリング前のがん特異的苦悩が大きいこと、BRCA1/BRCA2検査が陽性であることなどであった。この研究において、対側RRMは遺伝子検査結果の開示から1年経過時の苦悩とは関連していなかった。レトロスペクティブなコホートレビューでは、新規診断乳がんの治療に関して手術の決断を下す前にBRCA1/BRCA2遺伝子検査を受けた女性110人を対象に、両側乳房切除の実施が評価された。BRCA病原性多様体キャリアは、多様体が検出されなかった女性より、両側乳房切除を受ける傾向が高かった(83% vs 37%;P = 0.046)。[ 246 ]病原性多様体のない女性において、対側RRMを受ける唯一の予測因子は、既婚であった(P = 0.03)。年齢、人種、出産歴、病期とバイオマーカー、マンモグラフィでの乳腺密度の増加、および乳房MRIは、一次外科治療時点での対側RRMの決定に影響を及ぼさなかった。
2006年から2014年に米国の11の学術施設および地域施設で実施された研究では、乳がんの診断を受けた40歳以下の女性897人について、時とともにBRCA遺伝子検査の受診率が増加していることが明らかになった。[ 244 ]診断から1年以内に、対象者の87%がBRCA検査を受けた。この率は、2006年では新規に診断された女性の77%が検査を受けたが、2013年では95%に増加した。BRCAの病原性多様体に対する検査が陽性で、手術についての意思決定に検査が影響を及ぼしたと報告した女性(n = 88)のうち、86%が両側乳房切除術を受けたが、これに対して非キャリアでは51%であった(P < 0.001)。検査を受けなかった女性のうち、約3分の1は自身がBRCA検査の対象者であることを医療提供者から告げられなかったと報告した。しかし国のガイドラインを基準とすると、診断時の年齢だけで全員が検査に適格であった。
1994年から2002年に乳房再建術を伴う片側または両側のRRMを受けたオランダの女性(N = 114)を対象に、この手術への満足度を判定するレトロスペクティブな調査が行われた。[ 247 ]68%は、乳がんに罹患していないBRCA病原性多様体キャリアか、家系内でBRCA病原性多様体を有するリスクが50%の人のいずれかであった。回答者の60%が、彼女らは手技に満足している、95%がRRMを再び選択する、および80%が同じ乳房再建術を選択すると表明した。周術期または術後に何らかの合併症、現在の身体的愁訴、または何らかの身体的制限を報告した女性は半数に満たなかった。29%が手術後の女性らしさの感覚の変化を報告し、44%が性的関係の悪化を報告するとともに、35%はパートナーが性的関係の悪化を感じていると考えていると表明した。しかしながら、10%の女性は手術後の性的関係において肯定的な変化を報告した。この手技に満足していると表明した患者と比較して、満足しなかった患者は、手技とその結果に関してあまり知らされなかったと感じている、より多くの合併症および身体的愁訴を報告する、乳房が身体になじんでいないと感じる、および乳房再建術を再度選択するつもりはないと表明する可能性がより高かった。性的関係に対する否定的な影響を報告した女性は、以下の可能性がより高かった:
1997年から2005年の間にRRMを受けたスウェーデン人女性90人が、健康に関連したQOL、抑うつ、不安、性的能力、および身体像の変化を評価するために手術前、手術後6ヵ月、および手術後1年の時点で調査を受けた。3つの時点で健康に関連したQOLまたは抑うつにおける有意な変化は認められなかった;不安は時の経過とともに低下した(P = 0.0004)。80%を超える女性が、3つの時点すべてにおいて親密な関係が得られていることを報告した。性的に積極的であると報告した女性に対して、性的快感、不快感、嗜好、および性交渉頻度に関する質問に回答するよう求めた。頻度、嗜好、または不快感について統計的有意差は認められなかった。しかしながら、性的快感はベースライン時と手術後1年経過時とでは有意に低下していた(P = 0.005)。手術後1年時点で、魅力が少なくなったと感じると報告した女性が48%、照れくさく感じると報告した女性が48%、手術の痕に不満があると報告した女性が44%であった。[ 248 ]
リスク低減のための手術という選択肢に関する話し合いが検査前の遺伝カウンセリングの中で一貫して行われていない場合がある。1件の多施設研究では、高リスク乳がん家系の女性との相談でRRMおよびRRSOについて話し合ったのは、手術選択肢に関する話し合いがカウンセリーの期待と明らかに関連し、そのような情報は不安の増加と関連しないという事実にもかかわらず[ 251 ]、遺伝学の専門家のわずか半数であった。[ 249 ][ 250 ]
BRCA1またはBRCA2の病原性多様体を有する女性は、卵巣がんリスクの増加に直面することから、RRSOに関する情報を受ける女性は、手術の受診に大きな差(27%-72%)を示す。[ 9 ][ 124 ][ 229 ][ 232 ][ 252 ][ 253 ]1件の研究で、サーベイランスのみに対しRRSOの選択に関係する臨床的因子は、より高い年齢、1人以上の経産、および以前の乳がんの診断であることが示された。[ 254 ]この研究では、RRSOの選択は乳がんまたは卵巣がんの家族歴と関係しなかった。子宮摘出術は遺伝カウンセリング中に選択肢の1つとして提案され、RRSOを受けた女性の80%は子宮摘出術も受けることを選択した。
がんスクリーニングとリスク低減行動
現在では、がんリスク管理(例、スクリーニング、リスク低減のための介入)に関する忠告への理解度および遵守度に関して、研究が実施されるようになってきている。National Comprehensive Cancer Network Guidelinesにより定義されたがんスクリーニングの遵守度とリスク低減行動が、乳がんまたは卵巣がんの個人歴(n = 134)または家族歴(n = 80)を有する女性214人を対象にした横断研究で評価された。40歳以上の非罹患女性のうち、10%が調査の前年にマンモグラムまたは乳房視触診(CBE)のどちらも受けておらず、46%が乳房自己検査(BSE)を行っていなかった。以前に乳がんまたは卵巣がんに罹患していた女性では、21%がマンモグラムによる診察を受けたことがなく、32%がCBEを受けたことがなく、39%がBSEを行っていなかった。[ 255 ]
1997年から2005年の間にBRCA病原性多様体に対するカウンセリングと検査を受けた312人の女性から、遺伝性乳がんおよび卵巣がんに対する遺伝子検査の認識についての調査が回答された。調査には、スクリーニングおよびリスク低減のための手術などリスクを低下させるための選択肢に関する質問が含まれていた。217人(70%)の女性が乳がんと診断され、86人(28%)はBRCA1またはBRCA2遺伝子の検査で病原性多様体が陽性であった。BRCA陽性女性で、マンモグラムは不快感のために困難な処置であると認めた者はなかった一方で、BRCA陰性女性のうち11人(5.4%)がこの記載に賛成した。どちらのグループ(BRCA陽性およびBRCA陰性)も、リスク低減のための手術はがんリスクおよび心配を低下させるための最良の手段であることを認め、両グループのほとんどの患者が、リスク低減のための乳房切除術は過激すぎず、過剰に恐ろしいものではなく、それほど外観を損なうものではないという考えを示した。[ 256 ]
英国の1件のプロスペクティブ研究で、乳がん家族歴を有し、多施設スクリーニングプログラムの参加者であった35~49歳の女性1,286人を対象にマンモグラフィによるスクリーニングの心理学的影響が調査された。追加の評価が必要なマンモグラフィの異常が112人の女性で発見された。しかしながら、これらの女性は、こうした所見の結果としてがんに対する心配またはマイナスの心理的結果の統計的に有意な増加を示さなかった。マンモグラフィの異常を認めなかった女性1,174人では、結果を受け取った後に、ベースラインと比較してがんに対する心配およびマイナスの心理的結果が減少した。6ヵ月経過時ではコホート全体で、がんに対する心配および乳房スクリーニングの心理的結果の測定値が減少した。[ 257 ]
1件の定性的研究により、健康に良い予防のための行動(例、運動、食事)についての情報の提供に関する医療専門家の見解が調査された。7人の医療専門家および10人の遺伝カウンセラーがフォーカスグループでのセッション中または個別に面談を受けた。この研究の報告によると、健康に良い予防のための行動について提供される情報の内容および程度には大きな差があり、一般に参加者は、遺伝カウンセリングのセッションでそのような行動を促進するのは自分たちの役割ではないと考えていた。しかしながら、リスク評価クリニック内およびクリニック間でそうした情報の提供に関するコンセンサスを確立する必要については意見が一致した。[ 258 ]
スクリーニング受診率が、標的となっている集団について推奨されたガイドラインまたは特定の臨床シナリオの範囲内に収まっているかどうかは、すべての研究で明示されているわけではなく、またがんスクリーニングの推奨に影響する可能性がある他の変数について、すべての研究で報告されているわけでもない。例えば、異型乳管過形成の既往がある女性であれば、一般集団のスクリーニングの推奨とは異なるスクリーニングの推奨に従うよう助言される。
心理社会的アウトカム研究
リスク低減のための乳房切除術
オランダで実施されたプロスペクティブ研究によると、BRCA1/BRCA2病原性多様体キャリア26人のうち、乳房切除を選択した14人は、診断結果の開示前、開示6ヵ月後および12ヵ月後のいずれにおいても、経過観察を選択したキャリア12人および病原性多様体が陰性の女性53人と比べて大きな苦悩を抱えていた。しかしながら、全体的にみると、リスク低減のための乳房切除術(RRM)を受ける女性において不安は軽減されていた;1年の時点でのその不安スコアは、サーベイランスを選択した女性および病原性多様体が陰性の女性のスコアにより近づいていた。[ 259 ]興味深いことに、RRMを選択した女性では、検査前の自身の乳房と全般的身体像に対する満足度がサーベイランスを選択したキャリアまたはBRCA1/BRCA2病原性多様体の非キャリアよりも低かった。RRMを受けた女性のうち、1人を除く全員が診断結果開示後1年の時点でその決心を後悔していなかったが、多くが身体像、性的関心と機能、および自尊心の点で問題を抱えていた。RRMの影響について医師の説明が不十分だったという認識が後悔と関連していた。[ 259 ]追跡5年時点で、RRMを受けた女性は、体型および性的関係における変化があまり好ましくなかったが、がんが生じる恐怖は有意に減少していた。[ 260 ]リスク低減のための手術を受けた女性78人(BRCA1/BRCA2キャリアおよびBRCA1/BRCA2病原性多様体は検出されていないものの高リスク家系の女性を含む)を対象にした研究で、手術の2週間前、6ヵ月後、および12ヵ月後にがん特異的苦悩および一般的な苦悩が評価された。[ 261 ]サンプルには、RRMおよびRRSOの単独手術を受けた女性も、両方の手術を受けた女性も含まれた。1年間で苦悩の増加は観察されなかった。
Mayo ClinicでRRMを受けた女性609人の追跡研究(平均14年)では、混在した心理社会的アウトカムが報告された。70%がRRMに満足しており、11%は中立的で、19%が不満を抱いていた。18%は、もしもう一度選択する機会があれば、おそらくあるいは絶対にRRMを受けないだろうと考えていた。約4分の3は、がんについての心配は手術によって減少したと述べた。半数が身体像に対する満足度に変化がないと報告した;16%は手術後の身体像の向上を報告した。36%は、RRM後の自身の身体像に不満があると報告した。約4分の1の女性は、自身の性的関係および女性的感覚にRRMが悪影響を及ぼしていることを報告し、18%は自尊心の低下を報告した。RRMの満足度と強く関連する因子は、術後の外観についての満足度、ストレスの低下、再建をしないことまたはインプラントに伴う問題がないこと、性的関係において変化がないか改善したことであった。RRMの第一選択理由として医師のアドバイスを挙げた女性は、RRM後に不満を抱く傾向がみられた。[ 262 ]
RRMを受けた健康な女性60人を対象にした研究では、満足度、身体像、性機能、侵入と回避、およびその時点での心理的状態の水準が術後4年および4ヵ月の平均で測定された。このグループの76.7%は家族歴が強い(21.7%)か、BRCA1またはBRCA2の病原性多様体を保有していた(55%)。全体としては、調査対象となった女性の97%がRRMを受ける決定に満足(17%)またはきわめて満足(80%)し、1人を除いた全参加者がこの手技を他の女性に推奨したいと回答した。ほとんどの女性(66.7%)が手術は性生活に影響を及ぼさないと報告したが、31.7%は性生活の悪化を報告し、76.6%は、再建術の実施に関係なく、身体像の変化がないこと、または身体像の改善を報告した。手術後23.3%の女性により自己像の悪化が報告された。手術後の女性の平均的な苦悩のレベルは、正常なレベルをわずかに上回っているのみであったが、術後の乳がんリスクが高いと認識し続けた女性は、リスクが低いと認識していた女性よりも、全体的およびがんに関係した苦悩の平均的なレベルが高かった。さらに、BRCA1およびBRCA2病原性多様体キャリアと乳がんおよび/または卵巣がんの家族歴が強い女性は、家族歴が限定的な女性よりもがんに関係した苦悩の平均レベルが高かった。[ 263 ]
がんの診断がなされたときに、遺伝子検査の結果が治療の意思決定にどのように影響するのかについてはほとんど分かっていない。乳がん診断時の遺伝カウンセリングおよびBRCA1/BRCA2遺伝子検査について調査した研究が2件ある。[ 24 ][ 219 ]これらのうちの1件の研究では、診断時の遺伝子検査によって手術に関する意思決定がかなり変化し、病原性多様体キャリアの方が非キャリアよりも両側乳房切除術を多く選択していた。両側RRMは、病原性多様体が既知の女性の48%が選択し[ 219 ]、診断時に検査を受けた女性を対象にしたより小規模なシリーズ[ 24 ]では、病原性多様体が既知の女性の100%が選択した。病原性多様体が見つからなかった女性でも、24%が両側RRMを選択した。検査を断った人のうちの4%も両側RRMを受けた。病原性多様体キャリアにおける両側RRMの予測因子は、担当の医師がBRCA1/BRCA2検査および検査前の両側RRMを勧めたと患者が報告したかどうか、患者が陽性の検査結果を受け取ったかどうかなどであった。[ 219 ]がん診断時に実施される遺伝子検査後にRRMを受ける女性について、生活の質の転帰に関するデータは不足している。
オランダの1件のプロスペクティブ研究で、乳がんの女性に原発性乳がん治療のため乳房への放射線の開始時に遺伝カウンセリングおよび、適応があれば遺伝子検査を提供する場合の長期の心理学的結果が評価された。カウンセリングのアプローチを受けた女性のうち、遺伝子検査を受け、結果を受け取ることを選択した女性(n = 58)もいれば、アプローチを受けたが紹介の基準を満たさなかった女性(n = 118)も、カウンセリング/検査の選択を断った女性(n = 44)もいた。放射線療法を受けた別の女性のサブセットはカウンセリングのアプローチを受けなかった(n = 182)が、同じ方法を使って追跡された。心理的苦悩は、ベースライン時および放射線療法の最初の診察後4週、11週、27週、および43週時に測定された。4集団すべてにおいて、一般的不安、うつ病、または乳がん特異的苦悩における相違は認められなかった。[ 264 ]
乳がんの個人歴および家族歴を有し、対側RRMを1960年から1993年の間に受けた女性583人を対象にした質問票によるレトロスペクティブ研究で、乳房切除術後の全体的な満足およびこの手技による満足と不満に影響する因子が測定された。[ 265 ]平均追跡期間はリスク低減のための手術後10.3年であった。全体として、全参加者のうち83%が対側RRMに満足または非常に満足しており、8%は中立的で、9%が不満を抱いていた。ほとんどの女性がまた、手術後の自尊心、ストレスのレベル、および情緒的安定性に対して良好な効果があった、または変化はなかったと報告した(それぞれ、88%、83%、88%)。全体の満足は高いレベルであったにもかかわらず、33%が否定的な身体像を報告し、26%が女性的感覚の低下を報告し、23%が性的関係に対する否定的な影響を報告した。外科的手技の種類もまた満足のレベルに影響した。著者らはこの差は、単純乳房切除術を受けたグループ(15%)に対して皮下乳腺摘除術を受けた女性のグループ(43%)における予期しない再手術の割合が高かった(P < 0.0001)ことが原因であるとした。この研究に対する制限は、主として参加者が手術を受けた期間(すなわち、再建手術の選択肢の利用可能性)に関係している。[ 265 ][ 266 ]これらの女性で、BRCA1/BRCA2遺伝子の病原性多様体に対する遺伝子検査を受けたものはいなかった。それでもなお、この研究は、このグループの女性のほとんどが対側RRMに満足している一方で、すべての女性が1つ以上の有害な転帰を報告したことを示している。
BRCAキャリア137人を対象としたレトロスペクティブ調査では、両側RRMを受けた女性における乳頭および乳輪まで含めた部分(NAC)の温存による心理社会的影響について検討された。[ 267 ]この研究では、女性が受けたRRM の種類によって身体のイメージおよび性的な幸福感が著しく異なることが明らかになった。NACを温存した女性は、NACを温存しなかった女性より乳房への満足感が高く(72% vs. 61%)、手術結果への満足感が高く(85% vs. 74%)、また性的な幸福感が大きかった(68% vs. 52%)。がん関連の苦悩、不安、抑うつ、およびリスク認識については、2群間に差が認められなかった。BRCAキャリアにおける乳輪乳頭温存乳房切除術の腫瘍学的転帰は、NACを温存しないRRMに劣らなかった。[ 268 ](詳しい情報については、本要約のRRMのセクションを参照のこと。)
別の研究では、長期の生活の質の転帰について、1979年から1999年に両側RRMを受けた女性195人 vs スクリーニングを選択した乳がんリスクが高い女性117人が比較された。心理社会的アウトカムについては両群間で統計的有意差は検出されなかった。手術を選択した女性の84%が自身の決定に満足していると報告した。手術とスクリーニング両群の女性の61%が自身の生活の質に非常にまたは相当満足していることを報告した。[ 269 ]
RRMおよび一期再建と関連する心理社会的アウトカムの研究において、高リスク女性61人(病原性多様体キャリア27人、他の女性は高リスク家族歴を有する)について、31人は乳がんの既往歴があったが、手術後平均3~4年経過時に評価された。[ 270 ]この研究では「はい」か「いいえ」の回答を引き出すように意図された質問が用いられ、手術は十分に耐えられ、83%の参加者が再建術の結果は期待通りのものであったと報告し、90%が手術前に十分な情報を受けたと報告し、手術を後悔したと報告した女性はなく、全員がもう一度同じ状況になった場合は同じ方法を選択すると報告したことが明らかにされた。結果の満足度は、74%が乳房の形に満足しているから、89%が瘢痕の外見に満足しているまでに及んだ。生活の質の指標(Short Form 36 Health Survey Questionnaire [SF-36];Hospital Anxiety and Depression Scale調査票のスコア)について標準的なサンプルとこの集団を比較したところ、これらの女性における生活の質の低下は示されなかった。
RRMを受けた高リスク(BRCA1/BRCA2陽性)の女性21人が投稿したFORCEウェブサイト上の資料を調査した定性的研究では、これらの女性はRRM手術に関して友人および家族から否定的な反応を予測し、実際受けていたこと、およびこれらの女性が情緒的サポートおよび自身の決定に対する自己防衛を維持することで、なんとか結果を開示できたことが明らかになった。女性の多くが乳がんの侵入的想起および心配からの解放を表明し、手術の審美的結果に満足していた。[ 271 ]
対照的に、評価の平均9年前に両側または対側RRMを受けた女性684人を対象に長期の心理社会的アウトカムが別の研究で調査された。[ 272 ]過半数の女性(59%)は再建術も受けた。興味深いことに、リカート尺度によれば85%の女性が、RRMを受ける決定に満足しているまたは非常に満足していると報告した。しかしながら、定性的面談では、多数の女性が手術に関連した不満または否定的な心理社会的アウトカムを続いて報告した。著者らは、女性が乳がんのリスクについて依然として心配していることを報告し、および/または身体像、疼痛、および性欲に関する否定的な感情を報告する場合に、回答を否定的とコード化した。否定的なコメントをした女性の79%および混在したコメント(満足と不満の混在)をした女性の84%が、決定に満足しているまたは非常に満足していると回答していた。両側乳房切除術を受けた女性は、対側乳房切除術を受けた女性よりも2倍も多く否定的および混在したコメントを報告した。最も心配された領域は身体像、乳房インプラントに伴う問題、手術後の疼痛、および性欲であった。著者らは、対側の手技を受けた女性は既にがんは治療されていた一方で、両側の手技を受けた女性は以前に治療されておらず、このことが2群間の満足度の差を部分的に説明しうると提唱した。これらの知見から、RRMに関する女性の満足度は時間の経過に伴う複雑な反応により抑えられることが示唆されている。
RRMを受けたか、または検討していた女性108人を対象にした定性的研究において、RRMを受けた女性の半数以上が心理士との手術前の相談は賢明であると感じていた;3分の2近くが術後の相談もまた適切であると考えていた。RRMを検討していたすべての女性が心理士との手術前の相談は意思決定を容易にすると考えていた。[ 273 ]
リスク低減のための卵管-卵巣摘出術
RRSO実施時に35歳~74歳であった(57.5%が50歳未満であった)女性40人(オンタリオ州健康省を介して卵巣がん家族歴のためにこの手技を受けていた)のレトロスペクティブな自己で行う調査では、RRSOにより卵巣がんリスクの認識が有意に低下したことが明らかにされた。57%がRRSOの有益性として認識されたリスクの低下を確認し(35%はRRSOの有益性に関してコメントしなかった)、49%ががんリスクの低減のためにRRSOを繰り返したいと報告した。全体的な生活の質のスコアは、閉経期のまたはホルモンの研究に参加している女性について発表されたスコアと一致していた。[ 274 ]RRSOを受けた59人の女性の生活の質が、術後24ヵ月に評価された。[ 275 ]一般集団と乳がんの生存者の間で生活の質は類似しており、約20%がうつ病を報告していた。膣乾燥および性交痛を報告する30%の被験者は、この施術に不満をもつ傾向がより高かった。
カナダのプロスペクティブ研究では、BRCA1/BRCA2病原性多様体が既知の女性114人をサンプルとして、手術前および手術1年後の更年期症状および性機能に対するRRSOの影響を調査した。[ 276 ]RRSOを受ける決断についての満足度は、報告された症状とは無関係に高かった。手術時点で閉経前であった女性(n = 75)では、症状の悪化および性機能の減退が認められた。HRTは、性的快感の減退ではなく膣乾燥および性交疼痛症に対処するものであった。また、HRTによって、中等度から重度のほてりも少数に認められた。
このグループから報告された別の研究によると、1年前にRRSOを受けた女性127人(75人がBRCA1病原性多様体;52人がBRCA2病原性多様体)の大多数は、RRSOにより乳がんおよび卵巣がんの両方のリスクが低下したと考えていたことが明らかになった。[ 277 ]この集団が報告した卵巣がんに対するリスクの認識は広範囲に及んだ。BRCA1およびBRCA2病原性多様体キャリアの20%は、卵巣がんに対するリスクが完全に排除されたと考えていた;他のキャリアでは、手術前と手術後の両方で卵巣がんリスクの認識が高かった。これらの女性の少数の集団が手術から約3年後にさらに調査されたが、この延長された期間でリスクの認識は有意に変化していなかった。この所見は卵巣がんリスクについて重大な誤解がRRSO後に持続していることを示唆している。追加の遺伝学教育および遺伝カウンセリングが必要であろう。
より大規模な研究で、定期的婦人科スクリーニング(GS)を選択した vs RRSOを受けた卵巣がんリスクが高い女性における生活の質が評価された。846人の高リスク女性(このうち、44%はRRSOを受け、56%はGSを選択した)が、生活の質、がん特異的な苦悩、内分泌の症状、および性機能を評価する質問表に回答した。[ 278 ]RRSO群の女性は術後平均2.8±1.9年経過しており、GS群の女性は高リスクの管理のための婦人科医への初診から平均4.3年経過していた。RRSO群とGS群間で全生活の質における統計的差異は認められなかった。GS群と比較した場合、RRSOを受けた女性は性機能が乏しく、膣の乾燥、性交痛、ほてりなどの内分泌の症状が多くみられた。RRSOを受けた女性は、乳がんおよび卵巣がんについての悩みのレベルがより低く、がんリスクの認知がより良好であった。
遺伝性乳がんおよび卵巣がんのリスクがあり遺伝カウンセリングを受診した女性(N = 182)を対象に、卵巣がんリスクを管理するためにRRSOまたは定期的スクリーニング(PS)(年2回のTVUSによる内診およびCA-125測定)のいずれかを選択したことでの満足度に関する調査が行われた。[ 279 ]両選択肢での全体的な満足度はきわめて高かったが、PSよりRRSOを選択した女性で最も高かった。満足度を際立たせる人口統計学的因子および臨床的因子は他に認められなかった。PSを選択した女性では決心をためらう傾向が高かった。
RRSOを受けたBRCA病原性多様体キャリア98人を対象に、手術後に予想される症状に関する術前のカウンセリングについて、レトロスペクティブ研究で評価された。[ 280 ]RRSO時の平均年齢は45.5歳(範囲、32~63歳)であった。85%がBRCA病原性多様体を保有していることを知った後もRRSOを選択し、48.0%が手術時点で閉経前であった。参加者は、膣の乾燥(52.1%)、セックスへの関心の変化(50.0%)、睡眠障害(46.7%)、性生活の変化(43.9%)、およびほてり(42.9%)といった「頻繁」または「きわめて頻繁」な術後症状を報告した。術前に対策が行われていたことが多く記憶されていたのは膣の乾燥とほてりのみであった。参加者の96%は、手術をまた受けることになったら、性生活に対する手術の影響(59.2%)、冠動脈性心疾患のリスク(57.1%)、セックスカウンセリングが利用できること(57.1%)について話し合うことが役立つのではないかと報告した。
行動に関する結果
遺伝性乳がん家族の一員で、自らの紹介で受診した高リスクの(BRCA1/BRCA2病原性多様体を保有するリスクが10%を超える)女性216人を対象にしたスクリーニング行動の研究[ 281 ]で、ある範囲のスクリーニング実践が明らかになった。家族における既知の病原性多様体の存在は、勧められたスクリーニング実践に対する良好な遵守とは関連しなかった。50~64歳の女性の69%および40~49歳の女性の83%は前年にスクリーニングマンモグラムを撮っていた。参加者の20%はCA-125検査を、そして31%は骨盤超音波またはTVUSを受けたことがあった。情報価値の高いBRCAの検査結果を有する107人の女性を個々に詳しく調べた、同研究対象集団のさらなる解析[ 281 ]では、若いキャリアの受診率は低いものの、乳がんのスクリーニングをよく利用していることが分かった。この研究では、受診率が低い原因までは探索されなかった。[ 282 ]乳がん/卵巣がんリスクが高い女性におけるスクリーニング行動に関する1件の調査により、スクリーニングの遵守における重要な因子として医師の推奨が同定された。[ 283 ]
遺伝子検査を追求するために引用される動機として、病原性多様体キャリアは乳がんおよび/または卵巣がんのスクリーニングの推奨を遵守するだろうという期待がしばしば挙げられる一方で[ 281 ][ 284 ][ 285 ][ 286 ]、遺伝子検査受診者が経時的にスクリーニング行動を変えるかどうか、また、保険の補償範囲、医師の推奨事項または態度など、それらの行動に影響を与える他の変数についてのデータは限られている。スクリーニング行動に対するがん遺伝カウンセリングの影響が、4つのがん遺伝子クリニックでのカウンセリング後12ヵ月間追跡された293人の女性を対象にした英国の研究で評価された。[ 287 ]カウンセリング後は乳房自己検査(BSE)、臨床での乳房検査(CBE)、およびマンモグラフィが有意に増加した;しかしながら推奨に対する遵守度の差が注目された:35~49歳の女性の38%がカウンセリング後12ヵ月までにマンモグラムによる診察を受けていなかった。ほとんどの女性がBSEを推奨された時期と頻度で実施していなかった。
このことは、検査結果が陽性であった女性に対してだけでなく、検査結果が陰性であった女性、非決定的な結果を受け取った女性、または結果を受け取らないことを選択した女性におけるスクリーニングの遵守度に対しても非常に重要な問題である。遺伝子検査の陰性の結果により、認識リスクが低下し、それとともに実際に遵守度も低下する可能性がある。
さらに、がんに関係する不安と乳がんスクリーニング行動との連関に関してはまだいくつかの問題があるが、蓄積する証拠は曲線的な関係というよりも直線的な関係を支持しているとみられる。つまり、データが一時期一貫しておらず、過剰な不安は、推奨されるスクリーニング実践の利用を実際に減らしうる一方で、軽微から中等度の不安は遵守度を増すという仮説を支持するデータもあった。また、直線的な関係がよりありえるという考えを支持する報告もあり、すなわち、不安が増えればスクリーニングの推奨に対する遵守が増大することを意味する。しかしながら、遺伝子検査後の健康行動を評価するために女性を追跡した研究はほとんどない。したがって、心配の減少につながる陰性の検査結果がスクリーニングに対する遵守度の低下に理論的に帰着しうる。ある大規模な研究で、スクリーニングの実施に対する患者のコンプライアンスは、一般的な不安またはスクリーニング特有の不安と関係しなかった-BSEは例外であり、そのコンプライアンスは手技特有の不安と負の関連があることを明らかにした。[ 77 ]この潜在的な懸念を明確にするためにデザインされたさらなる研究では、追跡スクリーニングの必要性を検討するための包括的な遺伝カウンセリングの必要性が強調される。
さらに、この分野の研究を複雑にしているのは、遺伝子検査受診前に40歳または50歳を超えている女性におけるベースライン時のマンモグラフィ遵守度などの問題である。より具体的には、この方法に対する遵守度に有意な差を記すことができる力は、遺伝子検査を受ける女性たちの検査前のスクリーニング行動における高い遵守度に悪影響を受ける。診断結果が陽性で乳がん家族歴のある女性におけるマンモグラフィ使用に、著しい変化を見つけ出すことは容易であろう。最後に、予防的介入の価値に加えて、疑問視されている多くのスクリーニングの選択肢、例えば、若い女性に対するマンモグラフィ、BSEや卵巣がんスクリーニング(定期的な経膣超音波および血清CA-125測定)などの効果に対する、遺伝子検査を受診する女性およびその介護者の認識も、経時的遵守度に悪影響を及ぼす可能性がある。
乳がんおよび卵巣がんに対する遺伝子検査を受診する女性間でのスクリーニングに対する意思決定および遵守性の問題は、現在進行中である複数の試験の主題であり、きわめて必要とされた進行中の研究の分野である。
参考文献- Ropka ME, Wenzel J, Phillips EK, et al.: Uptake rates for breast cancer genetic testing: a systematic review. Cancer Epidemiol Biomarkers Prev 15 (5): 840-55, 2006.[PUBMED Abstract]
- Schwartz MD, Lerman C, Brogan B, et al.: Utilization of BRCA1/BRCA2 mutation testing in newly diagnosed breast cancer patients. Cancer Epidemiol Biomarkers Prev 14 (4): 1003-7, 2005.[PUBMED Abstract]
- Kieran S, Loescher LJ, Lim KH: The role of financial factors in acceptance of clinical BRCA genetic testing. Genet Test 11 (1): 101-10, 2007.[PUBMED Abstract]
- Susswein LR, Skrzynia C, Lange LA, et al.: Increased uptake of BRCA1/2 genetic testing among African American women with a recent diagnosis of breast cancer. J Clin Oncol 26 (1): 32-6, 2008.[PUBMED Abstract]
- Olaya W, Esquivel P, Wong JH, et al.: Disparities in BRCA testing: when insurance coverage is not a barrier. Am J Surg 198 (4): 562-5, 2009.[PUBMED Abstract]
- Levy DE, Byfield SD, Comstock CB, et al.: Underutilization of BRCA1/2 testing to guide breast cancer treatment: black and Hispanic women particularly at risk. Genet Med 13 (4): 349-55, 2011.[PUBMED Abstract]
- Landsbergen K, Verhaak C, Kraaimaat F, et al.: Genetic uptake in BRCA-mutation families is related to emotional and behavioral communication characteristics of index patients. Fam Cancer 4 (2): 115-9, 2005.[PUBMED Abstract]
- Denayer L, Boogaerts A, Philippe K, et al.: BRCA1/2 predictive testing and gender: uptake, motivation and psychological characteristics. Genet Couns 20 (4): 293-305, 2009.[PUBMED Abstract]
- Meijers-Heijboer EJ, Verhoog LC, Brekelmans CT, et al.: Presymptomatic DNA testing and prophylactic surgery in families with a BRCA1 or BRCA2 mutation. Lancet 355 (9220): 2015-20, 2000.[PUBMED Abstract]
- Wakefield CE, Ratnayake P, Meiser B, et al.: "For all my family's sake, I should go and find out": an Australian report on genetic counseling and testing uptake in individuals at high risk of breast and/or ovarian cancer. Genet Test Mol Biomarkers 15 (6): 379-85, 2011.[PUBMED Abstract]
- Schlich-Bakker KJ, ten Kroode HF, Wárlám-Rodenhuis CC, et al.: Barriers to participating in genetic counseling and BRCA testing during primary treatment for breast cancer. Genet Med 9 (11): 766-77, 2007.[PUBMED Abstract]
- Vadaparampil ST, McIntyre J, Quinn GP: Awareness, perceptions, and provider recommendation related to genetic testing for hereditary breast cancer risk among at-risk Hispanic women: similarities and variations by sub-ethnicity. J Genet Couns 19 (6): 618-29, 2010.[PUBMED Abstract]
- Meiser B: Psychological impact of genetic testing for cancer susceptibility: an update of the literature. Psychooncology 14 (12): 1060-74, 2005.[PUBMED Abstract]
- Pasacreta JV: Psychosocial issues associated with genetic testing for breast and ovarian cancer risk: an integrative review. Cancer Invest 21 (4): 588-623, 2003.[PUBMED Abstract]
- Simon MS, Petrucelli N: Hereditary breast and ovarian cancer syndrome : the impact of race on uptake of genetic counseling and testing. Methods Mol Biol 471: 487-500, 2009.[PUBMED Abstract]
- Hann KEJ, Freeman M, Fraser L, et al.: Awareness, knowledge, perceptions, and attitudes towards genetic testing for cancer risk among ethnic minority groups: a systematic review. BMC Public Health 17 (1): 503, 2017.[PUBMED Abstract]
- Meiser B, Gaff C, Julian-Reynier C, et al.: International perspectives on genetic counseling and testing for breast cancer risk. Breast Dis 27: 109-25, 2006-2007.[PUBMED Abstract]
- Armstrong K, Stopfer J, Calzone K, et al.: What does my doctor think? Preferences for knowing the doctor's opinion among women considering clinical testing for BRCA1/2 mutations. Genet Test 6 (2): 115-8, 2002 Summer.[PUBMED Abstract]
- McCuaig JM, Greenwood CM, Shuman C, et al.: Breast and ovarian cancer: the forgotten paternal contribution. J Genet Couns 20 (5): 442-9, 2011.[PUBMED Abstract]
- Burke W, Culver J, Pinsky L, et al.: Genetic assessment of breast cancer risk in primary care practice. Am J Med Genet A 149A (3): 349-56, 2009.[PUBMED Abstract]
- Mouchawar J, Klein CE, Mullineaux L: Colorado family physicians' knowledge of hereditary breast cancer and related practice. J Cancer Educ 16 (1): 33-7, 2001.[PUBMED Abstract]
- Yong MC, Zhou XJ, Lee SC: The importance of paternal family history in hereditary breast cancer is underappreciated by health care professionals. Oncology 64 (3): 220-6, 2003.[PUBMED Abstract]
- Bellcross CA, Leadbetter S, Alford SH, et al.: Prevalence and healthcare actions of women in a large health system with a family history meeting the 2005 USPSTF recommendation for BRCA genetic counseling referral. Cancer Epidemiol Biomarkers Prev 22 (4): 728-35, 2013.[PUBMED Abstract]
- Weitzel JN, McCaffrey SM, Nedelcu R, et al.: Effect of genetic cancer risk assessment on surgical decisions at breast cancer diagnosis. Arch Surg 138 (12): 1323-8; discussion 1329, 2003.[PUBMED Abstract]
- Kurian AW, Griffith KA, Hamilton AS, et al.: Genetic Testing and Counseling Among Patients With Newly Diagnosed Breast Cancer . JAMA 317 (5): 531-534, 2017.[PUBMED Abstract]
- Childers CP, Childers KK, Maggard-Gibbons M, et al.: National Estimates of Genetic Testing in Women With a History of Breast or Ovarian Cancer. J Clin Oncol 35 (34): 3800-3806, 2017.[PUBMED Abstract]
- Pal T, Bonner D, Kim J, et al.: Early onset breast cancer in a registry-based sample of African-american women: BRCA mutation prevalence, and other personal and system-level clinical characteristics. Breast J 19 (2): 189-92, 2013 Mar-Apr.[PUBMED Abstract]
- Weldon CB, Trosman JR, Gradishar WJ, et al.: Barriers to the use of personalized medicine in breast cancer. J Oncol Pract 8 (4): e24-31, 2012.[PUBMED Abstract]
- Hafertepen L, Pastorino A, Morman N, et al.: Barriers to genetic testing in newly diagnosed breast cancer patients: Do surgeons limit testing? Am J Surg 214 (1): 105-110, 2017.[PUBMED Abstract]
- Katz SJ, Ward KC, Hamilton AS, et al.: Gaps in Receipt of Clinically Indicated Genetic Counseling After Diagnosis of Breast Cancer. J Clin Oncol 36 (12): 1218-1224, 2018.[PUBMED Abstract]
- Schwartz MD, Peshkin BN, Isaacs C, et al.: Randomized trial of proactive rapid genetic counseling versus usual care for newly diagnosed breast cancer patients. Breast Cancer Res Treat 170 (3): 517-524, 2018.[PUBMED Abstract]
- Lerman C, Hughes C, Benkendorf JL, et al.: Racial differences in testing motivation and psychological distress following pretest education for BRCA1 gene testing. Cancer Epidemiol Biomarkers Prev 8 (4 Pt 2): 361-7, 1999.[PUBMED Abstract]
- Armstrong K, Micco E, Carney A, et al.: Racial differences in the use of BRCA1/2 testing among women with a family history of breast or ovarian cancer. JAMA 293 (14): 1729-36, 2005.[PUBMED Abstract]
- Kinney AY, Simonsen SE, Baty BJ, et al.: Acceptance of genetic testing for hereditary breast ovarian cancer among study enrollees from an African American kindred. Am J Med Genet A 140 (8): 813-26, 2006.[PUBMED Abstract]
- Halbert CH, Kessler L, Stopfer JE, et al.: Low rates of acceptance of BRCA1 and BRCA2 test results among African American women at increased risk for hereditary breast-ovarian cancer. Genet Med 8 (9): 576-82, 2006.[PUBMED Abstract]
- Thompson HS, Valdimarsdottir HB, Duteau-Buck C, et al.: Psychosocial predictors of BRCA counseling and testing decisions among urban African-American women. Cancer Epidemiol Biomarkers Prev 11 (12): 1579-85, 2002.[PUBMED Abstract]
- Kinney AY, Gammon A, Coxworth J, et al.: Exploring attitudes, beliefs, and communication preferences of Latino community members regarding BRCA1/2 mutation testing and preventive strategies. Genet Med 12 (2): 105-15, 2010.[PUBMED Abstract]
- Sussner KM, Edwards T, Villagra C, et al.: BRCA genetic counseling among at-risk Latinas in New York City: new beliefs shape new generation. J Genet Couns 24 (1): 134-48, 2015.[PUBMED Abstract]
- Zimmerman RK, Tabbarah M, Nowalk MP, et al.: Racial differences in beliefs about genetic screening among patients at inner-city neighborhood health centers. J Natl Med Assoc 98 (3): 370-7, 2006.[PUBMED Abstract]
- MacNew HG, Rudolph R, Brower ST, et al.: Assessing the knowledge and attitudes regarding genetic testing for breast cancer risk in our region of southeastern Georgia. Breast J 16 (2): 189-92, 2010.[PUBMED Abstract]
- Sussner KM, Thompson HS, Jandorf L, et al.: The influence of acculturation and breast cancer-specific distress on perceived barriers to genetic testing for breast cancer among women of African descent. Psychooncology 18 (9): 945-55, 2009.[PUBMED Abstract]
- Edwards TA, Thompson HS, Kwate NO, et al.: Association between temporal orientation and attitudes about BRCA1/2 testing among women of African descent with family histories of breast cancer. Patient Educ Couns 72 (2): 276-82, 2008.[PUBMED Abstract]
- McCarthy AM, Bristol M, Domchek SM, et al.: Health Care Segregation, Physician Recommendation, and Racial Disparities in BRCA1/2 Testing Among Women With Breast Cancer. J Clin Oncol 34 (22): 2610-8, 2016.[PUBMED Abstract]
- Hurtado-de-Mendoza A, Jackson MC, Anderson L, et al.: The Role of Knowledge on Genetic Counseling and Testing in Black Cancer Survivors at Increased Risk of Carrying a BRCA1/2 Mutation. J Genet Couns 26 (1): 113-121, 2017.[PUBMED Abstract]
- Cragun D, Weidner A, Lewis C, et al.: Racial disparities in BRCA testing and cancer risk management across a population-based sample of young breast cancer survivors. Cancer 123 (13): 2497-2505, 2017.[PUBMED Abstract]
- Cragun D, Weidner A, Kechik J, et al.: Genetic Testing Across Young Hispanic and Non-Hispanic White Breast Cancer Survivors: Facilitators, Barriers, and Awareness of the Genetic Information Nondiscrimination Act. Genet Test Mol Biomarkers 23 (2): 75-83, 2019.[PUBMED Abstract]
- Lerman C, Hughes C, Lemon SJ, et al.: What you don't know can hurt you: adverse psychologic effects in members of BRCA1-linked and BRCA2-linked families who decline genetic testing. J Clin Oncol 16 (5): 1650-4, 1998.[PUBMED Abstract]
- Lodder L, Frets PG, Trijsburg RW, et al.: Attitudes and distress levels in women at risk to carry a BRCA1/BRCA2 gene mutation who decline genetic testing. Am J Med Genet 119A (3): 266-72, 2003.[PUBMED Abstract]
- Foster C, Evans DG, Eeles R, et al.: Non-uptake of predictive genetic testing for BRCA1/2 among relatives of known carriers: attributes, cancer worry, and barriers to testing in a multicenter clinical cohort. Genet Test 8 (1): 23-9, 2004.[PUBMED Abstract]
- McInerney-Leo A, Biesecker BB, Hadley DW, et al.: BRCA1/2 testing in hereditary breast and ovarian cancer families II: impact on relationships. Am J Med Genet A 133 (2): 165-9, 2005.[PUBMED Abstract]
- Patenaude AF: Cancer susceptibility testing: risks, benefits, and personal beliefs. In: Clarke A, ed.: The Genetic Testing of Children. Oxford, England: BIOS Scientific, 1998, pp 145-156.[PUBMED Abstract]
- Richards M: The genetic testing of children: adult attitude's and children's understanding. In: Clarke A, ed.: The Genetic Testing of Children. Oxford, England: BIOS Scientific, 1998, pp 169-179.[PUBMED Abstract]
- Wertz DC, Fanos JH, Reilly PR: Genetic testing for children and adolescents. Who decides? JAMA 272 (11): 875-81, 1994.[PUBMED Abstract]
- Borry P, Stultiëns L, Nys H, et al.: Attitudes towards predictive genetic testing in minors for familial breast cancer: a systematic review. Crit Rev Oncol Hematol 64 (3): 173-81, 2007.[PUBMED Abstract]
- Hamann HA, Croyle RT, Venne VL, et al.: Attitudes toward the genetic testing of children among adults in a Utah-based kindred tested for a BRCA1 mutation. Am J Med Genet 92 (1): 25-32, 2000.[PUBMED Abstract]
- Bradbury AR, Patrick-Miller L, Pawlowski K, et al.: Should genetic testing for BRCA1/2 be permitted for minors? Opinions of BRCA mutation carriers and their adult offspring. Am J Med Genet C Semin Med Genet 148C (1): 70-7, 2008.[PUBMED Abstract]
- Points to consider: ethical, legal, and psychosocial implications of genetic testing in children and adolescents. American Society of Human Genetics Board of Directors, American College of Medical Genetics Board of Directors. Am J Hum Genet 57 (5): 1233-41, 1995.[PUBMED Abstract]
- Michie S, Marteau TM: Predictive genetic testing in children: the need for psychological research. In: Clarke A, ed.: The Genetic Testing of Children. Oxford, England: BIOS Scientific, 1998, pp 169-182.[PUBMED Abstract]
- MacDonald DJ, Lessick M: Hereditary cancers in children and ethical and psychosocial implications. J Pediatr Nurs 15 (4): 217-25, 2000.[PUBMED Abstract]
- Tercyak KP, Peshkin BN, Streisand R, et al.: Psychological issues among children of hereditary breast cancer gene (BRCA1/2) testing participants. Psychooncology 10 (4): 336-46, 2001 Jul-Aug.[PUBMED Abstract]
- Winer E, Winer N, Bluman L, et al.: Attitudes and risk perceptions of women with breast cancer considering testing for BRCA1/2. [Abstract] Proceedings of the American Society of Clinical Oncology 16: A1937, 537a, 1997.[PUBMED Abstract]
- Braithwaite D, Emery J, Walter F, et al.: Psychological impact of genetic counseling for familial cancer: a systematic review and meta-analysis. J Natl Cancer Inst 96 (2): 122-33, 2004.[PUBMED Abstract]
- Mikkelsen EM, Sunde L, Johansen C, et al.: Psychosocial conditions of women awaiting genetic counseling: a population-based study. J Genet Couns 17 (3): 242-51, 2008.[PUBMED Abstract]
- Dorval M, Bouchard K, Maunsell E, et al.: Health behaviors and psychological distress in women initiating BRCA1/2 genetic testing: comparison with control population. J Genet Couns 17 (4): 314-26, 2008.[PUBMED Abstract]
- Wang C, Gonzalez R, Janz N, et al.: The role of cognitive appraisal and worry in BRCA1/2 testing decisions among a clinic population. Psychol Health 22 (6): 719-36, 2007.[PUBMED Abstract]
- Hallowell N, Statham H, Murton F: Women's understanding of their risk of developing breast/ovarian cancer before and after genetic counseling. J Genet Couns 7 (4): 345-64, 1998.[PUBMED Abstract]
- MacDonald DJ, Choi J, Ferrell B, et al.: Concerns of women presenting to a comprehensive cancer centre for genetic cancer risk assessment. J Med Genet 39 (7): 526-30, 2002.[PUBMED Abstract]
- Matloff ET, Moyer A, Shannon KM, et al.: Healthy women with a family history of breast cancer: impact of a tailored genetic counseling intervention on risk perception, knowledge, and menopausal therapy decision making. J Womens Health (Larchmt) 15 (7): 843-56, 2006.[PUBMED Abstract]
- Meiser B, Price MA, Butow PN, et al.: Misperceptions of ovarian cancer risk in women at increased risk for hereditary ovarian cancer. Fam Cancer 13 (2): 153-62, 2014.[PUBMED Abstract]
- Bluman LG, Rimer BK, Berry DA, et al.: Attitudes, knowledge, and risk perceptions of women with breast and/or ovarian cancer considering testing for BRCA1 and BRCA2. J Clin Oncol 17 (3): 1040-6, 1999.[PUBMED Abstract]
- Iglehart JD, Miron A, Rimer BK, et al.: Overestimation of hereditary breast cancer risk. Ann Surg 228 (3): 375-84, 1998.[PUBMED Abstract]
- Bluman LG, Rimer BK, Regan Sterba K, et al.: Attitudes, knowledge, risk perceptions and decision-making among women with breast and/or ovarian cancer considering testing for BRCA1 and BRCA2 and their spouses. Psychooncology 12 (5): 410-27, 2003 Jul-Aug.[PUBMED Abstract]
- McCaul KD, O'Donnell SM: Naive beliefs about breast cancer risk. Womens Health 4 (1): 93-101, 1998 Spring.[PUBMED Abstract]
- Huiart L, Eisinger F, Stoppa-Lyonnet D, et al.: Effects of genetic consultation on perception of a family risk of breast/ovarian cancer and determinants of inaccurate perception after the consultation. J Clin Epidemiol 55 (7): 665-75, 2002.[PUBMED Abstract]
- Davis S, Stewart S, Bloom J: Increasing the accuracy of perceived breast cancer risk: results from a randomized trial with Cancer Information Service callers. Prev Med 39 (1): 64-73, 2004.[PUBMED Abstract]
- Katapodi MC, Dodd MJ, Lee KA, et al.: Underestimation of breast cancer risk: influence on screening behavior. Oncol Nurs Forum 36 (3): 306-14, 2009.[PUBMED Abstract]
- Lindberg NM, Wellisch D: Anxiety and compliance among women at high risk for breast cancer. Ann Behav Med 23 (4): 298-303, 2001 Fall.[PUBMED Abstract]
- Ritvo P, Irvine J, Robinson G, et al.: Psychological adjustment to familial-genetic risk assessment for ovarian cancer: predictors of nonadherence to surveillance recommendations. Gynecol Oncol 84 (1): 72-80, 2002.[PUBMED Abstract]
- Meiser B, Halliday JL: What is the impact of genetic counselling in women at increased risk of developing hereditary breast cancer? A meta-analytic review. Soc Sci Med 54 (10): 1463-70, 2002.[PUBMED Abstract]
- Green J, Richards M, Murton F, et al.: Family communication and genetic counseling: the case of hereditary breast and ovarian cancer. J Genet Couns 6 (1): 45-60, 1997.[PUBMED Abstract]
- Quillin JM, Ramakrishnan V, Borzelleca J, et al.: Paternal relatives and family history of breast cancer. Am J Prev Med 31 (3): 265-8, 2006.[PUBMED Abstract]
- O'Neill SM, Rubinstein WS, Wang C, et al.: Familial risk for common diseases in primary care: the Family Healthware Impact Trial. Am J Prev Med 36 (6): 506-14, 2009.[PUBMED Abstract]
- Rubinstein WS, O'neill SM, Rothrock N, et al.: Components of family history associated with women's disease perceptions for cancer: a report from the Family Healthware™ Impact Trial. Genet Med 13 (1): 52-62, 2011.[PUBMED Abstract]
- Theis B, Boyd N, Lockwood G, et al.: Accuracy of family cancer history in breast cancer patients. Eur J Cancer Prev 3 (4): 321-7, 1994.[PUBMED Abstract]
- Breuer B, Kash KM, Rosenthal G, et al.: Reporting bilaterality status in first-degree relatives with breast cancer: a validity study. Genet Epidemiol 10 (4): 245-56, 1993.[PUBMED Abstract]
- Parent ME, Ghadirian P, Lacroix A, et al.: The reliability of recollections of family history: implications for the medical provider. J Cancer Educ 12 (2): 114-20, 1997 Summer.[PUBMED Abstract]
- Kelly KM, Shedlosky-Shoemaker R, Porter K, et al.: Cancer family history reporting: impact of method and psychosocial factors. J Genet Couns 16 (3): 373-82, 2007.[PUBMED Abstract]
- Kerber RA, Slattery ML: Comparison of self-reported and database-linked family history of cancer data in a case-control study. Am J Epidemiol 146 (3): 244-8, 1997.[PUBMED Abstract]
- Kerr B, Foulkes WD, Cade D, et al.: False family history of breast cancer in the family cancer clinic. Eur J Surg Oncol 24 (4): 275-9, 1998.[PUBMED Abstract]
- Schwartz MD, Peshkin BN, Hughes C, et al.: Impact of BRCA1/BRCA2 mutation testing on psychologic distress in a clinic-based sample. J Clin Oncol 20 (2): 514-20, 2002.[PUBMED Abstract]
- Mancini J, Noguès C, Adenis C, et al.: Impact of an information booklet on satisfaction and decision-making about BRCA genetic testing. Eur J Cancer 42 (7): 871-81, 2006.[PUBMED Abstract]
- Green MJ, Biesecker BB, McInerney AM, et al.: An interactive computer program can effectively educate patients about genetic testing for breast cancer susceptibility. Am J Med Genet 103 (1): 16-23, 2001.[PUBMED Abstract]
- Green MJ, Peterson SK, Baker MW, et al.: Effect of a computer-based decision aid on knowledge, perceptions, and intentions about genetic testing for breast cancer susceptibility: a randomized controlled trial. JAMA 292 (4): 442-52, 2004.[PUBMED Abstract]
- Green MJ, McInerney AM, Biesecker BB, et al.: Education about genetic testing for breast cancer susceptibility: patient preferences for a computer program or genetic counselor. Am J Med Genet 103 (1): 24-31, 2001.[PUBMED Abstract]
- Dabney MK, Huelsman K: Counseling by computer: breast cancer risk and genetic testing. Developed by the University of Wisconsin-Madison Department of Medicine and the Program in Medical Ethics. Genet Test 4 (1): 43-4, 2000.[PUBMED Abstract]
- Green MJ, Peterson SK, Baker MW, et al.: Use of an educational computer program before genetic counseling for breast cancer susceptibility: effects on duration and content of counseling sessions. Genet Med 7 (4): 221-9, 2005.[PUBMED Abstract]
- Wang C, Gonzalez R, Milliron KJ, et al.: Genetic counseling for BRCA1/2: a randomized controlled trial of two strategies to facilitate the education and counseling process. Am J Med Genet A 134 (1): 66-73, 2005.[PUBMED Abstract]
- Joseph G, Beattie MS, Lee R, et al.: Pre-counseling education for low literacy women at risk of Hereditary Breast and Ovarian Cancer (HBOC): patient experiences using the Cancer Risk Education Intervention Tool (CREdIT). J Genet Couns 19 (5): 447-62, 2010.[PUBMED Abstract]
- Albada A, van Dulmen S, Lindhout D, et al.: A pre-visit tailored website enhances counselees' realistic expectations and knowledge and fulfils information needs for breast cancer genetic counselling. Fam Cancer 11 (1): 85-95, 2012.[PUBMED Abstract]
- Baty BJ, Kinney AY, Ellis SM: Developing culturally sensitive cancer genetics communication aids for African Americans. Am J Med Genet 118A (2): 146-55, 2003.[PUBMED Abstract]
- Permuth-Wey J, Vadaparampil S, Rumphs A, et al.: Development of a culturally tailored genetic counseling booklet about hereditary breast and ovarian cancer for Black women. Am J Med Genet A 152A (4): 836-45, 2010.[PUBMED Abstract]
- Pal T, Stowe C, Cole A, et al.: Evaluation of phone-based genetic counselling in African American women using culturally tailored visual aids. Clin Genet 78 (2): 124-31, 2010.[PUBMED Abstract]
- Calzone KA: Predisposition testing for breast and ovarian cancer susceptibility. Semin Oncol Nurs 13 (2): 82-90, 1997.[PUBMED Abstract]
- Smith KR, West JA, Croyle RT, et al.: Familial context of genetic testing for cancer susceptibility: moderating effect of siblings' test results on psychological distress one to two weeks after BRCA1 mutation testing. Cancer Epidemiol Biomarkers Prev 8 (4 Pt 2): 385-92, 1999.[PUBMED Abstract]
- Wylie JE, Smith KR, Botkin JR: Effects of spouses on distress experienced by BRCA1 mutation carriers over time. Am J Med Genet 119C (1): 35-44, 2003.[PUBMED Abstract]
- Kash KM, Holland JC, Halper MS, et al.: Psychological distress and surveillance behaviors of women with a family history of breast cancer. J Natl Cancer Inst 84 (1): 24-30, 1992.[PUBMED Abstract]
- Lerman C, Schwartz M: Adherence and psychological adjustment among women at high risk for breast cancer. Breast Cancer Res Treat 28 (2): 145-55, 1993.[PUBMED Abstract]
- Kelly PT: Understanding Breast Cancer Risk. Philadelphia, Pa: Temple University Press, 1991.[PUBMED Abstract]
- Baty BJ, Venne VL, McDonald J, et al.: BRCA1 testing: genetic counseling protocol development and counseling issues. J Genet Couns 6 (2): 223-44, 1997.[PUBMED Abstract]
- Richards MP, Hallowell N, Green JM, et al.: Counseling families with hereditary breast and ovarian cancer: a psychosocial perspective. J Genet Couns 4 (3): 219-33, 1995.[PUBMED Abstract]
- Hoskins KF, Stopfer JE, Calzone KA, et al.: Assessment and counseling for women with a family history of breast cancer. A guide for clinicians. JAMA 273 (7): 577-85, 1995.[PUBMED Abstract]
- Schneider KA: Genetic counseling for BRCA1/BRCA2 testing. Genet Test 1 (2): 91-8, 1997.[PUBMED Abstract]
- McKinnon WC, Baty BJ, Bennett RL, et al.: Predisposition genetic testing for late-onset disorders in adults. A position paper of the National Society of Genetic Counselors. JAMA 278 (15): 1217-20, 1997.[PUBMED Abstract]
- Cummings S, Olopade O: Predisposition testing for inherited breast cancer. Oncology (Huntingt) 12 (8): 1227-41; discussion 1241-2, 1998.[PUBMED Abstract]
- Lipkus IM, Klein WM, Rimer BK: Communicating breast cancer risks to women using different formats. Cancer Epidemiol Biomarkers Prev 10 (8): 895-8, 2001.[PUBMED Abstract]
- Butow PN, Lobb EA: Analyzing the process and content of genetic counseling in familial breast cancer consultations. J Genet Couns 13 (5): 403-24, 2004.[PUBMED Abstract]
- Lerman C, Audrain J, Croyle RT: DNA-testing for heritable breast cancer risks: lessons from traditional genetic counseling. Ann Behav Med 16(4): 327-333, 1994.[PUBMED Abstract]
- Pieterse AH, van Dulmen AM, Beemer FA, et al.: Cancer genetic counseling: communication and counselees' post-visit satisfaction, cognitions, anxiety, and needs fulfillment. J Genet Couns 16 (1): 85-96, 2007.[PUBMED Abstract]
- Hamilton JG, Lobel M, Moyer A: Emotional distress following genetic testing for hereditary breast and ovarian cancer: a meta-analytic review. Health Psychol 28 (4): 510-8, 2009.[PUBMED Abstract]
- Beran TM, Stanton AL, Kwan L, et al.: The trajectory of psychological impact in BRCA1/2 genetic testing: does time heal? Ann Behav Med 36 (2): 107-16, 2008.[PUBMED Abstract]
- Bosch N, Junyent N, Gadea N, et al.: What factors may influence psychological well being at three months and one year post BRCA genetic result disclosure? Breast 21 (6): 755-60, 2012.[PUBMED Abstract]
- O'Neill SC, Rini C, Goldsmith RE, et al.: Distress among women receiving uninformative BRCA1/2 results: 12-month outcomes. Psychooncology 18 (10): 1088-96, 2009.[PUBMED Abstract]
- Oberguggenberger A, Sztankay M, Morscher RJ, et al.: Psychosocial outcomes and counselee satisfaction following genetic counseling for hereditary breast and ovarian cancer: A patient-reported outcome study. J Psychosom Res 89: 39-45, 2016.[PUBMED Abstract]
- Foster C, Watson M, Eeles R, et al.: Predictive genetic testing for BRCA1/2 in a UK clinical cohort: three-year follow-up. Br J Cancer 96 (5): 718-24, 2007.[PUBMED Abstract]
- Halbert CH, Stopfer JE, McDonald J, et al.: Long-term reactions to genetic testing for BRCA1 and BRCA2 mutations: does time heal women's concerns? J Clin Oncol 29 (32): 4302-6, 2011.[PUBMED Abstract]
- Graves KD, Vegella P, Poggi EA, et al.: Long-term psychosocial outcomes of BRCA1/BRCA2 testing: differences across affected status and risk-reducing surgery choice. Cancer Epidemiol Biomarkers Prev 21 (3): 445-55, 2012.[PUBMED Abstract]
- Cella D, Hughes C, Peterman A, et al.: A brief assessment of concerns associated with genetic testing for cancer: the Multidimensional Impact of Cancer Risk Assessment (MICRA) questionnaire. Health Psychol 21 (6): 564-72, 2002.[PUBMED Abstract]
- Shkedi-Rafid S, Gabai-Kapara E, Grinshpun-Cohen J, et al.: BRCA genetic testing of individuals from families with low prevalence of cancer: experiences of carriers and implications for population screening. Genet Med 14 (7): 688-94, 2012.[PUBMED Abstract]
- Metcalfe KA, Poll A, Llacuachaqui M, et al.: Patient satisfaction and cancer-related distress among unselected Jewish women undergoing genetic testing for BRCA1 and BRCA2. Clin Genet 78 (5): 411-7, 2010.[PUBMED Abstract]
- Metcalfe KA, Mian N, Enmore M, et al.: Long-term follow-up of Jewish women with a BRCA1 and BRCA2 mutation who underwent population genetic screening. Breast Cancer Res Treat 133 (2): 735-40, 2012.[PUBMED Abstract]
- Armstrong J, Toscano M, Kotchko N, et al.: Utilization and Outcomes of BRCA Genetic Testing and Counseling in a National Commercially Insured Population: The ABOUT Study. JAMA Oncol 1 (9): 1251-60, 2015.[PUBMED Abstract]
- Dohany L, Gustafson S, Ducaine W, et al.: Psychological distress with direct-to-consumer genetic testing: a case report of an unexpected BRCA positive test result. J Genet Couns 21 (3): 399-401, 2012.[PUBMED Abstract]
- Mahon SM: Impact of direct-to-consumer genetic testing. J Oncol Pract 8 (4): 260, 2012.[PUBMED Abstract]
- Jeffers L, Morrison PJ, McCaughan E, et al.: Maximising survival: the main concern of women with hereditary breast and ovarian cancer who undergo genetic testing for BRCA1/2. Eur J Oncol Nurs 18 (4): 411-8, 2014.[PUBMED Abstract]
- Francke U, Dijamco C, Kiefer AK, et al.: Dealing with the unexpected: consumer responses to direct-access BRCA mutation testing. PeerJ 1: e8, 2013.[PUBMED Abstract]
- Meiser B, Quinn VF, Gleeson M, et al.: When knowledge of a heritable gene mutation comes out of the blue: treatment-focused genetic testing in women newly diagnosed with breast cancer. Eur J Hum Genet 24 (11): 1517-1523, 2016.[PUBMED Abstract]
- Ardern-Jones A, Kenen R, Eeles R: Too much, too soon? Patients and health professionals' views concerning the impact of genetic testing at the time of breast cancer diagnosis in women under the age of 40. Eur J Cancer Care (Engl) 14 (3): 272-81, 2005.[PUBMED Abstract]
- Wevers MR, Hahn DE, Verhoef S, et al.: Breast cancer genetic counseling after diagnosis but before treatment: a pilot study on treatment consequences and psychological impact. Patient Educ Couns 89 (1): 89-95, 2012.[PUBMED Abstract]
- Zilliacus E, Meiser B, Gleeson M, et al.: Are we being overly cautious? A qualitative inquiry into the experiences and perceptions of treatment-focused germline BRCA genetic testing amongst women recently diagnosed with breast cancer. Support Care Cancer 20 (11): 2949-58, 2012.[PUBMED Abstract]
- Tercyak KP, Peshkin BN, Brogan BM, et al.: Quality of life after contralateral prophylactic mastectomy in newly diagnosed high-risk breast cancer patients who underwent BRCA1/2 gene testing. J Clin Oncol 25 (3): 285-91, 2007.[PUBMED Abstract]
- Wevers MR, Ausems MG, Verhoef S, et al.: Does rapid genetic counseling and testing in newly diagnosed breast cancer patients cause additional psychosocial distress? results from a randomized clinical trial. Genet Med 18 (2): 137-44, 2016.[PUBMED Abstract]
- Wevers MR, Aaronson NK, Bleiker EMA, et al.: Rapid genetic counseling and testing in newly diagnosed breast cancer: Patients' and health professionals' attitudes, experiences, and evaluation of effects on treatment decision making. J Surg Oncol 116 (8): 1029-1039, 2017.[PUBMED Abstract]
- Lerman C, Peshkin BN, Hughes C, et al.: Family disclosure in genetic testing for cancer susceptibility: determinants and consequences. Journal of Health Care Law and Policy 1 (2): 353-73, 1998.[PUBMED Abstract]
- Elrick A, Ashida S, Ivanovich J, et al.: Psychosocial and Clinical Factors Associated with Family Communication of Cancer Genetic Test Results among Women Diagnosed with Breast Cancer at a Young Age. J Genet Couns 26 (1): 173-181, 2017.[PUBMED Abstract]
- Finlay E, Stopfer JE, Burlingame E, et al.: Factors determining dissemination of results and uptake of genetic testing in families with known BRCA1/2 mutations. Genet Test 12 (1): 81-91, 2008.[PUBMED Abstract]
- Hughes C, Lerman C, Schwartz M, et al.: All in the family: evaluation of the process and content of sisters' communication about BRCA1 and BRCA2 genetic test results. Am J Med Genet 107 (2): 143-50, 2002.[PUBMED Abstract]
- Baars JE, Ausems MG, van Riel E, et al.: Communication Between Breast Cancer Patients Who Received Inconclusive Genetic Test Results and Their Daughters and Sisters Years After Testing. J Genet Couns 25 (3): 461-71, 2016.[PUBMED Abstract]
- Wagner Costalas J, Itzen M, Malick J, et al.: Communication of BRCA1 and BRCA2 results to at-risk relatives: a cancer risk assessment program's experience. Am J Med Genet 119C (1): 11-8, 2003.[PUBMED Abstract]
- Patenaude AF, Dorval M, DiGianni LS, et al.: Sharing BRCA1/2 test results with first-degree relatives: factors predicting who women tell. J Clin Oncol 24 (4): 700-6, 2006.[PUBMED Abstract]
- MacDonald DJ, Sarna L, van Servellen G, et al.: Selection of family members for communication of cancer risk and barriers to this communication before and after genetic cancer risk assessment. Genet Med 9 (5): 275-82, 2007.[PUBMED Abstract]
- Kenen R, Arden-Jones A, Eeles R: Healthy women from suspected hereditary breast and ovarian cancer families: the significant others in their lives. Eur J Cancer Care (Engl) 13 (2): 169-79, 2004.[PUBMED Abstract]
- Claes E, Evers-Kiebooms G, Boogaerts A, et al.: Communication with close and distant relatives in the context of genetic testing for hereditary breast and ovarian cancer in cancer patients. Am J Med Genet 116A (1): 11-9, 2003.[PUBMED Abstract]
- Foster C, Eeles R, Ardern-Jones A, et al.: Juggling roles and expectations: dilemmas faced by women talking to relatives about cancer and genetic testing. Psychol Health 19 (4): 439-55, 2004.[PUBMED Abstract]
- Kenen R, Arden-Jones A, Eeles R: We are talking, but are they listening? Communication patterns in families with a history of breast/ovarian cancer (HBOC). Psychooncology 13 (5): 335-45, 2004.[PUBMED Abstract]
- Segal J, Esplen MJ, Toner B, et al.: An investigation of the disclosure process and support needs of BRCA1 and BRCA2 carriers. Am J Med Genet A 125 (3): 267-72, 2004.[PUBMED Abstract]
- Bradbury AR, Dignam JJ, Ibe CN, et al.: How often do BRCA mutation carriers tell their young children of the family's risk for cancer? A study of parental disclosure of BRCA mutations to minors and young adults. J Clin Oncol 25 (24): 3705-11, 2007.[PUBMED Abstract]
- Bradbury AR, Patrick-Miller L, Pawlowski K, et al.: Learning of your parent's BRCA mutation during adolescence or early adulthood: a study of offspring experiences. Psychooncology 18 (2): 200-8, 2009.[PUBMED Abstract]
- Manne S, Audrain J, Schwartz M, et al.: Associations between relationship support and psychological reactions of participants and partners to BRCA1 and BRCA2 testing in a clinic-based sample. Ann Behav Med 28 (3): 211-25, 2004.[PUBMED Abstract]
- Daly MB, Montgomery S, Bingler R, et al.: Communicating genetic test results within the family: Is it lost in translation? A survey of relatives in the randomized six-step study. Fam Cancer 15 (4): 697-706, 2016.[PUBMED Abstract]
- McAllister MF, Evans DG, Ormiston W, et al.: Men in breast cancer families: a preliminary qualitative study of awareness and experience. J Med Genet 35 (9): 739-44, 1998.[PUBMED Abstract]
- Liede A, Metcalfe K, Hanna D, et al.: Evaluation of the needs of male carriers of mutations in BRCA1 or BRCA2 who have undergone genetic counseling. Am J Hum Genet 67 (6): 1494-504, 2000.[PUBMED Abstract]
- Metcalfe KA, Liede A, Trinkaus M, et al.: Evaluation of the needs of spouses of female carriers of mutations in BRCA1 and BRCA2. Clin Genet 62 (6): 464-9, 2002.[PUBMED Abstract]
- Mireskandari S, Sherman KA, Meiser B, et al.: Psychological adjustment among partners of women at high risk of developing breast/ovarian cancer. Genet Med 9 (5): 311-20, 2007.[PUBMED Abstract]
- Sherman KA, Kasparian NA, Mireskandari S: Psychological adjustment among male partners in response to women's breast/ovarian cancer risk: a theoretical review of the literature. Psychooncology 19 (1): 1-11, 2010.[PUBMED Abstract]
- Daly MB: The impact of social roles on the experience of men in BRCA1/2 families: implications for counseling. J Genet Couns 18 (1): 42-8, 2009.[PUBMED Abstract]
- DudokdeWit AC, Tibben A, Frets PG, et al.: Males at-risk for the BRCA1 gene, the psychological impact. Psychooncology 5(3): 251-257, 1996.[PUBMED Abstract]
- Lodder L, Frets PG, Trijsburg RW, et al.: Men at risk of being a mutation carrier for hereditary breast/ovarian cancer: an exploration of attitudes and psychological functioning during genetic testing. Eur J Hum Genet 9 (7): 492-500, 2001.[PUBMED Abstract]
- Lerman C, Hughes C, Croyle RT, et al.: Prophylactic surgery decisions and surveillance practices one year following BRCA1/2 testing. Prev Med 31 (1): 75-80, 2000.[PUBMED Abstract]
- Hughes C, Lynch H, Durham C, et al.: Communication of BRCA1/2 Test Results in Hereditary Breast Cancer Families. Cancer Research in Therapy and Control Vol. 8, 1999, pp. 51-59.[PUBMED Abstract]
- Tercyak KP, Hughes C, Main D, et al.: Parental communication of BRCA1/2 genetic test results to children. Patient Educ Couns 42 (3): 213-24, 2001.[PUBMED Abstract]
- Tercyak KP, Peshkin BN, DeMarco TA, et al.: Parent-child factors and their effect on communicating BRCA1/2 test results to children. Patient Educ Couns 47 (2): 145-53, 2002.[PUBMED Abstract]
- McGivern B, Everett J, Yager GG, et al.: Family communication about positive BRCA1 and BRCA2 genetic test results. Genet Med 6 (6): 503-9, 2004 Nov-Dec.[PUBMED Abstract]
- Bradbury AR, Patrick-Miller L, Schwartz L, et al.: Psychosocial Adjustment in School-age Girls With a Family History of Breast Cancer. Pediatrics 136 (5): 927-37, 2015.[PUBMED Abstract]
- Bradbury AR, Patrick-Miller L, Schwartz LA, et al.: Psychosocial Adjustment and Perceived Risk Among Adolescent Girls From Families With BRCA1/2 or Breast Cancer History. J Clin Oncol 34 (28): 3409-16, 2016.[PUBMED Abstract]
- Tercyak KP, Peshkin BN, Demarco TA, et al.: Information needs of mothers regarding communicating BRCA1/2 cancer genetic test results to their children. Genet Test 11 (3): 249-55, 2007.[PUBMED Abstract]
- Wertz DC: International perspectives. In: Clarke A, ed.: The Genetic Testing of Children. Oxford, England: BIOS Scientific, 1998, pp 271-287.[PUBMED Abstract]
- Benkendorf JL, Reutenauer JE, Hughes CA, et al.: Patients' attitudes about autonomy and confidentiality in genetic testing for breast-ovarian cancer susceptibility. Am J Med Genet 73 (3): 296-303, 1997.[PUBMED Abstract]
- Staton AD, Kurian AW, Cobb K, et al.: Cancer risk reduction and reproductive concerns in female BRCA1/2 mutation carriers. Fam Cancer 7 (2): 179-86, 2008.[PUBMED Abstract]
- Friedman LC, Kramer RM: Reproductive issues for women with BRCA mutations. J Natl Cancer Inst Monogr (34): 83-6, 2005.[PUBMED Abstract]
- Smith KR, Ellington L, Chan AY, et al.: Fertility intentions following testing for a BRCA1 gene mutation. Cancer Epidemiol Biomarkers Prev 13 (5): 733-40, 2004.[PUBMED Abstract]
- Quinn G, Vadaparampil S, Wilson C, et al.: Attitudes of high-risk women toward preimplantation genetic diagnosis. Fertil Steril 91 (6): 2361-8, 2009.[PUBMED Abstract]
- Cunniff C; American Academy of Pediatrics Committee on Genetics: Prenatal screening and diagnosis for pediatricians. Pediatrics 114 (3): 889-94, 2004.[PUBMED Abstract]
- Rappaport VJ: Prenatal diagnosis and genetic screening--integration into prenatal care. Obstet Gynecol Clin North Am 35 (3): 435-58, ix, 2008.[PUBMED Abstract]
- Baruch S, Kaufman D, Hudson KL: Genetic testing of embryos: practices and perspectives of US in vitro fertilization clinics. Fertil Steril 89 (5): 1053-8, 2008.[PUBMED Abstract]
- Ogilvie CM, Braude PR, Scriven PN: Preimplantation genetic diagnosis--an overview. J Histochem Cytochem 53 (3): 255-60, 2005.[PUBMED Abstract]
- Vadaparampil ST, Quinn GP, Knapp C, et al.: Factors associated with preimplantation genetic diagnosis acceptance among women concerned about hereditary breast and ovarian cancer. Genet Med 11 (10): 757-65, 2009.[PUBMED Abstract]
- Quinn GP, Vadaparampil ST, King LM, et al.: Conflict between values and technology: perceptions of preimplantation genetic diagnosis among women at increased risk for hereditary breast and ovarian cancer. Fam Cancer 8 (4): 441-9, 2009.[PUBMED Abstract]
- Chan JL, Johnson LNC, Sammel MD, et al.: Reproductive Decision-Making in Women with BRCA1/2 Mutations. J Genet Couns 26 (3): 594-603, 2017.[PUBMED Abstract]
- Menon U, Harper J, Sharma A, et al.: Views of BRCA gene mutation carriers on preimplantation genetic diagnosis as a reproductive option for hereditary breast and ovarian cancer. Hum Reprod 22 (6): 1573-7, 2007.[PUBMED Abstract]
- Fortuny D, Balmaña J, Graña B, et al.: Opinion about reproductive decision making among individuals undergoing BRCA1/2 genetic testing in a multicentre Spanish cohort. Hum Reprod 24 (4): 1000-6, 2009.[PUBMED Abstract]
- Julian-Reynier C, Fabre R, Coupier I, et al.: BRCA1/2 carriers: their childbearing plans and theoretical intentions about having preimplantation genetic diagnosis and prenatal diagnosis. Genet Med 14 (5): 527-34, 2012.[PUBMED Abstract]
- Ormondroyd E, Donnelly L, Moynihan C, et al.: Attitudes to reproductive genetic testing in women who had a positive BRCA test before having children: a qualitative analysis. Eur J Hum Genet 20 (1): 4-10, 2012.[PUBMED Abstract]
- Quinn GP, Vadaparampil ST, Miree CA, et al.: High risk men's perceptions of pre-implantation genetic diagnosis for hereditary breast and ovarian cancer. Hum Reprod 25 (10): 2543-50, 2010.[PUBMED Abstract]
- Struewing JP, Abeliovich D, Peretz T, et al.: The carrier frequency of the BRCA1 185delAG mutation is approximately 1 percent in Ashkenazi Jewish individuals. Nat Genet 11 (2): 198-200, 1995.[PUBMED Abstract]
- Rothenberg KH: Breast cancer, the genetic "quick fix," and the Jewish community. Ethical, legal, and social challenges. Health Matrix Clevel 7 (1): 97-124, 1997 Winter.[PUBMED Abstract]
- Foster MW, Bernsten D, Carter TH: A model agreement for genetic research in socially identifiable populations. Am J Hum Genet 63 (3): 696-702, 1998.[PUBMED Abstract]
- Burhansstipanov L, Bemis LT, Dignan MB: Native American cancer education: genetic and cultural issues. J Cancer Educ 16 (3): 142-5, 2001 Autumn.[PUBMED Abstract]
- Hughes C, Fasaye GA, LaSalle VH, et al.: Sociocultural influences on participation in genetic risk assessment and testing among African American women. Patient Educ Couns 51 (2): 107-14, 2003.[PUBMED Abstract]
- Julian-Reynier CM, Bouchard LJ, Evans DG, et al.: Women's attitudes toward preventive strategies for hereditary breast or ovarian carcinoma differ from one country to another: differences among English, French, and Canadian women. Cancer 92 (4): 959-68, 2001.[PUBMED Abstract]
- Phillips KA, Warner E, Meschino WS, et al.: Perceptions of Ashkenazi Jewish breast cancer patients on genetic testing for mutations in BRCA1 and BRCA2. Clin Genet 57 (5): 376-83, 2000.[PUBMED Abstract]
- Vadaparampil ST, Quinn GP, Small BJ, et al.: A pilot study of hereditary breast and ovarian knowledge among a multiethnic group of Hispanic women with a personal or family history of cancer. Genet Test Mol Biomarkers 14 (1): 99-106, 2010.[PUBMED Abstract]
- Halbert CH, Kessler L, Troxel AB, et al.: Effect of genetic counseling and testing for BRCA1 and BRCA2 mutations in African American women: a randomized trial. Public Health Genomics 13 (7-8): 440-8, 2010.[PUBMED Abstract]
- Freedman TG: Genetic susceptibility testing: ethical and social quandaries. Health Soc Work 23 (3): 214-22, 1998.[PUBMED Abstract]
- Hubbard R, Lewontin RC: Pitfalls of genetic testing. N Engl J Med 334 (18): 1192-4, 1996.[PUBMED Abstract]
- Parens E: Glad and terrified: on the ethics of BRACA1 and 2 testing. Cancer Invest 14 (4): 405-11, 1996.[PUBMED Abstract]
- Winter PR, Wiesner GL, Finnegan J, et al.: Notification of a family history of breast cancer: issues of privacy and confidentiality. Am J Med Genet 66 (1): 1-6, 1996.[PUBMED Abstract]
- Geller G, Doksum T, Bernhardt BA, et al.: Participation in breast cancer susceptibility testing protocols: influence of recruitment source, altruism, and family involvement on women's decisions. Cancer Epidemiol Biomarkers Prev 8 (4 Pt 2): 377-83, 1999.[PUBMED Abstract]
- Rimer BK, Schildkraut JM, Lerman C, et al.: Participation in a women's breast cancer risk counseling trial. Who participates? Who declines? High Risk Breast Cancer Consortium. Cancer 77 (11): 2348-55, 1996.[PUBMED Abstract]
- Robson ME, Storm CD, Weitzel J, et al.: American Society of Clinical Oncology policy statement update: genetic and genomic testing for cancer susceptibility. J Clin Oncol 28 (5): 893-901, 2010.[PUBMED Abstract]
- Burke W, Daly M, Garber J, et al.: Recommendations for follow-up care of individuals with an inherited predisposition to cancer. II. BRCA1 and BRCA2. Cancer Genetics Studies Consortium. JAMA 277 (12): 997-1003, 1997.[PUBMED Abstract]
- Durfy SJ, Buchanan TE, Burke W: Testing for inherited susceptibility to breast cancer: a survey of informed consent forms for BRCA1 and BRCA2 mutation testing. Am J Med Genet 75 (1): 82-7, 1998.[PUBMED Abstract]
- Statement of the American Society of Clinical Oncology: genetic testing for cancer susceptibility, Adopted on February 20, 1996. J Clin Oncol 14 (5): 1730-6; discussion 1737-40, 1996.[PUBMED Abstract]
- Hallowell N, Foster C, Eeles R, et al.: Balancing autonomy and responsibility: the ethics of generating and disclosing genetic information. J Med Ethics 29 (2): 74-9; discussion 80-3, 2003.[PUBMED Abstract]
- Metcalfe KA, Poll A, O'Connor A, et al.: Development and testing of a decision aid for breast cancer prevention for women with a BRCA1 or BRCA2 mutation. Clin Genet 72 (3): 208-17, 2007.[PUBMED Abstract]
- Tiller K, Meiser B, Gaff C, et al.: A randomized controlled trial of a decision aid for women at increased risk of ovarian cancer. Med Decis Making 26 (4): 360-72, 2006 Jul-Aug.[PUBMED Abstract]
- van Roosmalen MS, Stalmeier PF, Verhoef LC, et al.: Randomized trial of a shared decision-making intervention consisting of trade-offs and individualized treatment information for BRCA1/2 mutation carriers. J Clin Oncol 22 (16): 3293-301, 2004.[PUBMED Abstract]
- Culver JO, MacDonald DJ, Thornton AA, et al.: Development and evaluation of a decision aid for BRCA carriers with breast cancer. J Genet Couns 20 (3): 294-307, 2011.[PUBMED Abstract]
- Metcalfe KA, Dennis CL, Poll A, et al.: Effect of decision aid for breast cancer prevention on decisional conflict in women with a BRCA1 or BRCA2 mutation: a multisite, randomized, controlled trial. Genet Med 19 (3): 330-336, 2017.[PUBMED Abstract]
- Schwartz MD, Lerman C, Brogan B, et al.: Impact of BRCA1/BRCA2 counseling and testing on newly diagnosed breast cancer patients. J Clin Oncol 22 (10): 1823-9, 2004.[PUBMED Abstract]
- Botkin JR, Smith KR, Croyle RT, et al.: Genetic testing for a BRCA1 mutation: prophylactic surgery and screening behavior in women 2 years post testing. Am J Med Genet A 118 (3): 201-9, 2003.[PUBMED Abstract]
- Beattie MS, Crawford B, Lin F, et al.: Uptake, time course, and predictors of risk-reducing surgeries in BRCA carriers. Genet Test Mol Biomarkers 13 (1): 51-6, 2009.[PUBMED Abstract]
- O'Neill SC, Valdimarsdottir HB, Demarco TA, et al.: BRCA1/2 test results impact risk management attitudes, intentions, and uptake. Breast Cancer Res Treat 124 (3): 755-64, 2010.[PUBMED Abstract]
- Schwartz MD, Isaacs C, Graves KD, et al.: Long-term outcomes of BRCA1/BRCA2 testing: risk reduction and surveillance. Cancer 118 (2): 510-7, 2012.[PUBMED Abstract]
- Garcia C, Wendt J, Lyon L, et al.: Risk management options elected by women after testing positive for a BRCA mutation. Gynecol Oncol 132 (2): 428-33, 2014.[PUBMED Abstract]
- Singh K, Lester J, Karlan B, et al.: Impact of family history on choosing risk-reducing surgery among BRCA mutation carriers. Am J Obstet Gynecol 208 (4): 329.e1-6, 2013.[PUBMED Abstract]
- Phillips KA, Jenkins MA, Lindeman GJ, et al.: Risk-reducing surgery, screening and chemoprevention practices of BRCA1 and BRCA2 mutation carriers: a prospective cohort study. Clin Genet 70 (3): 198-206, 2006.[PUBMED Abstract]
- Metcalfe KA, Birenbaum-Carmeli D, Lubinski J, et al.: International variation in rates of uptake of preventive options in BRCA1 and BRCA2 mutation carriers. Int J Cancer 122 (9): 2017-22, 2008.[PUBMED Abstract]
- Julian-Reynier C, Mancini J, Mouret-Fourme E, et al.: Cancer risk management strategies and perceptions of unaffected women 5 years after predictive genetic testing for BRCA1/2 mutations. Eur J Hum Genet 19 (5): 500-6, 2011.[PUBMED Abstract]
- Scheuer L, Kauff N, Robson M, et al.: Outcome of preventive surgery and screening for breast and ovarian cancer in BRCA mutation carriers. J Clin Oncol 20 (5): 1260-8, 2002.[PUBMED Abstract]
- Mannis GN, Fehniger JE, Creasman JS, et al.: Risk-reducing salpingo-oophorectomy and ovarian cancer screening in 1077 women after BRCA testing. JAMA Intern Med 173 (2): 96-103, 2013.[PUBMED Abstract]
- Friebel TM, Domchek SM, Neuhausen SL, et al.: Bilateral prophylactic oophorectomy and bilateral prophylactic mastectomy in a prospective cohort of unaffected BRCA1 and BRCA2 mutation carriers. Clin Breast Cancer 7 (11): 875-82, 2007.[PUBMED Abstract]
- Madalinska JB, van Beurden M, Bleiker EM, et al.: Predictors of prophylactic bilateral salpingo-oophorectomy compared with gynecologic screening use in BRCA1/2 mutation carriers. J Clin Oncol 25 (3): 301-7, 2007.[PUBMED Abstract]
- Rhiem K, Foth D, Wappenschmidt B, et al.: Risk-reducing salpingo-oophorectomy in BRCA1 and BRCA2 mutation carriers. Arch Gynecol Obstet 283 (3): 623-7, 2011.[PUBMED Abstract]
- Sidon L, Ingham S, Clancy T, et al.: Uptake of risk-reducing salpingo-oophorectomy in women carrying a BRCA1 or BRCA2 mutation: evidence for lower uptake in women affected by breast cancer and older women. Br J Cancer 106 (4): 775-9, 2012.[PUBMED Abstract]
- Lerman C, Narod S, Schulman K, et al.: BRCA1 testing in families with hereditary breast-ovarian cancer. A prospective study of patient decision making and outcomes. JAMA 275 (24): 1885-92, 1996.[PUBMED Abstract]
- van Dijk S, van Roosmalen MS, Otten W, et al.: Decision making regarding prophylactic mastectomy: stability of preferences and the impact of anticipated feelings of regret. J Clin Oncol 26 (14): 2358-63, 2008.[PUBMED Abstract]
- Claes E, Evers-Kiebooms G, Decruyenaere M, et al.: Surveillance behavior and prophylactic surgery after predictive testing for hereditary breast/ovarian cancer. Behav Med 31 (3): 93-105, 2005.[PUBMED Abstract]
- Ray JA, Loescher LJ, Brewer M: Risk-reduction surgery decisions in high-risk women seen for genetic counseling. J Genet Couns 14 (6): 473-84, 2005.[PUBMED Abstract]
- Hallowell N: 'You don't want to lose your ovaries because you think 'I might become a man". Women's perceptions of prophylactic surgery as a cancer risk management option. Psychooncology 7 (3): 263-75, 1998 May-Jun.[PUBMED Abstract]
- Schneider KA, Stopfer JE, Peters JA, et al.: Complexities in cancer risk counseling: presentation of three cases. J Genet Couns 6 (2): 147-67, 1997.[PUBMED Abstract]
- Tarkan L: My Mother's Breast: Daughters Face Their Mothers' Cancer. Dallas, TX: Taylor Publishing, 1999.[PUBMED Abstract]
- Stefanek ME, Helzlsouer KJ, Wilcox PM, et al.: Predictors of and satisfaction with bilateral prophylactic mastectomy. Prev Med 24 (4): 412-9, 1995.[PUBMED Abstract]
- Cortesi L, Razzaboni E, Toss A, et al.: A rapid genetic counselling and testing in newly diagnosed breast cancer is associated with high rate of risk-reducing mastectomy in BRCA1/2-positive Italian women. Ann Oncol 25 (1): 57-63, 2014.[PUBMED Abstract]
- Rosenberg SM, Ruddy KJ, Tamimi RM, et al.: BRCA1 and BRCA2 Mutation Testing in Young Women With Breast Cancer. JAMA Oncol 2 (6): 730-6, 2016.[PUBMED Abstract]
- Graves KD, Peshkin BN, Halbert CH, et al.: Predictors and outcomes of contralateral prophylactic mastectomy among breast cancer survivors. Breast Cancer Res Treat 104 (3): 321-9, 2007.[PUBMED Abstract]
- Howard-McNatt M, Schroll RW, Hurt GJ, et al.: Contralateral prophylactic mastectomy in breast cancer patients who test negative for BRCA mutations. Am J Surg 202 (3): 298-302, 2011.[PUBMED Abstract]
- Bresser PJ, Seynaeve C, Van Gool AR, et al.: Satisfaction with prophylactic mastectomy and breast reconstruction in genetically predisposed women. Plast Reconstr Surg 117 (6): 1675-82; discussion 1683-4, 2006.[PUBMED Abstract]
- Brandberg Y, Sandelin K, Erikson S, et al.: Psychological reactions, quality of life, and body image after bilateral prophylactic mastectomy in women at high risk for breast cancer: a prospective 1-year follow-up study. J Clin Oncol 26 (24): 3943-9, 2008.[PUBMED Abstract]
- Lobb E, Meiser B: Genetic counselling and prophylactic surgery in women from families with hereditary breast or ovarian cancer. Lancet 363 (9424): 1841-2, 2004.[PUBMED Abstract]
- Lobb EA, Butow PN, Meiser B, et al.: Tailoring communication in consultations with women from high risk breast cancer families. Br J Cancer 87 (5): 502-8, 2002.[PUBMED Abstract]
- Lobb EA, Butow PN, Barratt A, et al.: Communication and information-giving in high-risk breast cancer consultations: influence on patient outcomes. Br J Cancer 90 (2): 321-7, 2004.[PUBMED Abstract]
- Schwartz MD, Kaufman E, Peshkin BN, et al.: Bilateral prophylactic oophorectomy and ovarian cancer screening following BRCA1/BRCA2 mutation testing. J Clin Oncol 21 (21): 4034-41, 2003.[PUBMED Abstract]
- Kauff ND, Satagopan JM, Robson ME, et al.: Risk-reducing salpingo-oophorectomy in women with a BRCA1 or BRCA2 mutation. N Engl J Med 346 (21): 1609-15, 2002.[PUBMED Abstract]
- Schmeler KM, Sun CC, Bodurka DC, et al.: Prophylactic bilateral salpingo-oophorectomy compared with surveillance in women with BRCA mutations. Obstet Gynecol 108 (3 Pt 1): 515-20, 2006.[PUBMED Abstract]
- MacDonald DJ, Sarna L, Uman GC, et al.: Cancer screening and risk-reducing behaviors of women seeking genetic cancer risk assessment for breast and ovarian cancers. Oncol Nurs Forum 33 (2): E27-35, 2006.[PUBMED Abstract]
- Litton JK, Westin SN, Ready K, et al.: Perception of screening and risk reduction surgeries in patients tested for a BRCA deleterious mutation. Cancer 115 (8): 1598-604, 2009.[PUBMED Abstract]
- Tyndel S, Austoker J, Henderson BJ, et al.: What is the psychological impact of mammographic screening on younger women with a family history of breast cancer? Findings from a prospective cohort study by the PIMMS Management Group. J Clin Oncol 25 (25): 3823-30, 2007.[PUBMED Abstract]
- Rees G, Young MA, Gaff C, et al.: A qualitative study of health professionals' views regarding provision of information about health-protective behaviors during genetic consultation for breast cancer. J Genet Couns 15 (2): 95-104, 2006.[PUBMED Abstract]
- Lodder LN, Frets PG, Trijsburg RW, et al.: One year follow-up of women opting for presymptomatic testing for BRCA1 and BRCA2: emotional impact of the test outcome and decisions on risk management (surveillance or prophylactic surgery). Breast Cancer Res Treat 73 (2): 97-112, 2002.[PUBMED Abstract]
- van Oostrom I, Meijers-Heijboer H, Lodder LN, et al.: Long-term psychological impact of carrying a BRCA1/2 mutation and prophylactic surgery: a 5-year follow-up study. J Clin Oncol 21 (20): 3867-74, 2003.[PUBMED Abstract]
- Bresser PJ, Seynaeve C, Van Gool AR, et al.: The course of distress in women at increased risk of breast and ovarian cancer due to an (identified) genetic susceptibility who opt for prophylactic mastectomy and/or salpingo-oophorectomy. Eur J Cancer 43 (1): 95-103, 2007.[PUBMED Abstract]
- Frost MH, Schaid DJ, Sellers TA, et al.: Long-term satisfaction and psychological and social function following bilateral prophylactic mastectomy. JAMA 284 (3): 319-24, 2000.[PUBMED Abstract]
- Metcalfe KA, Esplen MJ, Goel V, et al.: Psychosocial functioning in women who have undergone bilateral prophylactic mastectomy. Psychooncology 13 (1): 14-25, 2004.[PUBMED Abstract]
- Schlich-Bakker KJ, Ausems MG, Schipper M, et al.: BRCA1/2 mutation testing in breast cancer patients: a prospective study of the long-term psychological impact of approach during adjuvant radiotherapy. Breast Cancer Res Treat 109 (3): 507-14, 2008.[PUBMED Abstract]
- Frost MH, Slezak JM, Tran NV, et al.: Satisfaction after contralateral prophylactic mastectomy: the significance of mastectomy type, reconstructive complications, and body appearance. J Clin Oncol 23 (31): 7849-56, 2005.[PUBMED Abstract]
- Schwartz MD: Contralateral prophylactic mastectomy: efficacy, satisfaction, and regret. J Clin Oncol 23 (31): 7777-9, 2005.[PUBMED Abstract]
- Metcalfe KA, Cil TD, Semple JL, et al.: Long-Term Psychosocial Functioning in Women with Bilateral Prophylactic Mastectomy: Does Preservation of the Nipple-Areolar Complex Make a Difference? Ann Surg Oncol 22 (10): 3324-30, 2015.[PUBMED Abstract]
- Yao K, Liederbach E, Tang R, et al.: Nipple-sparing mastectomy in BRCA1/2 mutation carriers: an interim analysis and review of the literature. Ann Surg Oncol 22 (2): 370-6, 2015.[PUBMED Abstract]
- Geiger AM, Nekhlyudov L, Herrinton LJ, et al.: Quality of life after bilateral prophylactic mastectomy. Ann Surg Oncol 14 (2): 686-94, 2007.[PUBMED Abstract]
- Isern AE, Tengrup I, Loman N, et al.: Aesthetic outcome, patient satisfaction, and health-related quality of life in women at high risk undergoing prophylactic mastectomy and immediate breast reconstruction. J Plast Reconstr Aesthet Surg 61 (10): 1177-87, 2008.[PUBMED Abstract]
- Kenen RH, Shapiro PJ, Hantsoo L, et al.: Women with BRCA1 or BRCA2 mutations renegotiating a post-prophylactic mastectomy identity: self-image and self-disclosure. J Genet Couns 16 (6): 789-98, 2007.[PUBMED Abstract]
- Altschuler A, Nekhlyudov L, Rolnick SJ, et al.: Positive, negative, and disparate--women's differing long-term psychosocial experiences of bilateral or contralateral prophylactic mastectomy. Breast J 14 (1): 25-32, 2008 Jan-Feb.[PUBMED Abstract]
- Patenaude AF, Orozco S, Li X, et al.: Support needs and acceptability of psychological and peer consultation: attitudes of 108 women who had undergone or were considering prophylactic mastectomy. Psychooncology 17 (8): 831-43, 2008.[PUBMED Abstract]
- Elit L, Esplen MJ, Butler K, et al.: Quality of life and psychosexual adjustment after prophylactic oophorectomy for a family history of ovarian cancer. Fam Cancer 1 (3-4): 149-56, 2001.[PUBMED Abstract]
- Robson M, Hensley M, Barakat R, et al.: Quality of life in women at risk for ovarian cancer who have undergone risk-reducing oophorectomy. Gynecol Oncol 89 (2): 281-7, 2003.[PUBMED Abstract]
- Finch A, Metcalfe KA, Chiang JK, et al.: The impact of prophylactic salpingo-oophorectomy on menopausal symptoms and sexual function in women who carry a BRCA mutation. Gynecol Oncol 121 (1): 163-8, 2011.[PUBMED Abstract]
- Finch A, Metcalfe K, Lui J, et al.: Breast and ovarian cancer risk perception after prophylactic salpingo-oophorectomy due to an inherited mutation in the BRCA1 or BRCA2 gene. Clin Genet 75 (3): 220-4, 2009.[PUBMED Abstract]
- Madalinska JB, Hollenstein J, Bleiker E, et al.: Quality-of-life effects of prophylactic salpingo-oophorectomy versus gynecologic screening among women at increased risk of hereditary ovarian cancer. J Clin Oncol 23 (28): 6890-8, 2005.[PUBMED Abstract]
- Westin SN, Sun CC, Lu KH, et al.: Satisfaction with ovarian carcinoma risk-reduction strategies among women at high risk for breast and ovarian carcinoma. Cancer 117 (12): 2659-67, 2011.[PUBMED Abstract]
- Campfield Bonadies D, Moyer A, Matloff ET: What I wish I'd known before surgery: BRCA carriers' perspectives after bilateral salipingo-oophorectomy. Fam Cancer 10 (1): 79-85, 2011.[PUBMED Abstract]
- Isaacs C, Peshkin BN, Schwartz M, et al.: Breast and ovarian cancer screening practices in healthy women with a strong family history of breast or ovarian cancer. Breast Cancer Res Treat 71 (2): 103-12, 2002.[PUBMED Abstract]
- Peshkin BN, Schwartz MD, Isaacs C, et al.: Utilization of breast cancer screening in a clinically based sample of women after BRCA1/2 testing. Cancer Epidemiol Biomarkers Prev 11 (10 Pt 1): 1115-8, 2002.[PUBMED Abstract]
- Tinley ST, Houfek J, Watson P, et al.: Screening adherence in BRCA1/2 families is associated with primary physicians' behavior. Am J Med Genet A 125 (1): 5-11, 2004.[PUBMED Abstract]
- Lerman C, Seay J, Balshem A, et al.: Interest in genetic testing among first-degree relatives of breast cancer patients. Am J Med Genet 57 (3): 385-92, 1995.[PUBMED Abstract]
- Struewing JP, Lerman C, Kase RG, et al.: Anticipated uptake and impact of genetic testing in hereditary breast and ovarian cancer families. Cancer Epidemiol Biomarkers Prev 4 (2): 169-73, 1995.[PUBMED Abstract]
- Jacobsen PB, Valdimarsdottier HB, Brown KL, et al.: Decision-making about genetic testing among women at familial risk for breast cancer. Psychosom Med 59 (5): 459-66, 1997 Sep-Oct.[PUBMED Abstract]
- Watson M, Kash KM, Homewood J, et al.: Does genetic counseling have any impact on management of breast cancer risk? Genet Test 9 (2): 167-74, 2005.[PUBMED Abstract]
- 本要約の変更点(05/15/2020)
-
PDQがん情報要約は定期的に見直され、新情報が利用可能になり次第更新される。本セクションでは、上記の日付における本要約最新変更点を記述する。
序
身体的活動と人体計測的特徴のサブセクションは広範囲にわたって改訂された。
本文に以下の記述が追加された;ほとんどの乳がんリスクモデルは、全体として適切に調整されていることが示されているが、女性のサブグループごとにモデルの能力が異なる可能性がある。特に、BRCA1またはBRCA2病原性多様体の検査が陰性の女性に対するリスクモデルについて、独立したプロスペクティブな検証により、最も一般的に使用される臨床リスクモデルでは、このグループの女性のリスクが過小予測されることが裏付けられた(引用、参考文献145としてMacInnis et al.)。血縁者の検査結果が知られているかどうかによっても、その能力は異なる。本モデルでは、検査結果が陰性であったが、血縁者が検査を受けていない女性でも、リスクが26.3~56.7%過少予測された。
高浸透度の乳がんおよび/または婦人科がん感受性遺伝子
本文に以下の記述が追加された;大規模な研究によると、PALB2に病原性多様体を有する524家系が国際的な取り組みを介して募集され、女性における乳がんの相対リスクは7.18で、80歳までの乳がんリスクが53%であることが報告された(引用、参考文献433としてYang et al.)。その他に報告されたリスク上昇は、卵巣がんで生涯リスクが5%、膵がんで生涯リスクが2~3%、および男性乳がんで生涯リスクが1%などであった。これらの知見から、女性における遺伝性乳がん遺伝子としてのPALB2の役割が確認されると同時に、卵巣がん、膵がん、および男性乳がんとの関連性が確固たるものになる。
BRCA病原性多様体キャリアの臨床管理
本文に以下の記述が追加された;多施設ランダム化試験により、BRCA1/BRCA2病原性多様体の検査が陰性であるが、家族の乳がん生涯リスクが20%以上ある女性で、年1回の乳房磁気共鳴画像法(MRI)、年1回の乳房視触診(CBE)、および年2回のマンモグラムが年1回のマンモグラムおよびCBEと比較された。MRI群では、マンモグラム単独群よりも浸潤がんが小さく、リンパ節転移陽性が少ないうえに、病期が低かった(引用、参考文献47としてSaadatmand et al.)。
本要約はPDQ Cancer Genetics Editorial Boardが作成と内容の更新を行っており、編集に関してはNCIから独立している。本要約は独自の文献レビューを反映しており、NCIまたはNIHの方針声明を示すものではない。PDQ要約の更新におけるPDQ編集委員会の役割および要約の方針に関する詳しい情報については、本PDQ要約についておよびPDQ® - NCI's Comprehensive Cancer Databaseを参照のこと。
- 本PDQ要約について
-
本要約の目的
医療専門家向けの本PDQがん情報要約では、乳がんおよび婦人科がんの遺伝学について、包括的な、専門家の査読を経た、そして証拠に基づいた情報を提供する。本要約は、がん患者を治療する臨床家に情報を与え支援するための情報資源として作成されている。これは医療における意思決定のための公式なガイドラインまたは推奨事項を提供しているわけではない。
査読者および更新情報
本要約は編集作業において米国国立がん研究所(NCI)とは独立したPDQ Cancer Genetics Editorial Boardにより定期的に見直され、随時更新される。本要約は独自の文献レビューを反映しており、NCIまたは米国国立衛生研究所(NIH)の方針声明を示すものではない。
委員会のメンバーは毎月、最近発表された記事を見直し、記事に対して以下を行うべきか決定する:
要約の変更は、発表された記事の証拠の強さを委員会のメンバーが評価し、記事を本要約にどのように組み入れるべきかを決定するコンセンサス過程を経て行われる。
本要約の内容に関するコメントまたは質問は、NCIウェブサイトのEmail UsからCancer.govまで送信のこと。要約に関する質問またはコメントについて委員会のメンバー個人に連絡することを禁じる。委員会のメンバーは個別の問い合わせには対応しない。
証拠レベル
本要約で引用される文献の中には証拠レベルの指定が記載されているものがある。これらの指定は、特定の介入やアプローチの使用を支持する証拠の強さを読者が査定する際、助けとなるよう意図されている。PDQ Cancer Genetics Editorial Boardは、証拠レベルの指定を展開する際に公式順位分類を使用している。
本要約の使用許可
PDQは登録商標である。PDQ文書の内容は本文として自由に使用できるが、完全な形で記し定期的に更新しなければ、NCI PDQがん情報要約とすることはできない。しかし、著者は“NCI's PDQ cancer information summary about breast cancer prevention states the risks succinctly: 【本要約からの抜粋を含める】.”のような一文を記述してもよい。
本PDQ要約の好ましい引用は以下の通りである:
PDQ® Cancer Genetics Editorial Board.PDQ Genetics of Breast and Gynecologic Cancers.Bethesda, MD: National Cancer Institute.Updated <MM/DD/YYYY>.Available at: https://www.cancer.gov/types/breast/hp/breast-ovarian-genetics-pdq.Accessed <MM/DD/YYYY>.[PMID: 26389210]
本要約内の画像は、PDQ要約内での使用に限って著者、イラストレーター、および/または出版社の許可を得て使用されている。PDQ情報以外での画像の使用許可は、所有者から得る必要があり、米国国立がん研究所(National Cancer Institute)が付与できるものではない。本要約内のイラストの使用に関する情報は、多くの他のがん関連画像とともにVisuals Online(2,000以上の科学画像を収蔵)で入手できる。
免責条項
これらの要約内の情報は、保険払い戻しの決定基準として使用されるべきものではない。保険の適用範囲に関する詳しい情報については、Cancer.govのManaging Cancer Careページで入手できる。
お問い合わせ
Cancer.govウェブサイトについての問い合わせまたはヘルプの利用に関する詳しい情報は、Contact Us for Helpページに掲載されている。質問はウェブサイトのEmail UsからもCancer.govに送信可能である。

 画像を拡大する
画像を拡大する